臨床藥師參與1 例顱內靜脈竇血栓形成伴蛛網膜下腔出血妊娠患者抗凝治療實踐*
施 超,陳 霞,舒德忠
(重慶市涪陵中心醫院,重慶 408099)
顱內靜脈竇血栓形成(CVST)為少見的特殊腦血管疾病,可發生于顱腦內淺靜脈、深靜脈或靜脈竇,以深靜脈及靜脈竇多見。該病無特定的發病年齡,病因、危險因素及臨床表現缺乏特異性,如不及時治療,預后差,伴顱內出血時危險性增加,預后更差。在此,探討了臨床藥師參與1 例CVST 伴蛛網膜下腔出血妊娠患者的藥學監護實踐,以及該病的抗凝治療策略。現報道如下。
1 臨床資料
患者,女,28 歲,身高 160 cm,體質量 55 kg。因“間斷陰道出血 12 d,嘔吐 10 d,抽搐 8 h”于 2019 年 4 月 9 日急診入院。12 d 前無誘因出現間斷陰道出血,量少,呈鮮紅色,無腹痛等不適;10 d 前開始出現嘔吐不適,食欲下降;6 d 前出現陣發性頭昏、頭痛,未予重視,隨后癥狀加重;3 d 前就診于當地醫院,腹部彩超提示宮內早孕,口服復合維生素B 及輸注維生素C 注射液,癥狀改善;8 h前無誘因突發抽搐,伴意識模糊及全身冒冷汗,無大小便失禁,立即完善頭顱CT,考慮小腦出血,遂由120 接診轉入我院。2 年前行“子宮肌瘤切除術”;既往自然分娩1 子,本次為第2 次妊娠,末次月經出現于2019 年2 月3 日,發現妊娠以來,自行服用復合維生素片(每次1 片,每日1 次)。否認食物、藥物過敏史,否認免疫性相關疾病及血栓相關性遺傳疾病史。入院體格檢查示,體溫36.6 ℃ ,脈搏 90 次 / 分,呼吸頻率 24 次 / 分,血壓122 /76 mmHg(1 mmHg = 0.133 kPa)。意識模糊,精神狀態一般,語言交流困難;頭顱未見異常,眼瞼無水腫、下垂,雙側瞳孔等大等圓(直徑約3.5 mm),對光反射靈敏。頸對稱,有抵抗感。其余查體無異常。輔助檢查,急診頭顱CT 血管造影示,左側橫竇、乙狀竇及左側頸內靜脈上段未見確切造影劑充填,考慮血栓形成;右側椎動脈較對側纖細,基底動脈開窗畸形,右側大腦前動脈較對側纖細;左側小腦半球腦出血,量約1 mL,小腦幕密度增高,考慮蛛網膜下腔出血可能;左側顳枕葉交界皮質區斑片狀密度減低影,考慮梗死灶。急診床旁超聲(心臟、腹部、婦科、雙下肢靜脈血管)提示宮內早孕(測值約相當于妊娠9+3周);余無異常。急查凝血指標示,活化部分凝血活酶時間(APTT)28.00 s、D -二聚體14.76 mg/L、抗凝血酶Ⅲ 65.7% 。血常規示,血紅蛋白(Hb)121 g/L,血小板計數(PLT)147 ×109/L。腎功能、電解質、血沉、同型半胱氨酸、自身抗體譜等無異常。入院診斷:妊娠并顱內靜脈血栓形成,蛛網膜下腔出血,繼發性癲癇,Ⅰ型呼吸衰竭,缺血缺氧性腦病,孕8 周,妊娠早期出血。
2 藥物治療經過
入院后予吸氧,預防癲癇、對癥補液治療。結合病史及輔助檢查,重癥醫學科、神經內科、神經外科、婦產科、抗凝臨床藥師共同討論后,并與患者家屬溝通,決定先行抗凝治療,后行流產術。臨床藥師建議先予肝素鈉(2 mL ∶12 500 IU)抗凝治療,每 4 ~ 6 h 測定 1 次凝血功能,將APTT 維持在正常值的2 倍左右,同時觀察陰道流血及頭痛情況。4 月12 日,患者在超聲引導下行負壓人工流產術,術前臨床藥師建議不停用肝素,手術順利,術后予以縮宮素對癥止血。4 月18 日,患者無頭痛、惡心、陰道出血等不適,病情穩定,臨床藥師建議過渡為華法林(初始給藥每次2.5 mg,每日1 次)抗凝治療,肝素與華法林重疊使用,國際標準化比值(INR)達標24 h后停用。隨后監測血常規、凝血功能,4 月23 日測得INR 為 2.13,4 月 24 日為 2.09,予以停用肝素,未出現過敏反應、血小板減少及其他出血情況。4 月30 日,復查頭顱CT 提示,蛛網膜下腔出血較前基本吸收;側顳枕葉交界皮質區斑片狀密度減低影,考慮梗死灶,密度較前降低。5 月 1 日復查 INR 為 1.96,繼續口服華法林抗凝,出院后定期于抗凝門診隨訪,INR 在 1.92 ~2.49波動,于2019 年9 月中旬復查頭顱CT 血管造影后停用華法林。患者使用肝素期間凝血功能監測結果見表1。4 月 16 日至 4 月 24 日的 PT 達標,APTT 為 61.2 ~ 68.3,符合要求,不再贅述。
3 討論
3.1 CVST 及蛛網膜下腔出血原因分析
CVST 的病因和危險因素復雜多樣,可分為感染性和非感染性[1]。感染性常繼發于頭面部或其他部位化膿性感染或非特異性炎癥,該患者發病前無任何感染征象及炎性反應,予以排除。非感染性則多與高凝狀態、血液瘀滯、血管壁損傷有關,如各種遺傳性或繼發性的血栓形成傾向(V 因子 Leiden 突變、蛋白 C、蛋白 S、抗凝血酶Ⅲ缺陷、高同型半胱氨酸血癥)、妊娠、產后、口服避孕藥、血液系統疾病、腫瘤和外傷,但仍有部分原因不明。該患者既往無基礎疾病,否認血栓相關疾病史,孕8 周伴陰道流血,未服用特殊藥物,入院查抗凝血酶Ⅲ輕微降低,同型半胱氨酸、自身抗體譜無異常;綜合考慮,患者發生顱內靜脈血栓與妊娠相關性最大,但不排除與凝血因子的相關性。
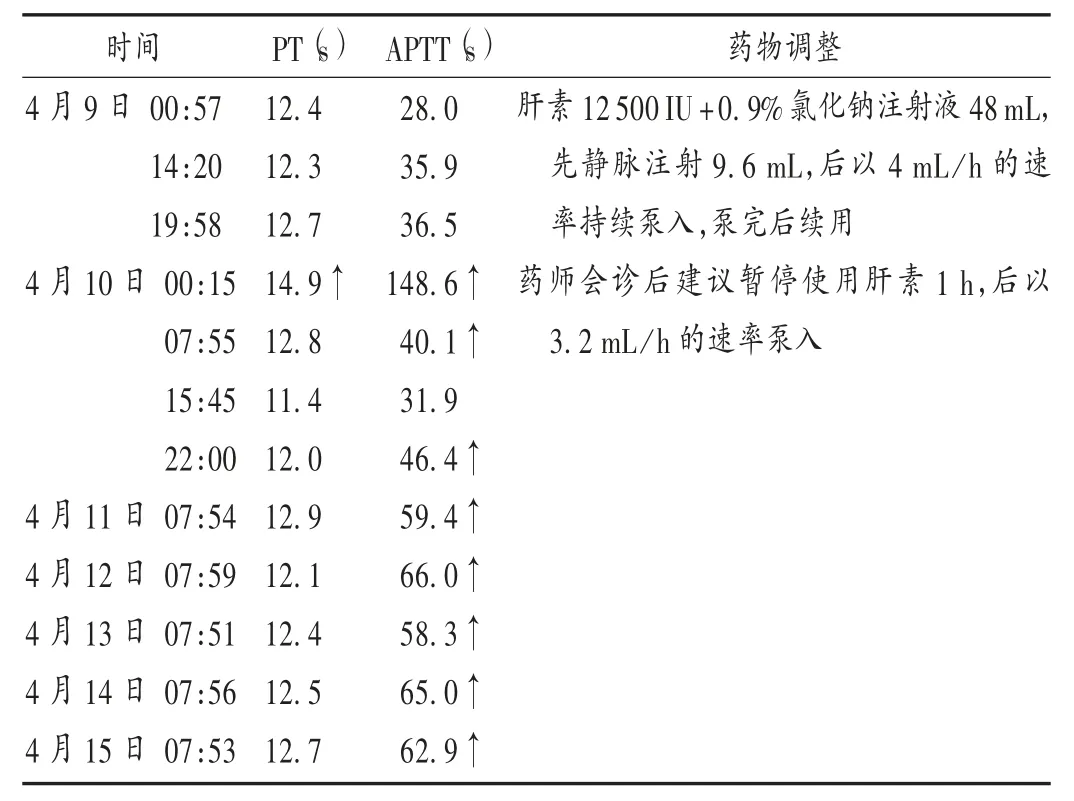
表1 患者使用肝素期間凝血功能監測及藥物調整情況Tab.1 The monitoring of coagulation function and adjustment of drugs during the use of heparin
CVST 患者中有 35% ~ 39% 伴顱內出血[2],但繼發蛛網膜下腔出血較罕見[3],且機制尚未完全清楚,目前已有結論為:CVST 導致局部的炎性反應,增加血管壁通透性,血液滲入蛛網膜下腔;CVST 引起腦皮質靜脈和橋靜脈擴張、靜脈壓增高,血管破裂,血液流入蛛網膜下腔;CVST 并腦靜脈性梗死后出血,血液滲入蛛網膜下腔。國內外研究發現,妊娠和產褥期、多個靜脈竇受累是CVST并腦出血的危險因素[4-5]。該患者明確有妊娠和多個靜脈竇受累(顱內CT 血管造影證實)2 個危險因素。
3.2 抗凝治療
CVST 的治療除查找病因和治療原發性疾病外,還應積極抗凝,以有效防止血栓進一步擴展,促進血栓溶解。抗凝治療是CVST 患者急性期的首選治療方案,同時也是基礎治療方案,患者總體預后良好[6]。目前國內指南[1]、歐洲神經病學聯盟和美國心臟協會指南[7-8]均推薦:CVST 一旦確診且無其他抗凝禁忌證,均應盡早進行抗凝治療,伴CVST 的少量顱內出血不是肝素抗凝治療的絕對禁忌證。指南中強調,伴CVST 的少量顱內出血患者急性期可選擇普通肝素或低分子肝素,且低分子肝素的安全性和有效性略優于普通肝素。對于抗凝治療前已存在的顱內出血,應嚴密監測患者的臨床癥狀及體征改善情況,動態影像監測血腫大小,若血腫有擴大,避免抗凝治療[9]。急性期后抗凝藥物選擇華法林(INR 維持在 2.0 ~ 3.0),而非新型口服抗凝藥(研究證據少,有待進一步研究),療程因血栓風險及復發風險大小而定,至少3 個月,原因不明確或復發性抗凝時間稍長。
該患者入院時病情急,充分評估無抗凝絕對禁忌證,立即決定抗凝治療,考慮到后期需行人工流產術及術后出血風險,臨床藥師建議使用普通肝素(指南[1]中要求使用普通肝素抗凝治療時需將APTT 延長至少1 倍),以防發生大出血。患者基礎APTT 為28 s,肝素抗凝過程中,一直維持在60 s 左右,抗凝強度適宜。患者病情平穩后(約10 d)啟動華法林抗凝,INR 穩定后即停用肝素,后期INR 一直維持在目標范圍,抗凝治療總計6 個月,患者恢復可,無殘留后遺癥,未復發,整個過程持續監測血常規及出血情況,無不良反應發生。
3.3 人工流產圍術期的抗凝管理
國內外指南[10-11]均指出:接受抗凝藥物治療的患者,圍術期是否停用抗凝藥,需根據手術類型綜合評估患者出血風險決定。接受低出血風險手術的患者,可繼續予以抗凝治療;其他手術患者術前應暫停使用抗凝藥物;對于正在服用華法林的患者,需根據血栓栓塞的發生風險決定停藥后是否行橋接抗凝治療。3 個月內的血栓栓塞患者如停止抗凝,圍術期血栓栓塞復發風險較高。
出血風險主要受手術或有創操作類型及患者的自身因素影響。國外指南[12]指出,不論是藥物流產還是手術流產,其出血量均很少,可根據危險因素情況劃分產后出血風險等級。剖宮產史少于2 次和無胎盤前置或胎盤植入史、無出血性疾病、無產科出血史為低危出血風險;剖宮產史不少于2 次、有剖宮產和胎盤前置史、出血性疾病、有產科出血史但無須輸血、高齡產婦、孕周大于20 周、子宮肌瘤、肥胖為中危出血風險;診斷胎盤植入、有產科出血史且需輸血為高危出血風險(臨床醫師可根據臨床實際情況將部分中危風險提升為高危風險)。操作時間長且涉及重要部位、血流豐富器官或大血管的手術或有創操作應視為高出血風險,而一些口腔科操作、皮膚活檢或白內障手術應視為低出血風險。且接受抗凝治療的婦女行人工流產術,出血量非常小[13-14],目前尚無證據表明84 d 以內的早期人工流產術需停用抗凝藥物[14]。劉曉妍[15]的研究發現,在超聲引導下行無痛人流術,手術時間和出血時間明顯縮短,出血量明顯減少。
綜上所述,該患者顱內靜脈血栓明確且風險高,需抗凝治療;既往自然分娩1 子,無剖宮產史,無胎盤前置或胎盤植入史,無其他出血性疾病,未發生過出血,且在超聲引導下行人工負壓流產術,整體出血風險低,術前無須停用肝素抗凝,但應加強術中、術后陰道流血情況的觀察及處理。術后,對癥給予縮宮素止血,未見陰道大量流血,1 周左右流血停止。表明臨床藥師的干預起到了積極作用,改善了患者的臨床轉歸。

