HPLC法同時測定薄荷配方顆粒中6種成分的含量
田偉 李葆林 張闖 甄亞欽 王鑫國 牛麗穎
摘要:為了提高薄荷配方顆粒的質量標準,建立其多指標定量評價體系,采用HPLC法同時測定薄荷配方顆粒中咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷6種成分的含量。采用Poroshell 120 EC-C18(4.6 mm×250 mm,5 μm)色譜柱,以甲醇(A)-乙腈(B)-5%冰乙酸(C)為流動相,梯度洗脫,流速為0.6 mL/min,柱溫為35 ℃,咖啡酸、迷迭香酸、蒙花苷的檢測波長為330 nm,橙皮苷、香蜂草苷的檢測波長為284 nm,香葉木苷的檢測波長為380 nm。結果表明,薄荷配方顆粒中6種待測成分的線性關系、分離度、重復性均符合要求,各成分的平均回收率分別為99.19%,98.06%,100.45%,98.90%,100.17%,99.78%。不同廠家的薄荷配方顆粒中6種化學成分的含量存在一定差異。建立的HPLC分析方法簡便、快速、準確,可以為薄荷配方顆粒的質量控制提供方法參考。
關鍵詞:中藥化學;薄荷;配方顆粒;高效液相色譜法;含量測定
中圖分類號:R284.1文獻標識碼:ADOI: 10.7535/hbgykj.2021yx03004
Abstract:In order to improve the quality standard of Herba Menthae formula granules and establish a quantitative evaluation system of multiple indexes, the contents of caffeic acid, hesperidin, rosmarinic acid, diosmin, didymin and buddleoside in Herba Menthae formula granules were determined by using the method of HPLC. The analysis was carried out on Poroshell 120 EC-C18 column (4.6 mm×250 mm, 5 μm) by gradient elution with methanol (A)-acetonitrile (B)-5% acetic acid (C) as the mobile phase at the flow rate of 0.6 mL/min. The column temperature was set at 35 ℃. The detective wavelength were 330 nm for caffeic acid, rosmarinic acid and buddleoside, 284 nm for hesperidin and didymin, 380 nm for diosmin, respectively. The results show that the linear relationship, separation and repeatability of the six constituents in Herba Menthae formula granules all meet the requirements. The average recovery rates of the constituents are 99.19%, 98.06%, 100.45%, 98.90%, 100.17% and 99.78%, respectively. There are certain differences in the six chemical constituents in Herba Menthae formula granules from different manufacturers. The method of HPLC is simple, accurate and reproducible, which can provide a method reference for the quality control of Herba Menthae formula granules.
Keywords:chemistry of Chinese material medical; Herba Menthae; formula granules; HPLC; content determination
薄荷為唇形科植物薄荷Mentha haplocalyx Briq.的干燥地上部分,其性涼,味辛,歸肺、肝經,具有疏散風熱,清利頭目等功效[1]。現代研究表明,薄荷所含化學成分復雜,主要有揮發油類、黃酮類、有機酸、氨基酸等化學成分[2],具有抗炎、抗氧化、抗腫瘤、抗病毒和抗生育等多種藥理作用[3]。目前有關薄荷的研究主要集中于其揮發油部分,薄荷傳統用藥方式主要為水煎,因此揮發油并非其唯一藥效成分,但是關于薄荷非揮發性化學成分以及質量控制的研究相對較少。徐晶晶等[4]建立了薄荷藥材特征圖譜,并釆用DPPH法、FRAP法分別測定其抗氧化活性,通過譜效關系研究表明薄荷中對抗氧化作用貢獻較大的化合物成分主要為黃酮類和酚酸類。薄荷黃酮類化合物目前主要分離出橙皮苷、蒙花苷、香葉木苷、香蜂草苷、香葉木素、蘆丁等,研究表明薄荷黃酮主要具有良好的抗炎、抗氧化、抗病毒等作用[5-6]。薄荷酚酸類化合物主要有迷迭香酸、咖啡酸、順式丹酚酸、紫草酸等,也是薄荷抗炎、抗菌、抗氧化活性的主要成分,與其臨床療效緊密聯系[7-8]。
配方顆粒是現代中藥飲片重要的發展形式,薄荷配方顆粒是以優質的薄荷飲片為原料,以水為溶媒經現代工藝提取、濃縮、干燥、制粒而成的單味中藥顆粒劑,具有服用量小,攜帶保存方便,衛生安全等優點[9-12]。目前薄荷配方顆粒水溶性指標成分為迷迭香酸,但是依靠單一成分定量的標準具有較強的局限性,因此需要建立薄荷配方顆粒中多指標定量的評價體系。目前采用高效液相色譜法同時測定薄荷配方顆粒中非揮發性成分咖啡酸、橙皮苷、迷迭香酸、香葉木素、香蜂草苷和蒙花苷的含量未見文獻報道,本實驗采用HPLC-DAD法同時測定薄荷配方顆粒中上述6種成分的含量,為薄荷配方顆粒質量的有效控制提供方法參考和數據支撐。第3期田偉,等:HPLC法同時測定薄荷配方顆粒中6種成分的含量河北工業科技第38卷
1儀器與試劑
1.1儀器
LC-20A型高效液相色譜儀,日本島津公司提供;Poroshell 120 EC-C18色譜柱(4.6 mm×250 mm,5 μm),美國安捷倫公司提供;TB-215D電子天平(十萬分之一),BSA224S-CW電子天平(萬分之一),德國賽多利斯集團提供;KQ-250型超聲波清洗器(功率250 W,頻率40 kHz),昆山超聲儀器有限公司提供。
1.2試劑
咖啡酸對照品(批號為110885-200102,純度為100.0%),橙皮苷對照品(批號為110721-201818,純度為96.2%),均購自中國食品藥品檢定研究院;迷迭香酸對照品(批號為111820-201404,純度為98.0%),蒙花苷(批號為111528-201509,純度為98.0%),均購自成都曼斯特生物技術有限公司;香葉木苷對照品(批號為PS020083,純度為98.0%),香蜂草苷對照品(批號為PS14081801,純度為98.0%),均購自成都普思生物科技股份有限公司;薄荷配方顆粒(編號為S1—S12)分別購自神威藥業集團有限公司、江陰天江藥業有限公司、華潤三九醫藥股份有限公司、四川新綠色藥業科技發展股份有限公司、廣東一方制藥有限公司、北京康仁堂藥業有限公司;乙腈、乙酸為色譜純,美國Fisher公司提供;水為超純水。
2實驗方法
以薄荷配方顆粒為研究對象,參考文獻[11]—文獻[22]設計實驗方案,完成方法學考察。
2.1對照品溶液的制備
精密稱取咖啡酸對照品、迷迭香酸對照品、香蜂草苷對照品適量分別置于25 mL量瓶中,加甲醇溶解并稀釋至刻度,搖勻即得質量濃度為0.384 8 mg/mL的咖啡酸儲備液、0.645 2 mg/mL的迷迭香酸儲備液、0.117 6 mg/mL的香蜂草苷儲備液;精密稱取橙皮苷對照品、香葉木苷對照品、蒙花苷對照品適量分別置于5 mL量瓶中,加二甲基亞砜溶解并稀釋至刻度,搖勻即得質量濃度為2.472 0 mg/mL的橙皮苷儲備液、1.256 0 mg/mL的香葉木苷儲備液、2.900 0 mg/mL的蒙花苷儲備液;分別精密吸取各儲備液適量置于同一50 mL量瓶中,加甲醇稀釋至刻度,搖勻即得每1 mL含咖啡酸7.70 μg、橙皮苷24.72 μg、迷迭香酸38.71 μg、香葉木苷12.56 μg、香蜂草苷7.06 μg、蒙花苷29.00 μg的混合對照品儲備液。
2.2供試品溶液的制備
取薄荷配方顆粒適量,研細,取約0.25 g,精密稱定,置于具塞錐形瓶中,加入體積分數(下同)75%的甲醇25 mL,密塞,稱定質量,超聲處理(功率250 W,頻率40 kHz)30 min,放冷,加75%甲醇補足減失的質量,搖勻,濾過,取續濾液,即得。
2.3陰性對照溶液的制備
取糊精適量,按照2.2項中供試品溶液制備方法制備陰性對照溶液。
2.4色譜條件
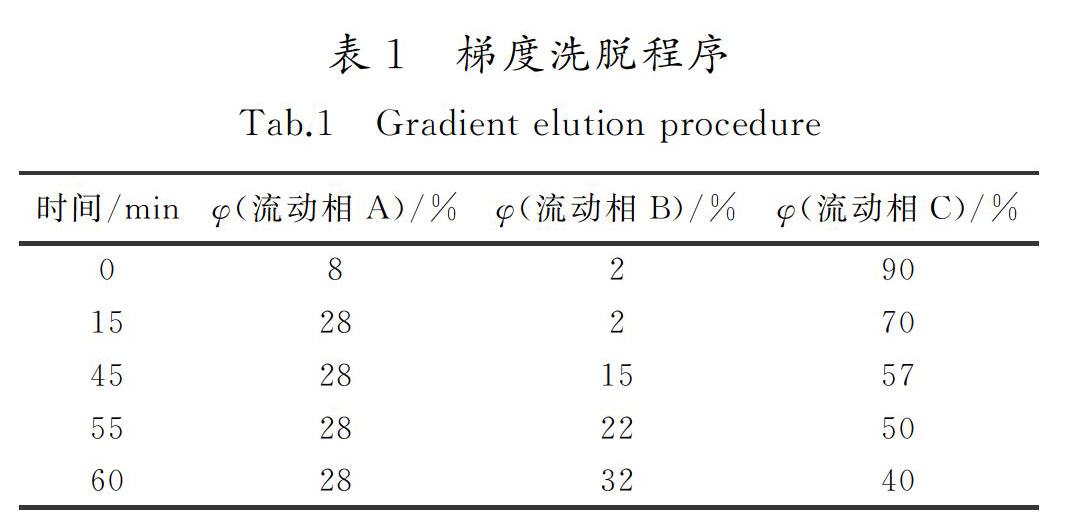
色譜柱為Poroshell 120 EC-C18柱(4.6 mm×250 mm,5 μm);以甲醇(A)-乙腈(B)-5%冰乙酸(C)為流動相,梯度洗脫程序見表1;咖啡酸、迷迭香酸、蒙花苷的檢測波長為330 nm,橙皮苷、香蜂草苷的檢測波長為284 nm,香葉木苷的檢測波長為380 nm;流速為0.6 mL/min;柱溫為35 ℃。
2.5方法學考察
2.5.1 專屬性試驗
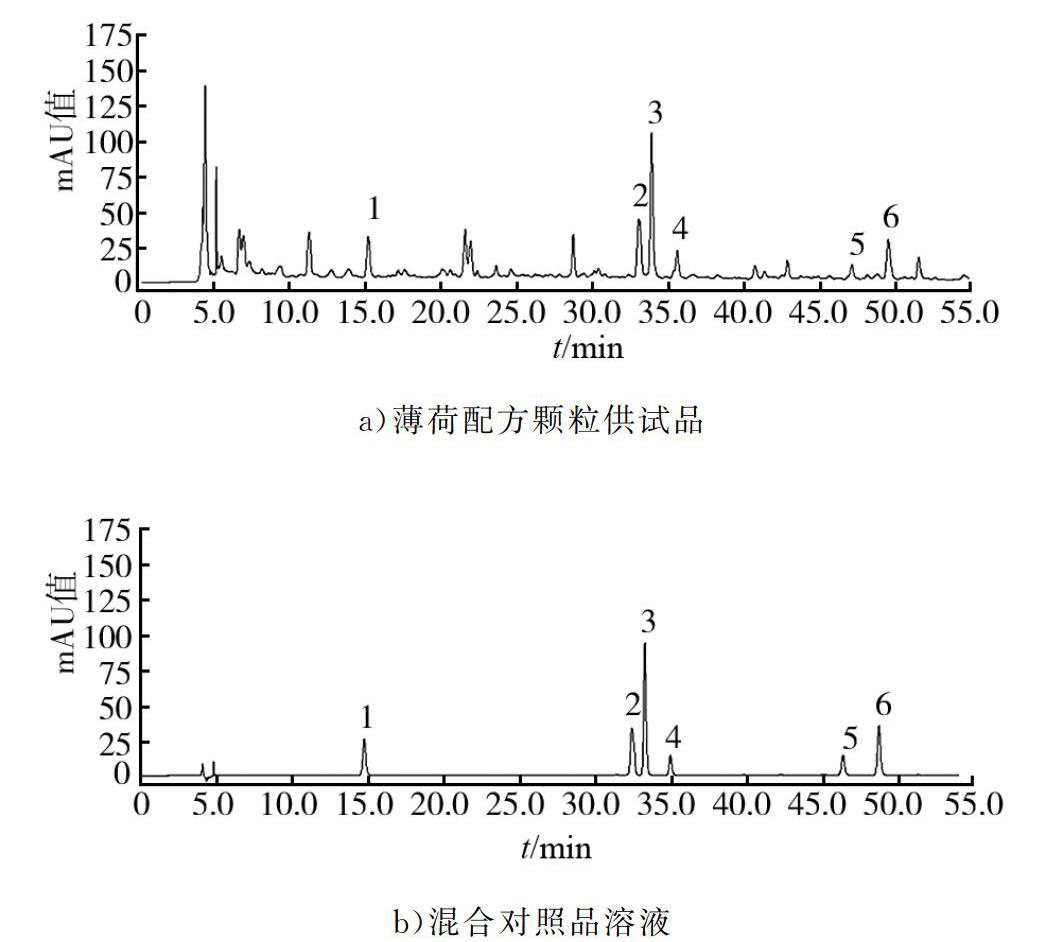
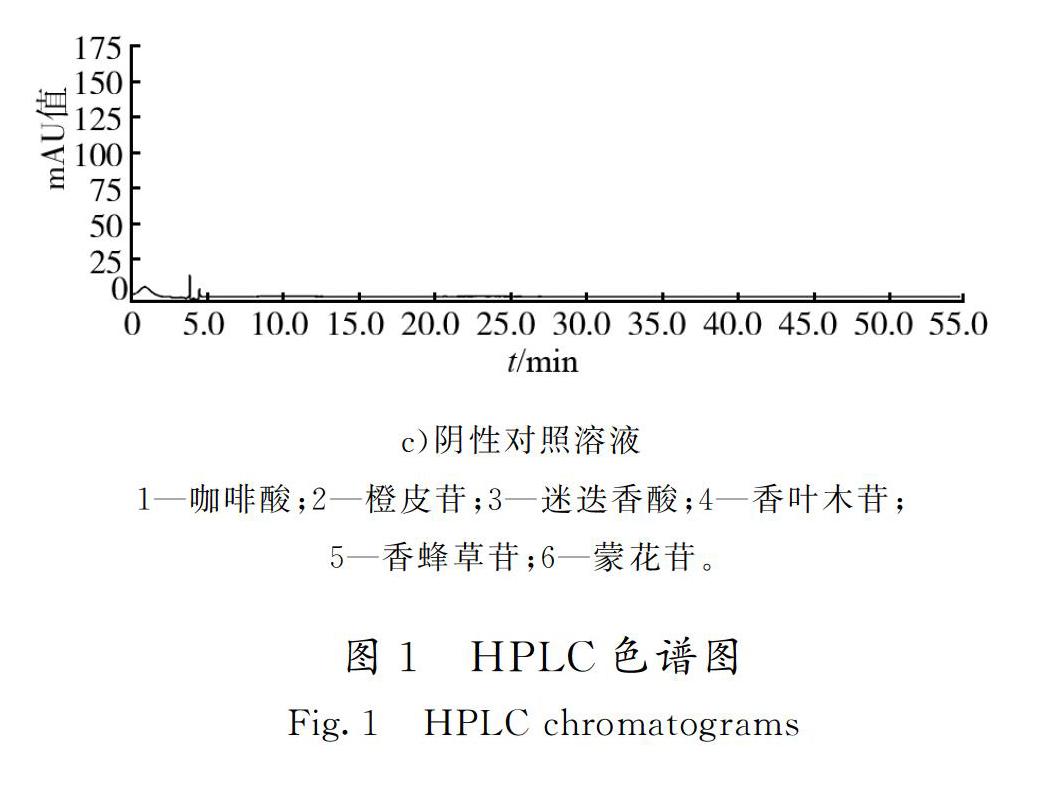
精密吸取陰性對照溶液、混合對照品溶液和供試品溶液各10 μL,按2.4項中色譜條件(檢測波長為284 nm)測定,結果表明在該色譜條件下,輔料對樣品測定無干擾。結果見圖1。
2.5.2線性關系考察
精密量取2.1項中混合對照品溶液0.5,1,2,4,6 mL,分別置于10 mL量瓶中,用甲醇稀釋至刻度,搖勻,得到系列濃度的6 種成分混合對照品溶液。分別精密吸取上述溶液及儲備液10 μL,按 2.4項中色譜條件(檢測波長為284 nm)測定,記錄峰面積。以峰面積為因變量、濃度為自變量進行線性回歸分析,各組分在其相應的濃度范圍內線性關系良好,見表 2。
2.5.3精密度試驗
精密吸取混合對照品溶液10 μL,連續進樣6次,計算咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的峰面積RSD分別為0.40%,0.32%,0.26%,0.26%,0.44%,0.27%,表明儀器精密度良好。
2.5.4穩定性試驗
取同一供試品溶液,分別于0,2,6,12,20,30 h進樣10 μL,按2.4項中色譜條件測定,計算咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的峰面積RSD分別為0.16%,1.29%,0.81%,0.20%,1.19%,1.28%(n=6)。結果表明,供試品溶液在30 h內穩定性良好。
2.5.5重復性試驗
取同一批薄荷配方顆粒樣品(S9),分別取低(0.125 g)、中(0.25 g)、高(0.375 g)3個樣品量,每個樣品量3份,按供試品溶液的制備方法制備供試品溶液,按2.4項中色譜條件測定,計算得到樣品中咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的平均含量(質量分數,下同)分別為0.38,1.30,1.79,0.58,0.22,1.14 mg/g,RSD分別為0.77%,1.05%,1.21%,2.37%,2.14%,2.53%(n=6)。結果表明該方法重復性良好。
2.5.6加樣回收率試驗
取同一批已知含量的薄荷配方顆粒(S9)9份,按每3份為一組,每組精密加入對照品咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的量相當于薄荷配方顆粒中各對照品含量的50%,100%,150%,按供試品溶液制備方法制備供試品溶液,按2.4項中色譜條件測定,分別計算咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的回收率,結果見表3-表8。
3結果及分析討論
3.1樣品測定
取不同廠家、不同批號的薄荷配方顆粒適量,研細,各取約 0.25 g,精密稱定,分別按照2.2項中制備供試品溶液,按照2.4項中色譜條件進樣10 μL,測定咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷的含量,結果見表9。
3.2分析討論
本研究采用二極管陣列檢測器對6種指標成分進行200~400 nm全波長掃描,發現咖啡酸、迷迭香酸和蒙花苷在330 nm處均有較大紫外吸收,橙皮苷和香蜂草苷在284 nm處有較大吸收,香葉木苷在345 nm處有最大吸收,但是在此波長下香葉木苷與相鄰峰無法實現基線分離,在380 nm波長時香葉木苷仍有較大紫外吸收,而影響香葉木苷測定的干擾峰在此波長下無紫外吸收,因此選擇380 nm作為香葉木苷的檢測波長。
橙皮苷、迷迭香酸和香葉木苷3種成分的色譜峰保留時間較為接近,考察乙腈-0.1%磷酸、乙腈-0.1%甲酸、乙腈-5%乙酸、甲醇-乙腈-5%乙酸等多種流動相系統,最終發現以甲醇-乙腈-5%冰乙酸作為流動相,采用梯度洗脫,混合對照品溶液和供試品溶液中6種待測指標成分色譜峰峰形均較好,分離度符合要求。
結果表明,不同廠家以及相同廠家不同批號的薄荷配方顆粒含量存在一定差異。造成此差異的因素很多,其中最重要的因素有2個:一為原料,二為生產工藝。有研究報道表明,部位、采收期、產地的不同均對薄荷藥材中有效成分的含量有不同程度的影響[23]。此外,不同廠家所采用的提取、干燥工藝不同也可能導致指標成分的差異。制劑工藝主要影響薄荷中有效成分的溶出與轉化、輔料用量等。在薄荷標準湯劑的研究中發現,咖啡酸在標準湯劑中的轉移率超過了150%,多批次薄荷標準湯劑樣品超過了200%。薄荷中迷迭香酸、丹酚酸等有機酸均含有咖啡酸的結構,在煎煮過程中可能發生化合鍵的斷裂從而生成咖啡酸。有研究表明迷迭香酸的抗氧化能力強于咖啡酸[24],因此為保證薄荷配方顆粒的質量和臨床療效應嚴格控制提取、濃縮等工藝條件。
4結語
薄荷配方顆粒中非揮發性成分是發揮藥效的重要成分,目前,采用高效液相色譜法同時測定薄荷配方顆粒中多種非揮發性成分的方法鮮有報道[11]。本實驗通過對流動相、檢測波長、提取方法等進行考察,最終確定了采用 HPLC法同時測定薄荷配方顆粒中咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷6種成分的含量,以甲醇-乙腈-5%冰乙酸為流動相,梯度洗脫,流速為0.6 mL/min,柱溫為35 ℃,檢測波長分別為咖啡酸、迷迭香酸、蒙花苷采用330 nm,橙皮苷和香蜂草苷采用284 nm,香葉木苷采用380 nm。結果表明,咖啡酸、橙皮苷、迷迭香酸、香葉木苷、香蜂草苷和蒙花苷分別在0.39~7.70,1.24~24.72,1.94~38.71,0.63~12.56,0.35~7.06,1.45~29.00 mg/L呈現良好的線性關系,相關系數r均大于0.999 7,各成分的平均回收率分別為99.19%,98.06%,100.45%,98.90%,100.17%,99.78%。該方法簡便快速、重復性好、專屬性強,可以為薄荷配方顆粒質量的有效控制提供方法參考和科學依據。
薄荷中含有多種黃酮類和酚酸類成分,具有抗炎、抗氧化、抗菌和抗病毒等藥理作用,與其臨床療效密切相關。本文僅對薄荷配方顆粒中6種成分進行了同時測定,未來應繼續深入研究薄荷配方顆粒中的其他黃酮類和酚酸類成分。中藥指紋圖譜是一種全面反映中藥或中藥制劑整體性化學特征的質量分析方法,被廣泛應用于中藥及中藥制劑的質量控制,而目前薄荷配方顆粒中多個色譜峰未能指認,未來可以通過多成分含量測定和指紋圖譜相結合的方式全面控制薄荷配方顆粒的質量。
參考文獻/References:
[1]國家藥典委員會.中華人民共和國藥典(2015年版一部)[M].北京:中國醫藥科技出版社,2015.
[2]華燕青.薄荷化學成分及其提取方法研究進展[J].陜西農業科學,2018,64(4):83-86.
[3]高榆嘉,張文靜,劉萌,等.薄荷藥理作用的研究進展[J].吉林醫藥學院學報,2020,41(3):215-217.
[4]徐晶晶,劉斌.基于DPPH、FRAP法的薄荷藥材抗氧化譜效關系研究[J].北京中醫藥大學學報,2015,38(6):405-410.
XU Jingjing, LIU Bin. Spectrum-effect relation in antioxidant activity of Menthae haplocalycis Herba based on DPPH and FRAP assay[J]. Journal of Beijing University of Traditional Chinese Medicine, 2015, 38(6): 405-410.
[5]陳向陽,張樂,吳瑩,等.LCMS-IT-TOF 法快速分析薄荷黃酮部位的主要化學成分[J].北京中醫藥大學學報,2015,38(8):546-550.
CHEN Xiangyang, ZHANG Le, WU Ying, et al. Rapid analysis of chemical compositions in the flavonoid fraction of Mentha haplocalyx Briq. with LCMS-IT-TOF[J]. Journal of Beijing University of Traditional Chinese Medicine, 2015, 38(8):546-550.
[6]鐘昆芮,張凡,姜艷艷,等.薄荷總黃酮的純化工藝優選[J].中國實驗方劑學雜志,2013,19(6):11-14.
ZHONG Kunrui, ZHANG Fan, JIANG Yanyan, et al. Optimization of purification technology for total flavonoids from Mentha haplocalyx[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2013, 19(6): 11-14.
[7]陳向陽.薄荷酚類部位化學成分及抗炎活性研究[D].北京:北京中醫藥大學,2016.
[8]周德勇,張樂,姜艷艷,等.薄荷酚類對照提取物HPLC含量測定研究及其在薄荷藥材質量控制中的應用[J].藥物分析雜志,2018,38(4):582-589.
ZHOU Deyong, ZHANG Le, JIANG Yanyan, et a1. HPLC assay of phenolic reference extract of mint and its application in quality evaluation of the herb[J]. Chinese Journal of Pharmaceutical Analysis, 2018, 38(4): 582-589.
[9]張紅梅,宋景政,譚紅勝,等.從湯劑到顆粒劑:中藥配方顆粒20年回顧與展望[J].世界科學技術-中醫藥現代化,2012,14(4):1740-1753.
ZHANG Hongmei, SONG Jingzheng, TAN Hongsheng, et a1.From traditional decoction to modern granule: Perspectives and prospects of Chinese medicine dispensing granules[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2012, 14(4): 1740-1753.
[10]江麗杰,胡鏡清,楊響光,等.臨床醫生對中藥配方顆粒應用認知初步調查[J].中成藥,2011,33(2):326-328.
[11]田偉,甄亞欽,王鑫國,等.HPLC法同時測定薄荷配方顆粒中3種成分[J].中成藥,2016,38(12):2602-2605.
TIAN Wei, ZHEN Yaqin, WANG Xinguo, et a1. Simultaneous determination of three constituents in Bohe Dispensing Granules by HPLC[J]. Chinese Traditional Patent Medicine, 2016, 38(12): 2602-2605.
[12]甄亞欽,田偉,李斯,等.HPLC法同時測定荊芥配方顆粒中4種成分的含量[J].中藥材,2016,39(10):2285-2287.
[13]田偉,甄亞欽,范帥帥,等.高效液相色譜法同時測定車前子配方顆粒中京尼平苷酸、咖啡酸、毛蕊花糖苷和異毛蕊花糖苷的含量[J].中國藥學雜志,2018,53(2):140-144.
TIAN Wei, ZHEN Yaqin, FAN Shuaishuai, et a1. Simultaneous determination of geniposidic acid, caffeic acid, acteoside and isoacteoside in Plantaginis Semen formula granules by HPLC[J]. Chinese Pharmaceutical Journal, 2018, 53(2): 140-144.
[14]孫福仁,高晗,李雪利,等.佛手標準湯劑中兩種成分的測定方法研究[J].河北工業科技,2019,36(3):221-226.
SUN Furen, GAO Han, LI Xueli, et a1. Simultaneous determination of two constituents in standard decoction of Citri sarcodactylis fuctus by UPLC[J]. Hebei Journal of Industrial Science and Technology, 2019, 36(3): 221-226.
[15]王迎春,麻景梅,王夢,等.基于相關性的麻黃配方顆粒HPLC特征圖譜研究[J].河北工業科技,2020,37(4):286-290.
WANG Yingchun, MA Jingmei, WANG Meng, et al. Correlation study on HPLC characteristic chromatograms of Ephedra formula granules[J]. Hebei Journal of Industrial Science and Technology, 2020, 37(4): 286-290.
[16]耿彥梅,高晗,孫福仁,等.蒼耳子標準湯劑質量研究[J].河北工業科技,2019,36(2):122-127.
GENG Yanmei, GAO Han, SUN Furen, et al. Study on quality of Xanthii Fructus standard dection[J]. Hebei Journal of Industrial Science and Technology, 2019, 36(2): 122-127.
[17]吳佳妮,夏書雪,李雪梅,等.薄荷標準湯劑的指紋圖譜及成分分析[J].中國實驗方劑學雜志,2019,25(16):128-134.
WU Jiani, XIA Shuxue, LI Xuemei, et al. HPLC fingerprint and chemical constituents of Menthae Haplocalycis Herba standard decoction[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2019, 25(16): 128-134.
[18]張肖建,張巖巖,高晗,等.牛蒡子標準湯劑質量評價體系的建立[J].河北工業科技,2019,36(1):47-52.
ZHANG Xiaojian, ZHANG Yanyan, GAO Han, et al. Establishment of quality evaluation system for standard decoction of Arctii fructus[J]. Hebei Journal of Industrial Science and Technology, 2019, 36(1): 47-52.
[19]徐晶晶,徐超,劉斌.不同采收期薄荷中4個黃酮苷的含量測定[J].藥物分析雜志,2013,33(12):2077-2081.
XU Jingjing, XU Chao, LIU Bin.HPLC simultaneous determination of four flavone glycosides in Menthae Haplocalycis Herba during different harvest periods [J]. Chinese Journal of Pharmaceutical Analysis, 2013, 33(12): 2077-2081.
[20]許世富.高效液相色譜法測定清肺顆粒中甘草酸的含量[J].現代農業科技,2020(7):222-223.
XU Shifu. Determination of glycyrrhizic acid content in Qingfei granule by HPLC[J]. Modern Agricultural Science and Technology, 2020(7): 222-223.
[21]姚沅平,李柯,符國成,等.五指柑藥材質量標準研究[J].中藥新藥與臨床藥理,2020,31(2):219-223.
YAO Yuanping, LI Ke, FU Guocheng, et al. Study on quality standard of Herba Viticix negundo[J]. Traditional Chinese Drug Research and Clinical Pharmacology, 2020, 31(2): 219-223.
[22]陳晶晶,張振凌,曹淼淼,等.百藥煎HPLC指紋圖譜的建立及其中5種成分的含量測定[J].中國藥房,2020,31(2):173-178.
CHEN Jingjing,ZHANG Zhenling, CAO Miaomiao, et al. Establishment of HPLC fingerprint of Chinese gall leaven and content determination of 5 Components[J]. China Pharmacy, 2020, 31(2): 173-178.
[23]胡少偉,鐘昆芮,楊佳穎,等.薄荷莖、葉中黃酮類成分在不同采收期的含量差異性研究[J].中國中藥雜志,2018,43(3):544-550.
HU Shaowei, ZHONG Kunrui, YANG Jiaying,et al. Study on difference of flavonoids content in stems and leaves of Mentha Haplocalycis Herba in different harvest periods[J]. China Journal of Chinese Materia Medica, 2018, 43(3): 544-550.
[24]羅思琳.不同抗氧化劑抗氧化性能的比較及其對小鼠采食量影響的研究[D].廣州:華南農業大學,2016.
LUO Silin. A Comparative Study on the Antioxidant Activity of Different Antioxidants and Their Effects on Food Intake in Mice[D].Guangzhou: South China Agricultural University, 2016.

