3-硝基吡咯烷-1-羧酸叔丁基酯的合成*
王曉霞,徐小娜
(咸陽職業技術學院 醫藥化工學院,陜西 咸陽 712000)
吡咯烷類結構單元常見于化學藥物、生物活性物質、精細化學品[1-5]等分子結構中,在有機結構的構建中具有廣泛的應用。吡咯烷酮衍生物及各種取代的吡咯烷衍生物是重要的化學合成原料及中間體,如促進智力發育藥物吡拉西坦(Piracetam)[6]、急性骨髓性白血病治療藥物艾伏尼布(Ivosidenib)[7]、廣譜性蛋白激酶抑制劑米哚妥林(Midostaurin)[8]、預防癌癥化療術后惡心嘔吐藥物羅拉吡坦(Rolapitant)[9]、抑制血糖作用的特力利汀(Teneligliptin)[10]、多發性骨髓瘤治療藥物來那度胺(Lenalidomide)[11]、抗菌作用的多尼培南(doripenem)[12]中都含有吡咯烷結構片段。吡咯烷酮及各種取代吡咯烷衍生物作為重要的化學中間體具有一定的開發價值。本文開發了3-硝基吡咯烷-1-羧酸叔丁基酯(1)的合成,并優化其合成工藝,為吡咯烷類物質的工藝優化、路線改造、新物質開發及藥物研發提供一定參考。
1 實驗部分
1.1 儀器與試劑
AV400型核磁共振儀(CDCl3為溶劑,TMS為內標 德國Bruker公司);Ultima Global Spectrometer型質譜儀(ESI源)(美國Waters公司);RE-52AA旋轉蒸發儀(上海亞榮生化儀器廠);SHB-Ш循環水式多用真空泵(鞏義市予華儀器有限責任公司)。
鹽酸羥胺(NH2OH·HCl)、過氧化脲(UHP)、三氟乙酸酐(TFAA),百靈威科技有限公司;柱層析硅膠(300~400目 青島海洋化工廠);Na2HPO4、NaHCO3、乙腈、乙醇等其他試劑均為市售分析純。
1.2 實驗方法
1.2.1 合成路線 以1-Boc-吡咯烷酮(2)為原料,在NaHCO3做堿的條件下與鹽酸羥胺發生氨肟化反應,得1-Boc-3-吡咯烷酮肟(3),化合物(3)在三氟乙酸酐存在下,經過氧化脲(UHP)氧化反應可得目的物3-硝基吡咯烷-1-羧酸叔丁基酯(1),合成路線見圖1。
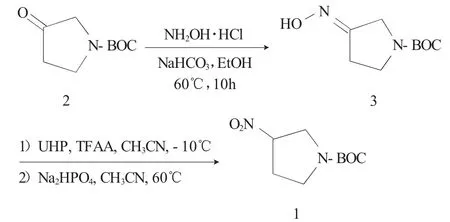
圖1 3-硝基吡咯烷-1-Boc的合成路線Fig.1 Synthetic route for 3-nitropyrrolian-1-Boc
1.2.2 合成方法
(1)1-Boc-3-吡咯烷酮肟(3)的合成 在10L反應釜中加入4L EtOH,1-Boc-吡咯烷酮(2)(685g,3.7mol),混合均勻后加入NaHCO3(466g,5.55mol),黃色溶液變為白色渾濁液,加入NH2OH·HCl(283g,4.07mol),升溫至60℃,反應過夜;TLC監測反應完畢,減壓濃縮除EtOH溶劑,加EA,抽濾除去白色固體,濾液加H2O萃取(4L),有機相用飽和NaCl洗滌,無水Na2SO4干燥,減壓濃縮,得白色固體729g,收率98.5%。1H NMR(CDCl3,400MHz):8.800~8.825(br,1H),4.024~4.117(dd,2H),3.565~3.588(dd,2H),2.668~2.776(m,2H),1.456(s,9H)。
(2)3-硝基吡咯烷-1-羧酸叔丁基酯(1)的合成 在3L三口瓶中加UHP(345g,3.75mol),乙腈(800mL),在N2保護下,用干冰丙酮浴控溫在-10~0℃,滴加三氟乙酸酐TFAA(692g,3.3mol)的乙腈溶液(1.2L),體系澄清呈淡黃色,備用。在另一個10L反應釜中加入化合物2(300g,1.5mol),乙腈1.8L,Na2HPO4(1064g,7.49mol),N2保護,升溫至60℃。將UHP體系緩慢滴加至化合物2體系中,邊滴加邊反應,TLC監測反應完畢,加水降溫(6L),乙酸乙酯萃取(2L×2),有機相用飽和NaHCO3調pH值為7,再經飽和Na2S2O3溶液、飽和NaCl溶液洗滌,有機相減壓濃縮,粗品經柱層析(PE∶EA=5∶1)純化得白色固體193g,收率60%。1H NMR(CDCl3,400MHz):4.964~5.023(m,1H),4.019~4.062(m,1H),3.686~3.751(m,1H),3.521~3.569(m,1H),2.558~2.578(m,1H),2.282~2.330(m,1H),1.450(s,9H)。ESI-MS(m/z):161.0[M-56]+。
2 結果與討論
2.1 物料比n鹽酸羥胺∶n2對化合物(3)收率的影響
1-Boc-吡咯烷酮(2)和鹽酸羥胺經肟化反應制備化合物(3),按照1.2.2第一步反應條件,在其他條件不變的情況下,考察了反應物料比,即n鹽酸羥胺:n2對化合物(3)收率的影響,結果見表1。

表1 物料比對化合物(3)收率的影響Tab.1 Effect of mole ratio on the yield of compound 3
由表1可知,當物料比n鹽酸羥胺∶n2=1.0∶1時,產物收率為88.5%。提高鹽酸羥胺的用量,收率有所升高,當n鹽酸羥胺∶n2=1.1∶1時,收率可高達到98.5%,反應基本完全,繼續增大羥胺用量,結果變化不大。考慮到反應完全及試劑節約化,因而適宜的物料比為n鹽酸羥胺∶n2=1.1∶1。
2.2 反應溫度對化合物(3)收率的影響
反應溫度對羥肟化反應有較明顯的影響。按照1.2.2節第一步操作方法,固定n鹽酸羥胺∶n2=1.1∶1,及其他條件不變的前提下,考察反應溫度對化合物(3)收率的影響,結果見表2。

表2 反應溫度對化合物(3)收率的影響Tab.2 Effect of reaction temperature on the yield of compound 3
由表2可看出,當反應溫度為40℃時,收率為48.8%,溫度為60℃時收率較高,繼續升高溫度,收率反而有所下降。可能是因為,溫度升高反應速率加快,低溫時反應不完全,溫度過高又對產物有所破壞。因而適宜的反應溫度確定為60℃。
2.3 物料比n UHP∶n3對產物(1)收率的影響
第二步氧化反應中,UHP作為氧化劑,其用量對反應有重要影響,按照1.2.2節第二步操作方法,在其他條件固定不變的前提下,考察了物料比nUHP∶n3對產物(1)收率的影響,結果見表3。

表3 物料比n UHP∶n3對產物(1)收率的影響Tab.3 Effect of mole ratio on the yield of compound 1
由表3可知,UHP用量對反應有較明顯影響,氧化劑用量較低,反應不完全,隨著UHP用量增大,收率有明顯提高,可能是因為氧化劑體系UHP/TFAA相對不穩定,需加入過量的UHP以保證足夠量的活性氧化劑參與反應。由此單因素水平反應可看到,在nUHP∶n3=2.5∶1時,收率較好,繼續增大用量,作用不顯著。因此,選定nUHP∶n3=2.5∶1為適宜的物料比。
2.4 溶劑種類對產物(1)收率的影響
第二步氧化反應中,用到了較多試劑參與和調節反應,如有機酸和無機鹽,體系的溶解情況對反應有一定影響,因此,考察了溶劑種類對產物(1)收率的影響。按照1.2.2節第二步操作方法,在滴加反應溫度為60℃等其他條件固定不變的前提下,考察了溶劑種類對反應結果的影響,結果見表4。

表4 溶劑種類對產物(1)收率的影響Tab.4 Effect of solvent on the yield of compound 1
由表4可知,用乙腈作溶劑,結果相對較理想,用氯仿和1,2-二氯乙烷作溶劑,產物收率較低。可能是因為乙腈對有機物及無機鹽均有相對較好的溶解度,同時極性、揮發度以及可到達的溫度滿足反應的需求,所以,選擇乙腈作為此步的反應溶劑。
2.5 反應溫度對產物(1)收率的影響
第二步氧化反應中,邊滴加邊反應,反應活性較強,為放熱型反應,反應溫度影響產物收率。以乙腈為溶劑,其他條件按照1.2.2節第二步操作方法,在此條件下,考察了滴加時反應溫度對結果的影響,見表5。
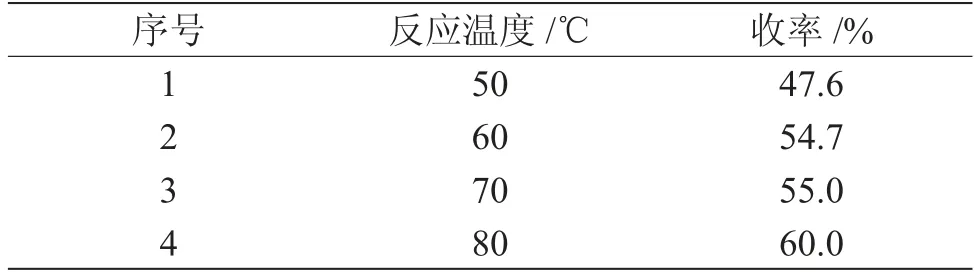
表5 反應溫度對產物(1)收率的影響Tab.5 Effect of reaction temperature on the yield of compound 1
由表5可知,隨著溫度的升高,產物收率升高,到接近乙腈沸點溫度80℃時,收率達60.0%。說明在穩定控制的情況下,升高反應溫度對反應有利,但溫度不宜再高,過高反應將不易控制。因此,選擇控制在80℃下滴加氧化劑體系進行反應。
3 結論
以1-Boc-吡咯烷酮(2)為原料,在NaHCO3做堿的條件下與鹽酸羥胺發生氨肟化反應,得1-Boc-3-吡咯烷酮肟(3),化合物(3)在三氟乙酸酐存在下,經過氧化脲(UHP)氧化,可得目標化合物3-硝基吡咯烷-1-羧酸叔丁基酯(1)。結構經1H NMR和LCMS表征確證。
優化了反應條件:第一步肟化反應中,物料比為n羥胺鹽酸鹽∶n1-Boc-3-吡咯烷酮=1.1∶1,反應溫度60℃;第二步氧化反應中,物料比nUHP∶n3=2.5∶1,溶劑用乙腈,反應溫度80℃。在優化條件下,氨肟化反應的最高收率達98.5%,氧化反應收率可達60%,總收率59.1%。此法合成途徑簡潔、條件溫和、產品質量好、總收率高。該方法為此類物質的合成提供了一種可參考的工藝。

