乳鐵蛋白基姜黃素納米載體顆粒的制備及其對大鼠抗疲勞能力的影響
賈前生,劉遠洋
(1.黑龍江八一農墾大學體育教研部,黑龍江大慶 163000;2.黑龍江八一農墾大學食品學院,黑龍江大慶 163000)
長期或高強度的運動、工作是導致機體出現“過度訓練綜合征”的重要成因,它不但使機體免疫力下降,還會引發食欲不振、精神萎靡、注意力不集中等疲勞癥狀[1?2]。疲勞的產生機理主要與機體氧化應激水平相關,研究表明過度訓練會誘發細胞凋亡并引起臟器運動性損傷,而高氧化應激水平會加速細胞凋亡的進程,因而對機體氧化應激水平的調控是延緩疲勞的重要途徑[3?5]。
多酚類天然提取物-姜黃素由于其安全性高、商業用途廣泛、具備多種藥用活性,使其成為了運動恢復與緩解疲勞類產品開發的重要研究對象[6?8]。研究證實姜黃素所具有的羥基活性基團能夠有效阻斷自由基的轉導通路、從而降低機體的氧化應激水平[9]。在此基礎上,通過過度訓練大鼠模型,研究發現姜黃素能夠減輕骨骼肌的氧化應激損傷降低疲勞性損傷[10]、抑制臟器細胞凋亡從而保護臟器[11]以及降低與自由基產生相關的生化指標水平,進而緩解運動性疲勞[12?13]。
盡管姜黃素在醫藥領域以及運動恢復產品中極具開發潛力,但姜黃素自身的疏水結構導致其水溶性極差,而人體攝入后會快速將其排除體外,姜黃素極易受到溫度、pH的影響并易發生降解,使其生物可利用度大大降低,因而尚未被視為有效的商業治療劑、營養補充劑[14?16]。為了克服姜黃素口服吸收的障礙,研究人員已嘗試使用遞送系統將姜黃素包埋[17],如納米顆粒載體技術。納米顆粒載體技術在當今的生物醫療領域已十分成熟,通過該技術不但可以保持姜黃素在存儲、運輸以及人體消化過程中結構的穩定性,還能使其更易進入小腸上皮細胞被人體所吸收,從而提高其在生物可利用度[18?19]。王瑋琛[20]建立了小鼠疲勞模型并發現以玉米蛋白-多糖為載體的姜黃素納米顆粒具有良好的生物利用率,并能夠修復由疲勞引起的氧化應激損傷。目前國內外大部分研究重點在于姜黃素單體的抗氧化以及體外作用機制的探究,姜黃素納米載體相關方面的研究局限于生物可利用度的提高,納米載體技術大多處于制備優化工藝階段;而對于姜黃素通過傳遞體系后在機體內相關生物學活性以及物質間協同作用的研究較少,對于姜黃素納米載體顆粒體內抗疲勞活性的研究也尚有較大拓展空間。
因而本實驗擬以乳鐵蛋白為載體建立姜黃素納米載體顆粒,通過體內消化吸收實驗以及運動性疲勞模型,以力竭運動時長、血乳酸、肌糖原、肝糖原以及體內相關抗氧化酶等參數對該納米載體顆粒的抗氧化性、抗疲勞活性進行綜合評判,以期為后續姜黃素納米載體顆粒在抗疲勞營養補充劑的相關研究中提供理論依據。
1 材料與方法
1.1 材料與儀器
UV-2600 紫外可見分光光度計 日本島津公司;1260 型高效液相色譜 安捷倫科技(中國)有限公司;FC酶標儀 美國賽默飛世爾科技公司;MYP11-2A恒溫磁力攪拌器 德國IKA公司;H1850 臺式高速離心機 湖南湘儀實驗室儀器開發有限公司;Zetasizer Nano ZS粒度分析儀 英國馬爾文儀器;TCS SP2 激光共聚焦顯微鏡(Confocal Laser Scanning Microscopy,CLSM)德國Leica公司;Morris恒溫水池 北京智鼠多寶生物科技有限責任公司。
1.2 實驗方法
1.2.1 姜黃素納米載體的制備 乳鐵蛋白-姜黃素納米載體顆粒的制備,參考江萍[21]的方法稍作修改,配制質量濃度為1 mg/mL的姜黃素無水乙醇溶液并于超聲浴(25 ℃,80 W)中超聲2 h使姜黃素充分溶解;配制質量濃度為1 mg/mL的乳鐵蛋白Tris-HCl緩沖液(pH=7.5),將一體積姜黃素溶液快速導入五體積乳鐵蛋白溶液中,于4 ℃靜置12 h后用0.22 μm的PES水系濾膜除去未被包埋的姜黃素,將濾液凍干后得到天然乳鐵蛋白-姜黃素納米載體顆粒。
1.2.2 姜黃素的檢測方法 姜黃素的HPLC檢測參考張聰聰[22]的方法稍加修改,進樣體積10 μL,流動相A為甲醇溶液,流動相B為5%的乙酸水溶液,流動相比例為85:15,等度洗脫流速0.5 mL/min;柱溫箱溫度30 ℃,檢測波長425 nm,洗脫時間15 min。標準品溶液濃度分別為10、20、50、100、200 ng/mL,以將大黃素為內標,以姜黃素峰面積與內標大黃素峰面積之比為Y軸,以姜黃素濃度為X軸作圖。
1.2.3 負載率和包封率的測定 負載率[21]:稱取一定量納米載體顆粒溶解于甲醇中,磁力攪拌2 h后,在4000 r/min條件下離心分離30 min取上層清液;包封率:稱取一定量納米載體顆粒溶解于蒸餾水中,在8000 r/min條件下離心30 min,取上層清液進行測定(方法如1.2.2),姜黃素的負載率和包封率按如下公式計算:
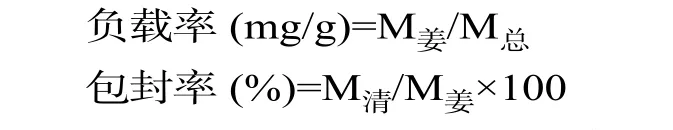
式中:M清為上清液中姜黃素的總質量,M姜為載體顆粒中姜黃素的總質量,M總為納米載體顆粒的總質量。
1.2.4 姜黃素納米載體的結構表征
1.2.4.1 粒徑分析 分別將天然乳鐵蛋白以及天然乳鐵蛋白-姜黃素納米載體顆粒復溶于純凈水溶液中,配制成蛋白濃度約為0.2 mg/mL的溶液,持續攪拌30 min確保充分混勻后,在室溫下使用粒度分析儀進行分析,系統平衡時間120 s,每組樣品掃描次數12 次。
1.2.4.2 激光共聚焦 根據Wang[20]的方法稍加修改,用異丙醇配置濃度為0.1%(m/v)的尼羅藍染液。將乳鐵蛋白-姜黃素納米載體顆粒復溶液稀釋后,取10 mL樣品溶液于試管中,用移液槍準確加入400 μL尼羅藍后充分振蕩混勻,并用錫紙包裹避光染色30 min。染色結束后取1 μL溶液于載玻片上,在20 倍物鏡視野下手動調焦并進行成像并觀測樣品顯微結構。
構建快篩快檢研發應用體系,提高市場打假效能。廣東省所為落實監管新要求,不斷在快篩快檢技術上發力,建立非法添加數據庫410種、產品數據庫360種,非法添加快篩方法30多種,申請發明專利45項,已被授權31項。其中25項實現了產品化,涵蓋藥品、保健食品、化妝品和食品領域,基本覆蓋市場上常見非法添加藥物。2012年,西布曲明快篩方法獲省科學技術三等獎。2013年,《食品藥品中非法添加化學成分的監督檢驗系統技術策略及其應用》獲省科學技術二等獎。2014年,全國藥檢系統中首個非法添加快檢技術系統研究平臺啟動。同時,該所通過舉辦培訓班、開展競賽等形式,推廣了快篩快檢技術在基層一線的應用。
1.2.5 動物實驗
1.2.5.1 姜黃素納米載體顆粒的體內吸收 選取健康SD種大鼠20 只隨機分為2 組,自由采食飲水,給予樣品前12 h禁食不禁水。分別給予姜黃素含量為100 mg/kg·bw·d的姜黃素納米載體顆粒和姜黃素溶液,并于灌胃后第0、15、30、45、60、90、120、180、240、300 min尾部采血0.3 mL,置入含有肝素的抗凝管中。
在血漿姜黃素的測定時,取100 μL血漿樣本加入10 μL大黃素(20 μg/mL),渦旋3 min后加入0.25 mL乙酸乙酯并劇烈振蕩搖勻,在4000 r/min條件下離心5 min,取上層有機相用以姜黃素的測定,測定方法見1.2.2。
1.2.5.2 運動性疲勞實驗 動物實驗模型參考胡戈[23]稍加修改,選取健康大鼠60 只隨機分為5 組,即對照組(Blank)、疲勞模型組(Con)、疲勞低劑量組Low(20 mg/kg·bw·d)、疲勞中劑量組Mid(60 mg/kg·bw·d)和疲勞高劑量組High(100 mg/kg·bw·d)。除對照組外,四組疲勞組于第1 周無負重游泳至力竭,于第2 周鼠尾負重約體重5%、第3、4 周負重10%,水溫30 ℃,每周休息1 d并記錄體重。總實驗周期持續28 d,期間采用灌胃法給予樣品,對照組及模型組提供0.9%生理鹽水,其余每組按劑量組給予乳鐵蛋白-姜黃素納米載體顆粒3 mL/d,當大鼠在水中沉沒持續10 s后未上浮即為力竭,記錄時間計為力竭時長(min)。
1.2.6 肝臟、肌肉以及血清樣本的采集 分別于最后一次大鼠游泳前、游泳后0、30、60、90 min鼠尾采血,并置于抗凝管中,1500 r/min條件下離心5 min,后用以測定血乳酸的含量。鼠尾采血結束后立即處死大鼠,眼球取血,并將采集到的新鮮血液于4 ℃靜置1 h后,在1500 r/min條件下分離15 min取上層血清,分別用以測定血漿姜黃素水平、血乳酸(LA)、血尿素氮(BUN)含量。解剖后,摘取肱四頭肌及肝臟組織,用0.9%NaCl清理后制成10%組織勻漿,分別用以測定肌糖原(MG)、肝糖原(LG)、超氧化物歧化酶(SOD)、谷胱甘肽過氧化物酶(GSH-Px)和丙二醛(MDA)含量嚴格按照試劑盒操作說明測定,剩余血清保存于?70 ℃超低溫冰箱中備用。
1.3 數據處理
應用SPSS 19.0 軟件對數據進行。實驗數據以均值±標準偏差(Mean±SD)表示,多樣本間比較采用T-Test,P<0.05 為差異顯著,P<0.01 為差異極顯著。采用Origin 2017 軟件進行圖表處理及圖譜分析處理。
2 結果與分析
2.1 姜黃素的HPLC分析及結構表征
2.1.1 姜黃素的HPLC分析 血漿空白對照組、姜黃素標準品及血漿樣本液相色譜圖見圖1,線性回歸方程為Y=0.94X+234.82,R2=0.9963。
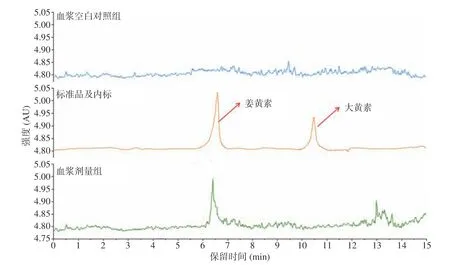
圖1 姜黃素標品及血漿樣本Fig.1 Curcumin standard and plasma samples
2.1.2 姜黃素納米載體顆粒結構表征 實驗通過HPLC法測定姜黃素納米載體顆粒的負載率為(152.03±2.43)mg/g,包封率約為63.57%±0.74%;乳鐵蛋白和姜黃素納米載體顆粒的水溶液經粒度分析儀測定所得粒徑分布圖如圖2,可以發現乳鐵蛋白(圖2A)和姜黃素納米載體顆粒(圖2B)的粒徑分布均較為均一,乳鐵蛋白粒徑(163.4 nm)明顯低于姜黃素納米載體顆粒(593.8 nm)。Chen等[24]在制備大豆分離蛋白姜黃素納米載體時發現,姜黃素負載量較高的納米顆粒會形成較大粒徑分布的顆粒體,與本文結果相符。這可能時由于乳鐵蛋白載體顆粒負載了姜黃素后,會通過姜黃素顆粒間的橋連作用,形成了更大粒徑的聚集體并能夠形成壓穩定狀態的分散系。此外,通過CLSM(圖2C)實驗結果也可以發現,姜黃素納米載體顆粒能夠以較為均一穩定的結構在溶液中存在。
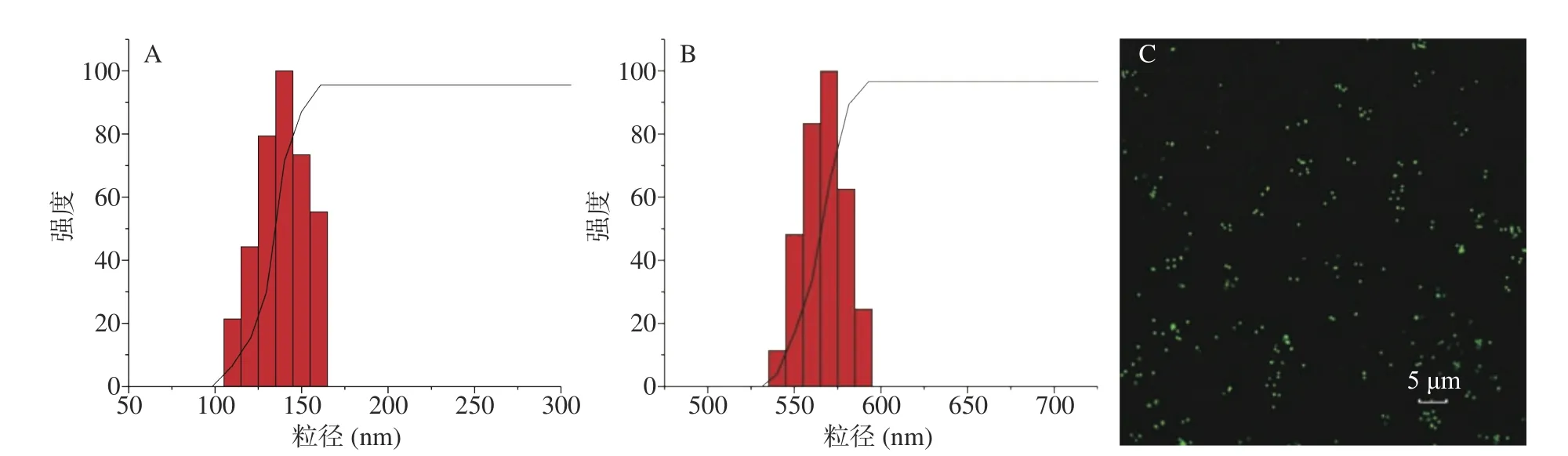
圖2 粒徑分布及CLSMFig.2 Particle size distribution and CLSM
2.1.3 姜黃素納米載體顆粒的體內吸收 實驗通過HPLC對大鼠6 h內姜黃素的血藥濃度進行了測定,并繪制了血藥濃度與時間的姜黃素動態變化曲線如圖3。從圖中可以發現,姜黃素能夠迅速提升血藥濃度并在約30 min后達到峰值,隨后血藥濃度迅速降低并于60 min后血藥濃度趨于平緩,這可能是由于姜黃素水溶性極差,從而影響其直接服用[14],此外由于首過效應致使姜黃素在消化道滅活、代謝,進入體循環的藥量減少[25];而姜黃素納米顆粒則需要約50 min使血藥濃度達到峰值并能夠維持一段時間,隨后在4 h內血藥濃度緩慢回落,這可能是由于姜黃素納米載體顆粒能極大提高姜黃素在溶液體系中的濃度,因而血藥濃度峰值較姜黃素水溶液高,另一方面納米載體顆粒對姜黃素起到了保護作用,降低了首過效應,納米載體的緩釋效果也能夠使姜黃素在體內得到更充分的吸收、代謝[26]。
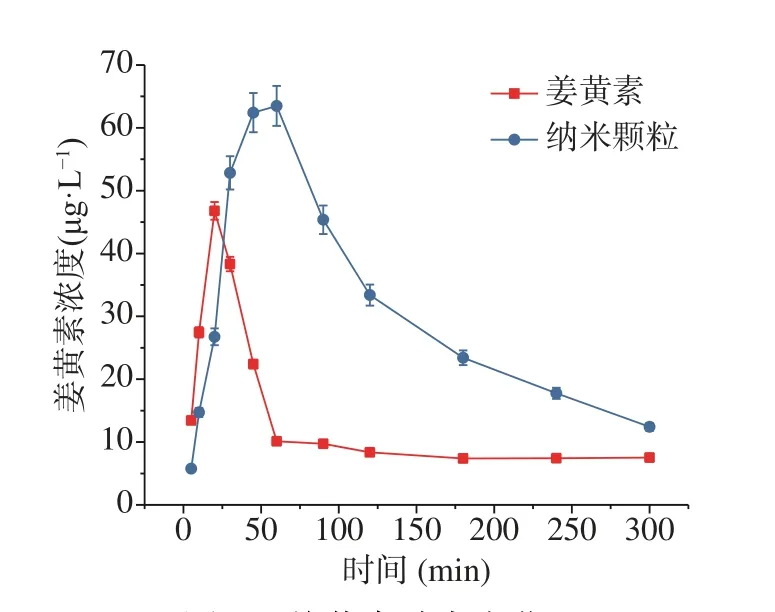
圖3 姜黃素動態變化Fig.3 Dynamic changes of Curcumin
2.2 動物實驗
2.2.1 運動型疲勞實驗 通過力竭游泳運動的時長能夠較為客觀的評判受試樣品的抗疲勞功效。在造模后各組大鼠在個體質量上并未出現顯著差異(P>0.05),且無死亡樣本,但模型組終末體重略低于劑量組。根據表1 數據結果顯示,模型組以及三組劑量組大鼠的力竭時長與對照組相比極顯著降低(P<0.01),表明運動性疲勞造模成功。與模型組相比,低劑量組未能顯著提高力竭運動時長(P>0.05),中、高劑量組能夠顯著提高力竭運動時長(P<0.05),表明中、高劑量組的姜黃素納米載體顆粒具有良好的抗運動性疲勞效果,其中高劑量組效果更佳,時長約提高了55.07%。

表1 大鼠體質量與力竭運動時長Table 1 Body weight and duration of exhaustive exercise in rats
2.2.2 乳酸變化曲線 通過對大鼠力竭游泳前后血乳酸含量變化的監測,可以判斷大鼠的疲勞程度以及恢復狀況[27],實驗結果如圖4,數據統計結果顯示力竭游泳前運動性疲勞模型下大鼠的血乳酸含量極顯著高于對照組(P<0.01),且模型組與劑量組組間差異不顯著(P>0.05)。游后0 min,模型組、Low、Mid、High四組大鼠血乳酸分別上升了17.49%、13.32%、8.30%、7.69%;游后30 min,四組大鼠乳酸分別下降了1.35%、1.77%、2.28%、4.45%;60 min后,四組大鼠乳酸分別下降了2.76%、3.56%、4.89%、8.67%;90 min后,四組大鼠乳酸分別下降了3.89%、5.40%、7.14%、13.06%。可以發現,大鼠在給予高劑量后,其體內的血乳酸含量較其他組別升高最少,并且在90 min內血乳酸相對含量下降最快,表明姜黃素納米顆粒能具有減少乳酸堆積的功效,在運動性疲勞模型下減少乳酸堆積能力與劑量正相關。
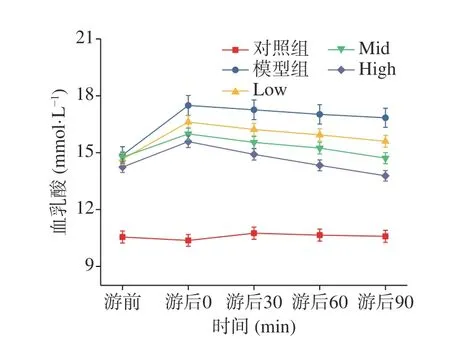
圖4 血乳酸動態變化Fig.4 Dynamic changes of blood lactic acid
2.3 肌糖原、肝糖原與血尿素氮
機體在運動的過程中會首先消耗肌糖原,為了維持運動強度所需的能量供給會逐漸消耗肝糖原。因而機體肌糖原與肝糖原的水平降低與體力耗盡具有一定相關性,實驗結果見表2。在運動性疲勞模型下大鼠的肝糖原均極顯著低于對照組(P<0.01),與模型組相比經喂飼納米顆粒的劑量組大鼠肝糖原均有極顯著提升(P<0.01);與對照組相比,模型組與低劑量組大鼠的肌糖原含量均顯著降低(P<0.01,P<0.05),而中、高劑量組大鼠的肌糖原差異不顯著(P>0.05),與模型組相比僅高劑量組差異顯著(P<0.05)且含量高于模型組;血尿素氮含量的統計結果顯示三組劑量組均能夠極顯著降低血尿素氮含量(P<0.01)。表明姜黃素納米載體顆粒能夠提高肌糖原與肝糖原的儲備,并能夠緩減體內蛋白質的消耗降低血尿素氮的含量。
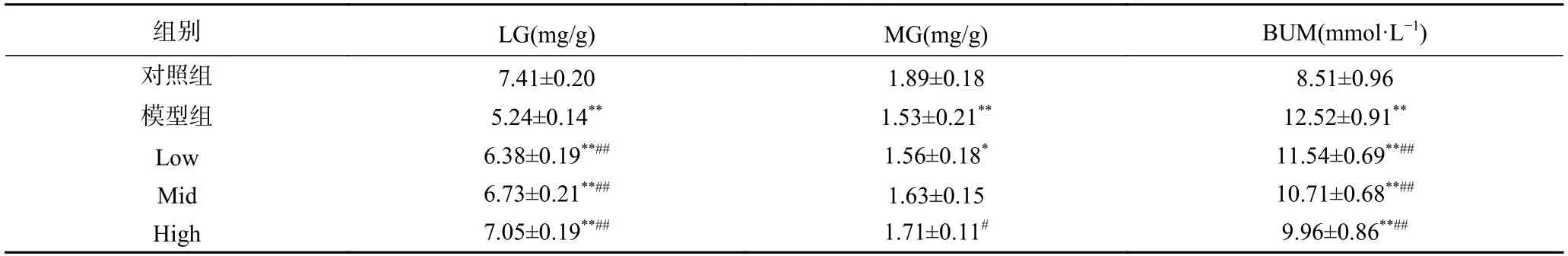
表2 肝糖原、肌糖原與血尿素氮Table 2 Liver glycogen,muscle glycogen and blood urea nitrogen
2.4 體內抗氧化活性分析
疲勞癥狀的出現通常與機體自由基水平升高有著密切聯系,通過對血液和組織中抗氧化物酶活性的檢測能夠較為清晰的反應機體自由基蓄積水平。本實驗通過SOD、GSH活性以及MDA含量解析姜黃素納米載體顆粒的抗氧化活性,數據統計結果見表3。
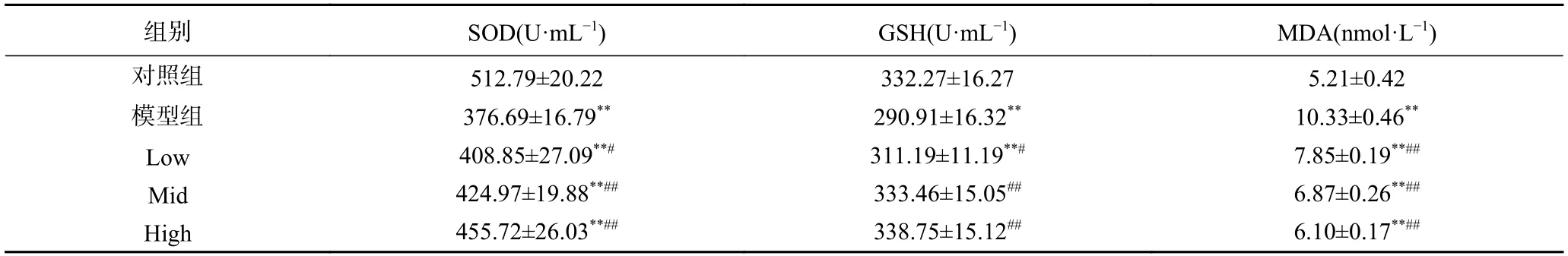
表3 姜黃素納米顆粒載體對大鼠生化指標的影響Table 3 Effects of curcumin nanoparticles on biochemical indexes in rats
SOD:經造模的四組疲勞組的SOD酶活性極顯著低于對照組(P<0.01),與模型組相比三組劑量組均能夠顯著(極顯著)提高SOD酶的活性(P<0.05、P<0.01),低、中、高劑量組分別提高了7.72%、11.96%和20.06%。
GSH:模型組的GSH酶活性極顯著低于對照組(P<0.01),與對照組相比,低劑量組GSH酶活性極顯著降低(P<0.01),而中、高劑量組能夠使GSH水平恢復至對照組水平(P>0.05);與模型組相比,低劑量組能夠顯著提高GSH酶活性(P<0.05),而中、高劑量組能夠極顯著提高GSH活性(P<0.01)。
MDA:運動性疲勞模型下的四組大鼠血清中丙二醛的含量極顯著高于對照組(P<0.01),經喂飼姜黃素納米載體顆粒后,三組劑量組均能使機體內丙二醛水平極顯著低于模型組(P<0.01),其中高劑量組效果最佳,下降了約30.66%。
3 討論
姜黃素的親脂特性致使其在人體消化系統中表現出較差的吸附性,姜黃素結構中的羥基結構極易發生氧化反應而變性[28],姜黃素得不到有效的吸收,因而生物利用率極低,而通過應用納米載體顆粒傳遞體系使該問題得到顯著改善。通過包封率和負載率的測定,可以發現姜黃素在溶液體系中的溶解性大大提高;粒徑與CLSM的實驗數據較好的說明,納米載體顆粒在溶液體系中能夠以穩定、均一的狀態分散;通過比對納米載體顆粒與姜黃素單體溶液的大鼠體內吸收實驗發現,納米載體顆粒溶液首過效應大大降低,并能夠在人體內存留更長時間,起到了緩釋作用使人體吸收更充分[29]。隨后通過力竭游泳建立了運動性疲勞大鼠模型,通過4 周力竭游泳造模后大鼠的終末體質量均有所減少,而在分別飼喂低、中、高劑量組的納米載體顆粒后發現,與模型組相比三組劑量組均能夠不同程度提高耐力運動時長,其中高劑量組提升效果最為明顯,表明其抗疲勞效果與劑量相關;通過對力竭運動后大鼠血乳酸動態變化的監測,可以發現,納米載體顆粒能夠有效加速血乳酸代謝水平,一定程度上延緩了由于糖原消耗過導致血乳酸堆積而誘發的肌肉收縮能力下降[30],表現為增強了大鼠耐力運動時長,此外,肌糖原與肝糖原儲備量的提升也能夠一定程度延緩血乳酸的堆積[31],同時降低了長期運動誘使的蛋白質代謝所產生的血尿素氮含量[32];機體疲勞的產生與氧化應激水平密不可分,在長期或高強度運動的情況下,機體內活性氧自由基的產生會遠超越其清除速率致使細胞受到氧化損傷[33],實驗通過對SOD、GSH-Px酶活性的檢測,發現姜黃素納米載體顆粒能夠加速活性氧自由基的清除速率從而保護組織和器官免受氧化損傷,并最終表現為過氧化代謝產物MDA含量的顯著降低,其抗氧化活性越高其耐力運動時長越長,表明乳鐵蛋白-姜黃素納米載體顆粒具有一定的抗疲勞功效。
4 結論
本實驗制備了一種具有較好包封率和負載率的乳鐵蛋白姜黃素納米載體顆粒,該顆粒在水溶液體系中具有良好的穩定性,較姜黃素單體溶液極大的提升了單位體積內姜黃素的溶解度,并通過大鼠體內吸收實驗充分佐證了其在機體內也具備良好的緩釋作用以及保護作用,一定程度上降低了首過效應并延長了姜黃素在機體內的存留時間,從而間接提升了其生物可利用率;通過運動型疲勞模型可以發現,納米載體顆粒能夠有效提升抗氧化物酶活性、提高機體糖原儲備、加速血乳酸代謝從而降低由長期高或強度運動引發的氧化代謝產物堆積、降低機體氧化應激水平、減輕氧化損傷,并最終表現為大鼠力竭耐力運動時長的提升,表明其具有一定的抗疲勞功效。
綜上,乳鐵蛋白姜黃素納米載體顆粒傳遞體系能夠有效提升姜黃素的生物可利用率,從而保障了其充分發揮抗疲勞活性,以期為姜黃素類相關抗疲勞制品提供理論參考。

