鉬靶、超聲聯合應用在微鈣化乳腺病變定性診斷中的效果研究
蘇文,劉燦
(1.濱州醫學院,山東 煙臺 264003;2.濱州醫學院煙臺附屬醫院 超聲科,山東 煙臺 264100)
0 引言
不管是良性乳腺疾病抑或惡性乳腺疾病,二者都可能出現微鈣化現象,而隨著臨床診斷技術的不斷提升,發現乳腺組織出現的微鈣化分布情況、形態以及密度等都跟乳腺腫瘤疾病的良惡性質有著十分密切的關系。醫學上將乳腺的微鈣化分為了典型良性、中間性以及惡性三大類,其中典型良性微鈣化主要包括了透明鈣化、血管狀鈣化以及爆米花樣鈣化等;中間性微鈣化則特指形態不規則或者鈣化模糊、邊界模糊等的鈣化灶;而惡性鈣化一般為直徑小于0.5 mm、形態多樣的鈣化灶,比如臨床上常見的泥沙樣鈣化、分支樣鈣化以及短棒樣鈣化等。研究乳腺鈣化灶的整體情況具有十分重要的診斷價值與意義,隨著臨床診斷技術的不斷改進與提示,可為患者實施的臨床診斷操作已從過去的單一技術慢慢過渡到了多種聯合性技術[1-2]。分析我院2018年12月至2020年12月間收治的150例乳腺微鈣化病變患者的病理及影像學資料,旨在探究鉬靶、超聲聯合應用在微鈣化乳腺病變定性診斷中的應用效果,現將研究結果整理如下。
1 資料與方法
1.1 一般資料。分析我院2018年12月至2020年12月收治的150例乳腺微鈣化病變患者的病理及影像學資料,隨機將患者分成三組,研究I組(n=41):術前經乳腺多普勒超聲檢查為乳腺微鈣化病變但其乳腺鉬靶未見明顯微鈣化;研究II組(n=48):術前經乳腺鉬靶檢查為乳腺微鈣化病變但多普勒超聲檢查無明顯微鈣化病變;研究III組(n=61):術前經乳腺鉬靶聯合超聲檢查,均發現乳腺有鈣化病變。研究I組年齡為27~60歲,平均(45.67±11.34)歲,BMI為22~27 kg/m2,平均(23.45±2.34)kg/m2,左側病變患者12例(29.27%),右側病變患者27例(65.85%),雙側病變患者2例(4.88%);研究II組年齡為28~62歲,平均(46.58±10.98)歲,BMI為22~26 kg/m2,平均(23.11±2.78)kg/m2,左側病變患者13例(27.08%),右側病變患者33例(68.75%),雙側病變患者2例(4.17%);研究III組年齡為27~61歲,平均(45.11±13.28)歲,BMI為23~28 kg/m2,平均(23.54±3.31)kg/m2,左側病變患者17例(27.87%),右側病變患者42例(68.85%),雙側病變患者2例(3.28%)。三組間一般資料等對比無明顯統計學差異,P>0.05,可進行對比。納入標準:①所有患者在手術治療前未接受任何輔助性的抗腫瘤治療,如化療、放療或者內分泌治療等;②所有患者具有完整的臨床病理資料,資料中主要包括患者年齡、性別、診療記錄、腫瘤詳情、病理類型以及淋巴結的受累情況等;③患者無其他重大的免疫系疾病。排除標準:①乳腺超聲圖像資料、診斷資料等不完整者,或不符合臨床診斷質控要求者;②存在既往其他腫瘤病史或乳腺癌腫瘤病史;③患者已接受過手術治療,本次為復發情況;④伴有其他嚴重基礎性疾病,如存在心臟、肺、及肝腎方面重大疾病;⑤手術治療前,患者已接受過中醫治療、新輔助性化療及生物靶向治療等。
1.2 方法。①應用美制全數學化乳腺鉬銠雙靶X線機,配備二維導絲定位裝置及活檢系統,對所有患者采取常規性攝雙乳軸位及內外側斜位,對常規體位下發現的可疑微鈣化,進行局部放大及局部加壓攝影處理,采用全自動的曝光條件;②采用日制超聲診斷儀,將探頭頻率設置為7.5 Mhz~12 Mhz。指導患者采取仰臥位,將雙側乳腺進行充分的暴露,利用探頭在乳房的各個象限中做多切面、多方位的系統化掃查。
1.3 觀察指標。由我院影像科3名臨床診斷經驗豐富的醫師在不清楚患者病理結果的前提下對超聲成片進行檢閱,根據診斷結果判斷患者乳腺病變的良惡性情況。對兩種診斷方法進行聯合分析,并對病例重新進行分組。
1.4 統計學分析。采用SPSS 21.0分析,計量資料以(±s)表示,經t檢驗,計數資料經χ2檢驗,以(%)表示,差異有統計學意義為P<0.05。
2 結果
研究結果顯示,各組乳腺微鈣化病變患者病理結果檢測體現出明顯的差異性。在超聲數據中可以看出,在纖維腺瘤的檢測項目中,超聲檢測與病理結果吻合度較高,準確率可以高達90.91%;從鉬靶數據中可與看出,在導管原位癌的檢測項目中,鉬靶檢測與病理結果吻合度較高,準確率可以高達90.00%;從超聲+鉬靶數據中可與看出,在浸潤性導管癌的檢測項目中,超聲+鉬靶檢測與病理結果吻合度較高,準確率可以高達91.67%。具體結果分析如表1。
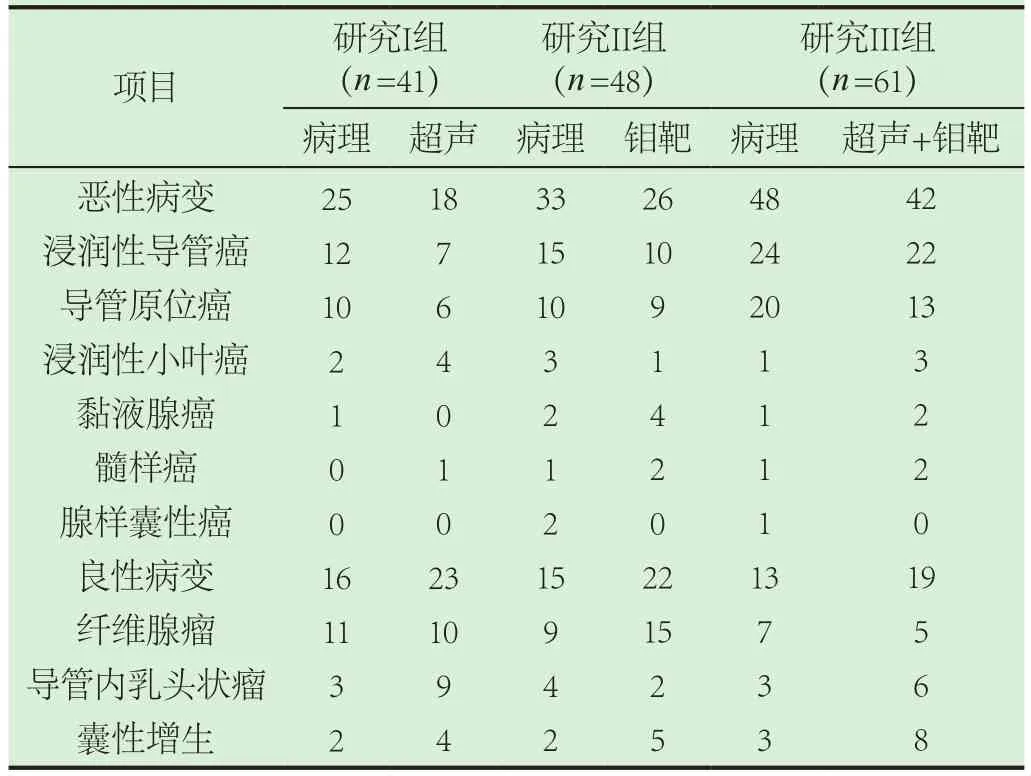
表1 各組乳腺微鈣化病變患者病理結果分析
多普勒超聲、鉬靶及二者聯合檢測乳腺微鈣化病變患者診斷效能。研究結果顯示多普勒超聲鉬靶及二者聯合檢測乳腺微鈣化病變的診斷效能體現明顯的差異性,從數據中可以看出多普勒超聲的準確率最低,鉬靶檢測次之,二者聯合則可以明顯提高乳腺微鈣化病變的診斷效能,數據比較,P=0.019,差異具有統計學意義;而三者在其靈敏度及特異度數據方面,差異性小,P值分別為0.112及0.134,差異不具有統計學意義;上述的結果向我們解釋道多普勒超聲與鉬靶聯合檢測可以明顯提升乳腺癌的檢出率,為下文的研究提供基礎,具體結果分析如表2所示。
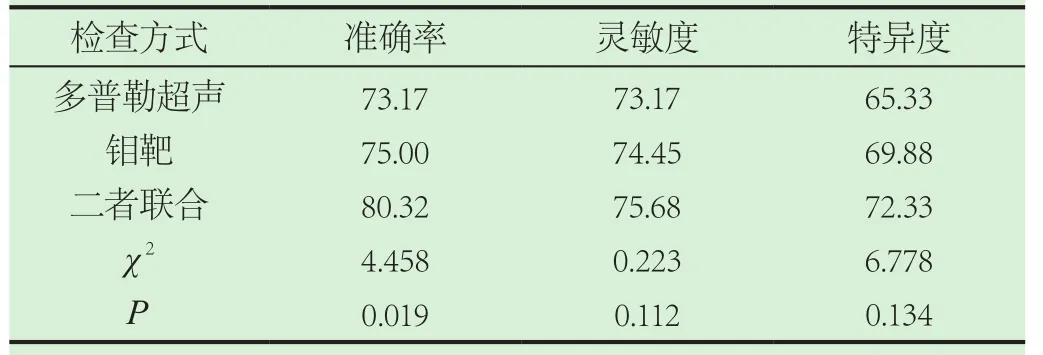
表2 多普勒超聲、鉬靶及二者聯合檢測乳腺微鈣化病變診斷效能分析
3 討論
目前,關于女性乳腺微鈣化的形成機制尚且不夠清楚,可以確定的是乳腺微鈣化現象與其細胞出現的變性問題、壞死問題以及細胞異常代謝等都具有一定的關聯。臨床治療發現,不管良性的乳腺疾病還是惡性的乳腺疾病,都可能存在微鈣化病灶,尤其是在女性乳腺癌癥中,微鈣化病灶更為明顯。相應醫學研究數據顯示,大約有13%~45%左右的乳腺微鈣化灶的最終活檢結果都為惡性病變,同時也有研究數據顯示在所有的微鈣化乳腺病灶中,就有大約50%左右的病例為惡性病變[3-4]。
在乳腺病變中,絕大多數的微鈣化都能夠在鉬靶診斷中顯示出來,但是在實際的臨床診斷中,也有部分病例經鉬靶診斷后無法顯示出微鈣化,這種情況一般多發于致密型的腺體中,且微鈣化病灶多位于患者的腫塊組織中,如此一來就容易出現漏診問題。盡管如此,鉬靶診斷仍舊是乳腺疾病臨床診斷中的主要方法之一,它主要是可以對患者出現的微鈣化灶以及結節影進行臨床分析,進而可對患者的病變性質進行判斷,而微鈣化病灶的分布情況、形態以及單位面積等都是鉬靶診斷病變性質中的重要指標;超聲在乳腺病變微鈣化灶的臨床診斷中的應用范圍也較為廣泛,利用超聲診斷技術可以對微鈣化灶的特點進行觀察,與鉬靶診斷技術不同的是,超聲診斷技術是通過對病變的邊界、形態、內部回聲等超聲圖像進行分析來判斷病變的良惡性,這樣就使得超聲診斷技術存在有一定的局限性,因為如果患者乳腺的局部超聲圖像并沒有出現明顯的改變,那么微鈣化灶的檢出率將無法得到提高,容易出現漏診問題,不利于臨床治療的準確性與有效性,不但會延誤疾病的治療與干預,還有可能誘發醫患之間的矛盾。在本此研究中,經對比,鉬靶、超聲診斷的準確率低于鉬靶-聯合超聲臨床診斷結果[5-6]。這提示鉬靶診斷與超聲診斷結合后,將顯著提高乳腺微鈣化病變的準確性,可降低漏診問題的概率,更有利于臨床上對乳腺病變進行判斷。
綜上所述,針對女性群體出現的微鈣化乳腺病變問題,鉬靶聯合超聲臨床診斷顯然優于鉬靶或者超聲等任何一種單一的臨床診斷技術,可顯著提高疾病在臨床診斷中的準確性,從而將在一定程度提高臨床治療的準確性,以便醫生更好為患者制定臨床治療方案。

