不同凡納濱對蝦養(yǎng)殖群體的微衛(wèi)星遺傳多樣性分析
唐芳 溫貝妮 劉紅


摘要:【目的】明確不同凡納濱對蝦(Litopenaeus vannamei)養(yǎng)殖群體間的遺傳信息豐富度和遺傳分化程度,為構(gòu)建適應(yīng)上海獨特氣候?qū)ξr品種繁育計劃中的交配系譜分析提供參考依據(jù)。【方法】選用13對微衛(wèi)星引物對來自厄瓜多爾恒興對蝦養(yǎng)殖公司2個養(yǎng)殖場(Pesquera和San Alfonso)共9個凡納濱對蝦養(yǎng)殖群體進行遺傳多樣性分析,探究不同群體間的遺傳信息豐富度和遺傳分化程度。【結(jié)果】13個微衛(wèi)星位點在9個凡納濱對蝦養(yǎng)殖群體中檢測到的等位基因數(shù)(Na)為2~6個,共有37個等位基因,多態(tài)信息含量(PIC)為0.1292~0.6799,平均為0.3326。在13個微衛(wèi)星位點中,僅有1個微衛(wèi)星位點(TUMXLV9.116)呈高度多態(tài)性,有4個微衛(wèi)星位點(TUMXLV10.147、TUMXLV5.45c、TUMXLV10.191c和TUMXLV10.96)呈低度多態(tài)性,其余8個微衛(wèi)星位點呈中度多態(tài)性。9個凡納濱對蝦養(yǎng)殖群體的觀測雜合度(Ho)為0.2225~0.3662,平均為0.2915;期望雜合度(He)為0.3317~0.4539,平均為0.3974;Hardy-Weinberg平衡指數(shù)(D)為0.0214~0.4214,其中San Alfonso P23群體和Pesquera P23群體的D相對更接近于0,其基因型分布接近于Hardy-Weinberg平衡狀態(tài)。9個凡納濱對蝦養(yǎng)殖群體的Fst平均值為0.1259,說明有12.59%的遺傳分化來源于群體間,而87.41%的遺傳分化來自群體內(nèi)部;群體間的平均基因流(Nm)為1.7356,表明遺傳漂變未能主導(dǎo)種群遺傳結(jié)構(gòu)的變化。在9個凡納濱對蝦養(yǎng)殖群體間,以Pesquera 29群體與Pesquera 15群體的遺傳距離最大(0.2426),San Alfonso 23群體與Pesquera 23群體的遺傳距離最小(0.0215);基于遺傳距離的UPGMA聚類分析結(jié)果表明,9個凡納濱對蝦養(yǎng)殖群體可分為兩大類,其中Pesquera 29群體和San Alfonso 12群體獨立聚為一類。【結(jié)論】在9個凡納濱對蝦養(yǎng)殖群體中存在觀測等位基因丟失現(xiàn)象,且遺傳多樣性較低,群體間分化程度為中等水平。因此,可通過引進不同地區(qū)擁有不同遺傳背景且親緣關(guān)系較遠(yuǎn)的群體作為親本,以豐富子代群體的遺傳多樣性。
關(guān)鍵詞: 凡納濱對蝦;養(yǎng)殖群體;微衛(wèi)星分子標(biāo)記;遺傳多樣性;遺傳分化
中圖分類號: S917.4? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 文獻(xiàn)標(biāo)志碼: A 文章編號:2095-1191(2021)04-1108-08
Microsatellite genetic diversity in different Litopenaeus
vannamei breeding populations
TANG Fang, WEN Bei-ni, LIU Hong*
(College of Fisheries and Life Science, Shanghai Ocean University/Key Laboratory of Aquatic Genetic Resources Exploration and Utilization of Ministry of Education, Shanghai? 201306, China)
Abstract:【Objective】To provide reference for mating and pedigree analysis in the breeding plan that the species in this research group could adapt to Shanghais unique climate, genetic information abundance and the degree of genetic differentiation among different Litopenaeus vannamei breeding populations were clarified. 【Method】Thirteen pairs of microsatellite primers were used to analyze the genetic diversity of nine L. vannamei breeding populations,which came from two farms(Pesquera and San Alfonso) of the L. vannamei breeding company in Ecuador. It could also explore the richness of genetic information and differentiation among different populations. 【Result】The number of alleles(Na) detected among nine L. vannamei breeding populations by 13 microsatellite loci ranged from 2 to 6, there were 37 alleles. Polymorphism information content index(PIC) was between 0.1292 and 0.6799, and the average PIC was 0.3326. Among the 13 microsatellite loci,only 1 microsatellite loci(TUMXLV9.116) had highly polymorphic,another 4 microsatellite loci(TUMXLV10.147, TUMXLV5.45c, TUMXLV10.191c and TUMXLV10.96) showed low polymorphism,and the remaining 8 microsatellite loci were moderately polymorphism. Otherwise, the observed heterozygosity(Ho) of 9 populations ranged from 0.2225 to 0.3662, and the average Ho was 0.2915. Expected heterozygosity(He)ranged from 0.3317 to 0.4539, and the average He was 0.3974. Hardy-Weinberg balance index(D) was ranging from 0.0214 to 0.4214. Among which the D of the San Alfonso P23 population and the Pesquera P23 population were relatively closer to 0, and their geno-type distribution was close to the Hardy-Weinberg balance state. The numerical valueof mean differentiation index(Fst) was 0.1259, indicating that there was 12.59% of genetic differentiation took place between the populations, and 87.41% of genetic differentiation occurred within the populations. Besides, the mean gene flow(Nm) between populations was 1.7356, indicating that genetic drift had not been able to dominate the change of population genetic structure. Among the 9 L. vannamei breeding populations, the genetic distance between Pesquera 29 and Pesquera 15 was the largest (0.2426), and the genetic distance between San Alfonso 23 and Pesquera 23 was the smallest(0.0215). According to the UPGMA clustering based on genetic distance, the 9 L. vannamei populations could be divided into two major groups, among which the Pesquera 29 population and the San Alfonso 12 population were grouped independently into one group. 【Conclusion】In the 9 breeding populations, lost observed allelic genes occurs, and they have low genetic diversity and mode-rate degree of differentiation among populations. It is possible to enrich the diversity of off spring populations by introdu-cing populations from different regions with different genetic backgrounds and long genetic distance as parents.
Key words: Litopenaeus vannamei; breeding populations; microsatellite molecular marker; genetic diversity; genetic differentiation
Foundation item: Shanghai Science and Technology Promoting Agriculture Project(2019-02-08-00-F01111)
0 引言
【研究意義】凡納濱對蝦(Litopenaeus vannamei)又稱南美白對蝦,是我國重要的養(yǎng)殖對蝦品種,但近年來其經(jīng)濟性狀明顯衰退且病害頻發(fā)(蔣葛等,2019),嚴(yán)重限制了凡納濱對蝦養(yǎng)殖產(chǎn)業(yè)的持續(xù)健康發(fā)展(包秀鳳,2014;彭敏等,2020)。培育抗逆性強且生長快的優(yōu)良對蝦養(yǎng)殖品種,是確保凡納濱對蝦養(yǎng)殖業(yè)健康發(fā)展的重要保障(楊銘等,2017)。國外學(xué)者針對凡納濱對蝦的存活率、生長性能、抗病毒等性狀已開展了一系列良種選育工作(Benzie et al.,1997;Argue et al.,2002;Gitterle et al.,2005);我國也選育出中興1號、壬海1號、海興農(nóng)2號等生長速度快、存活率高、可高密度養(yǎng)殖的凡納濱對蝦品種(唐揚等,2018),但能大規(guī)模應(yīng)用到實際生產(chǎn)的品種不多。本課題組多年來一直致力于開展耐低鹽、能適應(yīng)上海當(dāng)?shù)貧夂驐l件的凡納濱對蝦良種品系選育工作,現(xiàn)已完成F3代選育工作。為了更合理地利用這一種質(zhì)資源,高質(zhì)量開展良種選育工作,因此非常有必要對其種質(zhì)資源進行遺傳背景分析。【前人研究進展】微衛(wèi)星(Microsatellites)又稱為簡單重復(fù)序列(Simple sequence repeats,SSR),是由2~6個堿基組成基序(motif)串聯(lián)重復(fù)而形成的DNA序列(馬寧和曾地剛,2013),具有共顯性和多態(tài)性,且穩(wěn)定性較好,現(xiàn)已廣泛應(yīng)用于生物群體間的遺傳關(guān)系研究。Jerry等(2004)通過模擬和控制交配以開發(fā)日本對蝦微衛(wèi)星分子標(biāo)記,并證實其在后代指定親本方面的潛力,即微衛(wèi)星分子標(biāo)記可作為親緣關(guān)系鑒定中的保留系譜信息。劉海情等(2012)利用微衛(wèi)星分子標(biāo)記分析廣東省化州光輝養(yǎng)殖場有限公司新選育的吉富羅非魚第16代群體(F16)的遺傳多樣性,證實該吉富羅非魚群體具有較高的遺傳異質(zhì)性和較大的選育空間,可作為下一步選育工作的基礎(chǔ)選育群體。魯翠云等(2015)通過構(gòu)建鏡鯉全同胞家系的微衛(wèi)星遺傳圖譜,最終篩選出83個優(yōu)勢基因型。孫成飛等(2015)基于微衛(wèi)星分子標(biāo)記比較分析中國羅氏沼蝦和泰國羅氏沼蝦養(yǎng)殖群體的遺傳多樣性及遺傳結(jié)構(gòu),發(fā)現(xiàn)二者均具有較高的遺傳多樣性,但彼此親緣關(guān)系較遠(yuǎn)。黃小芳等(2020)選取8個微衛(wèi)星分子標(biāo)記對廣西不同地區(qū)的克氏原螯蝦群體進行遺傳多樣性分析,結(jié)果顯示廣西不同地區(qū)的克氏原螯蝦群體雜合子缺失現(xiàn)象普遍存在,應(yīng)通過適當(dāng)引種及加強不同地區(qū)群體間的遺傳交流。近年來,凡納濱對蝦微衛(wèi)星分子標(biāo)記的開發(fā)和應(yīng)用得到迅速發(fā)展(于洋,2014)。Meehan等(2003)最先公布了251個凡納濱對蝦微衛(wèi)星序列,并篩選出93個具有多態(tài)性的微衛(wèi)星引物,為凡納濱對蝦微衛(wèi)星分子標(biāo)記的開發(fā)奠定了基礎(chǔ)。Cruz等(2004)利用微衛(wèi)星分子標(biāo)記(Pvan1578和Pvan1815)監(jiān)測2代凡納濱對蝦的遺傳多樣性,結(jié)果顯示在育種計劃中無明顯的遺傳變異性損失,但等位基因的可變性降低,建議通過不同品系雜交以增加種群的遺傳變異。謝麗等(2009)采用9對微衛(wèi)星引物分析凡納濱對蝦4個選育群體(Molokai、OI、SIS和Kona Bay)的遺傳多樣性,結(jié)果顯示OI群體與Kona Bay群體的親緣關(guān)系最近,而SIS群體與Molokai群體的親緣關(guān)系最遠(yuǎn)。李東宇等(2016)建立了一套微衛(wèi)星多重PCR擴增體系并將其應(yīng)用于凡納濱對蝦家系親權(quán)鑒定,其模擬配對率和親權(quán)鑒定準(zhǔn)確率均為100%,尤其是全同胞和半同胞家系的鑒別效果良好。此外,王鴻霞等(2006)、劉洪濤等(2018)、方振朋等(2019)、黃小帥等(2019)、李強勇等(2020)也先后將微衛(wèi)星分子標(biāo)記應(yīng)用于凡納濱對蝦的多態(tài)性分析及家系鑒定研究領(lǐng)域。【本研究切入點】微衛(wèi)星分子標(biāo)記具有多態(tài)性高、穩(wěn)定性好、經(jīng)濟實惠、便于大批量分析等優(yōu)點(楊銘等,2017),可用于監(jiān)測育種方案中的群體遺傳力及遺傳變異水平。本課題組前期已培育出累計世代的自交和雜交群體,為了更好地繼續(xù)開展育種工作,亟需引進不同地區(qū)擁有不同遺傳背景且親緣關(guān)系較遠(yuǎn)的群體作為親本。【擬解決的關(guān)鍵問題】利用微衛(wèi)星分子標(biāo)記對來自厄瓜多爾恒興對蝦養(yǎng)殖公司2個養(yǎng)殖場(Pesquera和San Alfonso)共9個凡納濱對蝦養(yǎng)殖群體的遺傳背景進行分析,明確9個群體間的遺傳信息豐富度和遺傳分化程度,以期為構(gòu)建適應(yīng)上海獨特氣候?qū)ξr品種繁育計劃中的交配系譜分析提供參考依據(jù)。
1 材料與方法
1. 1 試驗材料
凡納濱對蝦樣品來自恒興對蝦養(yǎng)殖公司在厄瓜多爾的2個養(yǎng)殖場(Pesquera和San Alfonso),共9個養(yǎng)殖群體,其幼體來源于Texcumar公司,親本均為泥塘養(yǎng)殖群體,每個群體選取30尾活蝦,采集其肌肉組織置于無水乙醇中,-20 ℃保存?zhèn)溆谩?個凡納濱對蝦養(yǎng)殖群體的親本信息見表1。
1. 2 總DNA提取
采用海洋動物組織基因組DNA提取試劑盒[天根生化科技(北京)有限公司]提取凡納濱對蝦組織DNA,以Eppendorf分光光度計測定DNA濃度及OD值,并使用1.0%瓊脂糖凝膠電泳檢測DNA條帶完整性;最后用TE溶液稀釋至100 ng/μL,4 ℃保存?zhèn)溆谩?/p>
1. 3 微衛(wèi)星引物篩選與合成
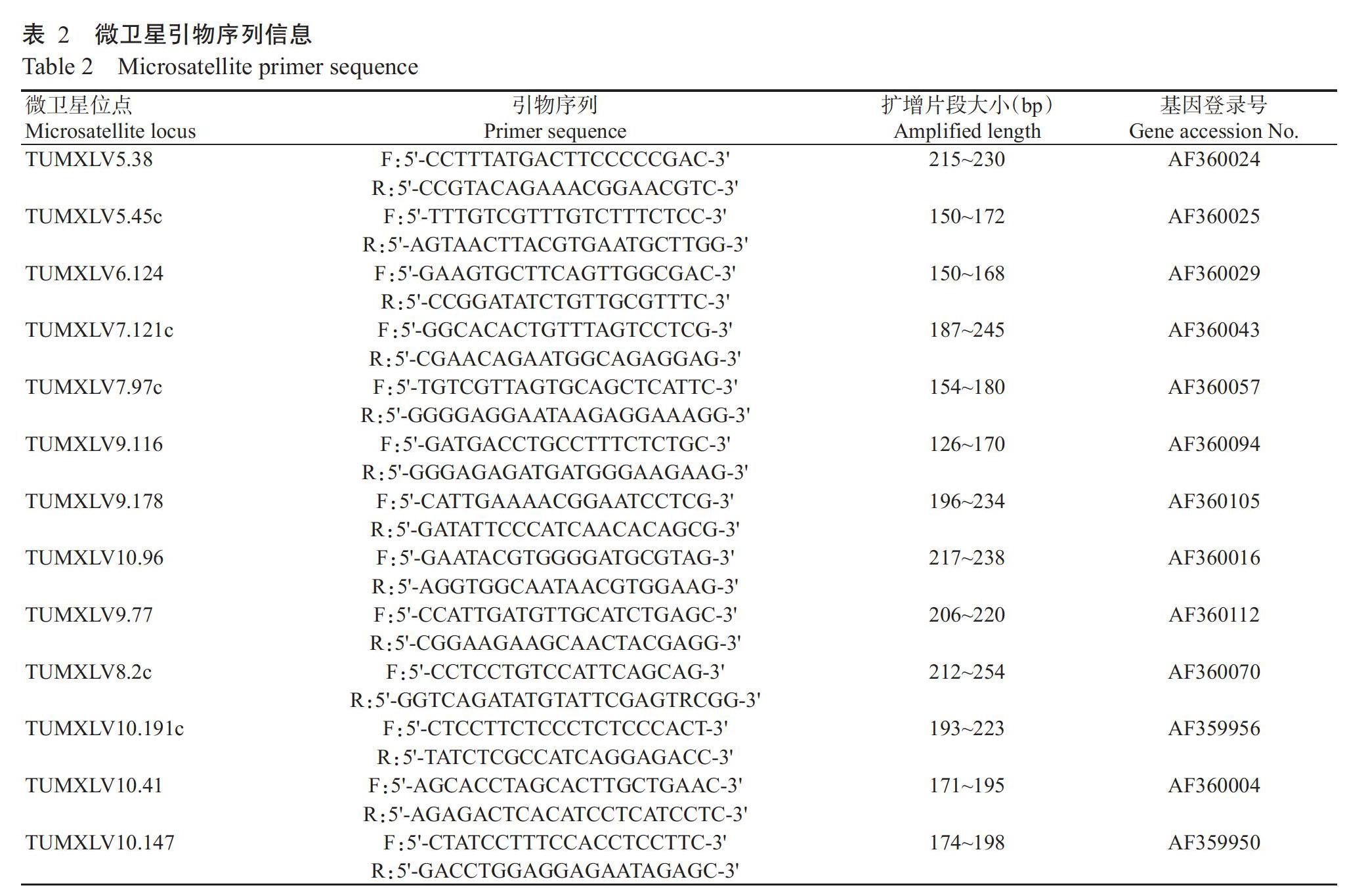
選用的13對微衛(wèi)星引物由本課題組成員張海強于2015年篩選獲得,委托生工生物工程(上海)股份有限公司合成。微衛(wèi)星引物序列見表2。
1. 4 PCR擴增及電泳分析
PCR反應(yīng)體系20.0 μL:2×Taq PCR MasterMix[生工生物工程(上海)股份有限公司]10.0 μL,DNA模板終濃度為10 ng/μL,上、下游引物各1.0 μL,加ddH2O補足至20.0 μL。擴增程序:95 ℃預(yù)變性4 min;94 ℃ 30 s,50~60 ℃ 30 s,72 ℃ 30 s,進行38個循環(huán);94 ℃ 40 s,45 ℃ 40 s,72 ℃ 40 s,進行13個循環(huán);72 ℃延伸5 min。采用8% SDS-PAGE進行分型,硝酸銀染色,觀察拍照。
1. 5 統(tǒng)計分析
獲得9個凡納濱對蝦養(yǎng)殖群體的基因分型數(shù)據(jù)后,采用PopGene32計算群體的等位基因數(shù)(Na)、有效等位基因數(shù)(Ne)、觀測雜合度(Ho)、期望雜合度(He)、Nei?s多樣性指數(shù)(H)及Hardy-Weinberg平衡指數(shù)(D)等群體遺傳學(xué)參數(shù)(Yeh and Boyle,1997);使用Cervus 3.0計算微衛(wèi)星位點的多態(tài)信息含量(PIC);參照Nei(1978)的無偏向性方法(Unbiased measures)計算群體間的遺傳距離和遺傳相似系數(shù);并根據(jù)9個凡納濱對蝦養(yǎng)殖群體的遺傳距離,采用MEGA 5.0進行UPGMA聚類分析。
2 結(jié)果與分析
2. 1 凡納濱對蝦微衛(wèi)星位點擴增結(jié)果
13對微衛(wèi)星引物均能從凡納濱對蝦組織中穩(wěn)定擴增出相應(yīng)的條帶,從9個凡納濱對蝦養(yǎng)殖群體中共檢測獲得37個等位基因,且等位基因大小主要集中在150~260 bp。微衛(wèi)星引物TUMXLV10.41在Pesquera 23群體中的PCR擴增產(chǎn)物經(jīng)8% SDS-PAGE分型,可觀察到單一(純合)或2條(雜合)目的擴增條帶(圖1)。
2. 2 凡納濱對蝦微衛(wèi)星位點遺傳多樣性分析結(jié)果
13個微衛(wèi)星位點在9個凡納濱對蝦養(yǎng)殖群體中的遺傳參數(shù)見表3。其中,Na為2~6個,平均為2.8462個;Ne的范圍在1.2074~4.6310個,平均為2.0269個,Ho的范圍在0.0171~0.5977,平均為0.2922;He的范圍在0.1453~0.7856,平均為0.4412;PIC的范圍在0.1292~0.6799,平均為0.3326。依據(jù)Botstein等(1980)的判斷標(biāo)準(zhǔn):PIC<0.25代表該位點呈低度多態(tài)性,0.25≤PIC≤0.50代表該位點呈中度多態(tài)性,PIC>0.50代表該位點呈高度多態(tài)性。在13個微衛(wèi)星位點中,僅有1個微衛(wèi)星位點(TUMXLV9.116)呈高度多態(tài)性,有4個微衛(wèi)星位點(TUMXLV10.147、TUMXLV5.45c、TUMXLV10.191c和TUMXLV10.96)呈低度多態(tài)性,其余8個微衛(wèi)星位點則呈中度多態(tài)性。
9個凡納濱對蝦養(yǎng)殖群體在13個微衛(wèi)星位點上的遺傳參數(shù)見表4。其中,Ne的范圍在1.6341~1.9992個,Ho的范圍在0.2225~0.3662,He的范圍在0.3317~0.4539。Pesquera 5群體的PIC最小(0.2772),San Alfonso 32群體的PIC最大(0.3573),9個凡納濱對蝦養(yǎng)殖群體的PIC均在0.25~0.50范圍內(nèi),表明這9個養(yǎng)殖群體的遺傳多態(tài)性均為中等水平。此外,凡納濱對蝦養(yǎng)殖群體的D范圍在0.0214~0.4214,均大于0,表明這9個凡納濱對蝦養(yǎng)殖群體的雜合子過剩,不同程度地偏離于Hardy-Weinberg平衡狀態(tài)。
2. 3 凡納濱對蝦群體遺傳分化分析結(jié)果
物種群體間的遺傳分化等級通常采用遺傳分化指數(shù)(Fst)和基因流(Nm)進行表示。由表5可知,有3個微衛(wèi)星位點的Fst在0~0.05范圍內(nèi),分別是TUMXLV10.147、TUMXLV8.2c和TUMXLV6.124,表明凡納濱對蝦群體在這3個微衛(wèi)星位點上的遺傳分化很小,可忽略不計;有2個微衛(wèi)星位點(TUMXLV 10.191c和TUMXLV10.96)的Fst均大于0.25,表明凡納濱對蝦群體在這2個微衛(wèi)星位點上存在明顯的遺傳分化;其余8個微衛(wèi)星位點的Fst在0.05~0.15范圍內(nèi),則表明凡納濱對蝦群體在這8個微衛(wèi)星位點上存在中等程度的遺傳分化。9個凡納濱對蝦養(yǎng)殖群體的Fst平均值為0.1259,說明有12.59%的遺傳分化來源于群體間,而87.41%的遺傳分化來自群體內(nèi)部。由于Nm與Fst呈負(fù)相關(guān),因此二者反映的群體遺傳分化結(jié)果具有趨同性。在13個微衛(wèi)星位點中,有3個微衛(wèi)星位點(TUMXLV10.147、TUMXLV8.2c和TUMXLV6.124)的Nm>4.000,有2個微衛(wèi)星位點(TUMXLV10.191c和TUMXLV10.96)的Nm<1.000,其余8個微衛(wèi)星位點的Nm則介于1.000~4.000。
由表6可知,在9個凡納濱對蝦養(yǎng)殖群體間,以Pesquera 29群體與Pesquera 15群體的遺傳距離最大(0.2426),而San Alfonso 23群體與Pesquera 23群體的遺傳距離最小(0.0215)。在遺傳相似性系數(shù)方面則表現(xiàn)為:Pesquera 29群體與Pesquera 15群體的遺傳相似系數(shù)最小(0.7846),San Alfonso 23群體與Pesquera 23群體的遺傳相似系數(shù)最大(0.9787)。可見,凡納濱對蝦養(yǎng)殖群體間的遺傳相似性系數(shù)與遺傳距離呈線性負(fù)相關(guān)。基于9個凡納濱對蝦養(yǎng)殖群體的遺傳距離,采用MEGA 5.0進行UPGMA聚類分析,以直觀呈現(xiàn)9個凡納濱對蝦養(yǎng)殖群體間的親緣關(guān)系。如圖2所示,9個凡納濱對蝦養(yǎng)殖群體可分為兩大類(I類和II類),其中Pesquera 29群體和San Alfonso 12群體獨立聚為I類。在II類中,Pesquera 15群體單獨作為一支,San Alfonso 32群體和Pesquera 5群體聚為一支,其余4個養(yǎng)殖群體則聚為另一支。
3 討論
3. 1 凡納濱對蝦的遺傳多樣性
本研究結(jié)果表明,從9個凡納濱對蝦養(yǎng)殖群體的13個微衛(wèi)星位點共檢測到37個等位基因,Na為2~6個,與張海強(2015)檢測到Na為3~5個的結(jié)論存在差異,可能是近交繁殖導(dǎo)致這9個凡納濱對蝦養(yǎng)殖群體連續(xù)世代中存在觀測等位基因丟失現(xiàn)象。等位基因較多的位點傾向于具有較高的等位基因分布值,因此所含信息量更大,更適用于養(yǎng)殖對蝦遺傳變異檢測。PIC反映某個遺傳標(biāo)記多態(tài)性可提供的信息量。在本研究中,13個微衛(wèi)星位點的PIC為0.1292~0.6799,平均為0.3326,略低于Meehan等(2003)研究得到的PIC(0.195~0.873),可能是在凡納濱對蝦育種過程中存在復(fù)雜的人為干擾,而對其種群的遺傳信息量產(chǎn)生影響。此外,9個凡納濱對蝦養(yǎng)殖群體在13個微衛(wèi)星位點上的Ho為0.2225~0.3622,平均為0.2915,低于Perez-Enriquez等(2009)、de Lima等(2010)檢測凡納濱對蝦養(yǎng)殖群體獲得的Ho(0.48~0.60和0.464~0.498)。說明本研究中的9個凡納濱對蝦養(yǎng)殖群體遺傳多樣性較低,究其原因可能是引進親本數(shù)量較少,零等位基因的存在減少了樣本量,或其親本使用了起源不確定的雜交種。因此,今后應(yīng)盡可能在較大范圍內(nèi)引進不同地區(qū)的親本來繁育后代,并完善親本遺傳背景分析,以保證子代處于較高的雜合水平。
Hardy-Weinberg平衡指數(shù)(D)表征Ho與He的平衡關(guān)系。D為正值表示雜合子過剩,D為負(fù)值則表示處于雜合子缺失狀態(tài);D越接近于0,表明其基因型分布越接近于Hardy-Weinberg平衡狀態(tài)(謝麗等,2009)。在本研究的9個凡納濱對蝦養(yǎng)殖群體中,San Alfonso P23群體和Pesquera P23群體的D分別為0.0214和0.0376,相對更接近于0,說明其基因型分布接近于Hardy-Weinberg平衡狀態(tài),另外7個群體則明顯偏離于Hardy-Weinberg平衡狀態(tài)。究其原因可能是人工選擇或組合交配育種過程中,凡納濱對蝦親本數(shù)量偏少,即子代群體是由少量親本組合雜交獲得,子代群體等位基因數(shù)量也相對減少,進而導(dǎo)致偏離Hardy-Weinberg平衡狀態(tài)及遺傳漂變(趙志英等,2018)。
3. 2 凡納濱對蝦的遺傳距離和遺傳分化
Fst是反映群體間遺傳分化程度的一個重要參數(shù)。本研究中,9個凡納濱對蝦養(yǎng)殖群體的平均Fst為0.1259,說明有12.59%的遺傳分化來源于群體間,而87.41%的遺傳分化來自群體內(nèi)部,群體間的分化程度為中等水平。Hamrick等(1995)研究認(rèn)為,Nm>1.000時能抵消遺傳漂變作用,阻止種群間發(fā)生分化;Nm<1.000時,遺傳漂變能主導(dǎo)種群遺傳結(jié)構(gòu)變化。本研究結(jié)果表明,9個凡納濱對蝦養(yǎng)殖群體間的平均Nm為1.7356,即遺傳漂變未能主導(dǎo)種群遺傳結(jié)構(gòu)的變化,各群體間的遺傳性趨向同一化,群體間的分化指數(shù)變小。Crawford和Littlepohn(1998)指出分化時間是影響群體間變異的主要決定因素,而遺傳距離能客觀反映群體間的分化時間及遺傳變異。在9個凡納濱對蝦養(yǎng)殖群體中檢測到的最大遺傳距離為0.2426、最小遺傳距離為0.0215,與Andriantahina等(2015)報道的最大遺傳距離(0.481)和最小遺傳距離(0.098)存在明顯差異。現(xiàn)代雜種優(yōu)勢理論認(rèn)為,子代的雜種優(yōu)勢與親本間的遺傳變異呈正相關(guān)(馮娜娜等,2012),因此在凡納濱對蝦人工繁育過程中,應(yīng)選擇遺傳距離較遠(yuǎn)群體中具有優(yōu)良性狀的個體作為親本,進行良種選育和親本擴繁。
4 結(jié)論
在9個凡納濱對蝦養(yǎng)殖群體中存在觀測等位基因丟失現(xiàn)象,且遺傳多樣性較低,群體間分化程度為中等水平。因此,可通過引進不同地區(qū)擁有不同遺傳背景且親緣關(guān)系較遠(yuǎn)的群體作為親本,以豐富子代群體的遺傳多樣性。
參考文獻(xiàn):
包秀鳳. 2014. 凡納濱對蝦選育群體遺傳多樣性分析[D]. 湛江:廣東海洋大學(xué). doi:10.7666/d.D522247. [Bao X F. 2014. Analysis of genetic diversity of selected stocks of Litopenaeus vannamei[D]. Zhanjiang:Guangdong Ocean University.]
方振朋,孟憲紅,李旭鵬,欒生,曹家旺,陳寶龍,孔杰,閆茂倉,胡利華. 2019. 基于微衛(wèi)星分子標(biāo)記的凡納濱對蝦商業(yè)苗種遺傳多樣性分析[J]. 漁業(yè)科學(xué)進展,41(5):101-109. doi:10.19663/j.issn2095-9869.20190527004. [Fang Z P,Meng X H,Li X P,Luan S,Cao J W,Chen B L,Kong J,Yan M C,Hu L H. 2019. Genetic diversity analysis of domestic commercial brands seedlings of Litopenaeus vannamei based on microsatellite molecular mar-kers[J]. Progress in Fishery Sciences,41(5):101-109.]
馮娜娜,徐真,馬洪雨,馬春艷,喬振國,馬凌波. 2012. 凡納濱對蝦7個不同家系遺傳差異的微衛(wèi)星標(biāo)記分析[J]. 生物技術(shù)通報,(11):133-138. doi:10.13560/j.cnki.biotech.bull.1985.2012.11.015. [Feng N N,Xu Z,Ma H Y,Ma C Y,Qiao Z G,Ma L B. 2012. Genetic variances in seven families of Litopenaeus vannamei revealed by microsatellite markers[J]. Biotechnology Bulletin,(11):133-138.]
黃小芳,唐章生,劉俊丹,張宏燕,鐘一治,盧智發(fā),侯樹鑒,王大鵬,陸專靈. 2020. 廣西不同地區(qū)克氏原螯蝦群體遺傳多樣性微衛(wèi)星分析[J]. 南方農(nóng)業(yè)學(xué)報,51(2):437-444. doi:10.3969/j.issn.2095-1191.2020.02.025. [Huang X F,Tang Z S,Liu J D,Zhang H Y,Zhong Y Z,Lu Z F,Hou S J,Wang D P,Lu Z L. 2020. Genetic diversity microsa-tellite analysis of Procambarus clarkii populations in different regions of Guangxi[J]. Journal of Southern Agriculture,51(2):437-444.]
黃小帥,徐煜,胡曉娟,徐武杰,蘇浩昌,文國樑,楊鏗,曹煜成. 2019. 利用微衛(wèi)星標(biāo)記分析7個凡納濱對蝦引進群體一代的遺傳多樣性[J]. 南方水產(chǎn)科學(xué),15(1):54-62. doi:10.12131/20180135. [Huang X S,Xu Y,Hu X J,Xu W J,Su H C,Wen G L,Yang K,Cao Y C. 2019. Genetic diversity analysis of first filial generation of seven introduced Litopenaeus vannamei populations using microsa-tellite DNA markers[J]. South China Fisheries Science,15(1):54-62.]
蔣葛,沈輝,萬夕和,喬毅,黎慧,王李寶,史文軍. 2019. 凡納濱對蝦急性肝胰腺壞死綜合癥病蝦與健康蝦腸道優(yōu)勢菌群比較分析[J]. 江蘇農(nóng)業(yè)學(xué)報,35(1):142-148. doi:10.3969/j.issn.1000-4440.2019.01.021. [Jiang G,Shen H,Wan X H,Qiao Y,Li H,Wang L B,Shi W J. 2019. Di-fference analysis of intestinal flora between healthy Litopenaeus vannamei and acute hepatopancreatic necrosis syndrome L. vannamei[J]. Jiangsu Journal of Agricultu-ral Sciences,35(1):142-148.]
李東宇,孔杰,孟憲紅,欒生,羅坤,盧霞,曹寶祥. 2016. 凡納濱對蝦(Litopenaeus vannamei)微衛(wèi)星多重PCR體系的建立及其在家系親權(quán)鑒定中的應(yīng)用[J]. 漁業(yè)科學(xué)進展,37(3):58-67. doi:10.11758/yykxjz.20151125002. [Li D Y,Kong J,Meng X H,Luan S,Luo K,Lu X,Cao B X. 2016. Development of multiplex PCR systems of microsatellite markers for Pacific white shrimp(Litopenaeus vannamei) and its application for parentage identification[J]. Progress in Fishery Science,37(3):58-67.]
李強勇,李旻,曾地剛,朱威霖,彭敏,楊春玲,劉青云,趙永貞,陳秀荔,陳曉漢. 2020. 凡納濱對蝦微衛(wèi)星分子標(biāo)記的開發(fā)及不同養(yǎng)殖家系遺傳多態(tài)性分析[J]. 南方農(nóng)業(yè)學(xué)報,51(2):429-436. doi:10.3969/j.issn.2095-1191. 2020.02.024. [Li Q Y,Li M,Zeng D G,Zhu W L,Peng M,Yang C L,Liu Q Y,Zhao Y Z,Chen X L,Chen X H. 2020. Development of microsatellite markers of Litopenaeus vannamei and genetic polymorphism analysis of different cultured families[J]. Journal of Southern Agriculture,51(2):429-436.]
劉海情,郭昱嵩,王中鐸,劉麗,劉楚吾. 2012. 利用微衛(wèi)星分析吉富羅非魚群體的遺傳多樣性[J]. 南方農(nóng)業(yè)學(xué)報,43(1):94-98. doi:10.3969/j:issn.2095-1191.2012.01.94. [Liu H Q,Guo Y S,Wang Z D,Liu L,Liu C W. 2012. Genetic diversity analysis amongst GIFT strains of Oreochromis niloticus using microsatellites[J]. Journal of Southern Agri-culture,43(1):94-98.]
劉洪濤,楊明秋,何玉貴,唐賢明. 2018. 凡納濱對蝦八個地理群體遺傳多樣性的微衛(wèi)星分析[J]. 海南大學(xué)學(xué)報(自然科學(xué)版),36(2):146-152. doi:10.15886/j.cnki.hdxbzkb.2018.0019. [Liu H T,Yang M Q,He Y G,Tang X M. 2018. Microsatellite analysis of genetic diversity in eight geographical populations of Litopenaeus vannamei[J]. Natural Science Journal of Hainan University,36(2):146-152.]
魯翠云,顧穎,李超,鄭先虎,程磊,曹頂臣,俞菊華,何立川,孫效文. 2015. 鏡鯉與建鯉生長性狀共享QTL標(biāo)記及優(yōu)勢基因型[J]. 中國水產(chǎn)科學(xué),22(3):371-386. doi:10. 3724/SP.J.1118.2015.14293. [Lu C Y,Gu Y,Li C,Zheng X H,Cheng L,Cao D C,Yu J H,He L C,Sun X W. 2015. Analysis of shared QTLs and preferred genotypes between mirror carp and Jian carp[J]. Journal of Fishery Sciences of China,22(3):371-386.]
馬寧,曾地剛. 2013. 凡納濱對蝦微衛(wèi)星序列的篩選[J]. 西南農(nóng)業(yè)學(xué)報,26(6):2629-2633. doi:10.16213/j.cnki.scjas. 2013.06.094. [Ma N,Zeng D G. 2013. Isolation of microsatellite sequences from Litopenaeus vannamei[J]. Southwest China Journal of Agricultural Sciences,26(6):2629-2633.]
彭敏,陳慧芳,李強勇,楊春玲,曾地剛,劉青云,趙永貞,陳曉漢,林勇,陳秀荔. 2020. 凡納濱對蝦連續(xù)3個世代選育群體的遺傳多樣性分析[J]. 南方農(nóng)業(yè)學(xué)報,51(6):1442-1450. doi:10.3969/j.issn.2095-1191.2020.06.026. [Peng M,Chen H F,Li Q Y,Yang C L,Zeng D G,Liu Q Y,Zhao Y Z,Chen X H,Lin Y,Chen X L. 2020. Genetic diversity of three consecutive generations of Litopenaeus vannamei[J]. Journal of Southern Agriculture,51(6):1442-1450.]
孫成飛,葉星,董浚鍵,田園園,梁健輝. 2015. 羅氏沼蝦6個養(yǎng)殖群體遺傳多樣性的微衛(wèi)星分析[J]. 南方水產(chǎn)科學(xué),11(2):20-26. doi:10.3969/j.issn.2095-0780.2015.02.003. [Sun C F,Ye X,Dong J J,Tian Y Y,Liang J H. 2015. Genetic diversity analysis of six cultured populations of Macrobrachium rosenbergii using microsatellite markers[J]. South China Fisherise Science,11(2):20-26.]
唐揚,孟小菲,沈瑞福,黃永春. 2018. 凡納濱對蝦家系選育的研究與應(yīng)用[J]. 水產(chǎn)科學(xué),37(4):555-563. doi:10.16378/j.cnki.1003-1111.2018.04.020. [Tang Y,Meng X F,Shen R F,Huang Y C. 2018. Research and application of family selective breeding in culture of Pacific white shrimp Litopenaeus vannamei[J]. Fisheries Science,37(4):555-563.]
王鴻霞,吳長功,張留所,相建海. 2006. 微衛(wèi)星標(biāo)記應(yīng)用于凡納濱對蝦家系鑒別的研究[J]. 遺傳,28(2):179-183. doi:10.16288/j.yczz.2006.02.010. [Wang H X,Wu C G,Zhang L S,Xiang J H. 2006. The application of microsa-tellite markers for parentage determination in selective breeding of Pacific white shrimp(Litopenaeus vannamei)[J]. Hereditas(Beijing),28(2):179-183.]
謝麗,陳國良,葉富良,栗志民. 2009. 凡納濱對蝦4個選育群體遺傳多樣性的SSR分析[J]. 廣東海洋大學(xué)學(xué)報,29(4):5-9. doi:10.3969/j.issn.1673-9159.2009.04.002. [Xie L,Chen G L,Ye F L,Li Z M. 2009. Genetic diversity of four selected stocks of Litopenaeus vannamei as revealed by SSR marker[J]. Journal of the Guangdong Ocean University,29(4):5-9.]
楊銘,于洋,張曉軍,王全超,劉敬文,李富花,相建海. 2017. 基于轉(zhuǎn)錄組數(shù)據(jù)的凡納濱對蝦微衛(wèi)星標(biāo)記開發(fā)[J]. 海洋科學(xué),41(2):96-102. doi:10.11759//hykx20160322002. [Yang M,Yu Y,Zhang X J,Wang Q C,Liu J W,Li F H,Xiang J H. 2017. Development of microsatellite markers from the transcriptome sequences of Pacific white shrimp (Litopenaus vannamei)[J]. Marine Science,41(2):96-102.]
于洋. 2014. 凡納濱對蝦分子標(biāo)記的開發(fā)及其在遺傳育種中的應(yīng)用[D]. 北京:中國科學(xué)院大學(xué). [Yu Y. 2014. Deve-lopment of molecular markers and their application in selective breeding of the Pacific white shrimp,Litopenaeus vannamei[D]. Beijing:The University of Chinese Academy of Sciences.]
張海強. 2015. 不同來源的凡納濱對蝦群體遺傳多樣性的初步分析[D]. 上海:上海海洋大學(xué). [Zhang H Q. 2015. Preliminary analysis of genetic diversity of different po-pulations of Litopenaeus vannamei[D]. Shanghai:Shanghai Ocean University.]
趙志英,梁麗運,白麗蓉. 2018. 斑節(jié)對蝦3個野生群體遺傳多樣性的微衛(wèi)星標(biāo)記分析[J]. 熱帶海洋學(xué)報,37(3):65-72. doi:10.11978/2017084. [Zhao Z Y,Liang L Y,Bai L R. 2018. Analysis of genetic diversity among three wild populations of Penaeus monodon using microsatellite mar-ker[J]. Journal of Tropical Oceanography,37(3):65-72.]
Andriantahina F,Liu X L,Huang H. 2015. Using microsatellite markers to identify heritability of Pacific whiteleg shrimp Litopenaeus vannamei[J]. Acta Oceanologica Sinica,34(6):59-65. doi:10.1007/s13131-015-0688-6.
Argue B J,Arce S M,Lotz J M,Moss S M. 2002. Selective breeding of Pacific white shrimp(Litopenaeus vannamei) for growth and resistance to Taura Syndrome Virus[J]. Aquaculture,204(3-4):447-460. doi:10.1016/S0044-8486(01)00830-4.
Benzie J A H,Kenway M,Trott L. 1997. Estimates for the heritability of size in juvenile Penaeus monodon prawns from half-sib matings[J]. Aquaculture,152(1-4):49-53. doi:10.1016/S0044-8486(96)01528-1.
Botstein D,White R L,Skolnick M,Davis R W. 1980. Construction genetic linkage map in man using restriction fragment length polymorphisms[J]. American Journal of Human Genetics,32(3):314-331.
Crawford A M,Littlepohn R P. 1998. The use of DNA marker in deciding conservation priorities in sheep and other livestock[J]. Animal Genetic Resources Information,23:21-26. doi:10.1017/S1014233900004909.
Cruz P,Ibarra A M,Mejia-Ruiz H,Gaffney P M,Pérez-Enríquez R. 2004. Genetic variability assessed by microsatellites in a breeding program of Pacific white shrimp (Litopenaeus vannamei)[J]. Marine Biotechnology,6(2):157-164. doi:10.1007/s10126-003-0017-5.
de Lima A P S,da Silva S M B C,O1iveira K K C,Maggioni R,Coimbra M R M. 2010. Genetics of two marine shrimp hatcheries of the Pacific white shrimp Litopenaeus vannamei (Boone,1931) in Pernambuco,Brazil[J]. Ciência Rural,40(2):325-331. doi:10.1590/S0103-8478 2010005000008.
Gitterle T,Salte R,Gjerde B,Cock J,Johansen H,Salazar M,Lozano C,Rye M. 2005. Genetic(co) variation in resistance to White Spot Syndrome Virus(WSSV) and harvest weight in Penaeus(Litopenaeus) vannamei[J]. Aquaculture,246(1-4):139-149. doi:10.1016/j.aquaculture. 2005.02.011.
Hamrick J L,Godt M J W,Sherman-Broyles S L. 1995. Gene flow among plant populations:Evidence from genetic markers. In Experimental and molecular approaches to plant biosystematics[M]//Hoch P G, Stephenson A G. Experimental and molecular to plant biosystematics. St Louis:Missouri Botanical Garden Press:215–232.
Jerry D R,Preston N P,Crocos P J,Keys S,Meadows J R S,Li Y T. 2004. Parentage determination of Kuruma shrimp Penaeus(Marsupenaeus) japonicus using microsatellite markers(Bate)[J]. Aquaculture,235(1-4):237-247. doi: 10.1016/j.aquaculture.2004.01.019.
Meehan D,Xu Z K,Gladys Z,Alcivar-Warren A. 2003. High frequency and large number of polymorphic microsatellites in cultured shrimp,Penaeus(Litopenaeus) vannamei[Crustacea:Decapoda][J]. Marine Biotechnology,5(4):311-330. doi:10.1007/s10126-002-0092-z.
Nei M. 1978. Estimation of average hetemzygosity and gene-tic distance from a small number of individuals[J]. Genetics,89(3):583-590.
Perez-Enriquez R,Hernández-Martínez F,Cruz P. 2009. Genetic diversity status of White shrimp Penoeus(Litopenaeus) vannamei broodstock in Mexico[J]. Aquaculture,297(1-4):44-50. doi:10.1016/j.aquaculture.2009.08.038.
Yeh F C,Boyle T J. 1997. Population genetic analysis of co-dominant and dominant markers and quantitative traits[J]. Belgian Journal of Botany,129(2):157.
(責(zé)任編輯 蘭宗寶)

