海綿共附生放線菌Streptomyces parvulus MA1076的次級代謝產物研究
張夢雪,李歡歡,邵 峰,李宏基,吳文惠,孫 鵬
(1.上海海洋大學食品學院,上海 201306;2.海軍軍醫大學藥學系,上海 200433;3.空軍都江堰特勤療養中心,四川都江堰 611830)
放線菌在自然界中分布廣泛,與人類的生產和生活關系極為密切,其次級代謝產物具有抗腫瘤、抗菌、免疫調節等多種重要的生物活性[1-5],目前報道的抗生素大約70%是放線菌產生的[6]。隨著人們對陸生放線菌的研究深入,挖掘結構新穎的活性天然產物難度越來越大,尋找新的活性化合物成為藥物研究的重要目標。20世紀60年代以來,人們將藥物研發的關注點轉向海洋微生物[7],海洋微生物不僅資源豐富,特殊的生存環境(高壓、高鹽、低溫、低光照等)也賦予了其獨特的代謝途徑,進而產生結構特異、活性顯著的天然產物。研究發現,大約27%種屬的海洋微生物具有抗菌活性[8],其中來源于放線菌的活性代謝產物約占微生物來源的45%,結構新穎的海洋放線菌代謝產物的發現為藥物研發開辟了新途徑[9]。
海洋放線菌廣泛棲息于海洋動植物體表、體內、海水及海底沉積物中[10]。尤其是具有獨特生理結構的多孔動物海綿(Pseudoceratina sp.),其共附生放線菌一直是人們的研究重點。VALLIAPPAN等[11]通過分析3 003株海洋放線菌的16SrRNA序列,發現其中63%是海綿共附生放線菌;XIN等[12]從海綿共附生放線菌Streptomyces sp.LS298中分離到的化合物Quinomycin G具有明顯的抗腫瘤活性,對Jurkat細胞系(T細胞白血病)有很強的抑制作用(IC50值為0.414μmol·L-1)。因此,選擇海綿共附生放線菌進行化學成分分析,篩選新型活性物質,對新藥研發有重要意義。本文對海綿共附生放線菌Streptomyces parvulus MA1076進行了菌株鑒定并對其次級代謝產物進行化學成分研究。
1 材料與方法
1.1 材料與試劑
海綿樣品于2012年8月采自于中國南海永興島,水深15~20 m,由中國科學院海洋研究所李錦和研究員鑒定,樣品標本儲藏于海軍軍醫大學藥學院天然藥化教研室(編號為GE3)。DNA提取使用細菌基因組DNA快速抽提試劑盒(生工生物工程股份有限公司)。活性測試使用CellTiter-Glo?熒光活性檢測試劑盒(普洛麥格生物技術有限公司)。
色譜填料包括Sephadex LH-20葡聚糖凝膠(Pharmacia Biotech,Sweden),硅膠(100~200目和200~300目,煙臺黃務硅膠開發實驗廠)和GF254 TLC預制硅膠板(煙臺黃務硅膠開發實驗廠)。化學試劑包括乙酸乙酯、二氯甲烷、甲醇(均為分析純)和高效液相甲醇(色譜純),均購自中國醫藥集團上海化學試劑公司;顯色劑為10%硫酸香草醛溶液。
分離培養基為MS固體培養基(黃豆粉20.0 g,D-甘露醇20.0 g,瓊脂20.0 g,去離子水1 L),種子培養基為TSB液體培養基(胰蛋白胨大豆肉湯30.0 g,去離子水1 L),發酵培養基為ISP2液體培養基(麥芽提取物10.0 g,酵母提取物4.0 g,胰蛋白胨4.0 g,去離子水1 L),細胞培養基為L Wnt-3A細胞專用培養基。
1.2 儀器設備
高壓滅菌鍋(松下健康醫療器械株式會社,MLS-3781L-PC型),微生物恒溫培養箱(上海躍進醫療器械廠,SPX-150 B型),小型高速離心機(德國艾本德有限公司,5418型),PCR擴增儀(伯樂生命醫學產品有限公司,T100型),NMR(Bruker,DRX600),LC-MS(Agilent,6224 TOFMS),多 標 記 微 孔 板 檢 測 儀(PerkinElmer,EnVision型),高效液相色譜儀(Agilent,1200型)。
1.3 微生物的分離和培養
1.3.1 菌株的分離
無菌水沖洗海綿樣品2~3遍,用無菌剪刀剪碎,無菌水重懸,接種環蘸取重懸液劃線于MS固體培養基,28℃培養箱中倒置培養,3~5 d后長出菌落,挑取生長形態與放線菌相似的菌落,接種至MS固體培養基上二次分離培養,挑選單菌落用液體培養基培養2~3 d后,用20%的甘油凍存于-20℃冰箱。
1.3.2 16SrDNA菌株鑒定
取-20℃凍存的保種管接種于含有5 mL TSB培養基的試管中,28℃、220 r·min-1進行發酵培養48 h,取發酵液2 mL,使用細菌基因組DNA快速抽提試劑盒,提取出鏈霉菌基因組DNA,采 用 鏈 霉 菌 通 用 引 物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-ACGGCTACCTTGTTACGACTT-3′)進 行PCR擴增,PCR擴增條件為25μL反應體系(12.5μL PCR預混液,11μL水,0.5μL引物,0.5μL DNA模板),擴增產物送生工生物工程(上海)股份有限公司進行16S rDNA測序,測序結果提交GenBank,并在NCBI網站上分析比對,相似序列用MEGA-7軟件根據neighbor-joining(NJ)方法對菌株構建系統發育樹,進行種屬鑒定。
1.4 MA1076菌株中化合物分離純化
1.4.1 菌株發酵培養
配制50 mL TSB液體培養基6瓶,121℃高溫滅菌30 min,接入MA1076菌株,28℃、220 r·min-1進行種子培養基發酵培養,48 h后得到種子液。取種子液5 mL接種到裝有200 mL ISP2培養基的1 L錐形瓶中,28℃、220 r·min-1搖床培養7 d,總發酵體積10 L。
1.4.2 菌株化合物的提取分離
發酵液加入10 L乙酸乙酯,超聲破菌,提取3次,濃縮后得粗浸膏4.1 g。粗浸膏進行正相硅膠柱色譜分離,以二氯甲烷-甲醇梯度洗脫(體積比依次為100∶0、100∶1、50∶1、25∶1、20∶1、15∶1、10∶1、5∶1、0∶100),得到8個組分(M1~M8)。將M7組分過Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇,體積比2∶1)及HPLC(80%甲醇,流速1.5 mL·min-1)得到化合物1(28 mg,tR=31 min),將M5組分過Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇,體積比2∶1)及HPLC(60%甲醇,流速1.5 mL·min-1)得到化合物2(16 mg,tR=19 min)和化合物6(7 mg,tR=21 min),將M6組分過Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇,體積比2∶1)及HPLC(60%甲醇,流速1.5 mL·min-1)得到化合物3(4 mg,tR=20 min)、化合物4(5 mg,tR=21 min)和化合物5(3 mg,tR=24 min)。
1.5 化合物活性測試
吸取50μL細胞懸液,轉入50 mL離心管中,加細胞培養基至50 mL,顛倒混勻,置于冰上。使用Multidrop自動分液器將細胞懸液以每孔45 μL均勻加入96孔板(注意設定第1列和第12列不加),細胞接種完畢后,置于37℃培養。細胞接種24 h后,對細胞96孔板進行加藥(化合物1)處理,每孔5μL,其中第2列和第11列為DMSO對照組。加藥完畢后置于37℃細胞培養箱。細胞加藥72 h后,使用CellTiter-Glo試劑進行細胞活力檢測。使用Multidrop自動分液器將CellTiter-Glo試劑以每孔50μL均勻加入96孔板(注意設定第1列和第12列不加),避光,置于水平搖床15 min,使用EnVision多標記微孔板檢測儀進行結果檢測。
2 結果與分析
2.1 測序結果
菌株DNA測序結果提交NCBI,利用GenBank生物信息學數據庫(https://pubmed.ncbi.nlm.nih.gov/)進行序列的相似性比較分析,選取比對結果中相似性較高的菌株,在MEGA-7軟件中根據neighbor-joining(NJ)方法對菌株構建系統發育樹(圖1)。基因序列同源性比對分析發現,菌株MA1076與Streptomyces屬parvulus種相似性最高,相似度為99.93%,鑒定菌株MA1076為Streptomyces parvulus(表1)。
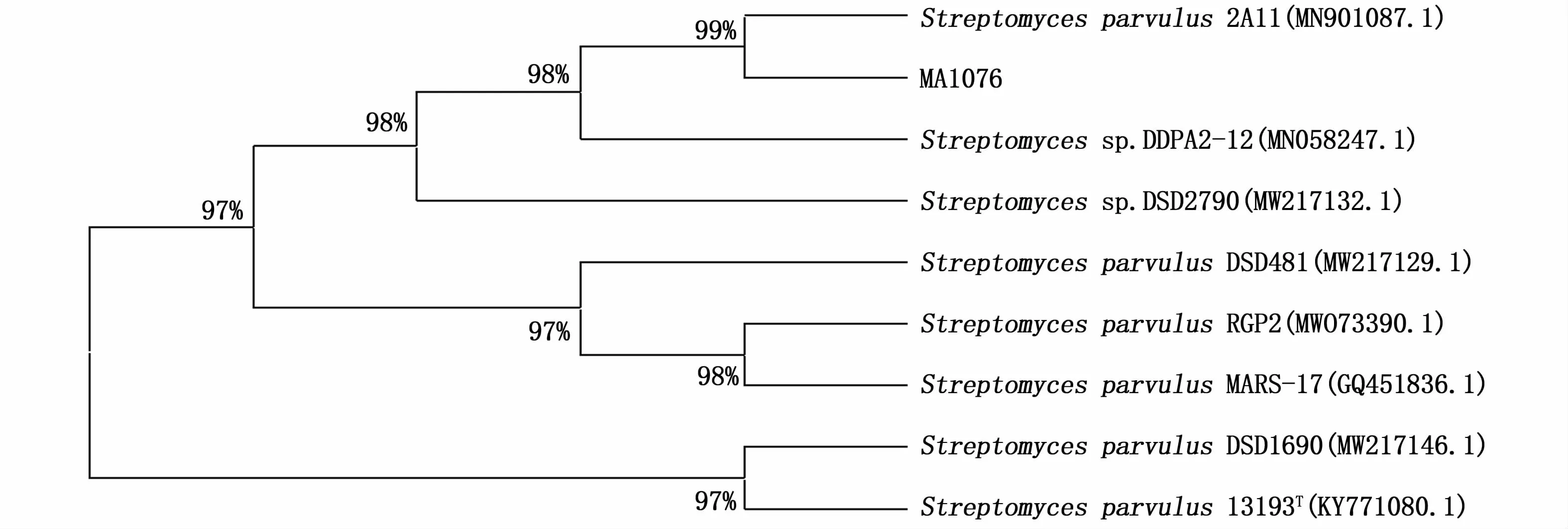
圖1 基于菌株MA1076的16S r DNA構建的系統發育樹Fig.1 Phylogenetic tree constructed on basis of 16Sr DNA of strain MA1076

表1 16S r DNA序列與NCBI中已知序列的比對結果Tab.1 16Sr DNA sequence blast with known sequences in NCBI
2.2 放線菌MA1076化合物的結構鑒定
從菌株MA1076中分離出的化合物,分別采用ESI-MS、1H-NMR和13C-NMR波譜學方法鑒定了其中6個化合物,結構見圖2。

圖2 化合物1~6的結構式Fig.2 Structures of compounds 1~6
化合物1:橙紅色粉末,ESI-MS m/z:1 255.4[M+H]+,分子式C62H86N12O16,不飽和度為20。在1H-NMR中,δH8.17(1H,d,J=5.4 Hz),δH8.01(1H,d,J=5.6 Hz),δH7.72(1H,d,J=6.6 Hz),δH7.62(1H,d,J=7.8 Hz)處有4個N-H的氫信號,在δH2.90(3H,s)和δH2.93(3H,s)處有兩個N-CH3信號峰,在13C-NMR中,δC166~174范圍內出現12個羰基碳信號。其苯氧環部分NMR數據歸屬如下:1H-NMR(600 MHz,CDCl3)δH:2.14(3H,s,H-4Me),2.46(3H,s,H-6Me),7.34(1H,d,J=7.7 Hz,H-7),7.59(1H,d,J=7.7 Hz,H-8);13C-NMR(150 MHz,CDCl3)δC:7.9(C-12),15.2(C-11),101.8(C-1),113.7(C-4),125.9(C-8),127.8(C-6),129.2(C-9a),130.4(C-7),132.7(C-9),140.6(C-5a),145.2(C-4a),146.0(C-10a),147.7(C-2),166.7(C-13),168.7(C-14),179.2(C-3)。環肽部分NMR數據見表2。以上數據與宋現芹等[13]報道的數據相符,確定該化合物為放線菌素D。
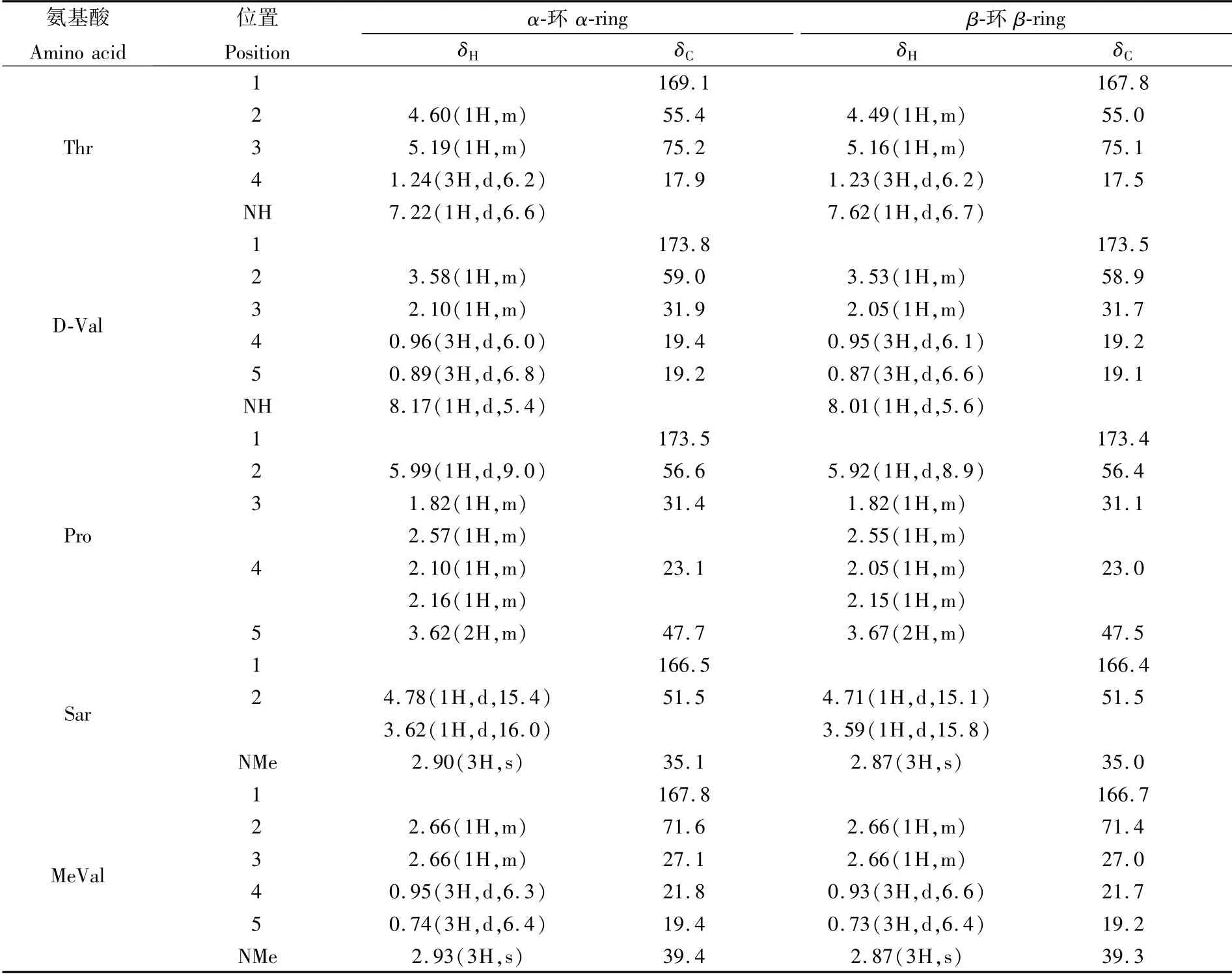
表2 化合物1的核磁數據Tab.2 NMR data of compound 1
化合物2:白色粉末,ESI-MS m/z:576.8[M+H]+,分子式C35H60O6,不飽和度為6。1H-NMR中顯示有6個甲基信號δH0.65(3H,s,H-18)、δH0.76-0.83(9H,m,H-26,H-27,H-29)、δH0.89(3H,d,J=6.6 Hz,H-21)、δH0.95(3H,s,H-19),13C-NMR中δC121.2(C-6)和δC140.5(C-5)顯示含有雙鍵結構,根據不飽和度推斷結構中含有5個環狀結構。其NMR數據歸屬如下:1HNMR(600 MHz,DMSO)δH:0.65(3H,s,H-18),0.76~0.83(9H,m,H-26,H-27,H-29),0.89(3H,d,J=6.6 Hz,H-21),0.95(3H,s,H-19),3.64~3.75(2H,m,H-2′,H-5′),3.85~3.92(1H,m,H-3),4.21~4.32(2H,t,J=7.8 Hz,H-3′,H-4′),4.43~4.46(2H,m,H-6′),4.86(1H,d,H-1′),5.35(1H,s,H-6);13C-NMR(150 MHz,DMSO)δC:11.7(C-18),11.8(C-29),18.7(C-21),19.0(C-27),19.1(C-19),19.7(C-26),20.6(C-11),22.7(C-28),23.9(C-15),25.5(C-23),27.8(C-16),28.8(C-25),29.3(C-2),31.4(C-8),31.5(C-7),33.4(C-22),35.5(C-20),36.3(C-10),36.9(C-1),38.4(C-12),41.9(C-13),45.2(C-24),49.7(C-9),55.5(C-17),56.2(C-14),61.1(C-6′),70.2(C-4′),73.5(C-2′),76.8(C-5′),76.8(C-3),77.0(C-3′),100.8(C-1′),121.2(C-6),140.5(C-5)。以上數據與韻小娟等[14]報道的數據相符,確定該化合物為daucosterol。
化合物3:白色粉末,ESI-MS m/z:209.5[MH]-,分子式C11H18N2O2,不飽和度為4。在1HNMR的高場區有δH0.94(3H,d,J=6.0 Hz)和δH0.96(3H,d,J=6.6 Hz)兩個甲基峰,13C-NMR低場區的δC172.8和δC168.9兩個信號表明此處是兩個羰基碳。其NMR數據歸屬如下:1HNMR(600 MHz,CD3OD)δH:0.95(3H,d,J=6.0 Hz),1.01(3H,d,J=6.6 Hz),2.01~2.04(1H,m),1.51~1.56(1H,m),1.93~1.97(1H,m),4.27(1H,t,J=7.1 Hz),4.13(1H,br.s),1.88~1.99(1H,m),2.30~2.34(1H,m),1.88~1.95,(1H,m),1.99~2.06(1H,m),3.52~3.55(2H,m);13C-NMR(150 MHz,CD3OD)δC:22.2(C-13),23.3(C-12),23.6(C-4),25.8(C-11),29.1(C-5),39.4(C-10),46.5(C-3),54.7(C-9),60.3(C-6),168.9(C-7),172.8(C-1)。以上數據與YANG等[15]報道的數據相符,確定該化合物為cyclo-((S)-Pro-(R)-Leu)。
化合物4:白色粉末,ESI-MS m/z:243.1[M+H]+,分子式為C10H14N2O5,不飽和度為5。1HNMR中僅在δH1.85(3H,s)處有一個甲基峰信號,13C-NMR中在δC62.8,δC72.2、δC86.3、δC88.8處有4個連氧的碳信號。其NMR數據歸屬如下:1H-NMR(600 MHz,CD3OD)δH:1.85(3H,s,H-7),2.22(2H,m,H-2′),3.71(1H,d,J=6.0,H-5′a),3.78(1H,d,J=6.0,H-5′b),3.89(1H,m,H-4′),4.39(1H,m,H-3′),6.27(1H,dd,J=6.0 Hz,H-1′),7.80(1H,s,H-6);13C-NMR(150 MHz,CD3OD)δC:12.4(C-7),41.2(C-2′),62.8(C-5′),72.2(C-3′),86.3(C-1′),88.8(C-4′),111.5(C-5),138.2(C-6),152.4(C-2),166.4(C-4)。以上數據與黃勝陽等[16]報道的數據相符,確定該化合物為thymidine。
化合物5:淡黃色固體,ESI-MS m/z:285.1[M+H]+,分子式為C12H16N2O6,不飽和度為6。其NMR數據歸屬如下:1H-NMR(600 MHz,CD3OD)δH:1.87(3H,s,H-7),2.08(3H,s,CH3COO),2.33(2H,m,H-2′),3.79(2H,m,H-5′),4.06(1H,m,H-4′),5.30(1H,m,H-3′),6.27(1H,dd,J=6.1 Hz,H-1′),7.83(1H,s,H-6);13C-NMR(150 MHz,CD3OD)δC:12.4(C-7),20.9(CH3COO),38.4(C-2′),63.0(C-5′),76.4(C-3′),86.2(C-4′),86.7(C-1′),111.9(C-5),137.9(C-6),152.4(C-2),166.4(C-4),172.2(C-1)。以上數據與GOUDOU等[17]報道的數據相符,確定該化合物為3′-O-acetylthymidine。
化合物6:淡黃色固體,ESI-MS m/z:161.9[M+H]+,分子式為C9H7NO2,不飽和度為7。其NMR數據歸屬如下:1H-NMR(600 MHz,CD3OD)δH:7.15~7.20(2H,m,H-6,7),7.42(1H,m,H-5),7.94(1H,s,H-2),8.06(1H,m,H-4);13C-NMR(150 MHz,CD3OD)δC:108.8(C-3),112.9(C-4),122.0(C-6),122.4(C-7),123.6(C-5),127.5(C-8),133.4(C-2),138.2(C-9),169.4(C-10)。以上數據與郭文娟和郭順星[18]報道的數據相符,確定該化合物為3-羧基吲哚。
2.3 化合物活性測試
測試6個化合物對兩株胰腺癌細胞系(pc-12和bc-16)的細胞增殖抑制活性,結果顯示,化合物1對兩株胰腺癌細胞均有明顯的增殖抑制活性(圖3),化合物2~6無明顯的細胞增殖抑制活性。
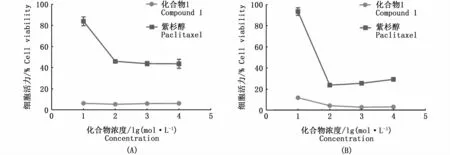
圖3 化合物1細胞增殖抑制活性結果Fig.3 Cell proliferation inhibitory activity of compound 1
3 討論
本文從海綿Pseudoceratina sp.共附生放線菌Streptomyces parvulus MA1076中分離得到6個已知化合物,除化合物1和2外,其他均為首次從放線菌中分離得到。化合物1最早分離自Streptomyces parvulus NBRC13193,且已用于藥物生產,是臨床常用的抗腫瘤藥之一,其能夠與DNA結合產生抗腫瘤作用,用于小兒腎母細胞瘤、侵襲性葡萄胎、絨毛膜上皮細胞癌以及橫紋肌肉瘤等惡性腫瘤的治療[19],體外活性測試發現,其對胰腺癌細胞有顯著的增殖抑制活性,后續可以通過體內實驗進一步探討該化合物的活性。化合物2是一種廣泛存在于植物中的甾醇,曾先后從內生真菌Rhizopus oryzae KSD-815和鏈霉菌Streptomyces cavourensis YBQ59的發酵產物中分離得到[3,20]。化合物2具有廣泛的生物學活性,其對乳腺癌、肝癌、結腸癌以及白血病等腫瘤細胞具有一定程度的抗增殖作用,在體內外實驗中有良好的抗氧化作用,另外還有抗病毒、抗炎、抗血小板聚集、調節免疫、促進神經干細胞增殖等作用[21-25]。化合物3曾從海綿中分離得到[26]。化合物4、5為核苷類化合物,其中化合物5對肝癌細胞有中等強度的抗增殖作用[27]。化合物6除了具有抗HIV活性外[21],還對多種革蘭氏陽性菌和陰性菌有抑制活性[28]。
近年來大規模的基因組測序結果顯示,大部分放線菌都包含30個以上生物合成基因簇,相對于放線菌龐大的生物合成基因簇,本文對菌株MA1076次級代謝產物進行研究僅分離得到6個已知化合物。后期可以通過使用不同的發酵培養基,或者高鹽、低光照等多種發酵條件,并擴大發酵規模,以獲得更多結構新穎、活性顯著的化合物。或者通過全基因組測序預測次級代謝產物,利用生物信息學分析基因簇中調控基因的作用,激活正調控或敲除負調控因子促使沉默基因表達;也可通過插入強啟動子、沉默基因過表達、異源表達等遺傳學手段激活其沉默基因,從而獲得更多結構新穎的次級代謝產物。
隨著對海綿及其共附生微生物研究的不斷深入,人們逐漸認識到海綿中不少化合物可能是其共附生微生物產生的,這些活性代謝物在海綿的生理代謝和生存防御中起著至關重要的作用,對海綿共附生放線菌的研究將豐富海洋天然產物的多樣性,為海洋藥物的研發提供科學基礎。

