重組人促紅細胞生成素治療急性腦梗死療效觀察
張瀟文
山東國欣頤養集團淄博醫院神經內一科,山東淄博 255100
急性腦梗死(cerebral infarction)是神經內科常見疾病之一,病情嚴重者有神經功能障礙等并發癥,嚴重影響人們健康[1]。近年來急性腦梗死的治療取得了很大的進展,腦組織缺血后神經功能的保護也越來越被重視,尋找新型的腦保護藥物成為研究的熱點[2]。重組人促紅細胞生成素(recombinant human erythropoietin,rHu-EPO)作為一種新型神經保護因子,廣泛用于各種貧血治療,取得了很好的臨床效果[3],有相關報道指出它對心臟、腎臟及中樞神經系統有良好的保護作用[4-6],推測其可能對治療急性腦梗死具有一定的療效。血清神經元特異性烯醇化酶(neuron specific enolase,NSE)和 S-100β蛋白是一類存在于神經細胞、神經內分泌細胞及神經膠質細胞中的亞細胞成分,作為神經損傷的標志物具有較高的特異性和敏感性,越來越多地應用于臨床診斷和評估預后。
本研究是在急性腦梗死患者常規治療的基礎上,觀察rHu-EPO對急性腦梗死患者血清NSE和S-100β蛋白水平的影響,并評價治療前后患者臨床神經功能的恢復,探討rHu-EPO對急性腦梗死患者的治療效果,尋求治療急性腦梗死的新方法。現報道如下。
1 資料與方法
1.1 一般資料
收集2018年2—8月我院神經內科急性腦梗死患者92例,年齡40~82歲,平均(62.24±15.51)歲,其中男55例,女37例。納入標準:所有患者根據2014年中華醫學會神經病學分會發表的《中國急性缺血性腦卒中診治指南》[7]的診斷標準,經頭部CT掃描確診為急性腦梗死。排除標準:①入院后即行溶栓治療者;②合并腦腫瘤或合并其他重要臟器疾病或既往神經功能障礙者;③紅細胞增多癥或嚴重高血壓未能有效控制者;④嚴重缺鐵或鐵代謝障礙;⑤對本試驗理想期望值過高或有不切實際要求者;⑥不同意EPO治療者。本研究方案經醫院醫學倫理委員會討論通過后授權,所有患者家屬或法定監護人簽署知情同意書。隨機分為EPO治療組(n=43)與對照組(n=41)。92例患者中有8例(好轉出院5例,患者及家屬中途拒絕繼續治療3例)退出研究,其中EPO治療組患者4例,對照組患者4例。最終共計84例患者進入統計學分析。EPO治療組43例,其中男27例,女16例,平均年齡(60.87±16.19)歲;對照組41例,其中男24例,女17例,平均年齡(62.15±17.63)歲。兩組患者的性別、年齡等一般資料比較,差異均無統計學意義(P>0.05),具有可比性。
1.2 方法
所有患者入院后按照急性腦梗死臨床路徑規范治療。兩組患者常規均口服阿司匹林腸溶片(商品名:拜阿司匹靈,規格:100 mg/片)100 mg,1次/d;氫氯吡格雷片(商品名:波立維,規格:75 mg/片)75mg,1次/d;阿托伐他汀鈣片(商品名:立普妥,規格:20 mg/片)20 mg,每晚1次。在此基礎上,治療組患者加用重組人促紅素(rHu-EPO)(上海凱茂生物醫藥有限公司生產,生產批號:E20170765,規格:3000 IU/支),于入院當天、第3、6、9、12天給予3000 IU皮下注射。兩組治療時間均為14 d。
1.3 觀察指標及評價標準
①NSE及S-100β的濃度:所有患者均在入院后第 1、4、7、10、14 天清晨空腹采集靜脈血,30 min內離心取上清液,-70℃保存。酶聯免疫吸 附 測 定(enzyme-linked immuno sorbent assay,ELISA)法進行檢測。NSE正常值為<13 ng/ml,S-100β正常值為<0.2 ng/ml。②NIHSS評分。入院時和治療后14 d由專人依照美國國立衛生院卒中量表(the National institutes of health stroke scale,NIHSS)[8]對所有患者行神經功能缺損評分。NIHSS評分內容包括11個評估項目,分別為意識水平程度、水平眼球運動、視野、面癱、上肢運動功能、下肢運動功能、共濟失調、感覺、語言、構音和忽視,每個項目計分分為3~5個等級,評分范圍0~42分,得分越高表示神經功能受損程度越嚴重。0~1分:正常或趨于正常;2~4分:輕度神經功能缺損;5~14分:中度神經功能缺損;15~20分:中重度神經功能缺損;21~42分:重度神經功能缺損。③監測治療前后患者的血壓(收縮壓、舒張壓)、血紅蛋白(haemoglobin,Hb)含量。④觀察EPO治療組有無可能和應用EPO導致的發熱、皮疹、瘙癢等副作用出現。
1.4 統計學處理
使用SPSS 17.0統計學軟件對數據進行分析,計量資料用()表示,同組治療前后數據比較采用t檢驗,兩組間數據比較采用t檢驗,重復測量數據采用方差分析,多樣本均數兩兩比較采用SNK-Q檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者NSE和S-100β蛋白比較
急性腦梗死患者患病后1 d、4 d,兩組患者血清中NSE、S-100β蛋白均明顯升高,兩組間比較無統計學意義(P>0.05)。隨著患病時間的延長,在治療后7、10、14 d,EPO治療組患者血清中NSE、S-100β蛋白含量降低明顯,與對照組比較,差異有統計學意義(P<0.05),見表1。
表1 兩組患者NSE和S-100β蛋白比較(,ng/ml)

表1 兩組患者NSE和S-100β蛋白比較(,ng/ml)
注:NSE-EPO 治療組:4 d vs. 1 d,q=1.581,P=0.089;7 d vs. 1 d,q=5.377,P=0.000;10 d vs. 1 d,q=6.272,P=0.000;14 d vs. 1 d,q=7.853,P=0.000;NSE 對照組:4 d vs. 1 d,q=1.479,P=0.156;7 d vs. 1 d,q=4.910,P=0.000;10 d vs. 1 d,q=5.843,P=0.000;14 d vs. 1 d,q=8.351,P=0.000;S-100β -EPO治療組:4 d vs. 1 d,q=2.318,P=0.053;7 d vs. 1 d,q=5.157,P=0.000;10 d vs. 1 d,q=6.542,P=0.000;14 d vs. 1 d,q=8.861,P=0.000;S-100β 對照組:4 d vs. 1 d,q=1.376,P=0.169;7d vs. 1 d,q=3.973,P=0.028;10 d vs. 1 d,q=4.596,P=0.001;14 d vs. 1 d,q=6.373,P=0.000
NSE治療后1 d 治療后4 d 治療后7 d 治療后10 d 治療后14 d F值 P值EPO 治療組 43 39.72±5.68 37.52±6.19 23.95±4.58 19.37±3.24 16.37±3.84 208.100 0.000對照組 41 38.06±5.57 36.37±5.11 29.95±4.01 26.37±3.10 24.37±2.59 83.100 0.000 t值 1.352 0.926 6.376 10.110 11.140 P值 0.180 0.357 0.000 0.000 0.000組別 n S-100β治療后1 d 治療后4 d 治療后7 d 治療后10 d 治療后14 d F值 P值EPO 治療組 43 0.28±0.06 0.25±0.08 0.21±0.06 0.18±0.04 0.16±0.04 1448.000 0.000對照組 41 0.27±0.07 0.25±0.06 0.24±0.05 0.22±0.06 0.19±0.05 11.150 0.000 t值 0.704 0.000 2.483 3.611 3.044 P值 0.483 0.999 0.015 0.001 0.003組別 n
2.2 兩組患者治療前后NIHSS評分比較
EPO治療組與對照組NIHSS評分在治療前比較,差異無統計學意義(P>0.05)。治療14 d后,兩組均低于治療前(P<0.05),EPO治療組低于對照組,差異有統計學意義(P<0.05),見表2。
表2 兩組患者治療前后NIHSS評分比較(,分)
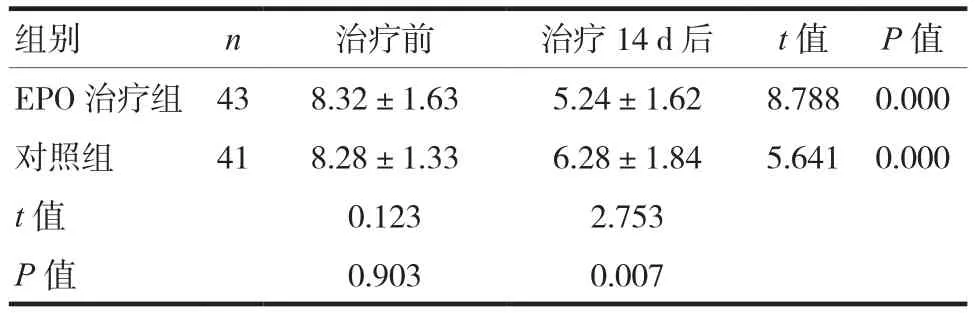
表2 兩組患者治療前后NIHSS評分比較(,分)
組別 n 治療前 治療14 d后 t值 P值EPO治療組 43 8.32±1.63 5.24±1.62 8.788 0.000對照組 41 8.28±1.33 6.28±1.84 5.641 0.000 t值 0.123 2.753 P值 0.903 0.007
2.3 兩組患者血壓、血紅蛋白及副作用比較
EPO治療組與對照組的血壓和血紅蛋白在治療前及治療14 d后比較,差異均無統計學意義(P>0.05)。治療14 d后,EPO治療組患者血壓及血紅蛋白數值均高于對照組,但差異無統計學意義(P>0.05),見表3。同期觀察EPO治療組患者,未發現可能由EPO導致的發熱、皮疹、瘙癢、面部發紅等副作應。
表3 兩組患者治療前后血壓及血紅蛋白含量比較()

表3 兩組患者治療前后血壓及血紅蛋白含量比較()
組別 n 收縮壓(mmHg) 舒張壓(mmHg) Hb含量(g/L)治療前 治療14 d后 t值 P值 治療前 治療14 d后 t值 P值 治療前 治療14 d后 t值 P值EPO治療組 43130.13±33.62124.27±26.320.9000.37193.47±18.7089.59±15.731.0410.301110.80±8.34114.52±9.231.9610.053對照組 41127.96±26.87119.54±22.831.5290.13094.12±20.6286.76±17.441.7450.085111.63±8.72113.88±7.321.8280.071 t值 0.329 0.878 0.152 0.782 0.446 0.351 P值 0.745 0.383 0.880 0.437 0.657 0.727
3 討論
急性腦梗死是指由各種原因引起的局部腦組織區域血液循環障礙,導致缺血、缺氧,發生缺血性壞死或軟化,形成不可逆性損害,從而導致對應的神經功能障礙的臨床事件,傳統上稱為“缺血性腦卒中”。腦梗死具有高發病率、高致殘率及致死率,嚴重影響人們健康,加重家庭和社會的負擔[1]。急性腦梗死發生后最佳的治療為立即溶栓治療,但溶栓治療受發病送至時間、醫療水平條件、患者狀況以及梗死類型等條件的制約,很多患者因為上述各種原因未能第一時間接受溶栓治療。對于這部分患者,如何在現有常規藥物治療基礎上,尋找更加有效的治療手段,成為目前研究的新熱點[2]。
促紅細胞生成素(EPO)是一種調節紅細胞生成的高糖蛋白類激素。成人EPO在腎臟合成,分泌進入血液系統,主要作用于骨髓的造血干細胞,刺激造血干細胞向紅細胞分化,神經系統中EPO受體主要存在于神經細胞、膠質細胞和血管內皮細胞[3]。有研究報道在腦缺血或腦組織代謝障礙時,EPO能夠保護神經元,提高神經元存活能力[6]。Vinberg等[9]研究發現EPO可以促進紅細胞產生,提高血氧濃度含量,改善局部組織的缺血、缺氧,并減少IL-6、TNF等炎癥介質產生,減少細胞凋亡,發揮神經保護功效。但對于急性腦梗死的患者,患病后短時間內不能產生足夠有效的內源性EPO,因此給予外源性EPO非常有必要[10]。而rHu-EPO與EPO具有同樣生物學作用。有研究發現rHu-EPO可以改善急性腦梗死患者的部分認知功能障礙,并認為其機制可能與rHu-EPO有助于促進新生血管成熟為功能血管,增強血管的生成及組織的可塑性有關[11]。國內肖以磊等[12]研究表明在顱腦損傷患者的治療中給予應用rHu-EPO,可以顯著改善重型顱腦損傷患者的神經功能及預后,取得良好的效果。本研究在急性腦梗死患者接受常規藥物治療的基礎上,額外給予rHu-EPO,評價治療前后患者臨床神經功能的恢復,觀察到rHu-EPO對急性腦梗死患者的治療有一定的效果。
NSE及S-100β蛋白是中樞神經系統損傷的特異性標志物。NSE是神經元和神經內分泌細胞的一個標志酶,神經細胞受損崩解會引起NSE釋放入血,使血清中NSE濃度升高[13]。S-100β蛋白是主要存在于星形膠質細胞中的酸性鈣結合蛋白,當神經細胞受損后,S-100β蛋白也會從胞液中滲出進入腦脊液及血液[14],因此兩者的水平可以反映神經細胞和神經膠質細胞的損害程度。大量國內外關于腦梗死后血清NSE、S-100β等炎性因子水平變化的研究[15]表明,腦梗死急性期血清NSE、S-100β濃度升高,其升高水平與腦梗死體積大小和病情嚴重程度呈正相關,因此可將NSE及S-100β作為急性腦梗死臨床研究評估預后的觀測指標。本研究發現,治療組經注射rHu-EPO,對急性腦梗死起到了顯著的治療作用,EPO組治療后7、10、14 d時血清NSE、S-100β蛋白水平均低于對照組,NIHSS評分較常規治療組也有明顯降低,結果均提示經rHu-EPO治療能減輕急性腦梗死的臨床癥狀,改善神經功能預后。
長期大量使用rHu-EPO會產生血壓升高、血紅蛋白升高、血黏度增加、血栓形成等副作用。有些患者會有發熱、皮疹、瘙癢、面部發紅等反應。本研究采用低劑量的rHu-EPO治療,療程14 d,治療效果滿意,患者的血壓和血紅蛋白含量雖然有所升高,但與對照組之間差異無統計學意義,可能與使用劑量、用藥時間有關。在全部研究過程中,也未發現與rHu-EPO有明顯相關的發熱、皮疹、瘙癢等不良反應。但本組病例數量較少,在后續研究中將會加大例數并進一步觀察。
目前rHu-EPO已廣泛應用于各種貧血的治療,效果確切,臨床不良反應少。在本研究中用于治療急性腦梗死,可以顯著降低患者的血清NSE和S-100β蛋白,降低NIHSS評分,改善神經功能及預后。研究過程中沒有發現明顯的不良反應,安全性較好。本研究結果表明,rHu-EPO對急性腦梗死有明確的治療作用,有希望為急性腦梗死的臨床治療提供新的方法。

