lncRNA VIM-AS1靶向miR-126-5p調(diào)控肺癌細(xì)胞放射敏感性分子機制研究
馬莉莎 王嶸 柴麗霞
肺癌(lung cancer)是世界上發(fā)病率最高的癌癥,患者5年生存率<15%,放療是其重要治療手段之一,患者后期產(chǎn)生的放射耐受是影響臨床治療效果的主要原因之一[1,2]。越來越多的研究證實,lncRNA(long non-coding RNA)和miRNA(micro RNA)在肺癌組織、細(xì)胞或體液中表達異常,通過EMT等途徑參與肺癌的發(fā)生發(fā)展、放化療耐受、預(yù)后及靶向治療等[3-5]。報道顯示,lncRNA VIM-AS1(VIM antisense RNA 1,VIM-AS1) 在前列腺癌和結(jié)直腸癌中高表達,下調(diào)其表達可抑制癌細(xì)胞的增殖等過程[6,7]。本研究通過startBase預(yù)測發(fā)現(xiàn),miR-126-5p可能是VIM-AS1的靶基因。miR-126-5p在肺腺癌組織和患者外周血中含量降低,與患者預(yù)后有關(guān)[8]。細(xì)胞凋亡是放療誘導(dǎo)腫瘤細(xì)胞死亡的主要機制,細(xì)胞凋亡的增加利于增強放療敏感性[9]。而VIM-AS1和miR-126-5p在提高肺癌放射敏感性中的作用及相互關(guān)系目前尚不清楚。本課題主要研究lncRNA VIM-AS1對A549細(xì)胞放射敏感性的影響,以及miR-126-5p在其中的作用,為肺癌臨床放療敏感性研究提供新的數(shù)據(jù)。
1 材料與方法
1.1 試劑與儀器 人正常肺上皮細(xì)胞BEAS-2B及人肺癌細(xì)胞A549、SPCA1和HCI-H596細(xì)胞購自中科院上海細(xì)胞庫;胎牛血清(fetal bovine serum,FBS)和DMEM高糖培養(yǎng)基購自美國Gibco公司,牛血清白蛋白(Bovine Serum Albumin,BSA)、胰蛋白酶Trypsin購自Sigma-Aldrich公司;雙熒光素酶報告系統(tǒng)(Dual-Luciferase Reporter Assay System)購自美國Promega公司;引物、miR-126-5p mimics(miR-126-5p)、miR-126-5p抑制劑(anti-miR-126-5p)、VIM-AS1干擾物(si-VIM-AS1)、空載體和對照物(miR-con、anti-NC和si-NC)及VIM-AS1突變型和野生型雙熒光素酶載體購自上海吉瑪制藥技術(shù)有限公司;Lipofectamine 2000轉(zhuǎn)染試劑、Total RNA提取試劑盒、real-time PCR 試劑盒、反轉(zhuǎn)錄試劑盒(RT-PCR)購自寶生物工程(大連)有限公司;Real-time PCR儀購自美國Bio-Rad公司;BCA蛋白試劑盒購自江蘇凱基生物技術(shù)股份有限公司。
1.2 方法
1.2.1 細(xì)胞培養(yǎng):將人正常肺上皮細(xì)胞BEAS-2B及人肺癌細(xì)胞A549、SPCA1和HCI-H596培養(yǎng)在含10% FBS的DMEM高糖培養(yǎng)液(添加100 U/ml青霉素和100 μg/ml鏈霉素)中,37℃ 5% CO2培養(yǎng)箱中培養(yǎng),濕度95%,將細(xì)胞培養(yǎng)至對數(shù)生長期,消化傳代。
1.2.2 細(xì)胞轉(zhuǎn)染:收集對數(shù)生長期的A549細(xì)胞,用培養(yǎng)液將細(xì)胞稀釋至1×106個/ml,以200 μl細(xì)胞/孔的密度接種于6孔板中,細(xì)胞培養(yǎng)至基本融合為一層時進行轉(zhuǎn)染。根據(jù)Lipofectamine 2000轉(zhuǎn)染試劑說明書進行轉(zhuǎn)染操作,將不同的載體轉(zhuǎn)染入培養(yǎng)好的A549細(xì)胞中,培養(yǎng)6 h后換成DMEM高糖完全培養(yǎng)基,轉(zhuǎn)染48 h后收集細(xì)胞進行實驗。根據(jù)轉(zhuǎn)染載體進行分組:si-NC組和si-VIM-AS1組、miR-con組和miR-126-5p組、si-VIM-AS1+anti-NC組和si-VIM-AS1+anti-miR-126-5p組。qRT-PCR檢測VIM-AS1和miR-126-5p的表達收集培養(yǎng)好的BEAS-2B、A549、SPC A1和HCI-H596細(xì)胞,用試劑盒提取細(xì)胞總RNA,測定濃度和純度,然后按照反轉(zhuǎn)錄試劑盒說明書合成cDNA,以cDNA為模板按照 real-time PCR的說明書進行反應(yīng)合成miR-126-5p和VIM-AS1,反應(yīng)程序為:95℃ 2 min;95℃ 15 s、55℃ 40 s、72℃ 30 s,35個循環(huán),用2-ΔΔCt方法進行數(shù)據(jù)分析。
1.2.3 克隆形成實驗:測定放射處理后細(xì)胞存活分?jǐn)?shù)收集轉(zhuǎn)染后的對數(shù)生長期各組A549細(xì)胞,消化并計數(shù),然后接種于6孔板,過夜培養(yǎng)。然后將細(xì)胞暴露于不同輻射劑量下(0、2、4、6、8 Gy)進行照射處理。輻射處理后細(xì)胞以500個/皿接種于細(xì)胞培養(yǎng)皿中,加入10 ml培養(yǎng)液混勻,培養(yǎng)10~14 d至出現(xiàn)肉眼清晰可見的細(xì)胞克隆,洗滌細(xì)胞2次,甲醛固定細(xì)胞,結(jié)晶紫染色,計數(shù),細(xì)胞克隆數(shù)>50個為有效。根據(jù)單擊多靶模型擬合細(xì)胞存活曲線,計算放射增敏比(SER)。細(xì)胞克隆形成率 = (克隆數(shù)平均值/鋪板細(xì)胞總數(shù))×100%,細(xì)胞存活分?jǐn)?shù)(survival fraction,SF) = 受照射細(xì)胞克隆形成率/對照細(xì)胞克隆形成率)×100%。
1.3 流式細(xì)胞術(shù)測定細(xì)胞凋亡率 手機轉(zhuǎn)染和(或)放射處理后培養(yǎng)48 h的各組A549細(xì)胞,接種于6孔板,培養(yǎng)72 h后棄去培養(yǎng)液,洗滌細(xì)胞并胰酶消化,離心收集細(xì)胞,按照 Annexin V/PI 凋亡試劑盒說明書進行操作,用流式細(xì)胞儀檢測細(xì)胞凋亡率。
1.4 雙熒光素酶報告實驗 按照方法1.2.2培養(yǎng)A549細(xì)胞和轉(zhuǎn)染,分別將構(gòu)建好的VIM-AS1的野生型(WT-VIM-AS1)和突變型(MUT-VIM-AS1)雙熒光素酶報告載體與miR-con或miR-126-5p共轉(zhuǎn)染A549細(xì)胞,轉(zhuǎn)染后培養(yǎng)48 h,收集細(xì)胞,將細(xì)胞裂解,離心收集裂解上清。發(fā)光儀檢測熒光素酶活性,以海腎熒光素酶活性為內(nèi)參照,計算相對螢火蟲熒光素酶活性。
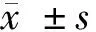
2 結(jié)果
2.1 肺癌細(xì)胞中VIM-AS1高表達miR-126-5p低表達 與正常肺上皮細(xì)胞BEAS-2B組比較,肺癌細(xì)胞A549、SPC A1和HCI-H596組中VIM-AS1含量均顯著升高(P<0.05),miR-126-5p的含量均顯著降低(P<0.05)。根據(jù)實驗結(jié)果,選擇A549進行后續(xù)實驗。見表1。

表1 VIM-AS1 和miR-126-5p 在肺癌細(xì)胞中的表達
2.2 沉默VIM-AS1對肺癌細(xì)胞A549的放射敏感性的影響 沉默lncRNA VIM-AS1后,克隆形成實驗結(jié)果表明,隨著照射劑量的增加,與si-NC組比較,si-VIM-AS1組A549的細(xì)胞存活分?jǐn)?shù)逐漸下降,且差異有統(tǒng)計學(xué)意義(P<0.05),放射增敏比為1.776。選擇具有顯著差異且對細(xì)胞傷害小的照射劑量2Gy進行后續(xù)實驗。見表2、3,圖1。

表2 沉默VIM-AS1 對A549 細(xì)胞的存活分?jǐn)?shù)(% )的影響

表3 沉默VIM-AS1 后單擊多靶模型的參數(shù)值
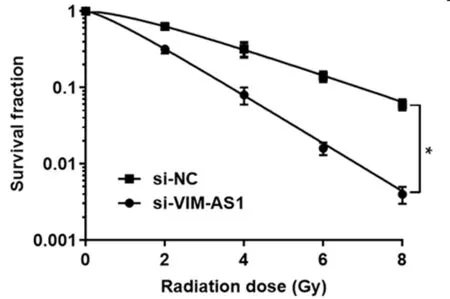
圖1 沉默VIM-AS1對肺癌細(xì)胞A549的放射敏感性的影響
2.3 沉默VIM-AS1對輻射照射誘導(dǎo)的A549細(xì)胞凋亡的影響 與Control組和si-NC組比較,2 Gy處理后,si-VIM-AS1組的肺癌A549細(xì)胞凋亡率顯著上升(P<0.05);與Control+Gy和si-NC+Gy組比較,si-VIM-AS1+Gy組A549細(xì)胞凋亡率也顯著升高(P<0.05)。表明沉默VIM-AS1可增加肺癌A549細(xì)胞的放射敏感性并促進細(xì)胞凋亡。見圖2,表4。
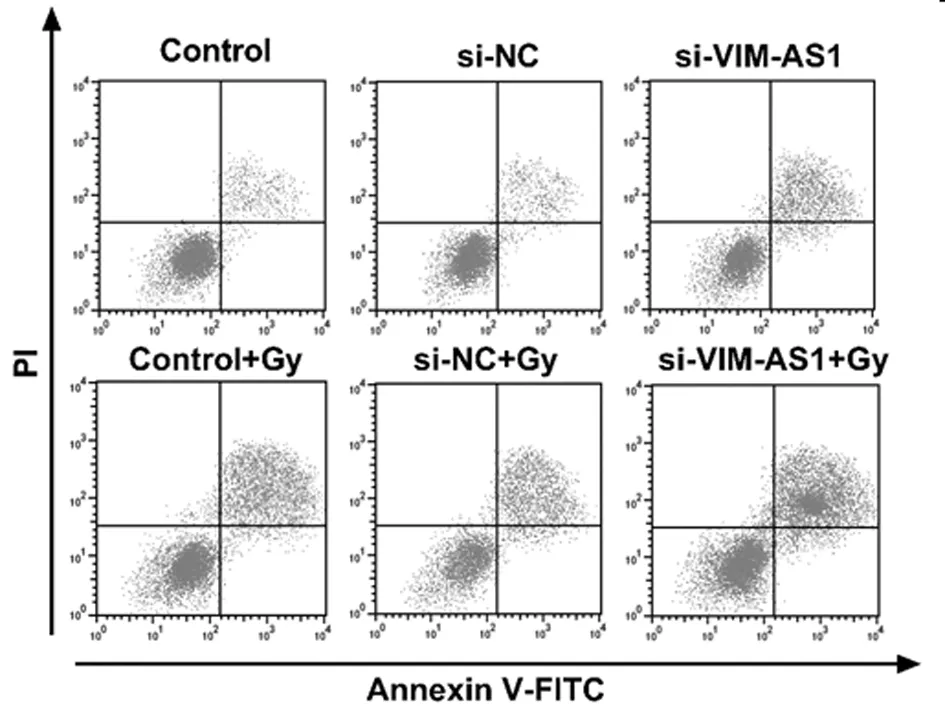
圖2 沉默VIM-AS1對2 Gy輻射處理后HCT116細(xì)胞凋亡的影響
2.4 VIM-AS1負(fù)調(diào)控miR-126-5p的表達 startBase預(yù)測結(jié)果顯示,miR-126-5p的序列中含有與VIM-AS1互補的核苷酸位點。雙熒光素酶報告顯示,與miR-con組比較,過表達miR-126-5p可下調(diào)野生型WT-

表4 沉默VIM-AS1 后6 組A549 細(xì)胞的凋亡率
VIM-AS1的螢火蟲熒光素酶相對活性(P<0.05);而突變型MUT-VIM-AS1的螢火蟲熒光素酶相對活性沒有明顯變化。qRT-PCR結(jié)果顯示,下調(diào)VIM-AS1表達可上調(diào)miR-126-5p含量(P<0.05)。說明VIM-AS1靶向負(fù)調(diào)控miR-126-5p的表達。見圖3,表5、6。

圖3 VIM-AS1與miR-126-5p互補結(jié)合的核苷酸位點

表5 雙熒光素酶試驗驗證VIM-AS1 與miR-126-5p 靶向結(jié)合

表6 lncRNA VIM-AS1 負(fù)調(diào)控miR-126-5p 的表達
2.5 VIM-AS1對miR-126-5p調(diào)控結(jié)肺癌細(xì)胞A549的放射敏感性的影響 為確認(rèn)lncRNA VIM-AS1調(diào)控miR-126-5p,在沉默VIM-AS1的同時抑制miR-126-5p,結(jié)果表明,2Gy放射處理后,與si-VIM-AS1+anti-NC組比較,si-VIM-AS1+ anti-miR-126-5p+Gy組的A549細(xì)胞存活分?jǐn)?shù)顯著升高(P<0.05),細(xì)胞增敏比為0.598,細(xì)胞凋亡率顯著降低(P<0.05),與2.2和2.3結(jié)果相反。說明抑制miR-126-5p表達可逆轉(zhuǎn)沉默VIM-AS1對A549細(xì)胞放射敏感性和凋亡的作用。見表7、8,圖4、5。
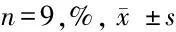
表7 抑制miR-126-5p 逆轉(zhuǎn)了沉默VIM-AS1 對A549細(xì)胞放射敏感性的影響
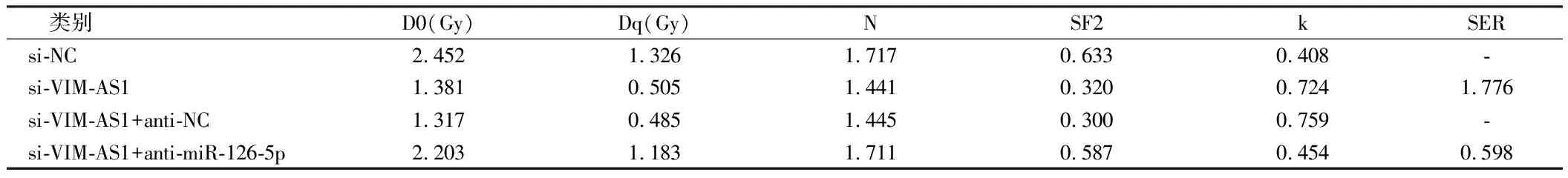
表8 抑制miR-126-5p 聯(lián)合沉默VIM-AS1 后單擊多靶模型的參數(shù)值
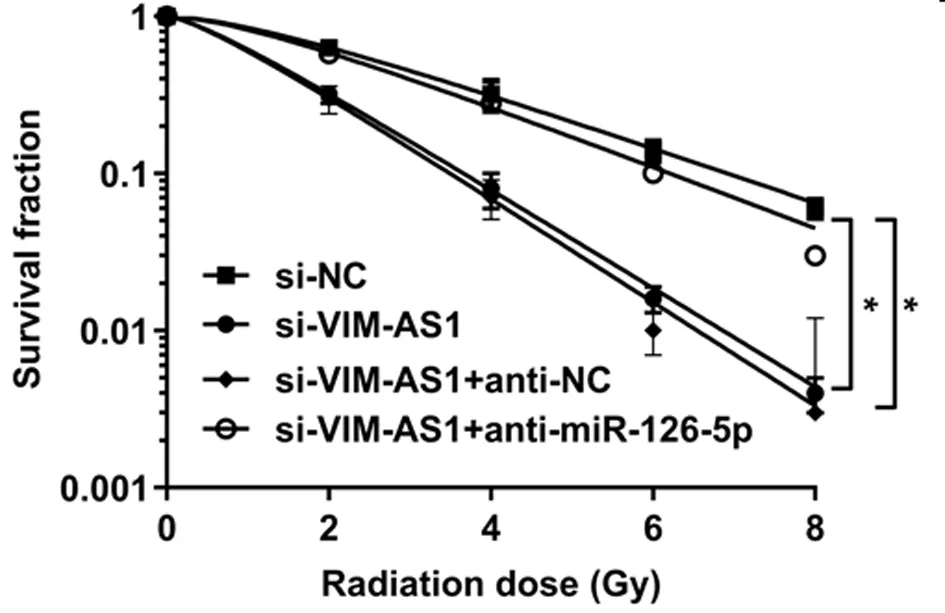
圖4 沉默VIM-AS1增加肺癌細(xì)胞A549的放射敏感性
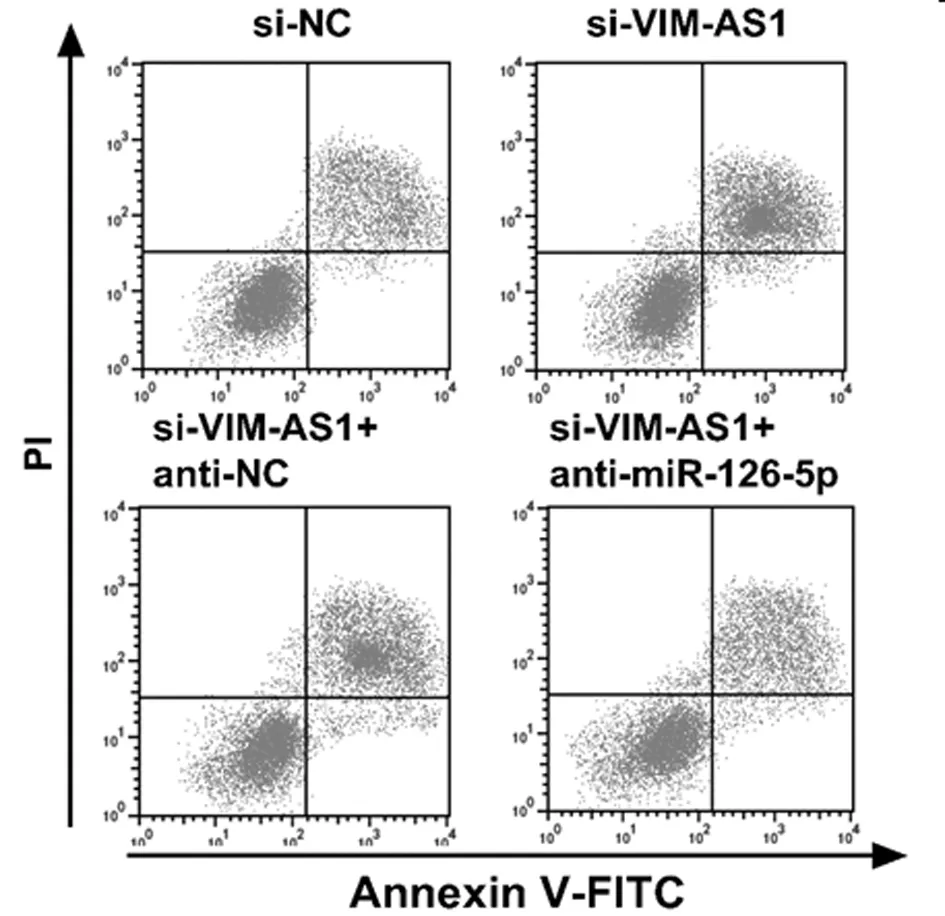
圖5 抑制miR-126-5p逆轉(zhuǎn)了沉默VIM-AS1對輻射照射A549細(xì)胞凋亡率的影響
3 討論
多項研究表明,lncRNA可通過miRNA在肺癌的放射敏感性中發(fā)揮重要作用[10-12]。有研究發(fā)現(xiàn),lncRNA VIM-AS1在前列腺癌中通過EMT調(diào)控癌細(xì)胞的增殖和侵襲[6],lncRNA VIM-AS1還通過EMT促進結(jié)直腸癌的進展和轉(zhuǎn)移[7]。lncRNA VIM-AS1在2型糖尿病和子癇前期也發(fā)揮重要作用[13,14],但其在肺癌細(xì)胞中的表達及其對肺癌放射敏感性的作用尚不清楚。本研究結(jié)果表明,VIM-AS1在肺癌細(xì)胞A549、SPC A1和HCI-H596中含量均顯著升高,不同放射劑量(0、2、4、6、8 Gy)處理A549細(xì)胞,細(xì)胞存活分?jǐn)?shù)逐漸下降,用影響較小的2 Gy處理A549細(xì)胞,細(xì)胞凋亡率也顯著升高,放射增敏比為1.776,說明沉默VIM-AS1可增強A549細(xì)胞放射敏感性并促進其凋亡,從而抑制肺癌細(xì)胞生長。
此外,本研究通過startbase預(yù)測發(fā)現(xiàn),miR-126-5p與VIM-AS1存在結(jié)合位點,其可能是VIM-AS1的靶基因。因此,本研究假設(shè)VIM-AS1通過靶向miR-126-5p影響肺癌細(xì)胞的放射敏感性。miR-126-5p是miR-126的成熟形式,位于第9號染色體,是來源于EGFL-7的保守型內(nèi)含子miRNA,主要在內(nèi)皮細(xì)胞中表達,在多種癌癥中異常表達,與腫瘤的發(fā)生發(fā)展密切相關(guān)[15]。miR-126-5p在胃癌細(xì)胞SGC-7901中可靶向EZH2增加胃癌細(xì)胞的放射敏感性[16]。miR-126-5p在非小細(xì)胞肺癌(NSCLC)中低表達,其過表達可抑制細(xì)胞中蘋果酸脫氫酶1(MDH1)的酶活性、線粒體呼吸并導(dǎo)致細(xì)胞死亡[17]。且有研究表明,在NSCLC患者放療敏感組中miR-126表達上調(diào)[18],miR-126通過PI3K-Akt途徑促進輻射誘導(dǎo)的NSCLC細(xì)胞凋亡[19]。以上結(jié)果均說明miR-126-5p對癌細(xì)胞的放療敏感性具有重要作用。本研究結(jié)果發(fā)現(xiàn),miR-126-5p在肺癌細(xì)胞A549、SPC A1和HCI-H596中含量均顯著下調(diào),與上述結(jié)果[17]一致;雙熒光素酶報告系統(tǒng)和qRT-PCR結(jié)果顯示,在A549細(xì)胞中,VIM-AS1靶向負(fù)調(diào)控miR-126-5p的表達,本研究還發(fā)現(xiàn),抑制miR-126-5p表達同時沉默VIM-AS1后A549細(xì)胞細(xì)胞存活分?jǐn)?shù)顯著升高,凋亡率顯著降低,細(xì)胞增敏比為0.598,逆轉(zhuǎn)沉默VIM-AS1對A549細(xì)胞凋亡和放射敏感性的影響,間接證實了二者在A549細(xì)胞中具有調(diào)控過程,并可增強細(xì)胞放射敏感性。
綜上所述,本研究闡述了在肺癌細(xì)胞A549、SPC A1和HCI-H596中l(wèi)ncRNA VIM-AS1上調(diào),miR-126-5p下調(diào),在肺癌A549細(xì)胞中l(wèi)ncRNA VIM-AS1靶向miR-126-5p調(diào)控A549細(xì)胞凋亡和放射敏感性。lncRNA VIM-AS1可能是肺癌的放射增敏靶點。

