Fas對鎘激活PC12細胞線粒體凋亡通路的影響
聞雙全,陳 潔,王 莉,鄒 輝,顧建紅,劉學(xué)忠,卞建春,劉宗平,袁 燕*
(1.揚州大學(xué)獸醫(yī)學(xué)院,揚州 225009; 2.江蘇高校動物重要疫病與人獸共患病防控協(xié)同創(chuàng)新中心, 揚州 225009; 3.江蘇省南通市動物疫病預(yù)防控制中心,南通 226011)
鎘是環(huán)境中常見的重金屬污染物,可經(jīng)皮膚、消化道和呼吸道進入人、畜體內(nèi)。進入機體內(nèi)的鎘排泄率極低,其生物半衰期長達10~30年。腦是鎘毒性作用的重要靶器官之一,鎘可增加血腦屏障通透性并進入大腦[1]。本實驗室前期研究發(fā)現(xiàn),鎘可在大鼠大腦皮質(zhì)內(nèi)蓄積[2]。大量研究表明,鎘可造成人和動物神經(jīng)系統(tǒng)功能障礙[3-5]。鎘致神經(jīng)系統(tǒng)毒性機制主要包括誘導(dǎo)氧化應(yīng)激、凋亡和自噬[6-7]。其中,細胞凋亡是鎘致神經(jīng)毒性的重要機制之一。
細胞凋亡是由基因調(diào)控的一種細胞程序性死亡,在調(diào)節(jié)細胞穩(wěn)態(tài)和多細胞生物發(fā)育過程中起著重要作用。Fas是腫瘤壞死因子受體超家族的一員,通過與其配體FasL結(jié)合在多種細胞凋亡中發(fā)揮關(guān)鍵作用[8-10]。當細胞受到凋亡刺激時, FasL與Fas結(jié)合,并通過進一步與Fas相關(guān)死亡結(jié)構(gòu)域蛋白(FADD)結(jié)合,激活半胱氨酸蛋白酶-8(caspase-8),引起細胞凋亡[11];另外,活化的caspase-8可剪切BH3相互作用域死亡激動劑(BID),誘導(dǎo)線粒體釋放細胞色素C(Cyt C),介導(dǎo)線粒體凋亡通路[12]。
本實驗室前期研究發(fā)現(xiàn)鎘可通過激活Fas/FasL通路和線粒體通路誘導(dǎo)神經(jīng)細胞凋亡[13-14]。但是,這兩條通路之間的關(guān)系以及Fas在鎘致神經(jīng)細胞凋亡線粒體通路中的作用和調(diào)控機制尚未完全闡明。本試驗以Fas基因沉默的大鼠腎上腺嗜鉻細胞瘤細胞(PC12)為模型,用鎘進行處理,通過Western blot、免疫熒光染色等方法探究Fas在鎘致PC12細胞凋亡中的作用及其對線粒體通路的調(diào)控機制,為揭示鎘的神經(jīng)毒性機制提供理論依據(jù)。
1 材料與方法
1.1 細胞
PC12細胞購自中國科學(xué)院上海生命科學(xué)研究院細胞庫。Fas基因沉默PC12細胞株(Fas shRNA組,靶序列:5′-GATCCGGTGCGTGTCAAGCT TTAATCTTCAAGAGAGATTAAAGCTTGACA CGCACCTTTTTTA-3′)和插入非特異性序列的對照細胞株(NC組)由實驗室構(gòu)建篩選獲得。
1.2 主要試劑與儀器
RPMI 1640、馬血清和胎牛血清購自Life Technologies公司;L-谷氨酰胺和青鏈霉素購自BBI公司;醋酸鎘和L-多聚賴氨酸購自Sigma公司;細胞線粒體分離試劑盒、Cy 3標記山羊抗兔熒光二抗和DAPI染色液購自碧云天生物技術(shù)研究所;凋亡誘導(dǎo)因子(AIF)和核酸內(nèi)切酶G(Endo G)兔多克隆抗體購自Abcam公司;Bcl-2相關(guān)X蛋白(Bax)、B細胞淋巴瘤/白血病-2基因(Bcl-2)、Cyt C、細胞色素C氧化酶亞基Ⅳ(COX-Ⅳ)、活化半胱氨酸蛋白酶-9(cleaved caspase-9)、活化半胱氨酸蛋白酶-3(cleaved caspase-3)、活化多聚二磷酸腺苷核糖聚合酶(cleaved PARP)、β-actin兔單克隆抗體和辣根過氧化物酶標記山羊抗兔二抗購自CST公司;BID兔多克隆抗體購自Novus公司;其余試劑均為國產(chǎn)分析純。
二氧化碳培養(yǎng)箱購自美國Thermo公司;5810R型低溫高速冷凍離心機購自德國Eppendorf公司;電泳儀、轉(zhuǎn)膜儀購自美國BIORAD公司;激光共聚焦顯微鏡購自德國Leica公司。
1.3 細胞的培養(yǎng)與處理
Fas基因沉默的PC12細胞株和對照細胞株接種于RPMI 1640培養(yǎng)基(含10%馬血清、5%胎牛血清、1%L-谷氨酰胺、1%青鏈霉素),置于37 ℃和5% CO2環(huán)境的培養(yǎng)箱中培養(yǎng),當細胞生長狀態(tài)良好且處于對數(shù)生長期時,用10 μmol·L-1Cd處理細胞12 h,分別命名為對照組(NC組)、鎘組(Cd組)、Fas shRNA干擾組(Fas shRNA組)、Fas shRNA與鎘共處理組(Fas shRNA+Cd組)。
1.4 細胞總蛋白、胞漿蛋白和線粒體蛋白的提取
收集各組細胞,加入適量含有蛋白酶抑制劑的細胞裂解液,冰上裂解30 min,超聲裂解20 s;4 ℃,12 000 g·min-1離心10 min,收集上清即為總蛋白。
收集各組細胞,加入適量含有蛋白酶抑制劑的線粒體分離試劑重懸細胞團塊,將細胞懸液轉(zhuǎn)移至預(yù)冷的玻璃勻漿器中,冰上研磨,隨后將勻漿轉(zhuǎn)移至預(yù)冷的離心管,4 ℃,600 g·min-1離心10 min,吸取上清至新的離心管,4 ℃,11 000 g·min-1離心10 min,收集上清即為細胞漿蛋白,沉淀為線粒體;向沉淀中加入適量含有蛋白酶抑制劑的線粒體裂解液,冰上裂解30 min,12 000 g·min-1離心10 min,收集上清即為線粒體蛋白。
使用BCA法測定蛋白濃度并將蛋白濃度調(diào)整一致,按照1∶4加入5 × SDS-PAGE Loading Buffer,沸水煮10 min,蛋白保存于-80 ℃?zhèn)溆谩?/p>
1.5 Western blot檢測相關(guān)蛋白的表達
取等量樣品進行SDS-PAGE電泳,轉(zhuǎn)印至PVDF膜上,5%脫脂乳室溫封閉1 h,4 ℃孵育相應(yīng)一抗(BID、Bax、Bcl-2、Cyt C、cleaved caspase-9、cleaved caspase-3、cleaved PARP、AIF、Endo G、β-actin、 COX-Ⅳ抗體按1∶1 000稀釋)過夜,室溫孵育二抗(按1∶10 000稀釋)1 h,ECL顯影檢測蛋白表達情況。使用Image J軟件分析條帶灰度值,目的蛋白與β-actin或COX-Ⅳ灰度值的比值即為目的蛋白的相對表達水平。
1.6 免疫熒光染色檢測AIF核轉(zhuǎn)位
用0.01% L-多聚賴氨酸包被爬片并將其置于24孔培養(yǎng)板中,將Fas shRNA組和NC組細胞接種于爬片,待其長至對數(shù)生長期時,用10 μmol·L-1Cd處理細胞12 h后,棄去培養(yǎng)基,磷酸鹽緩沖液(PBS)洗滌2次;4%多聚甲醛固定細胞30 min,棄去固定液,PBS洗滌3次;加入0.5% 曲拉通X-100,室溫透膜20 min,PBS洗滌3次;加入5% 牛血清白蛋白,室溫封閉1.5 h,棄去封閉液;4 ℃孵育AIF抗體(1∶100)過夜,PBS洗滌3次;室溫避光孵育Cy 3標記山羊抗兔熒光二抗(1∶200)1 h,PBS洗滌3次; 滴加DAPI染色液,室溫避光孵育5 min,PBS洗滌2次;封片,激光共聚焦顯微鏡觀察并拍照。
1.7 數(shù)據(jù)分析
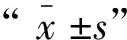
2 結(jié) 果
2.1 Fas基因沉默對鎘致PC12細胞BID活化的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,Western blot檢測BID和tBID蛋白表達水平。結(jié)果如圖1所示,與NC組相比,Cd組tBID/BID比值極顯著升高(P<0.01);與Cd組相比,F(xiàn)as shRNA+Cd組tBID/BID比值極顯著降低(P<0.01)。
2.2 Fas基因沉默對鎘致PC12細胞Bax/Bcl-2比值變化的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,Western blot檢測Bax和Bcl-2蛋白表達水平。結(jié)果如圖2所示,與NC組相比,Cd組Bax/Bcl-2比值極顯著升高(P<0.01);與Cd組相比,F(xiàn)as shRNA+Cd組Bax/Bcl-2比值極顯著降低(P<0.01)。
2.3 Fas 基因沉默對鎘致PC12細胞Cyt C釋放的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,Western blot檢測Cyt C在細胞內(nèi)分布情況。結(jié)果如圖3所示,與NC組相比,Cd組線粒體中Cyt C表達量極顯著降低(P<0.01),細胞質(zhì)中Cyt C表達量極顯著升高(P<0.01);與Cd組相比,F(xiàn)as shRNA+Cd組線粒體中Cyt C表達量極顯著升高(P<0.01),細胞質(zhì)中Cyt C表達量極顯著降低(P<0.01)。
2.4 Fas 基因沉默對鎘致PC12細胞caspase-9、caspase-3和PARP蛋白活化的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,Western blot檢測caspase-9、caspase-3和PARP蛋白活化情況。結(jié)果如圖4所示,與NC組相比,Cd組Cleaved caspase-9、Cleaved caspase-3和Cleaved PARP蛋白水平均極顯著升高(P<0.01);與Cd組相比,F(xiàn)as shRNA+Cd組Cleaved caspase-9蛋白水平顯著降低(P<0.05),Cleaved caspase-3和Cleaved PARP蛋白水平極顯著降低(P<0.01)。
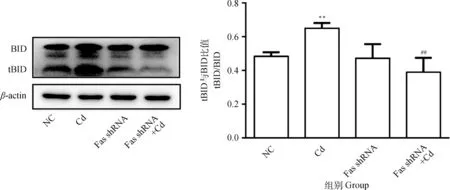
與NC組相比,**表示P<0.01;與Cd組相比,#表示P<0.05,##表示P<0.01。下同Compared with NC group, ** indicates P<0.01; Compared with Cd group, # indicates P<0.05, ## indicates P<0.01.The same as follows圖1 Fas基因沉默對鎘致PC12細胞BID活化的影響Fig.1 Effects of Fas silencing on the activation of BID in PC12 cells caused by cadmium
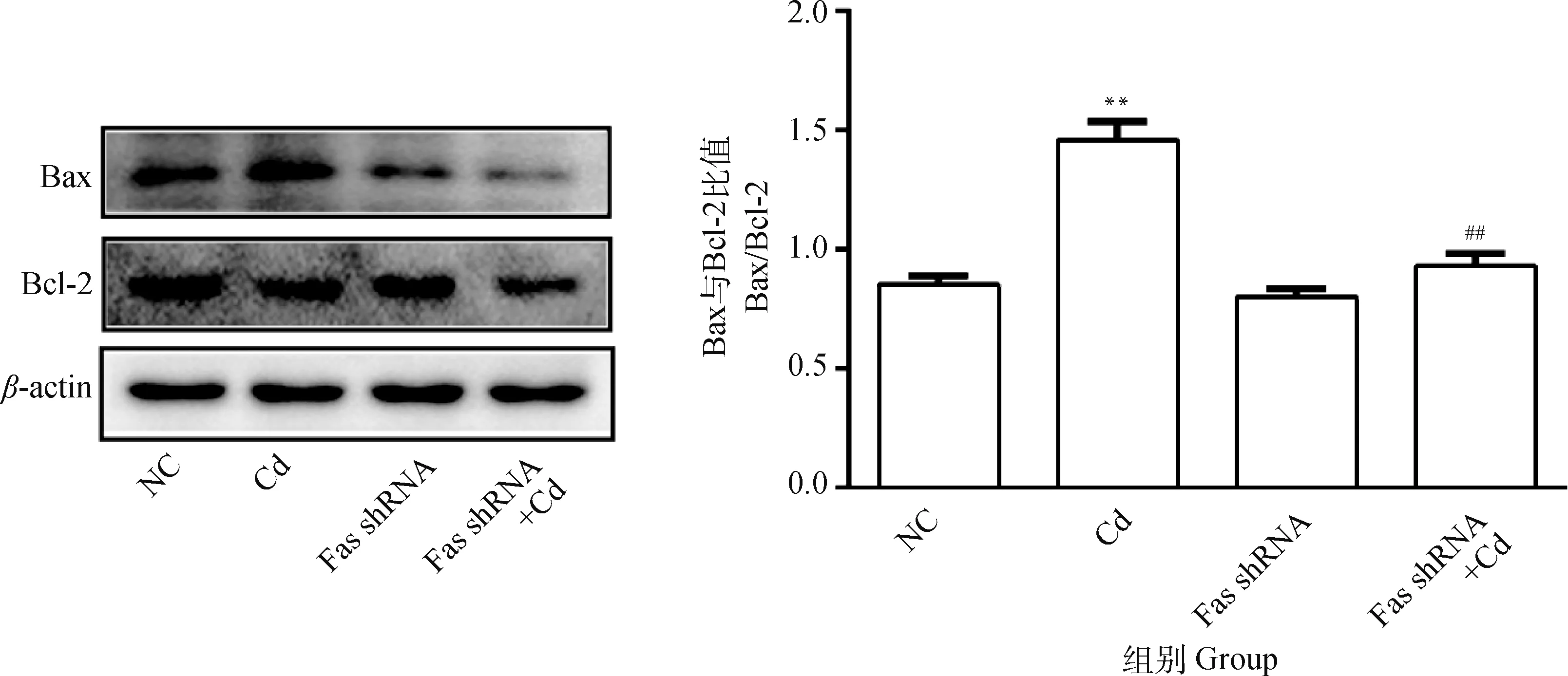
圖2 Fas基因沉默對鎘致PC12細胞Bax/Bcl-2比值變化的影響Fig.2 Effects of Fas silencing on the change of Bax/Bcl-2 ratio in PC12 cells caused by cadmium
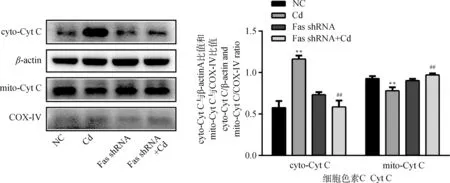
圖3 Fas基因沉默對鎘致PC12細胞Cyt C釋放的影響Fig.3 Effects of Fas silencing on the release of Cyt C in PC12 cells caused by cadmium
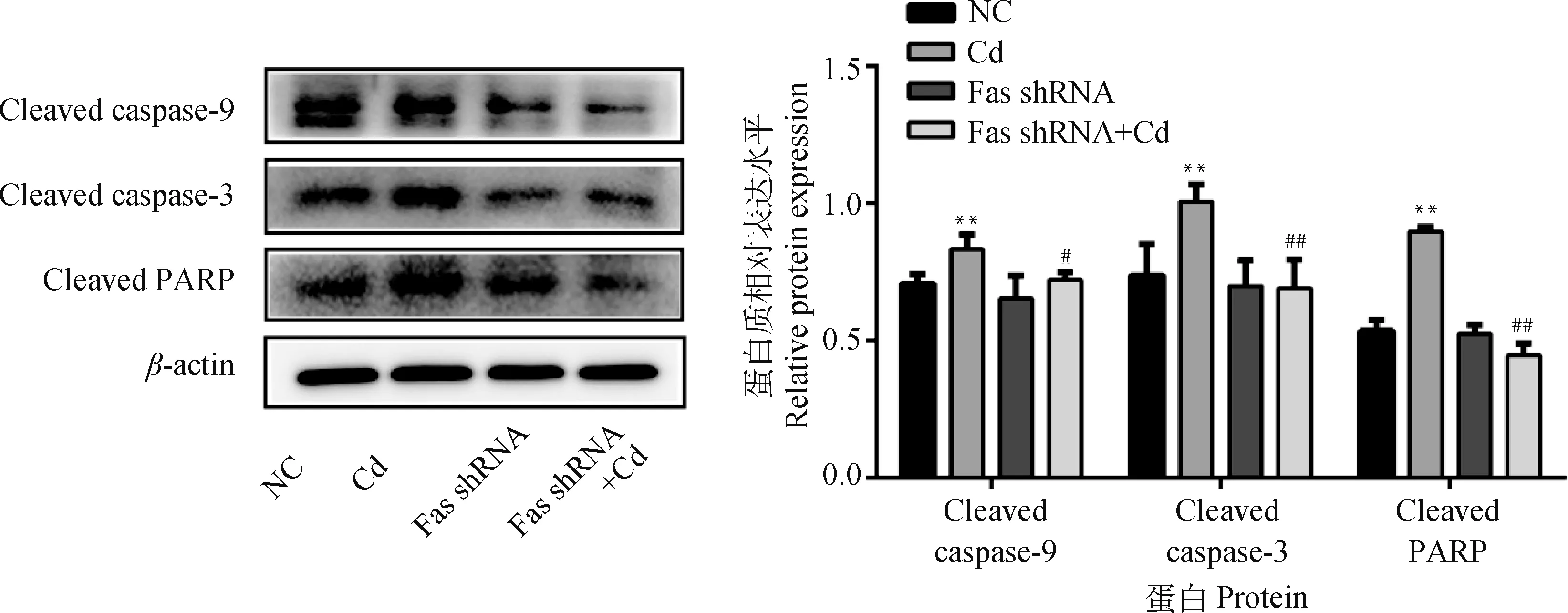
圖4 Fas基因沉默對鎘致PC12細胞caspase-9、caspase-3和PARP蛋白活化的影響Fig.4 Effects of Fas silencing on the activation of caspase-9, caspase-3 and PARP in PC12 cells caused by cadmium
2.5 Fas 基因沉默對鎘致PC12細胞AIF和Endo G蛋白表達的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,Western blot檢測AIF和Endo G蛋白表達水平。結(jié)果如圖5所示,與NC組相比,Cd組AIF和Endo G蛋白水平極顯著升高(P<0.01);與Cd組相比,F(xiàn)as shRNA+Cd組AIF和Endo G蛋白水平極顯著降低(P<0.01)。
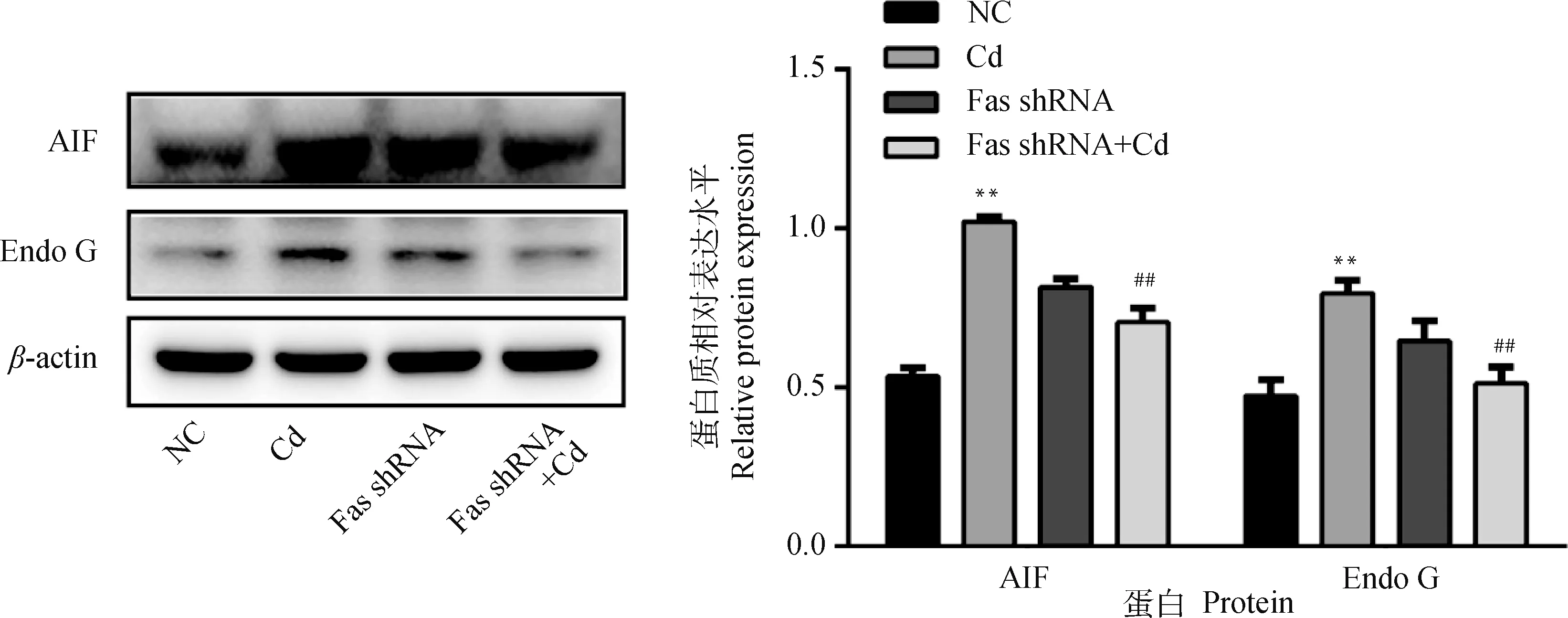
圖5 Fas基因沉默對鎘致PC12細胞AIF和Endo G蛋白表達的影響Fig.5 Effects of Fas silencing on the expression of AIF and Endo G in PC12 cells caused by cadmium
2.6 Fas 基因沉默對鎘致PC12細胞AIF核轉(zhuǎn)位的影響
10 μmol·L-1Cd分別處理NC組和Fas shRNA組細胞12 h,免疫熒光染色法檢測AIF核轉(zhuǎn)位情況。結(jié)果如圖6所示,與NC組相比, Cd組熒光標記蛋白AIF主要集中于細胞核;與Cd組相比,F(xiàn)as shRNA+Cd組熒光標記蛋白AIF主要分散于細胞質(zhì)。
3 討 論
細胞凋亡是由基因調(diào)控的程序性死亡,重金屬鎘可誘導(dǎo)包括神經(jīng)細胞在內(nèi)的多種細胞發(fā)生凋亡[6,15-16]。死亡受體通路是經(jīng)典凋亡通路之一,其中,F(xiàn)as/FasL信號通路備受關(guān)注。Fas/FasL信號通路主要通過Fas/FasL/FADD/caspase-8途徑介導(dǎo)細胞發(fā)生凋亡。體內(nèi)外研究表明,鎘可激活Fas/FasL信號通路誘發(fā)神經(jīng)細胞凋亡[13,17]。抑制Fas/FasL信號通路中的關(guān)鍵蛋白,能夠?qū)毎蛲銎鸬揭欢ㄒ种谱饔谩llah等[18]研究發(fā)現(xiàn),抑制Fas能夠降低腦缺血導(dǎo)致的細胞凋亡。Zhang等[19]研究發(fā)現(xiàn),干擾Fas顯著抑制氧糖剝奪再灌注誘導(dǎo)的人神經(jīng)母細胞瘤細胞凋亡。本實驗室前期研究發(fā)現(xiàn),利用Anti-FasL抑制FasL可減輕鎘導(dǎo)致的PC12細胞凋亡[20]。
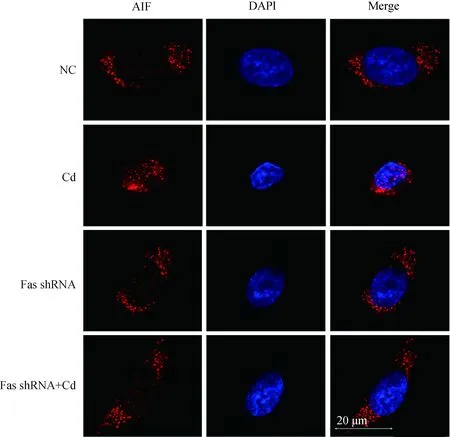
紅色熒光代表AIF,藍色熒光代表細胞核The red puncta represent AIF and the blue puncta represent nuclei圖6 Fas基因沉默對鎘致PC12細胞AIF核轉(zhuǎn)位的影響(標尺=20 μm)Fig.6 Effects of Fas silencing on the nuclear transposition of AIF in PC12 cells caused by cadmium (scale bar=20 μm)
線粒體在哺乳動物細胞凋亡過程中發(fā)揮重要作用。線粒體功能障礙會導(dǎo)致活性氧積累,引起氧化應(yīng)激和凋亡[21]。線粒體凋亡通路主要由Bcl-2家族蛋白介導(dǎo)。當各種凋亡刺激作用于線粒體時,會激活Bcl-2家族促凋亡成員,導(dǎo)致促凋亡和抗凋亡蛋白的失衡,從而影響線粒體膜通透性[22-23],導(dǎo)致線粒體釋放Cyt C等各種促凋亡因子[24-25]。釋放的Cyt C與凋亡蛋白酶活化因子-1(Apaf-1)結(jié)合形成復(fù)合物,激活caspase-9,進而激活caspase-3[26]。激活的caspase-3剪切PARP,抑制受損DNA的修復(fù),促進凋亡細胞死亡[27-28]。體內(nèi)外研究表明,鎘可激活線粒體通路誘發(fā)神經(jīng)細胞凋亡[17,29]。另外,線粒體通路和Fas/FasL通路之間存在緊密聯(lián)系,F(xiàn)as/FasL通路激活的caspase-8將BID剪切為tBID,tBID轉(zhuǎn)位到線粒體,誘導(dǎo)Cyt C釋放,從而激活線粒體通路[12]。Yu等[30]研究發(fā)現(xiàn),在小鼠脊髓損傷模型中,F(xiàn)as缺陷抑制BID、caspase-9和caspase-3的激活,增加抗凋亡蛋白Bcl-2和Bcl-xL的表達。Zhang等[19]研究發(fā)現(xiàn),干擾Fas能夠抑制氧糖剝奪再灌注導(dǎo)致的人神經(jīng)母細胞瘤細胞Bax和Caspase-3上調(diào)及Bcl-2下調(diào)。本研究結(jié)果顯示,F(xiàn)as基因沉默能夠顯著或極顯著抑制鎘引起的PC12細胞tBID/BID比值和Bax/Bcl-2比值升高,Cyt C釋放,caspase-9、caspase-3和 PARP蛋白活化。說明Fas通過調(diào)控caspase依賴的線粒體通路參與鎘致PC12細胞凋亡。
AIF和Endo G是位于線粒體膜間隙的核酸酶,凋亡發(fā)生時被釋放到細胞質(zhì)中并轉(zhuǎn)位到細胞核,通過caspase非依賴途徑介導(dǎo)細胞凋亡[31-33]。大量研究表明,在細胞凋亡過程中,F(xiàn)as可誘導(dǎo)AIF和Endo G從線粒體釋放到細胞質(zhì)或細胞核中[32,34-35]。Yu等[30]研究發(fā)現(xiàn),在小鼠脊髓損傷模型中,F(xiàn)as缺陷抑制AIF從線粒體轉(zhuǎn)位到細胞核。本研究結(jié)果顯示,F(xiàn)as 基因沉默能夠極顯著抑制鎘引起的AIF和Endo G蛋白表達升高,并抑制AIF核轉(zhuǎn)位。說明Fas通過調(diào)控caspase非依賴的線粒體通路參與鎘致PC12細胞凋亡。
4 結(jié) 論
鎘通過激活線粒體通路誘導(dǎo)PC12細胞凋亡,干擾Fas能夠抑制鎘激活的線粒體凋亡通路,說明Fas通過調(diào)控線粒體通路參與鎘致PC12細胞凋亡;這為揭示鎘的神經(jīng)毒性機制提供了新的理論基礎(chǔ)。

