不同注射條件對中華蜜蜂工蜂微量注射后生存的影響
劉佳霖 李亞迎 羅文華 曹蘭 高麗嬌 劉懷
(1 重慶市畜牧科學院,榮昌 402460;2 西南大學植物保護學院,重慶 400715)
蜜蜂成年工蜂的微量注射技術已廣泛應用于蜜蜂的生物學研究。在蜜蜂的RNA 干擾試驗中,利用微量注射技術將目的基因的dsRNA 注入工蜂體內,可干擾目的基因的表達,進而評價目的基因的功能[1]。例如,中華蜜蜂(Apis cerana cerana)工蜂微量注射0.5μLCYP301A1、CYP303A1和CYP306A1的dsRNA能夠顯著降低蟲體對應目的基因的相對表達量,而下調的這3 個P450(Cytochrome P450 monooxygenases)基因能夠顯著提高工蜂飼喂敵敵畏、噻蟲嗪、百草枯和溴氰菊酯后的死亡率,表明P450 家族基因參與了中華蜜蜂對多種農藥的解毒代謝[2]。此外,通過微量注射dsRNA 干擾卵黃原蛋白vitellogenin 基因的表達能夠顯著增加西方蜜蜂(Apis mellifera)的嗅覺敏感性[3],干擾IRS(Insulin receptor substrate)基因的表達能夠改變工蜂的采集行為[4]。這些研究表明,基于成年工蜂微量注射的RNA 干擾技術對研究蜜蜂基因的功能具有十分重要的作用。與此同時,工蜂的微量注射還應用于評價不同物質及病原微生物對蜜蜂的影響,如微量注射章魚胺和酪胺能夠顯著影響蜜蜂的運動行為[5]。注射接種蜜蜂殘翅病毒能夠顯著降低工蜂的壽命,下調卵黃原蛋白vitellogenin基因的相對表達量;同時暴露于DWV 和噻蟲嗪的工蜂表現出更低的壽命,并導致工蜂提前開始采集行為[6]。注射接種蜜蜂以色列急性麻痹病毒能夠改變采集蜂的嗅覺敏感性,降低采集結束后的回巢成功率[7]。
盡管蜜蜂成年工蜂的微量注射技術已廣泛地應用于蜜蜂的生物學研究,但不同注射條件是否能夠顯著影響工蜂注射后的生存仍沒有相關報道。因此,本研究基于以前研究中的蜜蜂成年工蜂微量注射方法,通過單因素試驗評價了不同注射日齡、麻醉方式、注射部位及注射量對工蜂注射后15d 生存的影響,以優化蜜蜂成年工蜂的微量注射技術,降低微量注射對蜜蜂的影響,為后續開展相關試驗奠定基礎。
1 材料
1.1 試驗材料
本試驗于2020年9月在重慶市榮昌區重慶市畜牧科學院進行,試驗蜜蜂為重慶本地中華蜜蜂,2 個配置有姐妹蜂王的試驗蜂群在自然條件下現代活框飼養,試驗蜂群群勢為5 足框蜂(2 脾子脾和2 脾蜜粉脾),試驗期間周圍環境日平均溫度21~27℃。試驗開始前,將即將出房的封蓋子脾帶回實驗室,并放置在黑暗的人工氣候箱(34℃,相對濕度70%)中過夜培養,以獲得新出房的工蜂。待工蜂出房后,24h 內將來自不同蜂群的33~35 只新出房工蜂隨機移入塑料飼喂盒(17cm×10cm×7cm)中飼養,每個飼喂盒提供3mL 50%(w/w)的蔗糖溶液,并放入另一個人工氣候箱(30℃,相對濕度60%)中黑暗飼養。每天更換飼喂盒中的蔗糖溶液。根據后續試驗設計,新出房的工蜂連續飼喂3d、7d 和12d 后用于中華蜜蜂成年工蜂的微量注射試驗。
1.2 主要儀器
人工氣候箱(RXZ智能型),購自寧波江南儀器廠;微量注射器(7632-01),購自美國Hamilton 公司;微量注射器針頭(30G),購自美國Hamilton 公司。
2 方法
基于已有研究的蜜蜂成年工蜂微量注射方法[3,8-10]及預實驗結果,本研究選擇的基礎注射條件為:3日齡工蜂,不麻醉,從中華蜜蜂工蜂背部的第4~5 腹節節間膜注入1μL 的DEPC 水。通過單因素試驗評價不同注射日齡、麻醉方式、注射部位及注射量對工蜂注射后15d 生存的影響。每個處理注射30 只工蜂,并重復3 次。注射完成后的30 只工蜂被放入一個新的飼喂盒中,提供3mL 50%的蔗糖溶液,置于人工氣候箱(30℃,相對濕度60%)中黑暗飼養。試驗共計持續15d,每天記錄各組工蜂的死亡數,移除死亡的工蜂,并更換蔗糖溶液。
2.1 不同注射日齡對中華蜜蜂工蜂注射后生存的影響
新出房的工蜂飼喂50%的蔗糖溶液3d、7d 和12d 后用于微量注射試驗。3日齡、7日齡或12日齡的工蜂,不麻醉,從背部的第4~5 腹節節間膜注入1μL 的DEPC 水。3 個日齡的工蜂于同一天上午完成注射,注射完成后的工蜂被放入新的飼喂盒中,提供蔗糖溶液,每天檢查工蜂的生存情況。
2.2 不同麻醉方式對中華蜜蜂工蜂注射后生存的影響
用玻璃試管取2~3 只3日齡的工蜂插入冰內放置2~3min(低溫麻醉),待工蜂被麻醉后,將工蜂取出并從背部的第4~5腹節節間膜注入1.0μL的DEPC水,同時設置不麻醉對照組。注射完成后的工蜂被放入新的飼喂盒中,提供蔗糖溶液,每天檢查工蜂的生存情況。
2.3 不同注射部位對中華蜜蜂工蜂注射后生存的影響
3日齡的工蜂,不麻醉,分別從背部的第2~3 腹節、第3~4 腹節、第4~5 腹節或第5~6 腹節節間膜注入1.0μL 的DEPC 水。注射完成后的工蜂被放入新的飼喂盒中,提供蔗糖溶液,每天檢查工蜂的生存情況。
2.4 不同注射量對中華蜜蜂工蜂注射后生存的影響
3日齡的工蜂,不麻醉,從背部的第4~5 腹節節間膜注入0.5μL、1.0μL 或2.0μL 的DEPC 水。注射完成后的工蜂被放入飼喂盒中,提供蔗糖溶液,每天檢查工蜂的生存情況。
2.5 統計學分析
試驗數據的統計學分析在SPSS 21.0 中實現。采用生存分析的Kaplan-Meier estimator 獲得不同試驗組工蜂的生存曲線,利用Log-rank test 分析不同試驗組生存曲線的統計學差異。與此同時,使用Cox 比例風險回歸模型(Cox proportional hazards model)獲得不同注射條件與基礎注射條件相比的風險比值,以明確不同注射條件對工蜂注射后生存的影響。當風險比值<1 時,表明該注射條件對工蜂注射后生存的風險小于基礎注射條件,當風險比值>1 時,表明該注射條件對工蜂注射后生存的風險大于基礎注射條件。當P<0.05 時,差異達到顯著水平,當P<0.01 時,差異達到極顯著水平。
3 結果與分析
3.1 不同注射日齡對中華蜜蜂工蜂注射后生存的影響
本研究顯示,不同注射日齡能夠顯著影響中華蜜蜂工蜂注射后的生存時間(圖1A,χ2=24.82,df=2,P<0.01)。7日齡和12日齡工蜂注射后的平均生存時間分別為9.22d(χ2=11.01,P<0.01)和7.67d(χ2=23.82,P<0.01),極顯著低于3日齡工蜂的11.44d;但7日齡工蜂和12日齡工蜂注射后的生存時間差異不顯著(χ2=3.16,P>0.05)。Cox 比例風險回歸模型分析顯示,與3日齡工蜂相比,7日齡工蜂和12日齡工蜂注射后的風險比為1.78(χ2=9.33,P<0.01)和2.38(χ2=21.67,P<0.01),高日齡(7日齡和12日齡)工蜂注射后的生存風險極顯著高于3日齡工蜂。
3.2 不同麻醉方式對中華蜜蜂工蜂注射后生存的影響
如圖1B 所示,低溫麻醉不能顯著影響工蜂注射后的生存時間(χ2=1.53,df=1,P>0.05)。與不麻醉相比,中華蜜蜂工蜂低溫麻醉后注射的風險比為1.27,雖然低溫麻醉能夠對工蜂注射后的生存產生更大的風險,但未達到顯著水平(χ2=1.44,P>0.05)。
3.3 不同注射部位對中華蜜蜂工蜂注射后生存的影響
不同注射部位能夠顯著影響工蜂注射后的生存時間(圖1C,χ2=134.28,df=3,P<0.01)。工蜂從背部第2~3 腹節節間膜注射后的平均生存時間為4.48d,極顯著低于從第3~4 腹節(χ2=61.59,P<0.01)、第4~5腹節(χ2=80.37,P<0.01)和第5~6腹節(χ2=64.66,P<0.01)節間膜注射;工蜂從第3~4 腹節、第4~5 腹節和第5~6 腹節節間膜注射后的生存時間差異不顯著(P>0.05)。與第4~5 腹節節間膜相比,從第2~3 腹節、第3~4 腹節和第5~6 腹節節間膜注射的風險比為4.91、1.27 和1.24,工蜂從背部第2~3 腹節節間膜微量注射的風險極顯著高于從第4~5 腹節節間膜注射(χ2=72.42,P<0.01)。
3.4 不同注射量對中華蜜蜂工蜂注射后生存的影響
注射量不能顯著影響中華蜜蜂工蜂注射后的生存時間(圖1D,χ2=3.17,df=2,P>0.05)。與1.0μL相比,微量注射0.5μL 和2.0μL 的風險比為1.04(χ2=0.03,P>0.05)和1.36(χ2=2.39,P>0.05),差異不顯著。
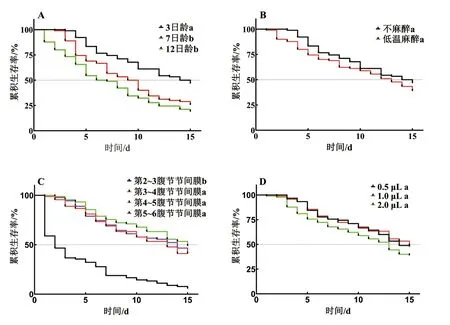
圖1 不同注射條件對中華蜜蜂工蜂微量注射后生存的影響
4 討論
為了優化中華蜜蜂成年工蜂的微量注射技術,明確不同注射條件是否能夠顯著影響工蜂注射后的生存,本研究利用單因素試驗評價了不同注射日齡、麻醉方式、注射部位及注射量對工蜂注射后15d 生存的影響。結果顯示,不同注射條件能夠對工蜂注射后的生存產生不同的影響。工蜂進行微量注射時的日齡能夠顯著影響工蜂注射后的生存時間,7日齡和12日齡工蜂微量注射后的生存風險顯著高于3日齡工蜂。該結果表明,低日齡的工蜂可能更適宜于開展蜜蜂的微量注射試驗。在以前的研究中,絕大部分學者采用低日齡(0~5日齡)的工蜂進行微量注射[2,10-13],間接表明利用低日齡的工蜂開展微量注射試驗能夠有效降低注射對蜜蜂的影響,提高后續試驗的準確性。此外,本研究采用實驗室飼養的方式獲得不同日齡的工蜂,但長時間的實驗室離群飼養可能會對工蜂產生不利的影響,進而提高微量注射對工蜂生存的風險。Li 等人[7]利用從蜂群中獲得的采集蜂評價了注射接種IAPV 對蜜蜂嗅覺敏感性的影響,表明利用從蜂群中獲得的高日齡工蜂開展微量注射試驗可能降低了注射對蜜蜂的影響。因此,若必須選擇高日齡的蜜蜂開展微量注射試驗,建議直接從蜂群中選擇對應日齡的工蜂,并縮短試驗時間,以降低微量注射對后續試驗結果的影響。
從工蜂腹部進行微量注射是以前研究中常用的注射方法,但不同研究中注射的部位存在很大差異[3,5,10,11,14]。本研究顯示,中華蜜蜂工蜂從背部第2~3 腹節節間膜注射后的平均生存時間顯著低于從第3~4 腹節、第4~5 腹節和第5~6 腹節節間膜注射,表明不同注射部位能夠對工蜂產生不同的影響。腹部是蜜蜂消化和生殖的中心,包含復雜的消化、循環、呼吸、神經、生殖和分泌等系統[15]。從腹部不同的部位進行微量注射可能會對其內部的復雜結構造成不同的傷害,最終對工蜂產生不同的影響。在開展中華蜜蜂工蜂微量注射時,應選擇從背部第3~4 腹節、第4~5 腹節或第5~6 腹節節間膜進行注射,以降低微量注射對工蜂的影響。
低溫麻醉是蜜蜂生物學研究中常用的麻醉方式[16-18],也廣泛應用于工蜂的微量注射[3,7,8]。本研究顯示,低溫麻醉并不能夠顯著影響工蜂注射后的生存。因此,低溫麻醉仍是提高蜜蜂工蜂微量注射效率的有效方式。此外,本研究選擇以前研究中常用的3 個注射量(0.5μL、1.0μL 和2.0μL)[2,5,19],評價了不同注射量對工蜂注射后生存的影響。結果顯示,微量注射0.5μL、1.0μL 和2.0μL 的DEPC 水并不能顯著影響注射后工蜂的生存,表明這3 個注射量均可在工蜂的微量注射中使用。劉麗等人研究顯示[10],與微量注射1μL 和2μL 的DEPC 水相比,注射3μL 和4μL 能夠提高工蜂的死亡率,表明注射量的提高能夠對蜜蜂產生更大的影響。因此,在實際的微量注射試驗中,需要盡可能提高注射溶液的溶度,減少注射量,降低微量注射對工蜂的影響,以保證后續試驗的準確性。
綜上,本研究認為,低日齡的工蜂更適宜于開展中華蜜蜂的微量注射試驗,在注射前可以采用低溫麻醉工蜂的方式提高注射效率,推薦的注射方法為:從中華蜜蜂工蜂背部第4~5 腹節節間膜微量注射1.0μL的注射液。

