大精酸對糖尿病大鼠脂質代謝和內質網應激的影響
唐慧勤, 李 麗, 王 劍, 閻 莉, 吳燕春, 李海濤
(1.廣西中醫藥大學藥學院,廣西 南寧 530001;2.廣西中醫藥大學壯瑤藥工程中心,廣西 南寧 530012;3.南京中醫藥大學藥學院,江蘇 南京 210023)
國際糖尿病聯盟(IDF)發布了第八版全球糖尿病地圖,其顯示全球有4.25億糖尿病患者,預計到2045年,將會有近7億糖尿病患者。我國成年糖尿病(20~79歲)患病人數達到1.14億,仍是全球糖尿病患病人數最多的國家[1]。而糖尿病往往引起多種并發癥,如糖尿病周圍神經病變、糖尿病腎病、糖尿病心肌病等,其發生發展追本溯源主要是因為體內糖、脂肪、蛋白質等物質紊亂引起,尤其是脂質代謝紊亂[2-4]。糖尿病患者由于血糖的增高,脂質代謝發生紊亂,常伴有血脂異常增高現象。大約60%~70%的糖尿病患者在血糖代謝紊亂的基礎上常伴有脂質代謝異常,而血脂異常可使糖尿病患者提前出現許多并發癥[5-8]。
大精酸(argirein)是從蘆薈等中藥中提取的活性成分大黃酸(rhein)和L-精氨酸(L-arginine)形成的共晶物,研究發現其可用于防治各種糖尿病的并發癥,如糖尿病心肌病、糖尿病腎病、糖尿病性睪丸病、糖尿病并發的男性性功能低下或陽痿等[9-11]。本研究以糖尿病大鼠為實驗對象,探討大精酸對脂質代謝的調節作用和作用機制,為大精酸防治糖尿病并發癥提供部分參考依據。
1 材料
1.1 藥物 大黃酸(含量>98%),湖北興銀河化工有限公司,批號20171106;L-Arginine(精氨酸),北京索萊寶科技有限公司,批號914B036。
1.2 動物 健康SD大鼠,SPF級,體質量約160~180 g,由湖南斯萊克景達實驗動物有限公司提供,動物生產許可證號SCXK(湘)2019-0004,常規飼養于廣西中醫藥大學實驗動物中心實驗室,分籠飼養,保持12 h/12 h晝夜節律,溫度(24±3)℃,相對濕度(60±5)%,自由攝水攝食。
1.3 試劑 膽固醇、牛膽堿鈉購自北京中生瑞泰科技有限公司,批號20180410、20180216。鹽酸二甲雙胍片購自廣州白云山天心制藥股份有限公司,批號160614。鏈脲佐菌素(STZ)購自上海前塵生物科技有限公司,批號S0130;甘油三酯(TG)、總膽固醇(TC)、低密度脂蛋白(LDL-C)、高密度脂蛋白(HDL-C)、天門冬氨酸氨基轉移酶(AST)、丙氨酸氨基轉移酶(ALT)購自上海執誠生物科技有限公司,批號ZCDECPO04、ZCJANQO02、ZCNOVL009、ZCMAYQ009、ZCMARR018、ZCJUNQ023,由廣西中醫藥大學第一附屬醫院檢驗科全自動分析儀檢測。ECL化學發光底物(超敏)、高效RIPA組織/細胞裂解液、BCA、蛋白酶抑制劑混合液(100xPIC)購自北京索萊寶科技有限公司,批號BL523A、R0010、PC0020、P6730;重鏈結合蛋白(Bip)、磷酸化蛋白激酶R樣內質網激酶(p-PERK)、蛋白激酶R樣內質網激酶(PERK)、轉錄激活因子4(ATF4)、半胱胺酸蛋白酶蛋白-12(caspase12)抗體均購自北京博奧森生物技術有限公司,批號1219R、bs-2469R、bs-2469R、1531R、1105R;CCAAT/增強子結合蛋白(CHOP)、β-actin購自英國Abcam公司,批號ab179803、ab8227。
1.4 儀器 TGL-160高速臺式離心機(上海安亭科學儀器廠);ADVIA 2400全自動生化儀(德國Siemens公司);PowerPac Basic電泳儀和蛋白轉印模塊(濕轉)(美國Bio-Rad Laboratories公司);Tanon 5200凝膠成像系統(上海天能科技有限公司);FilterMax F3多功能酶標儀(美國Molecular Devices公司)。
2 方法
2.1 藥物樣本制備 參考文獻[12]報道,稱取大黃酸和精氨酸(1∶1)混合放置燒杯中,加入適量的純水,在80 ℃水浴中保溫1.5 h并不斷攪拌,趁熱抽濾,加入無水乙醇,使含醇量為60%,在60 ℃水浴中減壓回收溶劑至體積減半,放至室溫,于4 ℃冰箱中靜置1周,析晶,抽濾,干燥,即得。
2.2 造模及給藥 取SD大鼠60只,體質量160~180 g,自由攝食攝水,適應性喂養1周后,按體質量采用隨機分組法分為正常組、模型組、二甲雙胍對照組、大精酸高、中、低劑量組共5組,每組12只。除正常組喂食基礎飼料外,模型組、二甲雙胍對照組、大精酸高、中、低劑量組均給予高脂飼料(配方基礎飼料76.6%、膽固醇3%、牛膽堿鈉0.4%、油10%、白砂糖10%)喂養,并同時給予各組大鼠相應的藥物干預,其中二甲雙胍對照組劑量為600 mg/kg,大精酸低、中、高劑量組分別為40、50、60 mg/kg,正常組和模型組給予按1 mL/100 g純凈水,均灌胃給藥。連續給藥8周后,模型組、陽性組及給藥組一次性腹腔注射STZ按40 mg/kg,注射STZ 72 h后采用尾靜脈采血空腹測血糖(FBG),FBG≥11.1 mmol/L者確定為Ⅱ型糖尿病大鼠模型;FBG<11.1 mmol/L者補打1次STZ(40 mg/kg),使其≥11.1 mmol/L。繼續給藥5周,實驗周期共13周。
2.3 大鼠一般情況觀察 觀察大鼠進食、飲水、行為、精神狀態、毛發、大小便等情況。
2.4 標本采集 13周后,大鼠禁食(不禁水)12 h,末次給藥1 h后,10%烏拉坦1 mL/100 g腹腔注射麻醉,取腹主動脈血5 mL,待自然凝固后,3 000 r/min離心10 min,分離血清,用于測定血清TC、TG、HDL-C、LDL-C、ALT、AST。處死后迅速摘取肝臟,生理鹽水漂洗,濾紙吸干,分別取適量存于離心管和多聚甲醛中用于后續實驗分析。
2.5 血清生化指標檢測 采用全自動生化儀,測定大鼠血清中TC、TG、HDL-C、LDL-C、ALT、AST水平。
2.6 肝臟中脂質水平檢測 同一位置取各組大鼠肝小葉上約300 mg肝組織,加入異丙醇到3 mL,離心后取上清液,用全自動生化儀測定大鼠TC、TG水平。
2.7 肝臟病理形態學檢測 取各組大鼠肝臟適量,4%多聚甲醛固定液固定,HE染色,病理切片,鏡下觀察肝臟脂肪變性情況。
2.8 蛋白免疫印記(Western blot)檢測蛋白表達 取適量肝組織加入冷裂解液后勻漿、離心提取總蛋白,核蛋白采用核蛋白提取試劑盒分離提取。BCA法測定蛋白濃度,SDS-PAGE電泳分離蛋白,結束后取出分離膠,移至PVDF膜上,用TBST配置的8%脫脂奶粉封閉液封閉3 h;按照相應抗體說明書稀釋抗體,4 ℃孵育12 h;洗膜,二抗稀釋液室溫孵育1 h后,TBST洗膜,勻滴加ECL化學發光液后進行曝光顯影。

3 結果
3.1 一般情況觀察 正常組大鼠活動、飲食飲水正常,無死亡現象;模型組大鼠腹腔注射STZ后,出現毛色變黃稀疏、行動遲緩、精神不振、多飲多尿,尿液散發爛蘋果味等現象;與模型組比較,各干預組大鼠均有不同程度的改善。整個造模期間,正常組無死亡,模型組有4只大鼠死亡,大精酸高、中劑量組各有2只大鼠死亡。
3.2 血清生化指標 與正常組比較,模型組大鼠血清中TC、TG、HDL-C、LDL-C水平均升高,其中TC、TG、LDL-C水平更明顯(P<0.05)。與模型組比較,陽性藥二甲雙胍可以降低TC、TG、LDL-C水平(P<0.05),對HDL-C影響不大;大精酸中劑量使TC、TG、LDL-C水平降低(P<0.05),HDL-C變化不大。見表1。與正常組比較,模型組大鼠的ALT活性升高(P<0.05);與模型組比較,除二甲雙胍組ALT活性升高(P<0.05)外,其余無顯著差異(P>0.05),見表2。
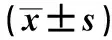
表1 大精酸糖尿病大鼠血脂的影響
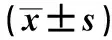
表2 大精酸對糖尿病大鼠肝功能的影響
3.3 肝臟脂質 相對于正常組,模型組大鼠肝臟中TC、TG水平升高(P<0.05);相對于模型組,二甲雙胍能降低TC、TG水平(P<0.05),大精酸各組大鼠的TC、TG水平有不同程度的降低,其中各劑量組TC水平更明顯(P<0.05),低劑量組TG水平更明顯(P<0.05)。見表3。
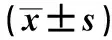
表3 大精酸對糖尿病大鼠肝臟脂質的影響
3.4 肝細胞HE染色 正常肝細胞呈放射狀排列,大小正常,胞質分布均勻,肝小葉組織結構完整;模型組大鼠肝細胞索和肝小葉消失,肝細胞排列無序,胞漿空泡化、核淡染,脂肪融合大空泡的出現把胞核擠到一邊,出現彌漫性的脂肪變性;二甲雙胍組肝細胞形態基本規則,細胞變大,胞漿有細小脂滴,但脂肪變性程度相對較輕;大精酸低劑量組胞漿可見數量不等的脂滴,有少數較大的空泡存在;中劑量組肝細胞體積增加稍有減輕,細胞內有少許脂肪空泡,脂肪變性程度較輕;高劑量組肝細胞變大,胞漿可見一定數量的大脂滴。見圖1。

圖1 大精酸對糖尿病大鼠肝臟組織病理組織學的影響(HE染色,×200)
3.5 對大鼠肝臟CHOP、Bip、p-PERK/PERK、ATF4、caspase12蛋白表達的影響 與正常組比較,模型組大鼠肝臟組織中CHOP、Bip、p-PERK/PERK、ATF4、caspase12的蛋白表達均升高(P<0.05);與模型組比較,大精酸各組的CHOP、Bip、p-PERK/PERK、ATF、caspase12蛋白表達降低 (P<0.05)。見圖2。

注:與正常組比較,ΔP<0.05;與模型組比較,*P<0.05。圖2 各組大鼠肝臟組織中CHOP、Bip、PERK/p-PERK、ATF4、caspase12蛋白表達(n=3)
4 討論
糖尿病是一種代謝異常綜合征的疾病,研究表明大約50%的糖尿病患者在血糖代謝紊亂的基礎上常伴有脂質代謝異常,因此糖尿病患者不光需要控制血糖,調節脂質代謝也是一項重要的措施。本研究中,大精酸不但可以降低血清TC、TG、LDL-C水平,表現出良好的調節血脂作用,還可減少肝細胞內脂滴,防止大空泡的形成,使肝組織中的TC、TG水平也降低。說明大精酸可以降低脂質在肝臟中的沉積,明顯改善肝臟病理組織改變,調節血脂異常,從而防治糖尿病大鼠脂質代謝異常。
如果人體血液循環中的游離脂肪酸(FFA)異常增加,超過了機體的代謝能力,會對肝細胞產生脂毒性,導致肝損傷發生[13]。肝損傷是糖尿病中的一種并發癥,肝臟細胞的損傷則會引起血清中由肝細胞合成的丙氨酸氨基轉移酶升高的異常升高[14]。本研究發現,與正常組比較,模型組大鼠AST、ALT的水平都升高,說明糖尿病大鼠存在著一定的肝損傷。雖然二甲雙胍組的降脂作用很明顯,但其升高了ALT水平,加重了肝損傷。大精酸雖然不能降低AST、ALT水平,但與模型組比較,也沒有引起AST、ALT水平升高(P>0.05),相對來說大精酸對肝沒有造成更嚴重的傷害性。
此外過多的FFA轉運進入肝臟,是形成肝臟胰島素抵抗(IR)和非酒精性脂肪性肝炎(NAFLD)的重要因素。NAFLD患者體內攝入過多的飽和脂肪酸時,會誘發肝臟炎癥反應和ERS[15]。而在富含TG的VLDL進入內質網進行裝配、與載脂蛋白結合轉運出去的過程中,過多的肝臟脂質通過滑面內質網(SER) 時也會引起ERS。作為一把“雙刃劍”,ERS早期可以維持細胞正常功能,但強烈或持續的應激存在時,則會啟動細胞凋亡機制,造成細胞損傷[16-17]。細胞要維持內質網的穩態,可以通過非折疊蛋白反應(UPR)激活一系列信號通路來實現,其主要包括3條通路:PERK通路,IRE1α通路和ATF6 通路[18-19]。上述信號通路中,PERK是位于 ER 膜上的跨膜轉錄因子[20]。在NAFLD模型中發現脂毒性誘導PERK途徑的細胞凋亡。高脂喂養的小鼠肝臟中ERS 標志蛋白PERK、IRE1α 表達增高[21]。當ERS發生時,PERK從Bip解離,生成p-PERK。本課題組對PERK活化的研究結果發現,模型組大鼠肝臟中p-PERK/PERK比值增加,說明p-PERK明顯增多,而用大精酸處理后其表達又降低,證實大精酸處可以抑制內質網應激信號通路的激活。激活的PERK磷酸化eIF-2α 51 位的絲氨酸(Ser51),從而對ATF4 mRNA 的翻譯產生誘導作用,ATF4 mRNA活化后激活其下游分子CHOP的表達[22-23]。在哺乳動物細胞中,CHOP處于普遍表達的狀態,是ERS引發凋亡的信號。在高脂喂養造成的小鼠脂肪肝模型中,肝細胞CHOP、caspase12 mRNA及蛋白表達均升高,凋亡程序發生變化,說明脂肪肝中肝細胞的凋亡是由內質網應激引起的[24]。本研究中,模型組大鼠肝臟ATF4、CHOP蛋白表達顯著升高,而大精酸可以抑制ATF4、CHOP的表達,表明大精酸能夠通過抑制PERK-ATF4-CHOP信號通路,抑制內質網應激相關細胞凋亡,從而改善脂質代謝。大精酸能明顯抑制腎臟、心肌、成纖維細胞和炎癥在內質網應激中的生物記號PERK的上調及凋亡相關基因的異常[9-11,25]。大精酸是大黃酸和L-精氨酸以弱共價鍵形成的超分子化合物,其進入體內釋放出大黃酸和精氨酸從而發揮雙重作用。有研究發現大黃酸可通過抑制固醇調節元件結合蛋白(STEBP-1c)的轉錄,增加能量消耗,降低TC和TG水平,從而減少肝臟脂肪沉積,改善肝脂肪變性[26]。大黃酸被證實抑制人前體脂肪細胞增殖與分化與CHOP表達上調有關[27]。精氨酸(Arg)是人體內必需氨基酸,在Arg缺乏時,外周血有絲分裂原激活的T淋巴細胞和Jurkat細胞的CHOP表達和XBP-1mRNA剪接會升高,導致ERS[28]。同樣在卵巢腺癌細胞(SKOV3)、膠質母細胞瘤細胞(U251)、人結腸癌細胞(HCT-116)等人實體瘤中發現Arg饑餓誘導了ERS[29]。
另外一條由內質網介導凋亡途徑是caspases級聯反應。已有報道顯示,在小鼠的肝細胞中,發現有內質網應激相關基因和特異性的表達[30]。與有caspase 12表達的細胞比較,caspase 12缺陷細胞更能抵抗對內質網應激介導的凋亡。本研究發現,大精酸也可以降低caspase 12的表達,從而抑制內質網應激。
然而,本研究藥物沒有體現出量效關系,原因主要有兩點:一是受劑量梯度的影響。本研究中所設劑量是根據前期預實驗結果決定。在預實驗中,設定了200、100、75、50、25 mg/kg等劑量梯度,發現劑量過高時,如200、100 mg/kg劑量下,大鼠出現大便溏爛、呈黃紅色,毛黃稀疏,精神不振等情況,而75 mg/kg劑量下,大鼠情況有所好轉。而劑量過低,如25 mg/kg劑量下,大鼠無上述反應,但沒有調脂作用。在50 mg/kg時,大鼠生理狀態與正常組相似,且實驗結果較理想和穩定,故選用了60、50、40 mg/kg的劑量梯度,而不是2~3倍的劑量比。二是大精酸作為大黃酸和精氨酸的共晶化合物,在被人體吸收的過程中,可能發生了構象改變或是釋放出大黃酸和精氨酸的速度不一致而造成活性改變,體現不出量效關系。本課題下一步計劃是在細胞上深入探討大精酸的脂質調節作用和檢測其藥物動力學指標,以進一步揭示其作用機制、藥效及藥動學的關系。
綜上所述,本文研究了大精酸對糖尿病大鼠脂質代謝的影響及其機制。結果表明,大精酸能夠降低血脂和肝臟脂質,減輕肝細胞脂肪樣病變,該作用可能與下調了CHOP、Bip、p-PERK/PERK、ATF4、caspase12等內質網應激相關蛋白表達有關。

