卵巢組織中BMP15、GPR30的表達與PCOS卵泡發育障礙的關系
忽平
(南陽市中心醫院婦產科,河南 南陽 473000)
多囊卵巢綜合征(PCOS)是婦科常見的生殖內分泌系統疾病,生育期婦女PCOS 發病率達4%~18%,占無排卵性不孕癥的50%~70%。PCOS 可誘發多種生殖系統腫瘤、代謝綜合征、精神癥狀等不良遠期并發癥,嚴重影響婦女的生活質量[1-3]。故研究PCOS 卵泡發育障礙發病機制,為其治療提供思路是生殖領域研究熱點。關于PCOS的發病機制研究目前尚未闡明。有報道指出[4]PCOS 發病原因主要與卵巢內部自分泌和旁分泌因子水平紊亂有關。有研究報道[5]骨形成蛋白15(BMP15)在PCOS卵泡發育障礙患者血清中水平異常,BMP15 是轉化生長因子β 超家族中的一員,可促進初級卵泡和原始卵泡的生長發育,并促進原始卵泡向次級卵泡進化。雌二醇(E2)及其受體可促進卵泡體細胞的增殖分化,對卵泡功能的完整性起著重要作用。雌激素受體G蛋白偶聯受體(GPR30)是新型雌激素受體,已有研究證實[6,7]其在正常人的卵巢和卵泡中有顯著作用,但是否在PCOS 發病過程中起作用,相關研究報道較少。本研究選取我院實施手術治療的41例PCOS患者卵巢組織(PCOS 組)、因良性腫瘤實施卵巢腫瘤切除術獲取的正常卵巢組織40例(對照組),對比分析兩組卵巢組織中的BMP15、GPR30表達差異,旨在確定上述指標在PCOS 診斷中的價值。報告如下。
1 資料與方法
1.1 臨床資料 選取我院2016年1 月-2018年1月實施手術治療的41例PCOS患者卵巢組織(PCOS 組)、因良性腫瘤實施卵巢腫瘤切除術獲取的正常卵巢組織40例為對照組。PCOS 組,年齡27~39 歲,平均30.6±2.0 歲。對照組,年齡26~40 歲,平均30.8±2.9 歲。兩組研究對象的年齡比較,差異均無統計學意義(P>0.05)。
1.2 入選排除標準 入選標準:⑴PCOS的診斷標準參考鹿特丹診斷標準:患者表現為稀發排卵、無排卵,高雄激素血癥,超聲檢查發現卵巢呈多囊性改變;⑵對照組為的月經周期規律,經期3~5d;⑶對照組卵巢組織經病理學檢查證實未被腫瘤侵犯;⑷本研究符合《赫爾辛基宣言》相關醫學倫理規定,對研究對象的各項資料保密。排除標準:⑴甲狀腺疾病;⑵先天性腎上腺皮質增生;⑶庫欣綜合征;⑷免疫系統疾病、風濕性疾病。
1.3 免疫組化染色 采用免疫組化Elivision 二步法。100 ml/L 甲醛溶液固定卵巢組織將其連續切片厚度為5μm,脫蠟至水,0.01 mol/L 檸檬酸溶液(pH 6.0)高壓蒸汽3 min,修復抗原。分別將組織切片與GPR30 一抗(兔來源多克隆抗體,濃度1:200,Invitrogen 公司生產)或BMPl5 一抗(兔來源單克隆抗體,濃度1:200,克隆號:JE51-47,Invitrogen 公司生產),4℃孵育過夜。PBs 洗滌3 遍,再與二抗(山羊抗兔IgG,濃度:1:2000,Invitrogen 公司生產)室溫孵育30min。PBS 洗滌3 遍,DAB 顯色。實驗均設立陰性對照和空白對照。染色后切片背景為紫藍色,陽性表達為黃色或棕褐色,每張切片均由2 名經驗豐富的病理醫生共同判斷。免疫組化結果判定:BMP15、GPR30 主要在卵母細胞細胞核和細胞膜中表達。BMP15蛋白、GPR30蛋白的陽性表達呈黃色、棕黃色、褐色表達,⑴根據著色強度:0 分為無色、1 分為淡黃色、2 分為棕黃色、3 分為褐色、黑色;⑵根據陽性細胞比例:陽性細胞數目所占比例≤10%為1 分、陽性細胞所占比例11%~50%為2 分、陽性細胞數51%~75%為3 分、陽性細胞數所占比例>75%為4 分,兩種積分相乘總分<3 分為陰性、≧3 分為陽性。
1.4 一般指標檢測 檢測兩組的體質量指數(BMI)、血清雌激素(E2)、促黃體生成素(LH)、促卵泡生成素(FSH)、睪酮(T)、胰島素抵抗指數(HOMA-IR)。BMI、E2、LH、FSH、T、HOMA-IR 檢測:采用ELISA 法,所需試劑盒均購自羅氏公司,操作步驟嚴格按照說明書要求進行。
1.5 統計學方法 本研究收集的所有數據均在SPSS21.0 中進行統計分析,計量數據分別采用進行統計描述,采用t 檢驗進行數據分析;采用χ2檢驗進行統計分析;P<0.05 為差異具有統計學顯著性。
2 結果
2.1 PCOS 組和對照組的BMI、生殖激素水平、HOMA-IR 比較 PCOS 組患者的BMI、血清E2、LH、T、HOMA-IR 測定值均高于對照組(P<0.05),PCOS 組的血清FSH 低于對照組(P<0.05),見表1。
表1 PCOS 組和對照組的BMI、生殖激素水平、HOMA-IR 比較()
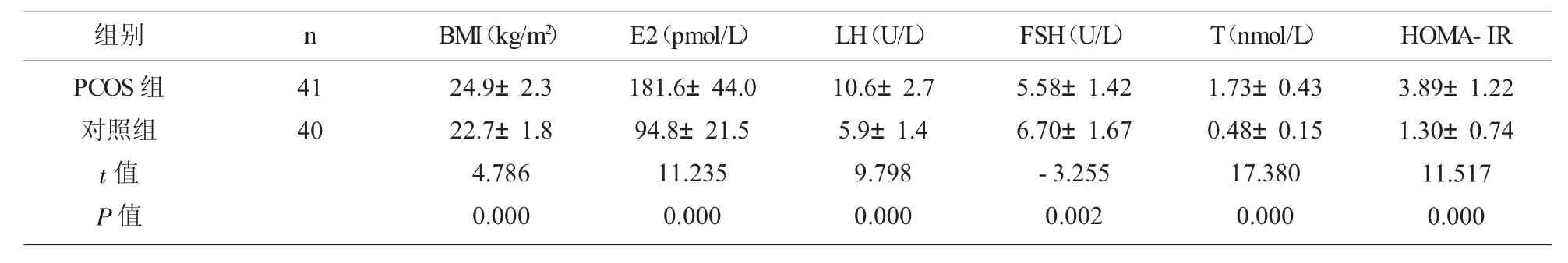
表1 PCOS 組和對照組的BMI、生殖激素水平、HOMA-IR 比較()
2.2 PCOS 組和對照組的原始卵泡中卵母細胞的BMP15蛋白、GPR30蛋白表達比較 PCOS 組的原始卵泡中卵母細胞的GPR30蛋白陽性率顯著高于對照組(P<0.05),BMP15蛋白陽性表達率低于對照組(P<0.05),見表2、圖1、圖2。
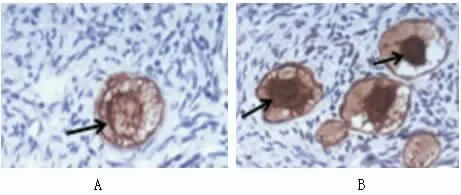
圖1 原始卵泡中卵母細胞的GPR30蛋白表達(如圖中箭頭所示細胞核中的GPR30蛋白著色顆粒),A 為對照組、B 為PCOS 組,400 倍。
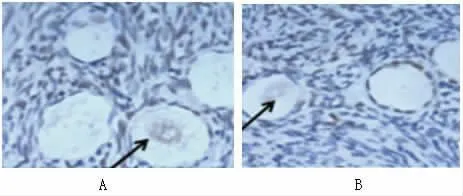
圖2 原始卵泡中卵母細胞的BMP15蛋白表達(如圖中箭頭所示細胞核中的BMP15蛋白著色顆粒),A 為對照組、B 為PCOS 組,400 倍。
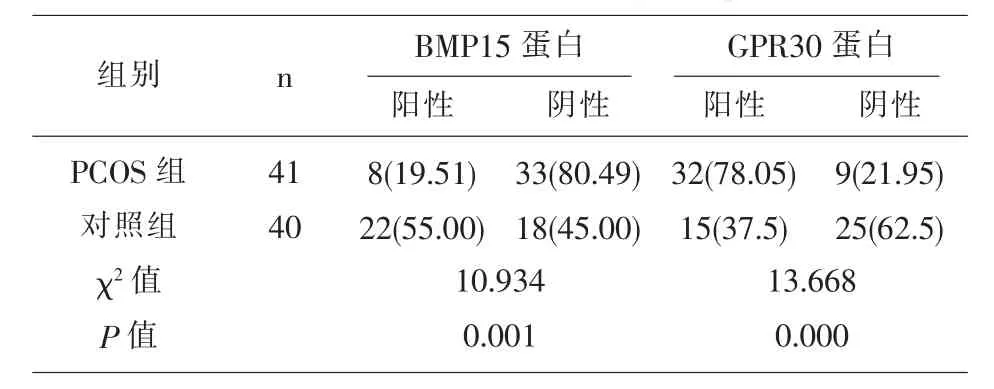
表2 原始卵泡中卵母細胞的BMP15蛋白、GPR30蛋白表達比較[n(%)]
2.3 PCOS 組和對照組的初級卵泡中卵母細胞的BMP15蛋白、GPR30蛋白表達比較 PCOS 組的初級卵泡中卵母細胞的GPR30蛋白陽性率顯著高于對照組(P<0.05),BMP15蛋白陽性表達率低于對照組(P<0.05),見表3、圖3、圖4。
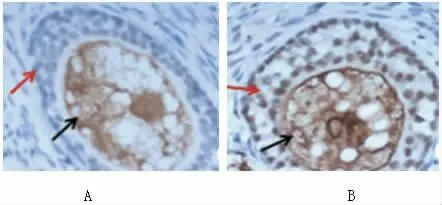
圖3 初級卵泡中卵母細胞的GPR30蛋白表達(圖中紅箭頭和黑色箭頭分別為細胞膜及細胞核中的GPR30蛋白著色顆粒),A 為對照組、B 為PCOS 組,400 倍。
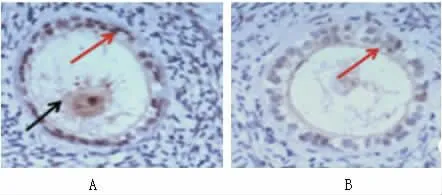
圖4 初級卵泡中卵母細胞的BMP15蛋白表達(圖中紅箭頭和黑色箭頭分別為細胞膜及細胞核中的BMP15蛋白著色顆粒),A 為對照組、B 為PCOS 組,400 倍。
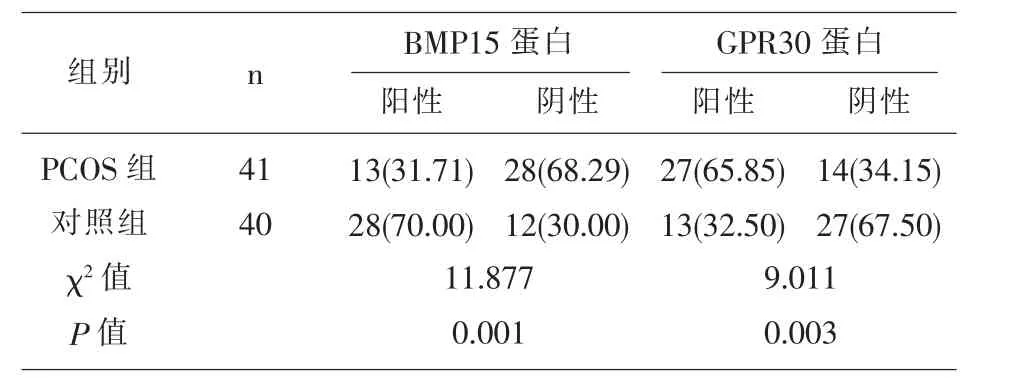
表3 初級卵泡中卵母細胞的BMP15蛋白、GPR30蛋白表達比較[n(%)]
3 討論
卵源性因子在卵泡發育和卵母細胞成熟過程中起重要作用[8]其中包括BMP15蛋白,有研究報道[9]BMP15 可促進原始卵泡和初級卵泡的形成,促進原始卵泡向次級卵泡的生長轉化,還能促進竇前卵泡向竇卵泡的轉化,誘導卵丘膨脹,在卵泡發育和卵母細胞成熟過程中起著重要作用。還有研究通過對比分析經過卵巢刺激的廢棄卵子復合物和正常卵巢顆粒細胞中BMP15水平發現,顆粒細胞中與卵子中BMP15水平一致,說明其同時在促進卵母細胞成熟和顆粒細胞增生過程中發揮作用。還有研究報道[10,11]BMP15 可直接調節顆粒細胞的增生、分化、代謝、黃素化和凋亡過程,上述一系列分泌信號可通過顆粒細胞的縫隙連接蛋白傳導至卵細胞,建立顆粒細胞和卵子間的交流,共同影響卵泡發育的整個過程。此外,有研究報道[12]BMP15 除了直接影響卵泡成熟和顆粒細胞增殖外,可通過調節黃體的生成和功能間接影響卵泡的發育和排卵過程。鑒于BMP15在卵泡發育過程中的多樣功能,推測BMP15 分泌異常可能參與PCOS 卵巢功能障礙的發病過程。本研究結果顯示,PCOS 組較正常卵巢組,原始卵泡中卵母細胞和初級卵泡中卵母細胞分泌的BMP15蛋白陽性表達率顯著下降,這與既往研究報道一致[13]。說明,BMP15 可促進初級卵泡和原始卵泡的成熟,對維持卵巢正常功能具有積極作用。
目前已有報道明確[14]甾體激素代謝異常是PC OS患者卵巢功能異常發病的主要因素,其中已證實,雄激素代謝異常在PCOS 發病機制的作用,關于雌激素代謝異常對PCOS患者卵巢功能影響的研究報道相對較少。有基礎研究報道[15]通過單獨使用戊酸雌二醇或聯合使用孕激素、雄激素、人絨毛膜促性腺激素(Human Chorionic Gonadotropin,HCG)及胰島素等均可建立PCOS 模型,但單獨使用戊酸雌二醇建立的PCOS 模型與人體PCOS 病理狀態更接近。另外有研究[16]通過使用抑制雌激素合成的藥物(如克羅米芬、他莫昔芬等)可誘導PCOS患者的卵泡繼續發育。以上研究報道均提示,雌激素過多可能是PCOS患者卵巢功能障礙的危險因素,故研究雌激素及其受體在PCOS患者卵細胞中的表達水平有利于加深卵泡發育機制的研究。經典的雌激素受體包括ERα和ERβ,定位于胞漿或胞核,通過調節不同基因發揮生理學效應,GPR30 是一種與傳統雌激素受體ERα、ERβ 不同源的新型雌激素受體,通過傳統的基因型效應和新型的非基因型效應調控雌激素水平。后者發生效應迅速,可在幾秒至幾分的短時間內誘導雌二醇與GPR30 結合,激活下游信號通路,促進細胞增殖或凋亡。有研究報道[17]斑馬魚中GPR30 可抑制卵母細胞減數分裂,抑制其成熟。目前已有研究發現GPR30在正常卵巢組織卵母細胞和卵泡膜細胞中的表達但未有報道表明其在PCOS患者卵巢組織中的表達狀況。本研究結果顯示,PCOS患者卵巢組織初級卵泡和原始卵泡中GPR30 較正常卵巢組織顯著高表達,證明,GPR30 作為新型雌激素受體在雌激素信號傳導中的作用及參與PCOS 卵巢功能障礙過程的作用。此外,本研究結果顯示,PCOS患者BMI、HOMA-IR、LH、T水平顯著升高與既往利用胰島素或孕激素的方法建立PCOS 模型的原理一致。而FSH水平顯著降低,是卵泡發育障礙的主要原因,與既往研究報道一致[18]。
綜上所述,PCOS患者卵巢組織中BMP15表達下調、GPR30表達上調,可能參與卵泡發育過程有關。本研究創新處,確定雌激素受體信號通路、卵源性因子BMP15在PCOS 卵巢功能障礙發病機制中的作用,為其臨床治療提供思路。

