從馬兜鈴內酰胺探討魚腥草安全性
尹明星,陳 婧,施春陽,王文清,方建國
華中科技大學同濟醫學院附屬同濟醫院 藥學部,湖北 武漢 430030
魚腥草為三白草科植物蕺菜Houttuynia cordataThunb.的新鮮全草或干燥地上部分,別名蕺兒菜、折耳根、葅菜、蕺菜、臭菜等,為藥食同源植物[1-2]。關于魚腥草之名,最初見于東漢《名醫別錄》,東漢《吳越春秋》中稱之為岑草,宋代《會稽賦》注:“岑草,蕺也。”漢代《說文解字》有云:“草祖,菜也。”清代段玉裁注解“草祖”即蕺菜[3]。
魚腥草產于我國長江流域以南各省,在古籍中常稱之為蕺。早在2000 多年前,便有種植、食用魚腥草的文字記載[3-4]。漢代張衡《南都賦》中寫道:“若其園圃,則有蓼蕺蘘荷,薯蔗姜韭潘,菥蓂芋瓜。”唐代蘇頌說:“江左人好生食,關中謂之菹菜,葉有腥氣,故俗稱:魚腥草。”近代《清稗類鈔》有更加詳細的描述:“蕺為蔬類植物,通稱蕺菜,野生,莖細長,高七八寸,葉為卵形。初夏開淡黃色小花,有苞四片,色白如花瓣,莖、葉皆有臭氣,亦稱魚腥草。可食,亦入藥。”由此可見,魚腥草作為食物,已有數千年歷史。特別在我國西南地區,深受人們的歡迎。
魚腥草亦可入藥,其味辛,性微寒,歸肺經,具有清熱解毒、消癰排膿、利尿通淋的功效,用于肺癰吐膿、痰熱咳喘、熱痢、熱淋、癰腫瘡毒等[1]。明代《本草經疏》記載魚腥草“治痰熱壅肺,發為肺癰吐膿血之要藥”。研究表明,魚腥草在抗病毒、抗菌、抗炎[5]、抗氧化等方面有著獨特的藥理活性,相關藥品已廣泛應用于臨床[2,6]。有代表性的中藥制劑有魚腥草滴眼液、復方魚腥草片、急支糖漿、連花清瘟膠囊、小兒咳喘顆粒、咳喘舒丸、祛痰靈口服液、宣肺止嗽合劑、辛夷鼻炎丸、止痛化癥片、復方鮮竹瀝液等。
隨著人們對魚腥草化學組分解析的不斷深入,部分生物堿成分,特別是馬兜鈴內酰胺引起了廣泛關注。一段時期以來,有關魚腥草是否致毒、是否安全的討論此起彼伏。盡管關于魚腥草食用藥用的安全性已有報道[7],但對魚腥草中的關鍵化學成分馬兜鈴內酰胺的安全性尚缺乏系統性梳理和討論。本文從魚腥草中馬兜鈴內酰胺的化學結構出發,從構效關系、量效關系、實驗研究等方面對現有文獻進行綜述,探討魚腥草的安全性,為相關食品藥品研發及應用提供參考。
1 從構效關系探討魚腥草中馬兜鈴內酰胺的安全性
魚腥草的化學成分復雜,主要含有揮發油、黃酮、酚酸、生物堿、萜類、苯乙醇苷、苯丙素等組分[5,7],除揮發油外,其他組分均不揮發。在上述組分中,揮發油、黃酮為研究最廣泛、最主要的藥效成分,可以抗病毒、抗菌、抗炎、抗氧化等;而生物堿,特別是馬兜鈴內酰胺,則是被廣泛關注的可能致毒組分。
截至2020年,已報道的魚腥草中生物堿成分有阿樸菲型、馬兜鈴內酰胺、酰胺類、吡啶類、其他類生物堿5 大類,其中馬兜鈴內酰胺類生物堿共發現了5 個[8-15]。1992年,Pr?bstle 等[9]和Bauer 等[10]首次從干魚腥草中分離得到3 個馬兜鈴內酰胺類化合物,分別是馬兜鈴內酰胺BII(aristolactam BII,又名頭花千金藤酮B,cepharanone B)、馬兜鈴內酰胺 AII (aristolactam AII)、胡椒內酰胺 A(piperolactam A,又名馬兜鈴內酰胺FI,aristolactam FI)。1993年,Jong 等[11]從干魚腥草中分離得到了馬兜鈴內酰胺BII。2001年,Kim 等[12]從干魚腥草中分離得到了馬兜鈴內酰胺BII、胡椒內酰胺A、馬兜鈴內酰胺AII。2011年,Qu 等[13]從鮮魚腥草中分離得到了5 個馬兜鈴內酰胺類化合物,分別是馬兜鈴內酰胺BII、馬兜鈴內酰胺AII、三白草內酰胺(sauristolactam)、胡椒內酰胺A、馬兜鈴內酰胺FII(aristolactam FII)。其中,三白草內酰胺和馬兜鈴內酰胺FII 為首次報道。2013年,姚新生團隊[14-15]從干魚腥草中分離得到了馬兜鈴內酰胺BII、胡椒內酰胺A、馬兜鈴內酰胺AII。
魚腥草中已知的5 種馬兜鈴內酰胺分別為馬兜鈴內酰胺BII、馬兜鈴內酰胺AII、胡椒內酰胺A、三白草內酰胺、馬兜鈴內酰胺FII。它們均在菲環的3、4 位上有甲氧基或羥基取代,化學結構見圖1。

圖1 魚腥草中5 種馬兜鈴內酰胺的化學結構Fig.1 Chemical structures of five aristololactams in Houttuyniae Herba
馬兜鈴內酰胺是一大類化合物的通稱。Kumar等[16]歸納,1982—2003年人們共從天然植物中分離鑒定出57 種馬兜鈴內酰胺類化合物,它們有共同的母體結構,不同的取代基(圖2)。在藥物化學中,藥物的藥效或毒性與化學結構密切相關。結構決定藥效,57 種馬兜鈴內酰胺類化合物的藥理毒理存在較大差異。

圖2 57 種馬兜鈴內酰胺化合物的化學結構Fig.2 Chemical structures of 57 kinds of aristololactams
研究認為,馬兜鈴酸和馬兜鈴內酰胺致毒機制是和DNA 加成形成馬兜鈴酸/馬兜鈴內酰胺-DNA 加成物,引發基因突變,其特征突變是AT-TA 突變[16-19]。由于要與DNA 形成穩定的加成物,馬兜鈴酸/馬兜鈴內酰胺的化學結構需要滿足一定的要求。
Balachandran 等[20]較為全面地研究了馬兜鈴酸致毒的構效關系。研究表明,馬兜鈴酸的硝基是致毒不可或缺的因素,硝基經過還原反應,可與羧基縮合形成酰胺鍵,即馬兜鈴內酰胺。因此,馬兜鈴內酰胺的構效關系與馬兜鈴酸具有一致性。并通過細胞實驗研究了多種具有馬兜鈴酸結構的化合物毒性,結果發現,馬兜鈴酸I [8-甲氧基-6-硝基-菲-(3,4-d)-1,3-二氧代-5-羧酸]的毒性最強;其他對于馬兜鈴酸I 結構的修飾,如加成、消除、取代、側鏈的移位等,均會較大程度地影響其毒性。馬兜鈴酸II [6-硝基-菲-(3,4-d)-1,3-二氧代-5-羧酸]和馬兜鈴酸I 相比,移去了側鏈上的甲氧基基團,它的毒性即有所減弱,但致突變性與馬兜鈴酸I 相當。天然致毒的馬兜鈴酸實質上是指馬兜鈴酸I 和馬兜鈴酸II 的混合物,在諸多馬兜鈴酸中,馬兜鈴酸I 和馬兜鈴酸II 的毒性最強,馬兜鈴酸家族中的其他化合物毒性大大減弱。如馬兜鈴酸C 去除了R1位的甲氧基,在R3位引入羥基,而變得無毒;馬兜鈴酸III 中R1位的甲氧基移位至R3位,毒性消失。
因此,對于馬兜鈴酸的構效關系,可以歸納為向馬兜鈴酸I 的結構中引入羥基,使其水溶性增加,可以有效解毒,如7-羥基馬兜鈴酸I、馬兜鈴酸D、馬兜鈴酸IVa 等。菲環3、4 位間的二氧代五元環的還原或甲基化亦可以使馬兜鈴酸毒性消失。馬兜鈴內酰胺因與馬兜鈴酸存在化學轉化,構效關系與馬兜鈴酸相同。
然而,魚腥草中的5 種馬兜鈴內酰胺卻非致毒結構。對于魚腥草中含有的5 種馬兜鈴內酰胺生物堿,馬兜鈴內酰胺AII、馬兜鈴內酰胺BII、胡椒內酰胺A、三白草內酰胺、馬兜鈴內酰胺FII 均在菲環上引入了羥基或甲氧基,菲環3、4 位間的二氧代五元環均被還原開環或取代,從而毒性消失(圖3)。
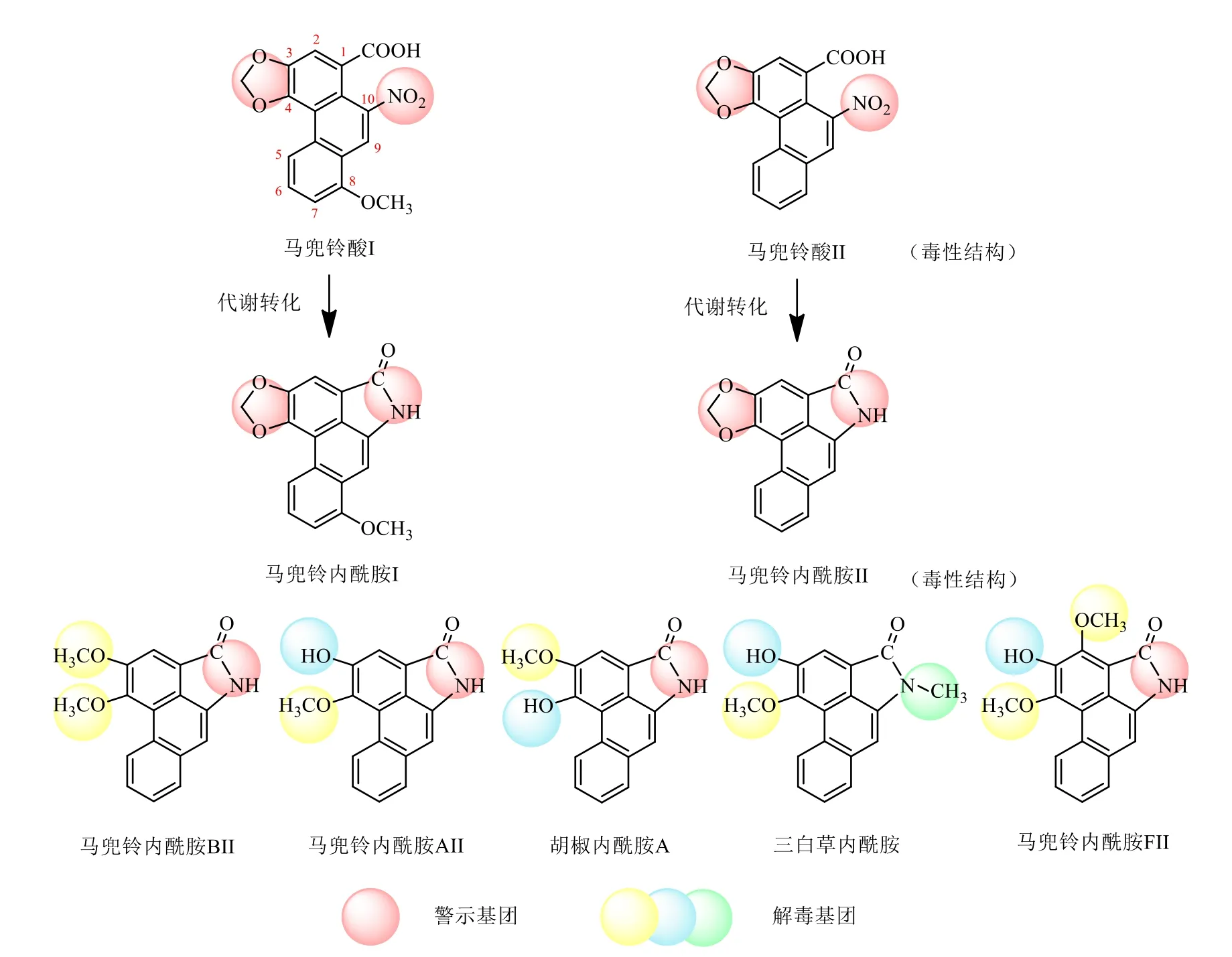
圖3 毒性馬兜鈴酸-馬兜鈴內酰胺的轉化示意圖 (上) 和魚腥草中5 種馬兜鈴內酰胺結構示意圖 (下)Fig.3 Transformation of toxic aristolochic acids to aristololactams (up),and structure diagram of aristololactams in Houttuyniae Herba (down)
此外,在PubChem 數據庫中檢索5 種馬兜鈴內酰胺的生物活性試驗可知,馬兜鈴內酰胺AII 通過CCRIS 突變性試驗(化學致癌研究信息系統中CCRIS 2996)被證實沒有致突變性;馬兜鈴內酰胺BII、胡椒內酰胺A、馬兜鈴內酰胺FII 具有抗炎生物活性,基因毒性比較數據庫(CTD)中未檢索到基因毒性信息;三白草內酰胺具有抗腫瘤活性,CTD中未檢索到基因毒性信息。以上檢索結果進一步證實了魚腥草中5 種馬兜鈴內酰胺生物堿的安全性。
2 從量效關系探討魚腥草中馬兜鈴內酰胺的安全性
在藥理學中,藥物的藥效或毒性與藥物劑量密切相關。一種藥物,只有達到一定的濃度,才會產生治療作用或毒副反應。為了科學、客觀地評價魚腥草的毒性,本文對魚腥草中馬兜鈴內酰胺含量進行了系統梳理。
Pr?bstle 等[9]和Bauer 等[10]研究表明,每350 g干魚腥草中含有馬兜鈴內酰胺BII、馬兜鈴內酰胺AII 和胡椒內酰胺A 分別為3、2、1.5 mg。Jong 等[11]測定每2 kg 干魚腥草中含有馬兜鈴內酰胺BII 25 mg。Kim 等[12]報道每2 kg 干魚腥草中含馬兜鈴內酰胺BII、胡椒內酰胺A、馬兜鈴內酰胺AII 分別為25、13、7 mg。Qu 等[13]測定每10 kg 鮮魚腥草中含馬兜鈴內酰胺BII、馬兜鈴內酰胺AII、三白草內酰胺、胡椒內酰胺A、馬兜鈴內酰胺FII 分別為2、6、10、5、6 mg。姚新生團隊[14-15]報道每5 kg 干魚腥草中含馬兜鈴內酰胺BII、胡椒內酰胺A、馬兜鈴內酰胺AII 分別為28.1、4.1、21.9 mg。
根據文獻報道[9-15]結合不同季節魚腥草鮮品與干品的平均折干比換算[21],每千克鮮魚腥草中5 種馬兜鈴內酰胺生物堿含量見表1。
由表1可以看出,鮮魚腥草中總馬兜鈴內酰胺質量分數為1.2~2.9 mg/kg,最高值為2.9 mg/kg,遠低于公認含馬兜鈴酸毒性藥材(如關木通、廣防己、青木香、細辛等)中馬兜鈴總酸含量。尚明英等[22]分析了20 批關木通藥材,測定其中馬兜鈴酸含量為6.300~2.84 g/kg,最高值為2.84 g/kg,約為魚腥草中總馬兜鈴內酰胺的10 000 倍。姜旭等[23]測定了不同產地青木香中馬兜鈴酸I的質量分數為916.9~1 907.6 mg/kg,最高值為1 907.6 mg/kg,約為魚腥草中總馬兜鈴內酰胺的660 倍。張翠英等[24]測定了3 種細辛果實中馬兜鈴酸I的含量,結果為95~2200 mg/kg,最高值為2200 mg/kg,約為魚腥草中總馬兜鈴內酰胺的760 倍。由此可見,魚腥草中總馬兜鈴內酰胺的含量遠低于毒性藥材中馬兜鈴酸的含量。假定上述5 種馬兜鈴內酰胺的致毒力與毒性最強的馬兜鈴酸I相當,按照《中國藥典》中關木通、青木香、細辛日服臨界劑量換算,若要達到中毒劑量,鮮魚腥草的服用量為2.3~60 kg/d,遠超正常食用、藥用劑量。故從劑量-毒性角度來看,含魚腥草藥物潛在的致毒劑量高,安全窗口大。

表1 鮮魚腥草中馬兜鈴內酰胺生物堿含量Table 1 Content of aristolochia lactam alkaloids in fresh Houttuyniae Herba
3 魚腥草安全性的實驗研究
3.1 魚腥草及其提取物的安全性
馬兜鈴內酰胺難溶于水,可溶于醇。Kang 等[25]從體外、體內多方面研究了魚腥草醇提取物的基因毒性。細菌逆轉突變試驗中,所有受試的沙門氏菌和大腸埃希菌在312.5~5000 μg/皿劑量下,無論是否加入S9 代謝活化劑,均未發生反向突變,不呈現劑量相關性,與陰性對照相比無顯著性差異。染色體畸變試驗顯示,魚腥草醇提物1.25~5 μg/mL 處理過的中國倉鼠卵巢細胞,染色體畸變細胞數與陰性對照組相比無顯著性差異。在小鼠骨髓微核細胞實驗中,研究者向ICR 小鼠ip 魚腥草醇提物最高劑量(2 g/kg),結果顯示,魚腥草醇提物處理的小鼠嗜多染紅細胞指數無劑量相關性,與陰性對照相比無顯著性差異,遠低于陽性對照苯并芘和絲裂霉素C。得出結論魚腥草醇提物在細菌、哺乳動物細胞、小鼠骨髓水平上均不顯基因毒性。
徐彩菊等[26]研究了魚腥草鮮汁原液的口服毒性和致突變性。結果表明,口服魚腥草鮮汁原液的大鼠和小鼠均未出現明顯的中毒癥狀及死亡,其半數致死量大于10 g/kg,屬于實際無毒物;Ames 試驗、微核試驗、精子畸形實驗等表明,魚腥草鮮汁原液無致突變性和致畸性。
李潔等[27]采用網絡藥理學的方法預測并分析了魚腥草中主要活性物質的毒性作用機制。研究結果顯示,與魚腥草化學成分聯系最密切的信號通路依次為Toll 樣受體信號通路、絲裂原活化蛋白激酶信號通路、核苷酸寡聚化結構域樣受體信號通路、視黃酸誘導基因蛋白I 樣受體信號通路、哺乳動物雷帕霉素靶蛋白信號通路等,這些通路均為炎癥相關信號通路,分析結果中未見致突變、致癌等顯著相關的不良反應/毒性活性。
丁超[28]采用橫斷面研究,分析了中國各地區人群魚腥草食用習慣對腎臟疾病的影響。結果顯示,不同魚腥草食用指數組別間腎病患病率無顯著性差異。在調整了年齡、性別等混雜因素后,魚腥草的食用習慣仍然與急慢性腎病患病率無相關性,且未發現罹患泌尿系統惡性腫瘤的病例。
魚腥草的醇提取物、鮮汁原液和可食用部分均含有馬兜鈴內酰胺成分,研究表明魚腥草醇提取物和鮮汁原液無基因毒性、致突變性和致畸性,食用魚腥草與急慢性腎病患病率無相關性。多項研究共同說明了魚腥草及其提取物無基因毒性的特性,這與本文探討魚腥草中馬兜鈴內酰胺的構效關系、量效關系得出的結論相吻合。
3.2 含魚腥草制劑的安全性
當前,已批準的含魚腥草制劑涵蓋口服制劑、眼用制劑、鼻用制劑、注射劑等多種劑型,其中口服制劑和外用制劑的安全性均較好。復方魚腥草顆粒和復方魚腥草滴丸治療急性上呼吸道感染不良反應發生率極低,與對照組相當[29-31];魚腥草滴眼液、魚腥草滴鼻液和魚腥草鼻用噴霧劑等局部給藥制劑,臨床使用安全可靠,未見明顯不良反應[32-37]。含魚腥草制劑的不良反應更多發生在注射劑領域。2006年2月,浙江金華1 例4 歲患者在靜脈滴注魚腥草注射液時發生抽搐、昏迷等嚴重不良反應事件;2006年5月,湖北武漢1 例3 歲患者在靜脈滴注魚腥草注射液時發生過敏性休克,不治身亡[38];2006年6月,國家藥品監督管理局緊急停用魚腥草注射液等7 種中藥注射液[39]。后續研究發現,魚腥草注射液的不良反應可能與吐溫80 這一輔料密切相關[39-40]。李連達等[41]進一步測算,魚腥草注射液的實際致死率約為0.000 021%,遠低于青霉素、慶大霉素等化學藥注射劑。但筆者認為,魚腥草注射液應進行嚴格的安全性再評價及質量控制,對于這類制劑的使用現階段仍應持審慎態度。
相比于注射劑,含魚腥草的口服制劑及外用制劑的安全性更高,未見嚴重不良反應事件報道。對于含魚腥草藥物安全性的評價,應以不同的劑型、不同的給藥方式分開看待。
4 結語
魚腥草清熱解毒、消癰排膿、利尿通淋,為治療肺癰之要藥。作為藥食同源植物,魚腥草藥用、食用歷史均已逾千年,我國西南地區更有常年食用魚腥草的習慣。本文從魚腥草中馬兜鈴內酰胺的化學結構出發,從構效關系、量效關系、實驗研究等方面深入探討了魚腥草的安全性,結果表明含魚腥草的食品及口服、外用藥品具有較高的安全性。
(1)魚腥草中含有5 種結構的馬兜鈴內酰胺(馬兜鈴內酰胺BⅡ、馬兜鈴內酰胺AⅡ、胡椒內酰胺A、馬兜鈴內酰胺FⅡ、三白草內酰胺),它們在魚腥草中質量分數(1.2~2.9 mg/kg)非常低,遠低于含馬兜鈴酸毒性藥材中有毒組分含量(僅為毒性藥材中馬兜鈴酸I質量當量的1/10 000~1/660),正常食用或制成藥物攝入量十分有限;(2)這5 種結構的馬兜鈴內酰胺根據構效關系分析均為無毒結構(菲環3、4 位的二氧代五元環開環、菲環上有羥基取代);(3)體外、體內實驗聯合證實,魚腥草鮮汁原液和醇提取物無致突變性和致畸性;(4)除魚腥草注射液外,含魚腥草的口服、外用制劑均未見嚴重不良反應報道。
本文從化學單體、部分提取物、魚腥草藥材及制劑3 個維度進行了深入分析,這3 個維度彼此聯系,互相佐證,由量效關系、構效關系結合植物提取物的實驗結果外推至魚腥草藥材的安全性,并與現有含魚腥草口服外用制劑的臨床研究相結合,辯證分析了魚腥草在不同使用方式下的安全性,希望能夠推動魚腥草醫藥大健康產品的研發工作,同時為含魚腥草藥品的合理應用提供指導和依據。
利益沖突所有作者均聲明不存在利益沖突

