運動調(diào)控高鹽膳食果蠅運動能力和生命周期的機制
——基于Salt與Foxo基因過表達
文登臺,后文其,郗增輝,翟帥帥
(魯東大學體育學院,山東煙臺 264025)
適量用鹽(主要為NaCl)能改善人體生理功能,如維持神經(jīng)、肌肉的正常興奮性等[1]。但長期過量攝入食用鹽將誘發(fā)高血壓、胃癌、糖尿病、心力衰竭等多種重大慢性疾病,并使死亡率增加[2-3]。世界衛(wèi)生組織推薦每天食用鹽的攝入量應不多于5 g,而我國居民每天食用鹽攝入量高達13.5 g,是世界衛(wèi)生組織推薦量的2.5倍多。動物實驗研究[4]發(fā)現(xiàn),高鹽膳食能抑制大鼠骨骼肌血管的生成,導致骨骼肌收縮功能障礙,其主要機制與骨骼肌的氧化應激增加有關。運動鍛煉是全世界公認的、能有效促進健康的方式之一,能預防或減輕許多慢性疾病并提高生存率[5]。有研究[6]發(fā)現(xiàn),運動鍛煉能促進人體骨骼肌血管生成,提高骨骼肌的抗氧化能力,從而增強骨骼肌的收縮功能。但長期運動訓練與高鹽攝入共存時,前者能否有效對抗后者誘發(fā)的壽命縮短和運動能力降低,這一問題仍有待明確,相關的分子機制也需進一步闡明。
果蠅是遺傳學研究的經(jīng)典模式生物,在果蠅中發(fā)現(xiàn)的許多信號分子通路及基因功能與哺乳動物及人具有同源性[7],且其與哺乳動物一樣對運動和營養(yǎng)具有保守性,因此,果蠅逐漸被運用于運動與肥胖、運動與衰老、運動與心肌病的分子機制研究[8-11]。果蠅鹽(Salt)基因與人類溶質(zhì)載體家族5成員12(Solute Carrier Family 5 member 12,SLC5A12)基因?qū)偻椿颍瑑烧咴诠δ苌暇哂斜J匦裕芫幋a鈉-溶質(zhì)同向轉(zhuǎn)運體。研究[12-13]表明:果蠅高鹽膳食后壽命縮短,其主要機制與高鹽誘發(fā)果蠅Salt基因表達上調(diào)有關;果蠅Salt基因過表達也能造成壽命縮短,這與高鹽膳食效應類似;Salt基因敲減能增加高鹽膳食果蠅的存活率。因此,研究提示,Salt基因是調(diào)控鹽耐受性的關鍵基因,但其在運動抵抗高鹽中發(fā)揮的作用仍不清楚。
本文首先對野生型果蠅進行運動訓練和高鹽膳食干預,通過檢測果蠅運動能力、壽命和骨骼肌超氧化物歧化酶(Superoxide Dismutase,SOD)活力水平、丙二醛(Malondialdehyde,MDA)水平、活性氧(Reactive Oxygen Species,ROS)水平、Salt基因及叉頭轉(zhuǎn)錄因子O(transcription factor of the forkhead box class O,F(xiàn)oxo)基因表達情況,初步分析運動抵抗高鹽應激誘發(fā)果蠅運動能力和壽命損害的分子機制;然后,通過上游激活序列(Upstream Active Sequence,UAS)/半乳糖調(diào)節(jié)上游啟動子元件(galactose-regulated upstream promoter element,Gal4)系統(tǒng)構建Salt基因、Foxo基因過表達模型,進一步研究Salt基因與Foxo/SOD通路在運動抵抗高鹽應激中的作用,旨在為高鹽攝入群體的運動健身提供理論依據(jù)。
1 材料與方法
1.1 果蠅品系
野生型w1118(品系號:3605)、arm-Gal4(品系號:39249)、Salt-UAS-過表達型(品系號:58888)和Foxo-UAS-過表達型(品系號:9575)4種品系果蠅均來自伯明頓果蠅品系中心(Bloomington Drosophila Stock Center)。將含UAS和Gal4序列不同品系的果蠅雜交,構建UAS/Gal4系統(tǒng),對目的基因進行表達調(diào)控[14]。所有果蠅放置在恒溫25℃、恒濕50%、12 h晝夜循環(huán)的環(huán)境下培養(yǎng)。
1.2 雜交及分組
將雄性野生型w1118、Salt-UAS-過表達型(基因型:w*;TI{TI}miR-1014KOSaltmiR-1014-KO)、Foxo-UAS-過表達型(基因型:y1w*;P{UAS-Foxo.P}2)果蠅分別與雌性arm-Gal4果蠅雜交,收集的F1代羽化12 h內(nèi)的雄蠅分別是基因正常表達(arm-Gal4>w1118)、Salt過表達(arm-Gal4>Salt-UAS-過表達)和Foxo過表達(arm-Gal4>Foxo-UAS-過表達)果蠅(圖1)。其中:arm-Gal4>w1118果蠅分為對照組、高鹽組、運動組和高鹽運動組;arm-Gal4>Salt-UAS-過表達果蠅分為Salt組和Salt+運動組;arm-Gal4>Foxo-UAS-過表達果蠅分為Foxo組和Foxo+高鹽組。共8組,每組350只果蠅,共2 800只。
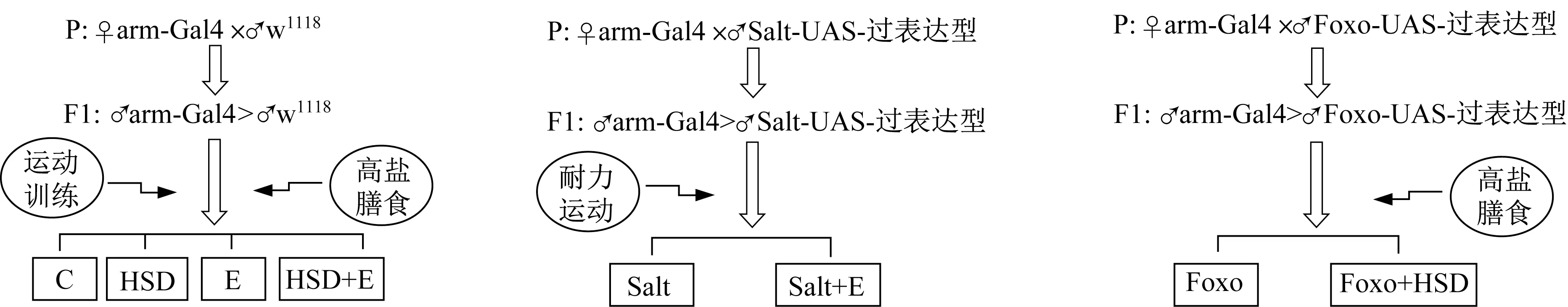
圖1 果蠅雜交及分組示意Figure 1 Diagram of Drosophila hybridization and grouping
1.3 運動訓練方案
利用果蠅逆重力攀爬特性,使其在運動平臺(自主研發(fā),專利號:ZL201920960000.4)上進行攀爬運動訓練。試管固定于試管夾上并與地面垂直,此時果蠅做垂直于地面的攀爬運動,當果蠅爬到試管頂部時,試管自動翻轉(zhuǎn)180°,果蠅又回到試管底部,繼續(xù)攀爬運動訓練(圖2),攀爬時的負重等于果蠅體質(zhì)量。運動組果蠅均放到運動裝置上,每管20只,果蠅每次翻轉(zhuǎn)至試管底部后,給予10 s做向上攀爬運動,試管長約8 cm,每天運動1.5 h,每周連續(xù)運動干預5 d,休息2 d,持續(xù)運動干預2周,在第2周齡末檢測各指標。通過觀察果蠅攀爬過程中能否跟上翻轉(zhuǎn)速度,以及是否保持逆重力攀爬和趨光特性來判斷是否產(chǎn)生運動疲勞。由于逆重力攀爬是果蠅自發(fā)的運動,且運動持續(xù)時間達到1.5 h才產(chǎn)生疲勞現(xiàn)象,因此,國內(nèi)外學者將其定義為果蠅耐力運動[10-11]。
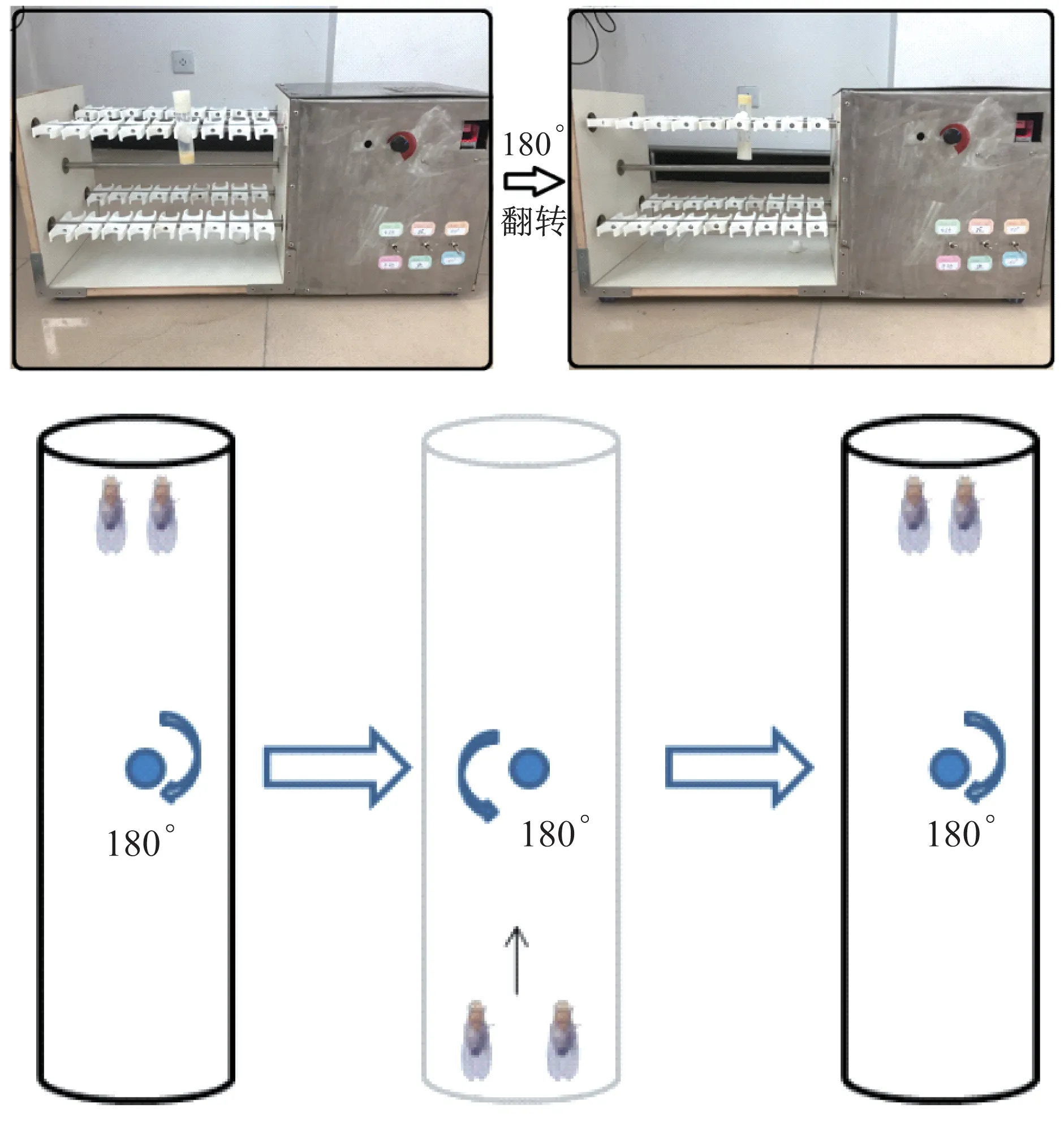
圖2 果蠅運動平臺和攀爬訓練示意Figure 2 Schematic diagram of Drosophila exercise platform and climbing training
1.4 正常膳食和高鹽膳食配制
(1)正常膳食:在鍋中加入水、黃豆粉、酵母粉、玉米粉攪勻,并在加熱過程中加入瓊脂,直至溶液沸騰。沸騰后停止加熱,冷卻過程中加入蔗糖和麥芽糖,待蔗糖和麥芽糖充分溶解后,加入防腐劑丙酸和對羥基苯,充分攪拌后立即分裝于潔凈的培養(yǎng)管中,每管培養(yǎng)基厚度約為0.5 cm。
(2)高鹽膳食:在正常食物配制過程中加入2%的食用鹽(99%NaCl),充分溶解。
(3)膳食方案:從第2天齡開始,將高鹽組果蠅從正常食物中轉(zhuǎn)移至高鹽食物中飼養(yǎng),直至果蠅死亡。對于正常膳食果蠅和高鹽膳食果蠅,每天早晚向試管壁加入0.2 mL純凈水,供其飲用(圖3),相對于前人研究[12]中只喂食高鹽膳食而未提供飲用水,本實驗的膳食條件為溫和的高鹽膳食。

圖3 高鹽膳食果蠅正在飲水Figure 3 Drosophila on a high-salt diet are drinking water
1.5 各指標檢測方法
1.5.1 酶聯(lián)免疫吸附試驗(Enzyme Linked Immunosorent Assay,ELISA)檢測果蠅SOD活力水平、MDA水平和ROS水平
每管取10只果蠅骨骼肌置于500μL磷酸鹽緩沖液中,用于檢測SOD活力水平、MDA水平和ROS水平,重復3次,共需30只果蠅。ELISA檢測步驟如下:用細胞破碎儀使果蠅骨骼肌細胞破裂,將勻漿液于4℃、2 504g離心15 min,取上清備用。于各標準品孔加不同濃度的標準品50μL;樣本孔中加入待測樣本50μL,設3個復孔;空白孔不加。除空白孔外,于標準品孔和樣本孔中,每孔加入辣根過氧化物酶標記的檢測抗體100μL,用封板膜封住反應孔,37℃水浴鍋或恒溫箱孵育60 min。棄去液體,于吸水紙上拍干;每孔加滿洗滌液(350μL)靜置1 min,甩去洗滌液,于吸水紙上拍干,如此重復洗板5次。然后每孔加入底物A、B各50μL,37℃避光孵育15 min。每孔加入終止液50μL,15 min內(nèi)在450 nm波長處測定各孔的光密度值。以所測標準品的光密度值為橫坐標,濃度值為縱坐標,在坐標紙上或用相關軟件繪制標準曲線,并得到直線回歸方程,然后將樣品的光密度值代入方程,計算出樣品的濃度。
1.5.2 實時熒光定量聚合酶鏈反應(quantitative Re?al-Time Polymerase Chain Reaction,qRT-PCR)檢測基因信使核糖核酸(messenger Ribose Nu?cleic Acid,mRNA)表達情況
每管取10只果蠅骨骼肌,加入1 mL的TRIzol試劑提取總RNA,取2μL RNA進行反轉(zhuǎn)錄獲得互補DNA。以核糖體蛋白L32(Ribosomal Protein L32,Rp49)基因為內(nèi)參照,利用美國Bio-Rad公司產(chǎn)96孔熒光定量實時PCR儀、日本TaKaRa公司產(chǎn)RR820A SYBR?PCR試劑盒進行PCR擴增。使用Premiers 5.0軟件設計引物序列,并經(jīng)NCBI BLAST基因庫檢索驗證,與其他基因無高度同源性。然后由生工生物工程(上海)股份有限公司合成引物并純化,引物序列如下:Salt上游引物5′-TTAATCGCAGGCGCGTCAGTG-3′,下游引物5′-GGACGAGACCACCGTGTTAATCAG-3′;Foxo上游引物5′-AACAACAGCAGCATCAGCAG-3′,下游引物5′-CTGAACCCGAGCATTCAGAT-3′;Rp49上 游 引 物5′-CTAAGCTGTCGCACAAATGG-3′,下游引物5′-AACTTCTTG AA TCCGGTGGG-3′。PCR反應體系:2×SYBR?Premix Ex Taq?試劑15μL、上 游 引 物(10μmol/L)0.5μL、下 游 引 物(10μmol/L)0.5μL、參比染料0.6μL、cDNA模板5μL、雙蒸水8.4μL;總體系30μL,每個樣本分3個復孔,每孔10μL。PCR反應條件:95℃30 s,95℃5 s、60℃30 s循環(huán)40次。每組重復3次,共需30只果蠅。PCR擴增后用2%的瓊脂糖凝膠電泳鑒定,并計算各組基因的mRNA相對表達量及過表達率。
1.5.3 電子顯微鏡觀察骨骼肌超微結構
將果蠅麻醉,去掉翅膀、頭部及腹部,將胸部放入固定液(含2.5%戊二醛的磷酸鹽緩沖液)固定至少2 h,用0.1 mol/L磷酸漂洗液漂洗3次,每次10~15 min。然后用1%鋨酸固定液固定1~2 h,用0.1 mol/L磷酸漂洗液漂洗3次,每次10~15 min。用50%丙酮10~15 min、70%丙酮10~15 min、90%丙酮10~15 min、100%丙酮15~20 min(中途更換1次)進行梯度脫水。用純丙酮+包埋液(體積比為1∶1)37℃12 h或純包埋液37℃10~12 h進行浸泡和包埋。37℃烘箱內(nèi)過夜或60℃烘箱內(nèi)12~24 h固化。采用超薄切片機切片,層厚50~100 nm;用3%醋酸鈾及硝酸鉛進行雙染色。使用HT-7700透射電子顯微鏡觀察并拍照。
1.5.4 運動能力檢測
每組取100只果蠅,每管20只果蠅,用NVGS400攝像機拍攝果蠅震落至培養(yǎng)管底部后負趨地性爬行的行為學特征,以果蠅攀爬高度評定果蠅運動能力,即將全部果蠅個體震落至試管底部后,測量出第2 s時所有果蠅的攀爬高度。
1.5.5 生命周期統(tǒng)計
每組取200只果蠅,每天18︰00—19︰00觀察和記錄果蠅死亡數(shù),直到各組果蠅全部死亡為止,繪制果蠅存活曲線。全部果蠅壽命的算術平均數(shù)為果蠅的平均壽命,平均壽命延長率=(實驗組平均壽命-對照組平均壽命)/對照組平均壽命×100%。統(tǒng)計各組果蠅平均壽命和平均壽命延長率。
1.6 統(tǒng)計學方法
應用SPSS 17.0軟件和GraphPad Prism 8軟件分別進行統(tǒng)計學分析和制圖。數(shù)據(jù)以平均數(shù)±標準差形式表示,若方差齊則用參數(shù)檢驗的獨立樣本t檢驗進行組間比較,若方差不齊則用t’檢驗進行組間比較。果蠅存活率的比較采用非參數(shù)log-rank檢驗。檢驗水準(α)為0.05。
2 結果
2.1 果蠅Salt基因mRNA及抗氧化指標的檢測結果
高鹽組果蠅Salt基因的mRNA表達水平高于對照組(P<0.01),相對過表達率約為142.00%;運動組果蠅Salt基因的mRNA表達水平與對照組相比無顯著性差異(P>0.05);高鹽運動組果蠅Salt基因的mRNA表達水平低于高鹽組(P<0.05),相對過表達率約為-11.16%;Salt組果蠅Salt基因的mRNA表達水平高于對照組(P<0.01),相對過表達率約為55.00%;Salt+運動組果蠅Salt基因的mRNA表達水平與Salt組相比無顯著性差異(P>0.05);Foxo組果蠅Salt基因的mRNA表達水平與對照組相比無顯著性差異(P>0.05);Foxo+高鹽組果蠅Salt基因的mRNA表達水平低于高鹽組(P<0.05),相對過表達率約為-13.63%。見表1。
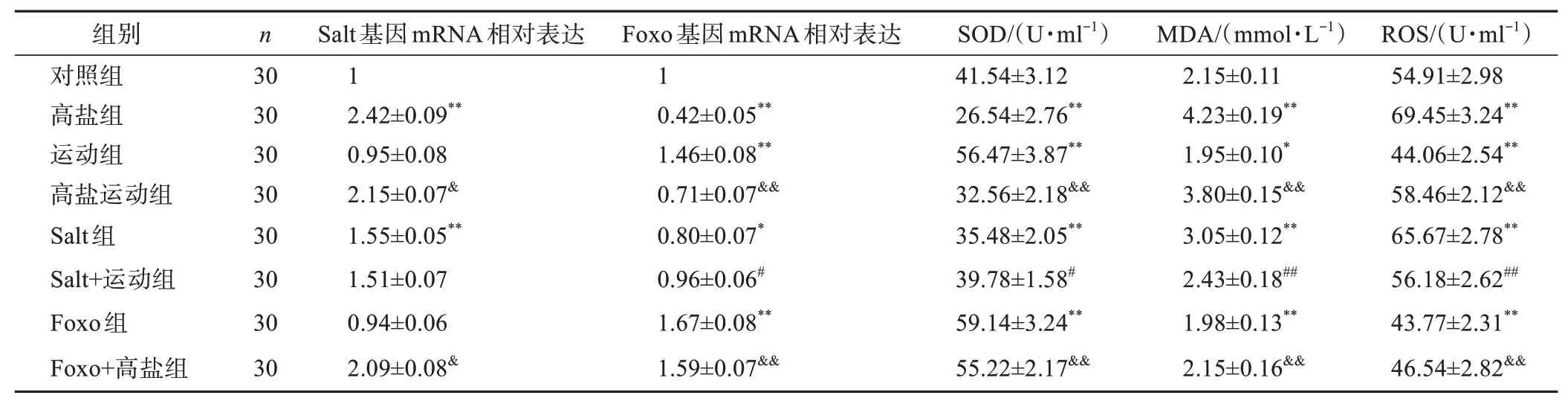
表1 Salt基因表達及氧化應激各指標檢測結果(xˉ±s)Table 1 Salt gene expression and oxidative stress index detection results(xˉ±s)
高鹽組果蠅Foxo基因的mRNA表達水平低于對照組(P<0.01),相對過表達率約為-58.00%;運動組果蠅Foxo基因的mRNA表達水平高于對照組(P<0.01),相對過表達率約為46.00%;高鹽運動組果蠅Foxo基因的mRNA表達水平高于高鹽組(P<0.01),相對過表達率約為69.05%;Salt組果蠅Foxo基因的mRNA表達水平低于對照組(P<0.05),相對過表達率約為-18.00%;Salt+運動組果蠅Foxo基因的mRNA表達水平高于Salt組(P<0.05),相對過表達率約為20.00%;Foxo組果蠅Foxo基因的mRNA表達水平高于對照組(P<0.01),相對過表達率約為67.00%;Foxo+高鹽組果蠅Foxo基因的mRNA表達水平高于高鹽組(P<0.01),相對過表達率約為278.00%。見表1。
高鹽組果蠅SOD活力水平低于對照組(P<0.01),MDA和ROS水平均高于對照組(P<0.01);運動組果蠅SOD活力水平高于對照組(P<0.01),MDA和ROS水平均低于對照組(P<0.05、P<0.01);高鹽運動組果蠅SOD活力水平高于高鹽組(P<0.01),MDA和ROS水平均低于高鹽組(P<0.01);Salt組果蠅SOD活力水平低于對照組(P<0.01),MDA和ROS水平均高于對照組(P<0.01);Salt+運動組果蠅SOD活力水平高于Salt組(P<0.05),MDA和ROS水平均低于Salt組(P<0.01);Foxo組果蠅SOD活力水平高于對照組(P<0.01),MDA和ROS水平均低于對照組(P<0.01);Foxo+高鹽組果蠅SOD活力水平高于高鹽組(P<0.01),MDA和ROS水平均低于高鹽組(P<0.01)。見表1。
2.2 果蠅運動能力檢測結果
對照組果蠅2 s攀爬高度大于高鹽組[P<0.01,圖4(a)],高鹽組果蠅胸腔骨骼肌電子顯微鏡圖像顯示骨骼肌中肌原纖維遭受較嚴重的破壞(圖5)。運動組果蠅2 s攀爬高度大于對照組[P<0.05,圖4(b)],果蠅骨骼肌中肌原纖維與對照組相比破壞減少(圖5)。高鹽運動組果蠅2 s攀爬高度大于高鹽組[P<0.01,圖4(c)],果蠅骨骼肌中肌原纖維遭受的破壞明顯少于高鹽組(圖5)。對照組果蠅2 s攀爬高度與Salt組果蠅相比無顯著性差異[P>0.05,圖4(d)],但Salt組果蠅骨骼肌中肌原纖維遭受的破壞比對照組嚴重(圖5)。Salt+運動組果蠅2 s攀爬高度大于Salt組[P<0.05,圖4(e)],骨骼肌中肌原纖維破壞與Salt組相比較少(圖5)。Foxo組果蠅2 s攀爬高度大于對照組[P<0.01,圖4(f)],骨骼肌中肌原纖維破壞與對照組相比較少(圖5)。Foxo+高鹽組果蠅2 s攀爬高度大于高鹽組[P<0.01,圖4(g)],骨骼肌中肌原纖維破壞與高鹽組相比明顯減少(圖5)。
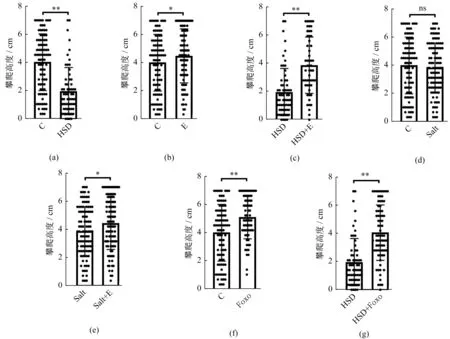
圖4 各組果蠅1周齡末2 s攀爬高度的比較Figure 4 Climbing height comparision of 1-week-old Drosophila in 2 secends
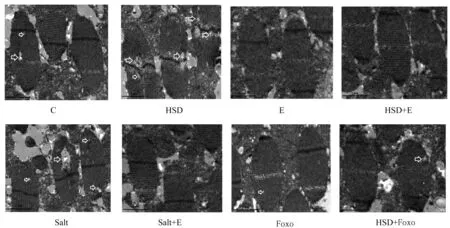
圖5 各組果蠅骨骼肌透射電子顯微鏡圖像結果Figure 5 Results of obvious transmission electron microscope image of Drosophila skeletal muscle
2.3 果蠅生命周期檢測結果
對照組果蠅的存活率高于高鹽組(P<0.01),對照組果蠅的平均壽命約為59 d,高鹽組果蠅的平均壽命約為47 d,高鹽組壽命縮短率為20.34%。高鹽運動組果蠅的存活率高于高鹽組(P<0.05),高鹽運動組果蠅的平均壽命約為53 d,高鹽組果蠅的平均壽命約為47 d,高鹽運動組壽命延長率為12.77%。運動組果蠅的存活率高于對照組(P<0.05),運動組果蠅的平均壽命約為65 d,對照組果蠅的平均壽命約為59 d,運動組壽命延長率為10.17%。對照組果蠅的存活率高于Salt組(P<0.01),對照組果蠅的平均壽命約為59 d,Salt組果蠅的平均壽命約為45 d,Salt組壽命縮短率為23.73%。Salt+運動組果蠅的存活率高于Salt組(P<0.05),Salt+運動組果蠅的平均壽命約為52 d,Salt組果蠅的平均壽命約為45 d,Salt+運動組壽命延長率為15.56%。Foxo組果蠅的存活率高于對照組(P<0.05),F(xiàn)oxo組果蠅的平均壽命約為64 d,對照組果蠅的平均壽命約為59 d,F(xiàn)oxo組壽命延長率約為8.47%。Foxo+高鹽組果蠅的存活率高于高鹽組(P<0.01),F(xiàn)oxo+高鹽組果蠅的平均壽命約為59 d,高鹽組果蠅的平均壽命約為47 d,F(xiàn)oxo+高鹽組壽命延長率為25.53%。見圖6。
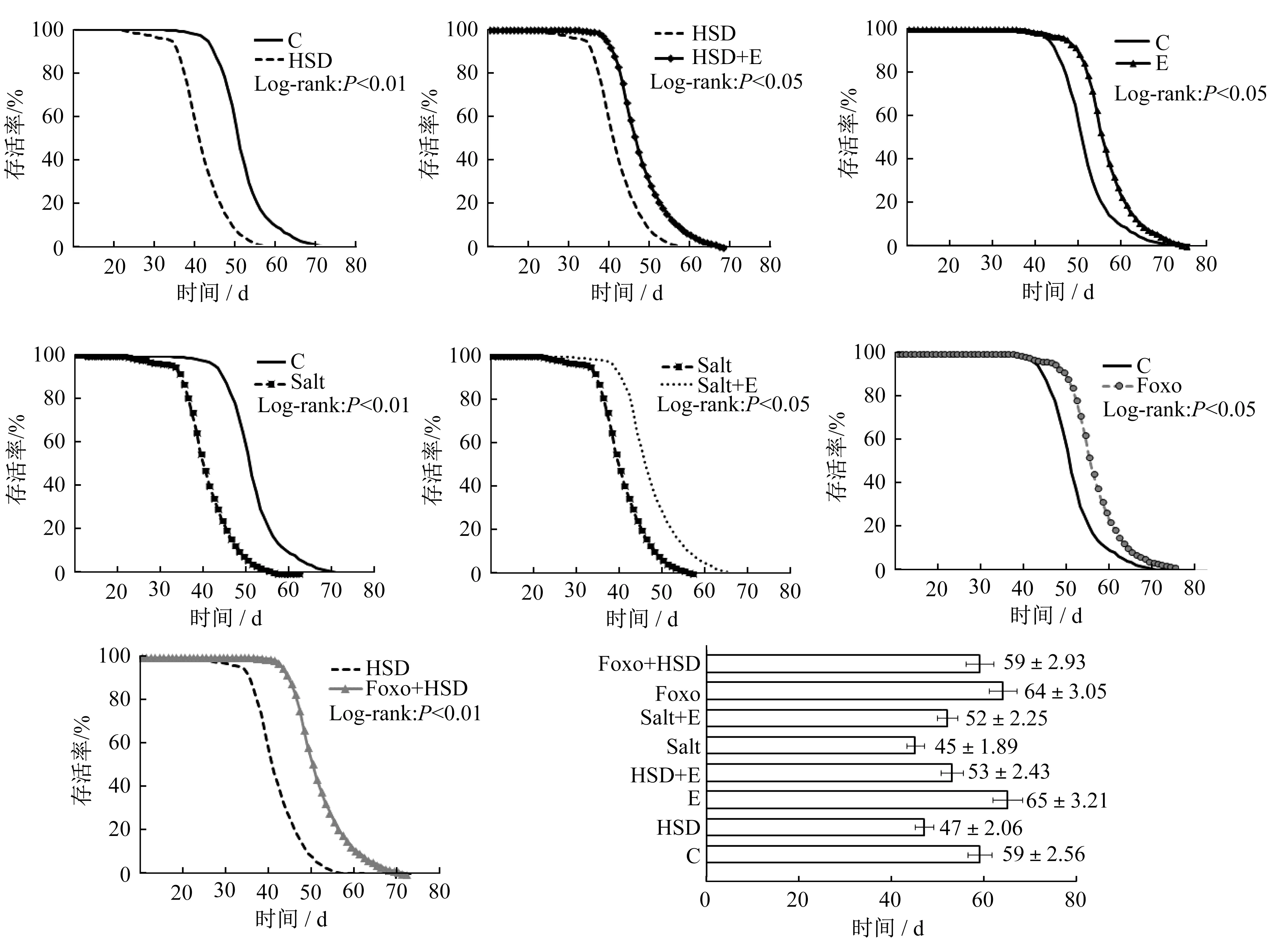
圖6 果蠅存活率和平均壽命比較Figure 6 Comparison of survival results and mean lifespan in Drosophila
3 討論
3.1 耐力運動對高鹽膳食果蠅運動能力和壽命的影響
研究[15]表明,在哺乳動物中,高鹽膳食能減弱機體組織器官(如腎臟、心臟和大腦等)的抗氧化功能,增強氧化應激及損傷,從而誘發(fā)疾病。此外,高鹽膳食能通過抑制血管緊張素Ⅱ和增強氧化應激損害骨骼肌功能[4]。相反,運動訓練能促進骨骼肌血液循環(huán)和提高抗氧化能力,從而提高骨骼肌收縮能力[6]。但運動鍛煉能否抵抗高鹽膳食對骨骼的損害,其分子機制如何,國內(nèi)外鮮有相關報道。
本文通過給予果蠅高鹽膳食和運動訓練干預發(fā)現(xiàn),高鹽膳食能明顯降低果蠅快速攀爬能力,并破壞骨骼肌的正常結構。此外,本文結果還顯示,高鹽膳食不僅能誘發(fā)果蠅Salt基因表達上調(diào),也減弱了機體的抗氧化能力,增加脂毒性物質(zhì)MDA,提升ROS水平;但通過運動訓練干預,高鹽膳食果蠅的快速攀爬能力明顯提升,壽命得到顯著延長,Salt基因表達明顯下降,機體抗氧化能力明顯提高。這一結果提示,運動訓練能明顯改善高鹽膳食對果蠅運動能力和壽命的不利影響,其分子機制與Salt基因表達改善和機體抗氧化能力提高有關。Salt基因編碼的鈉-溶質(zhì)同向轉(zhuǎn)運體是溶質(zhì)轉(zhuǎn)運家族的成員,參與機體對鹽分失調(diào)的應答[16]。研究[17-18]證實,鹽敏感性與氧化應激反應增強、超氧陰離子產(chǎn)生增加密切相關,高鹽攝入能激活腎素-血管緊張素-醛固酮系統(tǒng),造成ROS產(chǎn)生增多,導致氧化應激增強,其主要機制與高鹽攝入增加還原型煙酰胺腺嘌呤二核苷酸磷酸(Nicotinamide Adenine Dinucleotide Phosphate,NADPH)氧化酶的活性使體內(nèi)超氧陰離子生成增多有關。在進行有氧耐力鍛煉的過程中,機體會逐漸出現(xiàn)缺氧現(xiàn)象,氧自由基逐漸產(chǎn)生,運動疲勞隨之而來。運動后,機體通過一系列反應來糾正內(nèi)環(huán)境穩(wěn)態(tài)破壞的狀態(tài),包括不斷合成抗氧化因子SOD、過氧化氫酶(Catalase,CAT)和谷胱甘肽(GSH)等,以及清除氧自由基和減少脂毒性損傷等。因此,運動鍛煉和適當休息能使機體不斷經(jīng)歷“氧化應激-自由基清除-一時性超量恢復-氧化應激”這一循環(huán)過程。這種長期有規(guī)律的刺激導致機體抗氧化因子隨著每次的“一時性-適應性增強”逐漸轉(zhuǎn)變?yōu)椤俺志眯栽鰪姟保ㄊ筍OD活力水平升高及Foxo基因表達增加等[19-20]。因此,有規(guī)律的、適宜的運動鍛煉能提高機體的抗氧化能力,減少組織器官(包括骨骼肌、心臟和大腦等)的氧化損傷。
在果蠅中,氧化應激增加是導致果蠅運動能力減弱、死亡率增加及衰老加快的主要原因[21]。研究[22]報道,果蠅進行飛行訓練后壽命顯著縮短,其主要原因是果蠅的飛行屬于高強度運動,運動過程中產(chǎn)生大量氧自由基,這使氧化應激超出果蠅承受和恢復的極限。相反,果蠅規(guī)律的攀爬運動已被國內(nèi)外學者證實能延長果蠅壽命,提高心臟功能和運動能力[23]。此外,果蠅規(guī)律的攀爬運動能減少高脂膳食帶來的脂質(zhì)堆積,減少脂毒性損傷,降低脂毒性心肌病的發(fā)生風險,并延長生命周期[8]。其機制與規(guī)律運動提高果蠅SOD活力水平、增強Foxo基因表達、減少MDA和ROS有關。因此,耐力運動能通過增強高鹽膳食果蠅的抗氧化能力和下調(diào)Salt基因表達來改善其運動能力和存活率,并有效保護其骨骼肌和肌原纖維的完整性。盡管如此,本文結果還顯示,運動鍛煉并不能完全逆轉(zhuǎn)高鹽膳食對果蠅壽命的損害,其主要機制與該組果蠅的氧化應激和Salt基因表達未恢復到正常飲食果蠅水平有關,這說明高鹽膳食對壽命的危害大于運動的延長壽命效益。此外,在正常飲食的果蠅中,運動并不能明顯下調(diào)Salt基因表達,提示Salt基因可能不參與耐力運動對高鹽膳食果蠅影響的機制調(diào)節(jié)。
3.2 耐力運動對Salt基因過表達果蠅運動能力和壽命的影響
果蠅Salt基因與人類SLC5A12基因?qū)偻椿颍幋a鈉-溶質(zhì)同向轉(zhuǎn)運體,果蠅Salt基因表達上調(diào)能使鈉-溶質(zhì)同向轉(zhuǎn)運體表達增加,這將造成過多鈉離子被腸道吸收,果蠅血液、淋巴和細胞質(zhì)中鈉離子濃度增加,內(nèi)環(huán)境穩(wěn)態(tài)破壞,因此,Salt基因過表達果蠅在正常飲食情況下壽命也會縮短[12,16]。關于人類SLC5A12基因是否與人體鹽耐受性有關,國內(nèi)外研究[21-23]仍較少。本文結果顯示,果蠅Salt基因過表達對其壽命的影響與既往研究結果類似,Salt基因過表達能縮短果蠅壽命。此外,本文還發(fā)現(xiàn),果蠅Salt基因過表達能削弱其運動耐受性,這可能與Salt基因過表達果蠅的骨骼肌遭受損傷有關。與果蠅高鹽膳食結果類似,果蠅Salt基因過表達能顯著下調(diào)Foxo基因表達,減少SOD的活力,使毒性產(chǎn)物MDA和ROS增加。研究[6]表明,在果蠅Salt基因敲減的情況下,高鹽膳食不能顯著縮短果蠅的壽命。因此,推測果蠅Salt基因過表達導致其鹽耐受性降低,機體內(nèi)鈉離子代謝紊亂,鈉離子超載造成果蠅機體抗氧化能力降低,氧自由基攻擊骨骼肌致使運動能力減弱,同時,氧自由基也會攻擊其他組織和器官導致果蠅壽命縮短[24]。
研究[25]表明,耐力運動對哺乳動物和果蠅的運動能力和壽命產(chǎn)生良好效應,其機制與抗氧化能力增強密切相關,在不同的遺傳背景下,運動訓練可能對運動能力和壽命造成不利影響。為進一步證實抗氧化性是否為耐力運動增強鹽耐受性的主要原因,本文利用UAS/arm-Gal4系統(tǒng)通過雜交使果蠅Salt基因遺傳性地全身過表達,發(fā)現(xiàn)耐力運動同樣對遺傳性Salt基因全身過表達果蠅的攀爬能力和壽命有明顯提升效果。與耐力運動對高鹽膳食果蠅的影響不同的是,Salt基因全身過表達果蠅在耐力運動干預后,Salt基因表達并未發(fā)生明顯改變,而抗氧化能力顯著增加。這一結果提示,耐力運動能改善Salt基因全身過表達對果蠅運動能力和壽命造成的不利影響,其機制與果蠅機體抗氧化能力增強有關,與Salt基因及鈉-溶質(zhì)同向轉(zhuǎn)運體活性無關。與果蠅不同的是,人類在運動過程中,通過汗腺的排泄,機體的鈉離子含量將減少,這能否改善高鹽膳食對人類的危害,有待進一步研究證實。
3.3 Foxo過表達對高鹽膳食果蠅運動能力和壽命的影響
為進一步證實機體抗氧化能力是改善高鹽膳食對果蠅運動能力和壽命危害的重要因素,本文同樣利用UAS/arm-Gal4系統(tǒng)通過雜交使目標基因Foxo成功地全身過表達。Foxo是一個重要的轉(zhuǎn)錄調(diào)節(jié)因子,在細胞的凋亡、應激、DNA損傷/修復及糖脂代謝調(diào)節(jié)中起著重要作用。Foxo亞家族具有高度保守的磷酸化位點,這些位點是蛋白激酶B(protein kinase B,Akt/PKB)激酶的磷酸化靶位點,F(xiàn)oxo活性受翻譯后修飾(包括磷酸化和乙酰化)調(diào)節(jié)[26-27]。
研究[28]表明,F(xiàn)oxo對SOD轉(zhuǎn)錄合成有上游調(diào)節(jié)作用,而SOD是清除氧自由基的重要蛋白酶,因此,F(xiàn)oxo與氧化應激密切相關。研究[29-30]證實,果蠅Foxo過表達或激活能使其壽命顯著延長,本文結果與既往研究結果類似。此外,本文還發(fā)現(xiàn),果蠅Foxo過表達能增強果蠅的快速攀爬能力,這可能與Foxo過表達使SOD活力增加,導致果蠅機體抗氧化能力增強、毒性產(chǎn)物MDA減少有關。在運動過程中產(chǎn)生的大量氧自由基是導致運動疲勞的重要原因,而Foxo過表達能提高機體(包括骨骼肌)的抗氧化能力,這能減少氧化應激對骨骼肌的損害,并使其運動能力得以增強[19-20]。
此外,本文結果還顯示,F(xiàn)oxo過表達能顯著減少高鹽膳食對果蠅的損害,如Foxo過表達能顯著延長高鹽膳食果蠅的壽命,增強其運動耐受性和抗氧化能力,減少自由基損傷,并能有效地下調(diào)高鹽膳食誘發(fā)的Salt基因過表達。已有研究[17-18]證實,高鹽膳食能增強機體氧化應激,而遺傳性地增強果蠅抗氧化能力能增強其高鹽耐受性,這提示增強機體的抗氧化能力是抵抗高鹽膳食對健康危害的重要手段之一。本文結果顯示,無論是Foxo過表達還是耐力運動,都無法使高鹽膳食果蠅的壽命、運動能力、抗氧化能力恢復到正常膳食果蠅水平,這可能與高鹽膳食可能還損害果蠅其他重要臟器和組織內(nèi)環(huán)境穩(wěn)態(tài)系統(tǒng)(如滲透壓平衡等)有關,但有待進一步證實。
4 結論
Foxo/SOD通路活性增強和Salt基因表達下調(diào)是耐力運動后高鹽膳食果蠅的運動能力提升和壽命延長的重要分子機制;果蠅Salt基因過表達對Foxo/SOD通路活性有下游調(diào)節(jié)作用,并能降低運動能力和縮短生命周期;耐力運動能通過提高Foxo/SOD通路活性,減緩Salt基因過表達誘發(fā)的果蠅運動能力下降和壽命衰減。
作者貢獻聲明:
文登臺:提出論文主題,設計論文框架,撰寫論文,實驗取材;
后文其:果蠅雜交及收集,核實數(shù)據(jù);
郗增輝:果蠅運動訓練,修改論文;
翟帥帥:審核、統(tǒng)計數(shù)據(jù)。

