一種MOFs材料2,5-吡啶羧酸鋰鹽的電化學性能研究
郝麗敏,甘 露
(重慶航天職業技術學院 重慶 400021)
1 引言
金屬有機骨架化合物MOFs是Metal Organic Frameworks的英文簡稱,它是指由無機金屬中心(金屬離子或金屬簇)與橋連的有機配體通過自組裝作用相互連接,形成的一類具有周期性網絡結構的晶態多孔材料。MOFs材料是一種既不同于無機多孔材料,也不同于一般有機配合物的雜化材料,通常也稱其為有機-無機配位聚合物,兼具無機材料的剛性和有機材料的柔性。MOFs材料由于其獨特的性能特征,在現代材料研究、生物、化學等多個領域方面呈現出巨大的發展潛力,具有重要的研究價值。
吡啶羧酸類配體是一類含有N和羧基配體的多功能典型性配體,能夠充分結合并體現出含N和羧基配體二者的優點,因此,在配位能力和配位形式上具有了豐富且突出的特點。由吡啶羧酸類配體通過與金屬離子組裝配合而成的一類MOFs材料稱為吡啶羧酸鹽類材料[1]。根據羧基在含N吡啶環上所處位置的不同,吡啶二甲羧酸有2,5-吡啶二甲酸、3,5-吡啶二甲酸、2,6-吡啶二甲酸和3,4-吡啶二甲酸等多種異構體。因此,吡啶羧酸類MOFs材料具有了不對稱性,且其能通過配位與N、O形成不同功能的原子,金屬離子在與其發生配位取代時可以具有不同的選擇性,能夠以多種方式與金屬離子結合。此外,吡啶羧酸類MOFs材料還能通過發生一系列自組裝反應,從而形成具有次級單元和多核結構的聚合物。近年來,某課題組成員選用2,5-吡啶二甲酸(C7H5NO4)與氫氧化鈉(NaOH)反應,得到了吡啶羧酸類MOFs材料2,5-吡啶二甲酸鈉,通過電化學性能測試,該含氮環吡啶二甲酸鈉鹽的可逆容量達到了190 mAh/g[2]。
本文通過溶液法制備2,5-吡啶羧酸鋰鹽,對該鄰位取代羧酸鋰鹽的電化學性能進行分析研究,討論探索吡啶羧酸鹽類材料用作鋰離子電池負極材料的可能性。
2 材料制備
采用溶液法制備2,5-吡啶羧酸鋰鹽,首先稱取LiOH·H2O 0.084 g溶于20 mL無水乙醇(EtOH)并充分溶解;另稱取2,5-吡啶二甲酸(C7H5NO4)0.167 g溶于20 mL無水乙醇(EtOH)中,待充分溶解后,將以上兩種溶液混合并充分攪拌2 h,完全混合均勻后過濾,將過濾后的溶液在80 ℃真空環境中干燥直至所用溶劑完全蒸發,得到反應成品白色粉末。
根據基本的化學反應原理:酸堿相遇后會發生中和反應,兩種原料分別屬于酸類和堿類,因此,預測該反應的生成物可能為吡啶羧酸鋰鹽,圖1為該鋰鹽的化學結構制備示意圖。
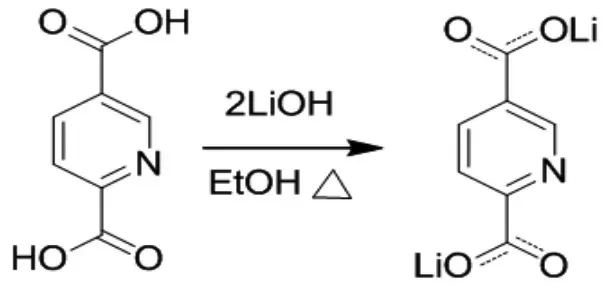
圖1 實驗制備2,5-吡啶羧酸鋰鹽的化學結構示意圖
3 測試結果研究
3.1 XRD (X-射線衍射分析X-ray Diffraction)圖譜分析
圖2為本實驗所制備的2,5-吡啶羧酸鋰鹽的XRD圖譜,以及反應原料2,5-吡啶二甲酸的XRD圖譜對比。由圖可見,兩者的衍射峰出現在不同角度,2,5-吡啶羧酸鋰鹽的物相分析中未出現原料2,5-吡啶二甲酸的晶相圖譜,這說明反應原料2,5-吡啶二甲酸與LiOH·H2O發生化學反應生成了新物相2,5-吡啶羧酸鋰鹽,該鋰鹽與反應所取原料2,5-吡啶二甲酸完全不同[3]。但目前暫時未對反應所生成的2,5-吡啶羧酸鋰鹽進行單晶結構分析,所以無法準確表述2,5-吡啶羧酸鋰鹽的具體物相和結構類型。
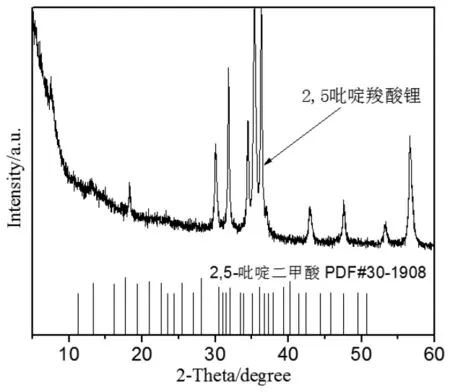
圖2 2,5-吡啶羧酸鋰鹽與2,5-吡啶二甲酸的標準PDF卡對比
3.2 紅外圖譜分析(FTIR)
圖3為本實驗所制備的2,5-吡啶羧酸鋰鹽及其對應的反應原料2,5-吡啶二甲酸配體的紅外圖譜。由圖可見,在1 700 cm-1時,反應原料2,5-吡啶二甲酸會有一個較強的吸收峰,這主要歸結為其所帶羰基的特征峰。當反應原料2,5-吡啶二甲酸與鋰離子發生化學反應后,在1 700 cm-1時,實驗制備的2,5-吡啶羧酸鋰鹽基本沒有出現吸收峰,且在低波數700 cm-1和1 500 cm-1時出現了羧基的對稱反對稱伸縮振動峰,這充分說明了原料2,5-吡啶二甲酸中羰基上的質子已脫掉完全[4],并與鋰離子結合形成了2,5-吡啶羧酸鋰鹽。

圖3 2,5-吡啶二甲酸及其對應產物2,5-吡啶羧酸鋰鹽的紅外圖譜
結合圖2中的XRD圖譜分析結果,可以完全確認,反應物2,5-吡啶二甲酸已經與LiOH·H2O兩種原料已經發生化學反應,生成了新物質2,5-吡啶羧酸鋰鹽。
3.3 SEM掃描電鏡測試(Scanning Electron Microscope)圖譜分析
圖4為本實驗所制備的2,5-吡啶羧酸鋰鹽的SEM圖譜。從該圖譜中可分析反應生成物2,5-吡啶羧酸鋰鹽的形貌。由圖可知,2,5-吡啶羧酸鋰鹽團聚現象較為嚴重,呈現為層狀結構的一次粒子,粒子大小約為4 μm。此外,圖中能觀察到的散落在2,5-吡啶羧酸鋰鹽旁邊的更細小的不明微粒,可能是反應生成的中間產物,這是由于所測樣品本身的導電性能較差,且形成該中間產物與樣品制備時的工藝、溶劑及蒸發溫度等多種因素均有關。

圖4 反應生成物2,5-吡啶羧酸鋰的SEM圖譜
3.4 恒電流充放電(Galvanostatic Charge/Discharge Measurement)測試和循環伏安(Cyclic Voltammetry,CV)性能分析
圖5為本實驗所制備的2,5-吡啶羧酸鋰鹽的充放電曲線及其循環穩定性曲線。將實驗制備的2,5-吡啶羧酸鋰鹽電極活性材料充分研磨后,將質量比為7:2:1的電極材料、super P與PVDF均勻混合,同時加入N-甲基吡咯烷酮少許,充分攪拌,得到黏稠的黑色漿料。該漿料即為待測活動性材料,將其均勻涂抹在銅片(直徑約為16 mm)上,真空條件下,100 ℃干燥,10 h后可得到實驗所需的負極材料電極片。將該電極片與金屬鋰片、隔膜、正極殼、負極殼和適量電解液在充滿高純度Ar氣的手套箱內組裝成2025型扣式電池,用于測試材料的電化學性能。

圖5 實驗制備2,5-吡啶羧酸鋰鹽電化學性能分析圖
實驗所用測試電壓:0.2~3 V,電流密度:50 mA/g,CV曲線的掃描速率:0.3 mV/s。
由圖a可知,2,5-吡啶羧酸鋰首次放電比容量達到380.6 mAh/g,在1.5 V左右時出現了放電平臺,其首次充電比容量約為220.7 mAh/g,由此可得出2,5-吡啶羧酸鋰鹽在首次充放電循環中出現的不可逆容量為159.9 mAh/g,這可能是由于2,5-吡啶羧酸鋰鹽在首次充放電過程中的結構尚不穩定,且在充放電時材料表面形成了鈍化層SEI膜[2],該膜會消耗一定量的鋰離子活性,產生較大的不可逆比容量。由圖b可知,2,5-吡啶羧酸鋰鹽的循環穩定性總體比較穩定,在循環過程中其比容量略有衰減,循環60次后,其充電比容量為195.0 mAh/g,放電比容量為201.2 mAh/g。由此得出,2,5-吡啶羧酸鋰鹽在循環過程中的比容量較高,循環性能也較為穩定。
經實驗測試,反應原料2,5-吡啶二甲酸和LiOH·H2O的充放電比容量極低,而反應產物2,5-吡啶羧酸鋰鹽具有不同于原料的充放電性能,這同時也從另一方面進一步證明了2,5-吡啶二甲酸和LiOH·H2O兩種原料確實已經發生了化學反應,形成了新物質2,5-吡啶羧酸鋰鹽。
4 小結
本文以2,5-吡啶二甲酸和LiOH·H2O為反應原料,用溶液法制備形成了層狀2,5-吡啶羧酸鋰鹽,該材料的具體結構暫時未知,對2,5-吡啶羧酸鋰鹽這種有機羧酸鋰鹽材料進行了充放電性能測試分析,初步分析研究了2,5-吡啶羧酸鋰鹽的電化學性能。結果表明,當電流密度為50 mA/g,電壓范圍為0.2~3 V進行充放電時,2,5-吡啶羧酸鋰鹽的充放電性能較好,循環性能較為穩定。
目前,將吡啶羧酸鋰鹽類MOFs材料用作鋰離子電池電極材料的研究仍處于起步階段,今后的研究方向將繼續鎖定在該吡啶羧酸鋰鹽的單晶結構的確定、多種異構體吡啶羧酸鋰鹽的電化學性能比較、縮小吡啶羧酸鋰鹽的顆粒尺寸所需反應條件以及提高吡啶羧酸鋰鹽材料的電化學性能等方向。

