基于網絡藥理學探究盆炎靈合劑治療盆腔炎性疾病的作用機制
龔琳娜, 鄒 威, 董雅倩, 方超英, 劉孟華*
(1.南方醫科大學藥學院,廣東 廣州 510515;2.湖南省婦幼保健院,長沙市婦產科中藥制劑研發中心,湖南 長沙 410008)
盆腔炎性疾病是一組由病原菌引起的感染性和炎癥性疾病,主要發生在女性生殖道上,病情嚴重時會對患者的健康生活和生命安全造成重大的威脅[1]。西醫主要采用抗生素進行治療,其對控制病原體效果明顯,但對慢性炎癥的作用效果不理想。
盆炎靈合劑是一種中藥制劑,由湖南省婦幼保健院研制,其治療慢性盆腔炎的臨床療效已得到證實。該制劑包括丹酚酸B、芍藥苷、甘草苷、延胡索乙素、綠原酸、紅景天苷、阿魏酸等有效成分[2]。其性狀為黃棕色液體,味苦微甜,具有清熱解毒、活血化瘀、理氣止痛等功效,臨床常用于治療急慢性盆腔炎、附件炎、子宮內膜炎、慢性子宮頸炎、輸卵管不通性不孕癥以及月經不調等。其在臨床上對慢性盆腔炎有良好的治療效果[2],已有實驗證實盆炎靈合劑對盆腔炎大鼠具有抗炎作用,能顯著抑制盆腔炎大鼠子宮炎癥的發生發展[3]。但其治療盆腔炎性疾病的藥理作用機制尚不明確,因此本文采用網絡藥理學技術對盆炎靈合劑的藥效物質基礎及作用機制進行分析,希望為其臨床合理應用提供科學依據。
1 材料與方法
1.1 試劑與藥物 盆炎靈合劑由湖南省婦幼保健院提供(湘藥制字Z20070201,250 mL/瓶,批號20180726)。紅景天苷(批號110818-201206)、去甲異波爾定(批號111825-201402)、綠原酸(批號110753-201314)、芍藥苷(批號110736-201438)、阿魏酸(批號110773-201614)、甘草苷(批號111610-201106)、丹酚酸B(批號111562-201212)、藁本內酯(批號111737-201204)、甘草酸(批號110731-201116)、齊墩果酸(批號110709-201206)對照品均購自中國食品藥品檢定研究院;酪氨酸(批號0215868010)對照品均購自上海寶曼生物科技有限公司;精氨酸(貨號B21920)、奎寧酸(貨號B21879),枸櫞酸(貨號B21313)、馬錢苷酸(貨號B20823)、對羥基苯丙酸(貨號B20325)對照品均購自上海源葉生物科技有限公司。甲醇(批號1727207407)、乙腈(批號JA077330)為色譜純,購自德國Merck公司;甲酸(批號F112034)為分析純,購自上海阿拉丁生化科技股份有限公司。
1.2 動物 10只SPF級9周齡SD雌性大鼠,體質量220~240 g,由湖南斯萊克景達實驗動物有限公司提供,實驗動物生產許可證號SCXK(湘)2011-0003,質量合格證編號43004700011989,隨機分為空白組、給藥組,每組5只,禁食12 h,自由飲水,稱定體質量,按每天10 mL/kg劑量分別灌胃給予純化水、盆炎靈合劑,連續5 d,末次給藥45 min后,腹腔注射10%水合氯醛(3.5 mL/kg)麻醉,15 min后心臟取血,迅速對含EDTA抗凝劑的血液離心(3 000 r/min)5 min,取血漿,置于-80 ℃冰箱中冷凍備用。
1.3 對照品溶液制備 精密稱取各對照品適量,甲醇制成一定質量濃度的溶液,0.22 μm微孔濾膜過濾,取續濾液,即得。
1.4 血漿樣品處理 將血漿置于4 ℃冰箱中解凍,取給藥組5只大鼠血漿各100 μL,混勻,加入3倍體積的甲醇-乙腈(1∶1)混合溶液,加入內標渦旋3 min后置于4 ℃冰箱中過夜,進行蛋白沉淀,13 000 r/min離心10 min,取上清液,過0.22 μm微孔濾膜,濾液即為含藥血漿供試品溶液。同法制備空白血漿供試品溶液。
1.5 血中移行成分分析 采用由Agilent 1290 LC系統和Agilent 6540 Q-TOF-MS系統組成的LC-Q-TOF-MS系統(美國安捷倫公司),對含藥血漿供試品、空白血漿供試品、對照品溶液進行分析。色譜條件為Agilent ZORBAX Eclipse XDB-C18色譜柱(3.0 mm×150 mm,3.5 μm),流動相水(含0.1%甲酸)(A)-乙腈(B),梯度洗脫,程序見表1;體積流量0.5 mL/min;柱溫25 ℃;進樣量5 μL。質譜條件為毛細管電壓3 500 V;噴嘴電壓(Expt)500 V;碎裂能量120 V;氣體溫度250 ℃;鞘氣溫度350 ℃;正負離子掃描,m/z50~1 250;干燥氣、碰撞氣氮氣;碰撞能量20 V。

表1 梯度洗脫程序
1.6 蛋白靶點篩選 將盆炎靈合劑入血化合物的三維立體結構導入PharmMapper服務器,采用默認參數對上述藥物分子的體內靶點進行預測,將反向分子對接獲得的蛋白信息與DrugBank、TTD、HIT數據庫中盆腔炎性疾病相關靶點進行對比和篩選,并利用UniProt數據庫將最終得到的靶點名轉換為其編碼的基因名。
1.7 入血平移成分數據庫構建 將盆炎靈合劑的入血成分和相關蛋白通過SYBYL-X7.3軟件進行分子對接,以對接分值≥6.0作為活性化合物的篩選條件,篩選出具有較高活性的化合物。
1.8 化合物-靶點網絡構建 將活性化合物及相關靶點導入Cytoscape3.7.1軟件,構建化合物-靶點網絡。
1.9 蛋白互作(PPI)網絡構建 將相關靶基因上傳至STRING11.0在線軟件,獲取蛋白相互作用信息,并將打分值>0.7的蛋白相互作用值視為高置信度數據,將蛋白相互作用數據導入Cytoscape3.7.1軟件,構建PPI網絡,并在Excel中對PPI網絡中的蛋白繪制條形圖。
1.10 基因本體(GO)功能富集分析 采用David v6.8數據庫,對PPI網絡中的蛋白進行GO生物學過程富集分析。
1.11 京都基因與基因組百科全書(KEGG)通路富集分析 采用David v6.8數據庫,對PPI網絡中的蛋白進行KEGG通路富集分析。采用Cytoscape3.7.1軟件,對KEGG通路富集分析中的信號通路構建靶點-通路網絡。
2 結果
2.1 活性化合物篩選 通過SYBYL-X7.3軟件將29種入血成分分別與121個蛋白進行分子對接,共篩選出分子對接分值≥6.0的27個化合物及110個相關蛋白,活性化合物提取離子流圖見圖1,基本信息見表2。
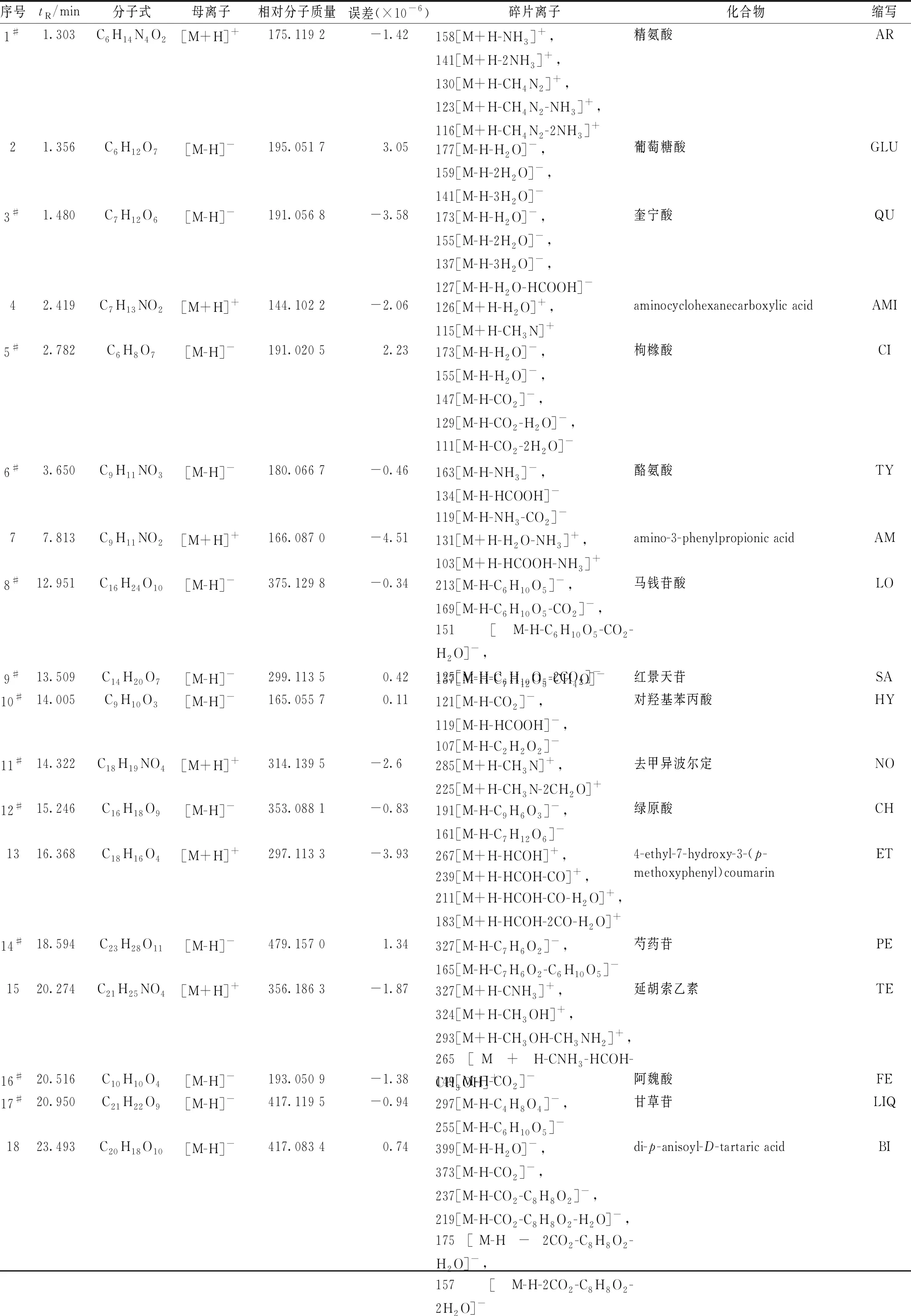
表2 活性化合物基本信息
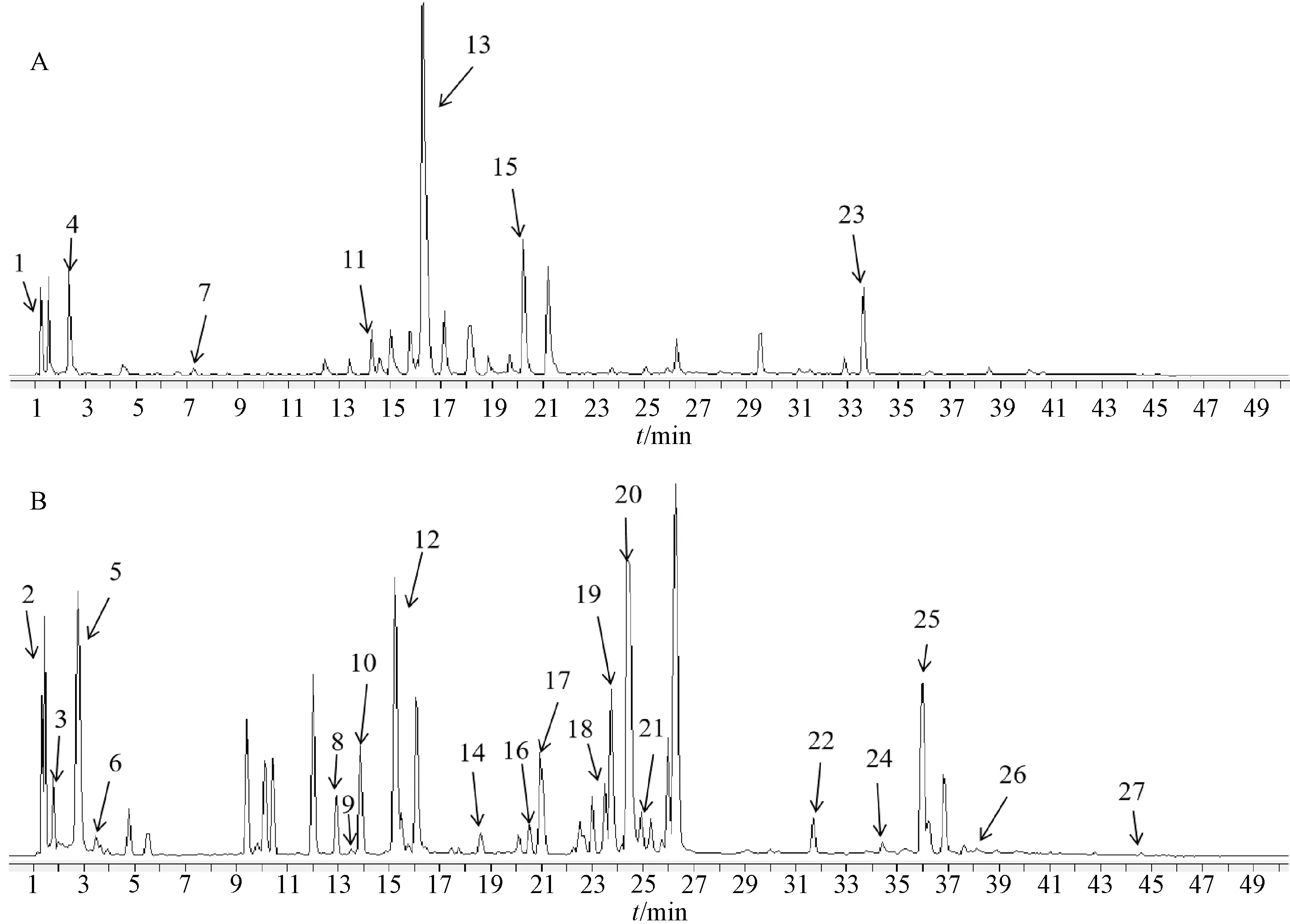
圖1 活性化合物在正離子(A)、負離子(B)模式下的提取離子流圖
2.2 盆炎靈合劑化合物-靶點相互作用網絡 化合物-靶點網絡包含137個節點(27個化合物節點、110個靶點節點)和812條相互作用連線,見圖2。由此可知,有66.67%的化合物作用靶點≥10個,≥50個的有7個,從化合物角度來看,Degree排名前5位的是SAB、SAA、GI、AR、RH;從靶點角度來看,Degree排名前4位的是白細胞介素-1受體相關激酶(IRAK1)、Toll樣受體8(TLR-8)、Tristetraprolin(TTP)、Rho激酶2(ROCK2);化合物平均靶點數目為30.22個,每個靶點平均與7.33個化合物發生作用。
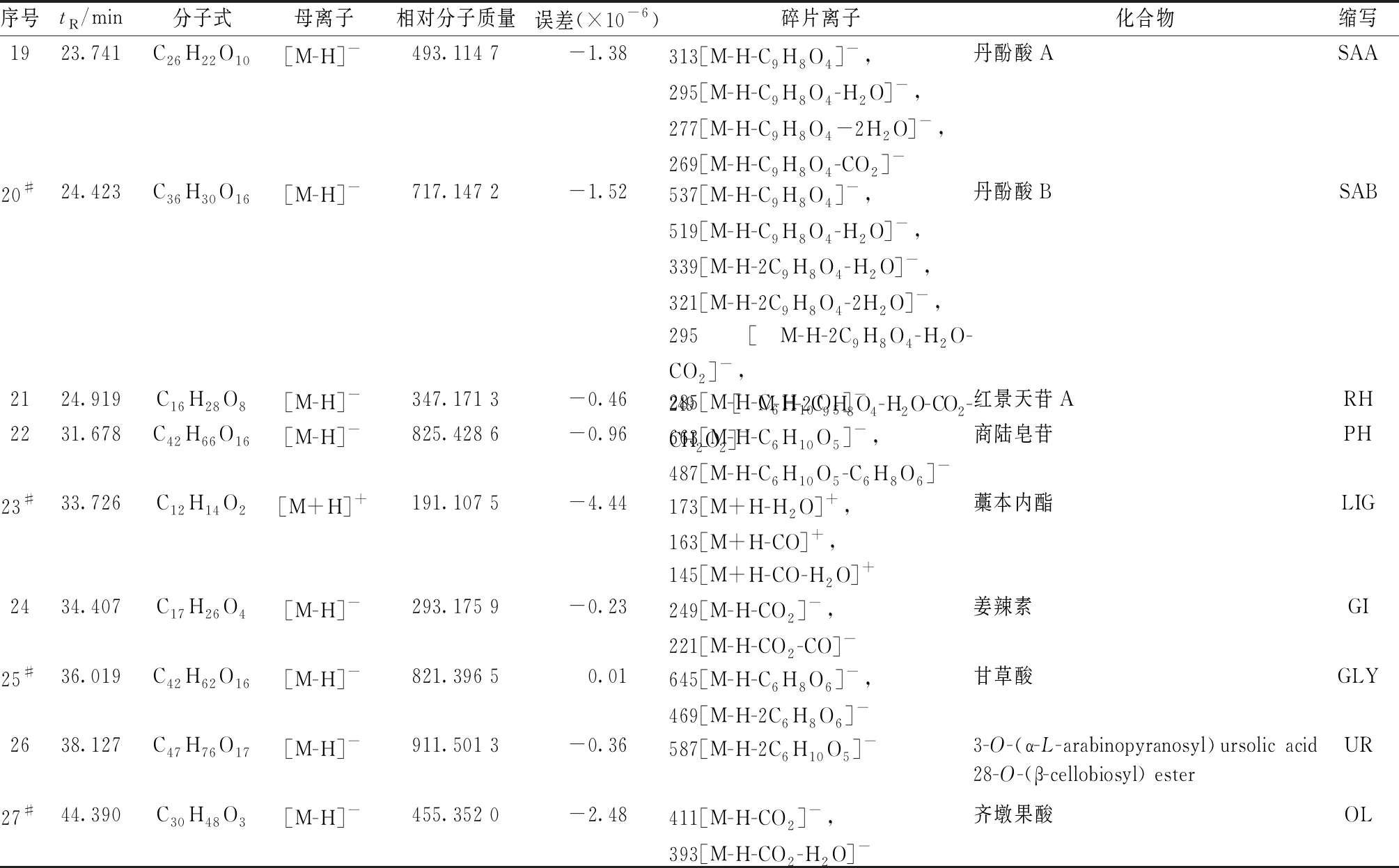
續表2

注:藍色表示化合物,紅色表示靶點。
2.3 盆炎靈合劑靶點PPI網絡的構建與分析 PPI網絡(圖3)包含75個節點,411條邊,其中節點表示蛋白,每條邊則表示蛋白與蛋白之間的相互作用關系;Degree≥20的節點包括Toll樣受體4(TLR4)、信號傳導及轉錄激活因子3(STAT3)、白細胞介素-6(IL-6)、絲裂原活化蛋白激酶1(MAPK1)、絲裂原活化蛋白激酶8(MAPK8)、AKT絲氨酸/蘇氨酸激酶(AKT1)、趨化因子CXCL8(CXCL8)、信號傳導及轉錄激活因子1(STAT1)、白細胞介素-4(IL4)、核轉錄因子-κB 1(NFκB1)、前列腺素內過氧化物合酶2(PTGS2)、髓樣分化因子88(MYD88),其中TLR4、STAT3和IL-6度值最大,分別能與34、33、30個蛋白發生相互作用。前30個關鍵蛋白質節點的Degree所繪制出的條形圖見圖4。
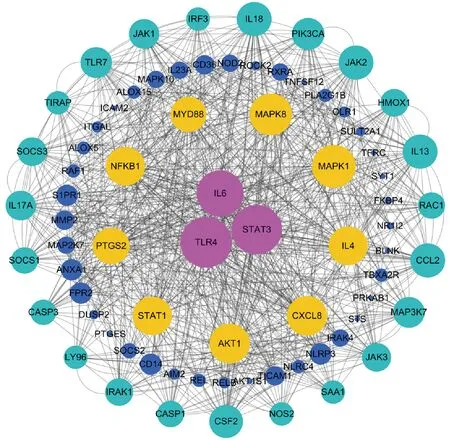
注:洋紅色表示Degree≥30的蛋白,黃色表示20≤Degree<30的蛋白,綠寶石色表示10≤Degree<20的蛋白,深藍色表示Degree<10的蛋白。
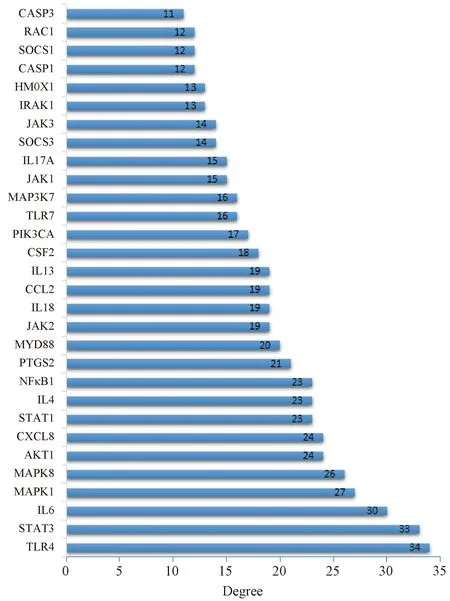
注:數字表示節點的Degree。
2.4 GO功能富集分析 根據錯誤發現率(FDR)<0.05,確定了123個GO條目(表3根據FDR列出前20個),主要涉及對細胞壞死以及凋亡的調控、多細胞生物過程的調控、級聯反應、有機物質的反應、分子功能的調控、系統過程的調控等方面,見表3。
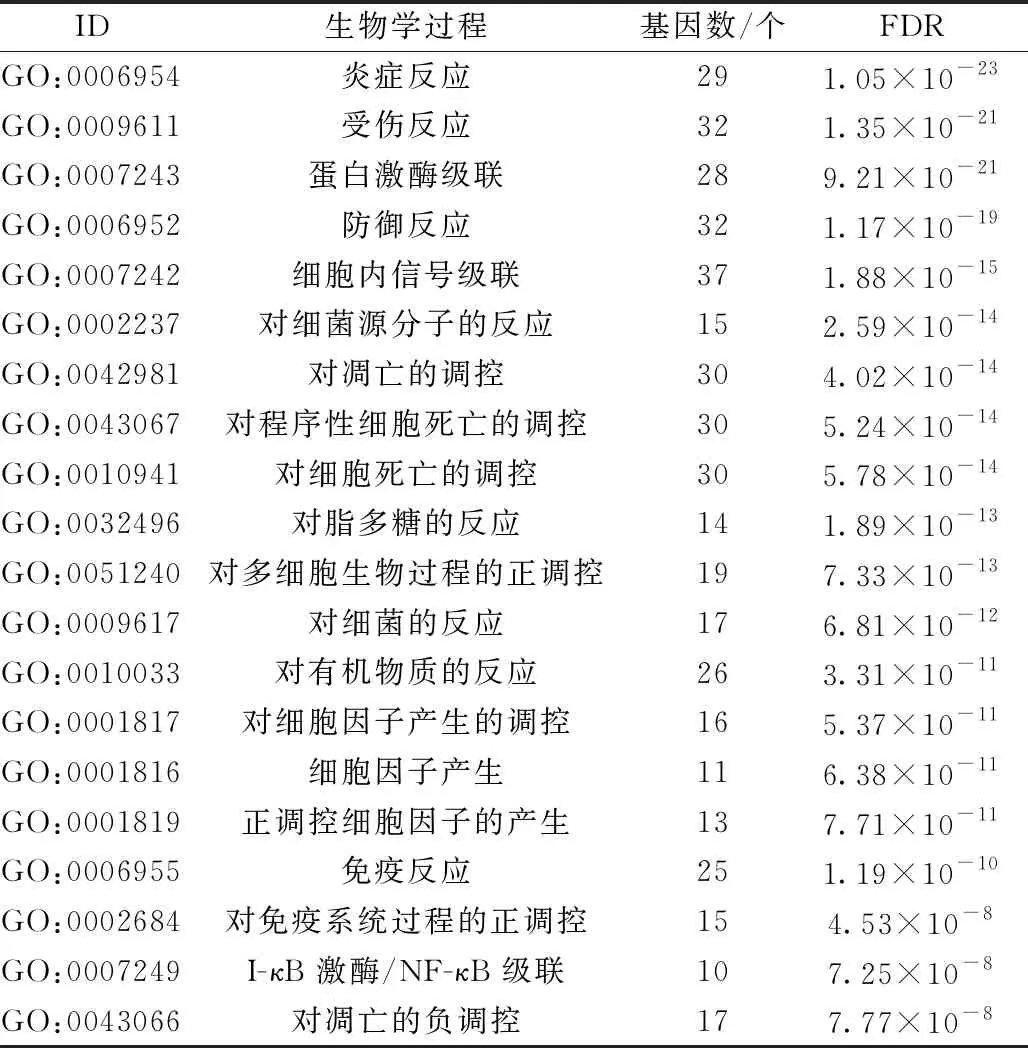
表3 盆炎靈合劑PPI網絡中的GO條目(FDR<0.05)
2.5 KEGG通路富集分析 共得到41條信號通路,以FDR<0.05為標準篩選出12條,包括Toll樣受體信號通路(Toll-like receptor signaling pathway)、NOD樣受體信號通路(NOD-like receptor signaling pathway)、Fc epsilon RI信號通路和JAK-STAT信號通路(JAK-STAT signaling pathway)等,見表4、圖5。

注:深青色表示蛋白靶點,紅色表示信號通路ID。
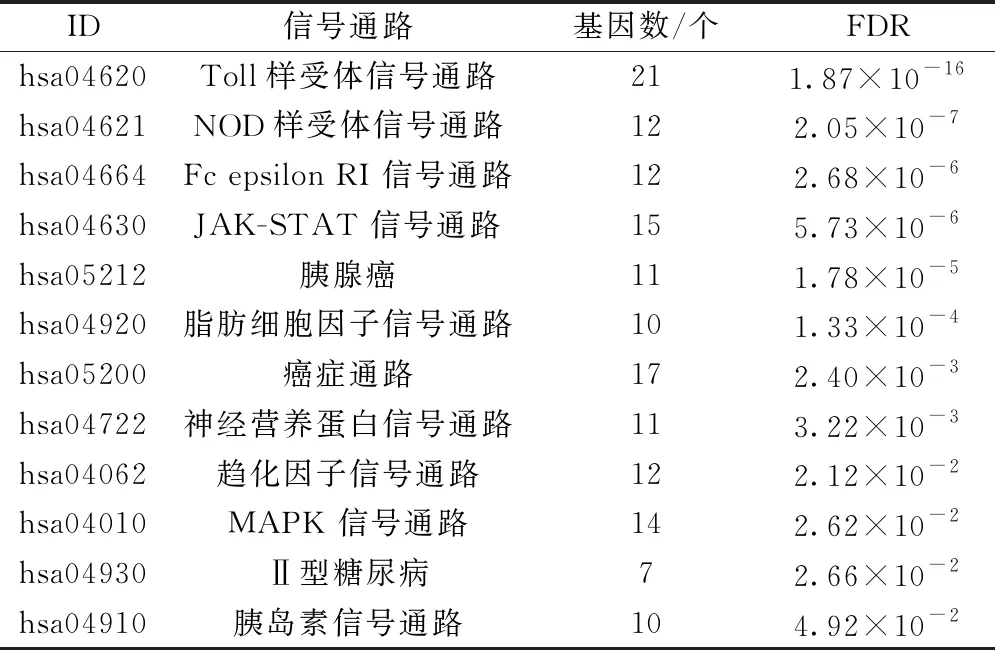
表4 盆炎靈合劑PPI網絡中的通路(FDR<0.05)
3 討論
盆炎靈合劑作為治療婦科炎癥的中藥制劑,在治療濕熱蘊結、濕熱下注型盆腔炎性疾病方面具有顯著療效[3]。本研究以盆炎靈合劑的27個活性化合物為基礎,構建了化合物-靶點網絡,其中關鍵靶點包括IRAK1、TLR-8、TTP等。IRAK1通過參與Toll樣受體和白細胞介素-1信號通路,調節先天免疫和炎癥[4]。有研究表明,靶向IRAK1可抑制NF-κB通路[5],而盆炎靈合劑中的成分PE對IRAK1-NF-κB通路具有抑制作用[6],可見調控IRAK1的表達可以抑制炎癥損傷[7]。TLR8主要對細胞的增殖、分化、轉化和凋亡進行調節,同時還與炎癥和腫瘤等疾病存在緊密聯系[8-9]。激活TLR8后可介導炎癥免疫,進而清除體內腫瘤細胞和受病毒感染的細胞[10]。TTP在分化、代謝、增殖、炎癥、腫瘤發生和免疫等多種生理病理過程中發揮著重要作用[11-14]。TTP介導的NLRP3炎性激活的減少還可以減少慢性炎癥疾病的發展,例如動脈粥樣硬化、結腸炎和關節炎[15]。在PPI網絡中,TLR4、STAT3和IL-6的Degree遠高于其它蛋白,其中TLR4在炎癥反應及癌癥發展中扮演著重要的角色[16-19],被認為是連接炎癥與腫瘤微環境的重要樞紐[20]。通過抑制TLR4/NF-κB和TLR4/MAPK信號通路可以抑制炎癥反應[21]。STAT3在細胞生長、分化、免疫功能、造血功能和腫瘤相關炎癥中發揮重要作用[22-23]。STAT3的持續激活可促進腫瘤細胞增殖侵襲、血管增生、免疫抑制、誘導和維持癌前炎性微環境等病理過程的發生發展[24]。因此推測,盆炎靈合劑可能是通過對這些關鍵靶點進行調控,從而達到治療目的。
GO功能富集分析發現,盆炎靈合劑在治療疾病時主要涉及有機物質的反應、受體活性、細胞組分等方面,而在KEGG通路富集分析中,基因主要富集到了Toll-like receptor signaling pathway、NOD-like receptor signaling pathway、Fc epsilon RI signaling pathway和Chemokine signaling pathway上。有研究發現SAB具有良好的抗炎活性,其免疫調節作用與抑制TLR4信號通路有關[25]。SA能夠顯著地抑制TXNIP的表達,進而降低NLRP3炎癥小體的表達水平,從而通過NOD樣受體信號通路中的TXNIP-NLRP3炎癥小體途徑減輕細胞氧化應激和細胞外基質的積累[26]。AR的抗炎作用與參與肥大細胞細胞因子表達的信號分子的活化水平降低有關,例如趨化因子信號通路中的Akt等[27]。由此推測,盆炎靈合劑可能通過作用于與炎癥反應和免疫反應直接相關的通路,從而對炎癥起到治療作用。此外,在與細胞生長及內分泌系統相關的通路上也富集到了大量基因,說明盆炎靈合劑的治療作用也與這些通路密切相關。
綜上所述,本研究對盆炎靈合劑中入血成分與網絡數據庫中篩選出的疾病靶點進行分子對接分析及網絡分析,為盆炎靈合劑治療盆腔炎性疾病的作用機制提供了科學依據,下一步將開展細胞、動物實驗,對上述結果進行驗證。

