槲皮素對牙髓間充質(zhì)細胞成骨能力及兔顱骨缺損修復的影響
胡韶光,劉珂珂,汪芹芹,韓 旭,桂雙英,徐 燕
(1.安徽醫(yī)科大學口腔醫(yī)學院,安徽醫(yī)科大學附屬口腔醫(yī)院,安徽省口腔疾病研究中心實驗室, 安徽 合肥 230032;2.安徽中醫(yī)藥大學藥學院, 安徽 合肥 230012)
牙周病作為一種常見的口腔疾病,是導致牙齒脫落的主要原因,同時也會造成全身性影響[1]。牙周治療的主要目標是阻止慢性炎癥過程,恢復牙周附著和喪失的牙槽骨以及防止牙周袋的形成,從而保護天然牙列[2]。牙周炎造成的骨缺損往往難以恢復,近年來通過組織工程的方法,利用種子細胞,細胞外基質(zhì)/支架材料,信號/生長因子可以促進軟硬組織再生[3]。牙髓間充質(zhì)細胞(human dental pulp mesenchymal stromal cells,hDPSCs)具有較好的增殖潛力,又能多系分化,非常適合作為種子細胞[4]。槲皮素(quercetin)是一種常見的黃酮類化合物,可以從蜂膠中大量獲得,它具有多種生物學活性,包括抗炎、抗氧化和抗凋亡等[5]。此外槲皮素具有保護作用,能夠防止骨質(zhì)流失,同時促進成骨細胞形成[6]。為了探索槲皮素是否能夠加強牙周組織工程的成骨效果,本文重點研究槲皮素對體外培養(yǎng)的hDPSCs成骨能力的影響,并致力探究將其用于組織工程,在體內(nèi)促進成骨的作用。
1 材料與方法
1.1 材料
1.1.1主要試劑與儀器 槲皮素(MCE,美國,25265);Bio-Oss?(Geistlich,瑞士,81900483);胎牛血清(BI,以色列,2030101);DMEM 培養(yǎng)基(HyClone,美國,AF29498406); 0.25%胰蛋白酶(碧云天,中國,200601091);青鏈霉素(碧云天,中國,190901084);CCK-8試劑盒(Dojindo,日本,PG657);地塞米松(索萊寶,中國,20190424);維生素C(索萊寶,中國,20200615);β-甘油磷酸鈉(Sigma,美國,MKDL3872);茜素紅S(Sigma,美國,MKCF4917);堿性磷酸酶檢測試劑盒(碧云天,中國,061820200929),BCIP/NBT堿性磷酸酯酶顯色試劑盒(碧云天,中國,031820200525);人間充質(zhì)干細胞流式抗體(CD73、CD44、CD34、CD45)(BD,美國,8341000、9099646、9212666、8533548);PrimeScriptTMRT Master Mix 逆轉(zhuǎn)錄試劑盒,TB Green?Premix Ex TaqTMqPCR試劑盒(TaKaRa,日本,AK51810A);引物(β-actin,BMP2,Runx2,OPN,OCN)(上海生工,中國,1923361079-88);戊巴比妥(Sigma,美國,MKAF3846)。
1.1.2實驗動物 ♂新西蘭兔10只,2.5-3.0 kg,購自安徽醫(yī)科大學實驗動物中心并提供飼養(yǎng)。經(jīng)由安徽醫(yī)科大學實驗動物倫理委員會批準(LLSC20190122)。
1.2 方法
1.2.1hDPSCs分離培養(yǎng)與傳代 實驗所需牙髓組織來源于安徽醫(yī)科大學附屬口腔醫(yī)院口腔頜面外科,年齡為18-30周歲患者的完整無齲正畸減數(shù)拔除的前磨牙,拔除后置于含5%雙抗的DMEM取材液中。在超凈工作臺中用含有2%雙抗的PBS反復沖洗牙齒表面。將牙髓組織取出后剪碎放入含有1 ∶1混合的I型膠原酶和中性蛋白酶的EP管中,37 ℃培養(yǎng)箱中消化15 min后加入等體積完全培養(yǎng)液終止消化。10 000 r·min-1離心5 min,棄上清。將消化好的組織塊移入6孔板中,上方覆蓋一枚蓋玻片,加入含1%雙抗20%胎牛血清(FBS)的完全培養(yǎng)液,放入37 ℃、5% CO2培養(yǎng)箱中培養(yǎng)。待組織塊周圍有細胞爬出并達蓋玻片的80%左右時,使用含0.25% EDTA的胰蛋白酶消化細胞,并按1 ∶3比例傳代,10% FBS完全培養(yǎng)液培養(yǎng)。
1.2.2流式細胞術(shù)鑒定hDPSCs表面標志物 取生長狀況良好的第3代細胞(P3)用PBS清洗2遍,胰酶消化離心,PBS重懸,清洗過篩。使用CountStar細胞計數(shù)板計數(shù),以1×106個細胞分裝至5個流式管后,分別加入表面抗體CD73、CD44、CD34、CD45和陰性對照,37 ℃避光孵育30 min,PBS清洗后上CytoFLEX分析流式細胞儀鑒定。
1.2.3細胞增殖檢測 將P3代細胞,加入胰酶消化,離心,用培養(yǎng)基重懸細胞。將各組細胞按密度5×103個/孔,接種到96孔板中。置于37 ℃,5% CO2培養(yǎng)箱中培養(yǎng)24 h,棄去培養(yǎng)基,用PBS清洗,分組加入培養(yǎng)液,每組設(shè)5個復孔,置于培養(yǎng)箱中繼續(xù)培養(yǎng)。其中對照組(Control組):加入等量DMSO的完全培養(yǎng)基;實驗組:含有不同濃度槲皮素的完全培養(yǎng)基。槲皮素濃度分別為0.01、0.1、1、10、100 μmol·L-1,連續(xù)培養(yǎng)3 d,分別在24、48、72 h時加入CCK-8孵育2 h后,酶標儀測量450nm處吸光度值(A值)。
1.2.4堿性磷酸酶(ALP)定量檢測 將狀態(tài)良好的P3代細胞以1×104個/孔接種到96孔板中,待細胞融合至70%-80%時,加入含不同濃度槲皮素的成骨誘導培養(yǎng)基(含50 μmol·L-1抗壞血酸,10 mmol·L-1β-甘油磷酸鈉,100 nmol·L-1地塞米松),設(shè)常規(guī)完全培養(yǎng)基為陰性對照組(negative),每隔2 d更換一次培養(yǎng)液。分別在d 7、10時棄去培養(yǎng)液,PBS清洗2遍,冰上加入Western/IP裂解液,槍頭吹打裂解細胞,加入配制好的顯示底物。同時根據(jù)試劑盒說明書配制標準品孔,標準品的用量分別為0、4、8、16、24、32和40 μL。混勻后37 ℃搖床孵育30 min后加入反應(yīng)終止液,測量405 nm處吸光度值,使用610 nm為校正波長。根據(jù)標準品孔繪制標準曲線,將OD值換算成DEA酶活力單位。
1.2.5堿性磷酸酶及茜素紅S染色 將狀態(tài)良好的P3代細胞以1×105個/孔接種到6孔板中,待細胞融合至70%-80%時,加入0和1 μmol·L-1槲皮素的成骨誘導培養(yǎng)基2 mL,設(shè)常規(guī)培養(yǎng)基為對照組,每3 d更換一次培養(yǎng)液。在d 14時棄去培養(yǎng)液,PBS清洗2遍,加入4%多聚甲醛固定30 min。PBS清洗2遍后按照BCIP/NBT堿性磷酸酯酶顯色試劑盒配置顯色液,每孔加入500 μL,避光孵育2 h后用去離子水清洗2遍后觀察。配制茜素紅S染色液:在0.2%的茜素紅S溶液中加入1% Tris,調(diào)節(jié)pH值至8.3。在d 21時按上述方法固定細胞后,加入配制好的茜素紅S染色液后室溫下孵育30 min后觀察。
1.2.6實時熒光定量PCR(qPCR) 按照上述同樣的方法分組在6孔板內(nèi)接種細胞,在d 14的時候用TRIzol試劑提取細胞中的總RNA,使用PrimeScriptTMRT Master Mix逆轉(zhuǎn)錄試劑盒從400 ng總RNA中制備cDNA。然后用TB Green?試劑盒配制成20 μL PCR反應(yīng)體系上機檢測。相對mRNA水平通過2-ΔΔCt方法定量計算,β-actin作為標準化基因。引物序列見Tab 1。

Tab 1 Primer sequence of qPCR
1.2.7hDPSCs在支架材料上的接種與檢測 將P3代細胞以1×106個接種到Bio-Oss?骨粉上,2 h后更換培養(yǎng)液,分別加入0和1 μmol·L-1槲皮素的培養(yǎng)液。培養(yǎng)3 d后,取少量支架復合物,用PBS清洗2次,4%多聚甲醛固定2 h,60%-100%乙醇梯度脫水,臨界點干燥,樣品表面噴金后掃描電鏡觀察。
1.2.8動物模型制備與檢測 10只新西蘭兔術(shù)前30 min肌肉注射青霉素,術(shù)中使用3%戊巴比妥,以1 mL·kg-1耳緣靜脈全麻,備皮鋪巾消毒,沿顱骨中線切開,鈍性分離骨膜,暴露骨面。以矢狀縫、冠狀縫將顱骨分為4個區(qū)域,分別用8 mm環(huán)鉆制作圓形全層骨缺損,超聲骨刀修整邊緣。造模完成后將4個缺損分為4組:A組為含1 μmol·L-1槲皮素的支架復合物,B組為不含槲皮素的支架復合物,C組為普通完全培養(yǎng)液潤濕的Bio-Oss?骨粉,D組為空白組。將復合物隨機放入缺損中,術(shù)者對復合物內(nèi)容單盲,另一人記錄。分層縫合切口,局部涂抹紅霉素軟膏預(yù)防感染。術(shù)后3 d每天對創(chuàng)口碘伏消毒并肌注青霉素。術(shù)后4、8周處死,在顱骨缺損造模的位置外2 mm處截取,4%多聚甲醛固定,進行Micro-CT檢測。
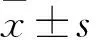
2 結(jié)果
2.1 hDPSCs的流式鑒定通過流式細胞儀對hDPSCs進行表面抗原的檢測,可見CD44(99.20%)、CD73(99.56%)陽性高表達,CD34(0.12%)、CD45(0.11%)陰性表達,符合人間充質(zhì)細胞特征,見Fig 1。

Fig 1 Cell surface markers of hDPSCs by flow cytometry
2.2 槲皮素對細胞增殖的影響在CCK-8檢測中,通過酶標儀測得450 nm處的OD值。進行換算后如Fig 2所示,與對照組相比1 μmol·L-1的槲皮素在d 3可引起hDPSCs明顯增殖,差異有統(tǒng)計學意義(P<0.05)。然而更高濃度100 μmol·L-1的槲皮素相比于對照組則出現(xiàn)了抑制作用(P<0.05)。

Fig 2 CCK-8 cell proliferation n=5)*P<0.05 vs control
2.3 成骨誘導后ALP定量檢測如Fig 3所示,通過在d 7和d 10時的ALP定量檢測可以發(fā)現(xiàn),在這兩個時間點加入成骨誘導液的各組較常規(guī)完全培養(yǎng)基(陰性對照組)有明顯升高(P<0.05),說明成骨誘導是有效的。在d 10時,0.1和1 μmol·L-1槲皮素組與成骨誘導對照組和其他濃度組相比,堿性磷酸酶活性有了明顯提升,差異有統(tǒng)計學意義(P<0.05),而這兩個濃度沒有差別(P>0.05)。

Fig 3 ALP quantitative analysis n=5) *P<0.05 vs control
2.4 堿性磷酸酶及茜素紅S染色經(jīng)過14 d成骨誘導, BCIP/NBT堿性磷酸酶試劑盒染色后,如Fig 4所示加和不加槲皮素成骨誘導組相比于普通培養(yǎng)液組顏色均有明顯加深,同時槲皮素組的顏色較成骨誘導組略深。在d 21的時候進行了茜素紅染色。由Fig 5可見經(jīng)過成骨誘導之后,茜素紅染色呈現(xiàn)紅色,加入槲皮素組顏色較深。同時,通過顯微鏡可觀察到堿性磷酸酶水解BCIP形成的藍紫色的產(chǎn)物和鈣結(jié)節(jié)。見Fig 6。

Fig 4 ALP staining A:control; B:Ost; 4c:1 μmol·L-1 quercetin+Ost

Fig 5 Alizarin Red staining A:control; B:Ost; 5c:1 μmol·L-1 quercetin+Ost

Fig 6 Alkaline phosphatase staining and calcium nodulesA:ALP stain staining; B: Alizarin red staining
2.5 成骨基因的表達通過對14 d樣本的實時熒光定量PCR的檢測可以發(fā)現(xiàn)成骨誘導液組(Ost)組BMP2、Runx2、OPN和OCN等成骨相關(guān)基因的表達量高于對照組(P<0.05),說明成骨誘導有效。加入1 μmol·L-1槲皮素后相較于Ost組,表達顯著提高 (P<0.05)。由此可以看出槲皮素在體外能夠有效的促進成骨基因的表達,見Fig 7。

Fig 7 Relative expression of osteogenic related genes n=3)
2.6 支架材料復合物的檢測通過掃描電鏡,可以觀察到細胞在常規(guī)完全培養(yǎng)基(對照組)和含有槲皮素的培養(yǎng)基環(huán)境下,均能在骨粉上大量附著生長。見Fig 8。

Fig 8 The scaffold composites observed by SEM B:Bio-Oss?; C:cells
2.7 Micro-CT結(jié)果將得到的Micro-CT數(shù)據(jù)是由dataviewer校正方向后,用CTan打開圖像,選取圓形缺損區(qū)域為感興趣的區(qū)域(Region of interest, ROI),計算區(qū)域的骨體積分數(shù)(BV/TV)。通過圖像分析,可以看到4周時空白組(D組)如Fig 9A所示骨缺損區(qū)幾乎沒有明顯的新骨生成,F(xiàn)ig 9B顯示8周時在缺損的邊緣有少量新骨的形成;而加入了骨粉的A、B、C組如Fig 9C所示在4周時均可見新骨形成,8周時如Fig 9D所示可見大量的新生的骨組織。通過進一步骨體積分數(shù)的計算,可以發(fā)現(xiàn)本次實驗中4周時含細胞的支架復合物組(AB組)相比純骨粉組(C組)BV/TV較高(P<0.05), 8周時BC兩組沒有明顯差別(P>0.05)。加入了1 μmol·L-1槲皮素培養(yǎng)的復合物組在4周和8周時對其他各組BV/TV均明顯升高(P<0.05),表現(xiàn)出良好的促進成骨的能力,見Tab 2。

Fig 9 Micro CT image reconstruction of rabbit calvarial defects

Tab 2 Bone volume fraction in calvarial defect area of rabbits n=5)
3 討論
在牙周治療的各種方法中,傳統(tǒng)的潔治、刮治及牙周手術(shù)等手段可以有效地消除病因,但如何重建已被破壞的牙周骨組織仍是難點[7]。Iwata等[8]學者指出目前治療手段牙周組織的再生量遠不能滿足重度牙周炎患者牙周再生的需要。近年來再生醫(yī)學不斷發(fā)展,為牙周組織修復提供了一種創(chuàng)新的替代方法,通過組織工程與人類的自我修復能力相結(jié)合,修復組織缺損,并恢復其功能[9]。采用患者自身來源的干細胞作為種子細胞在體外進行擴增,然后與支架材料結(jié)合,同時加入一些生長因子或是信號分子,回植到患者缺損部位這一模式,成為解決牙周組織重建這一難題的一個發(fā)展方向[10]。牙髓間充質(zhì)細胞因其良好的增殖和分化的潛力,常常是口腔組織再生中首選的種子細胞。由于本研究牙髓來源為正畸拔牙,患者大多為年輕人,因此可以獲得大量年輕的hDPSCs,這樣可以克服由于細胞老化或系統(tǒng)性疾病引起的干細胞功能障礙[11]。槲皮素是一種常見的天然小分子活性物質(zhì),主要來源于蜂膠中的黃酮類,具有多種生物學效應(yīng),有較強的抗炎、抗氧化、清除氧自由基、抗菌、抗血栓、抗病毒、調(diào)節(jié)免疫的作用[12]。還有研究表明,槲皮素不僅能夠誘導破骨細胞的凋亡、抑制破骨細胞對骨質(zhì)的吸收[13],還能夠增強成骨細胞分化活性[14]。
本實驗研究表明,較低濃度的槲皮素可以促進牙髓間充質(zhì)細胞的增殖,較高濃度出現(xiàn)了抑制作用。綜合考慮槲皮素促進hDPSCs增殖的最優(yōu)濃度1 μmol·L-1和堿性磷酸酶的活性定量檢測中的最優(yōu)濃度0.1和1 μmol·L-1,最終選擇加入1 μmol·L-1藥物再次進行了體外培養(yǎng)。通過相關(guān)體外成骨檢測,包括堿性磷酸酶定性染色,茜素紅對鈣結(jié)節(jié)的染色,部分成骨相關(guān)的mRNA的表達(BMP2,Runx2,OPN,OCN),發(fā)現(xiàn)槲皮素在體外成骨方面有著明顯的促進作用。為了進一步驗證其在體內(nèi)的作用,將hDPSCs接種于Bio-Oss?骨粉支架上,通過掃描電鏡的觀察確認支架材料上確實存在大量牙髓細胞,進而使用該復合體修復兔顱骨臨界骨缺損。為了減少實驗中因為槲皮素細胞復合物放入量的差異而產(chǎn)生的誤差,本研究選擇了術(shù)者對復合物的成分單盲的方法,以期達到更加準確的結(jié)果。根據(jù) Micro-CT結(jié)果表明,加入和不加槲皮素的兩組細胞復合物和單純骨粉組均有新骨形成,且加入槲皮素組形成的新骨更多;空白組新骨形成較少。因此可以認為槲皮素也可以有效促進牙髓間充質(zhì)細胞的體外成骨能力。有研究表明,雖然異種來源的細胞在移植后很可能會被宿主所排斥,但異種牙髓間充質(zhì)干細胞在一定程度上能夠抑制受體宿主的免疫反應(yīng)[15]。本研究中人類來源的間充質(zhì)細胞作為異種細胞被用于移植到免疫功能正常的動物身上,通過對比加入細胞的復合物組和單純骨粉組結(jié)果,顯示良好的成骨效果,沒有出現(xiàn)因明顯的免疫排斥反應(yīng)而導致的炎癥反應(yīng)、組織壞死和實驗動物死亡等嚴重后果。這和本課題組前期研究的結(jié)果也是一致的[16]。
本研究旨在探討槲皮素對體外培養(yǎng)的人牙髓間充質(zhì)細胞的增殖和成骨分化的影響,及使用組織工程的方法,在動物體內(nèi)將槲皮素作為藥物刺激種子細胞增殖與分化,研究促進成骨的可能性。在此研究基礎(chǔ)上,后期還會進一步研究,構(gòu)建槲皮素的原位液晶緩釋遞藥系統(tǒng)[17],實現(xiàn)對牙周局部用藥,控制牙周炎癥與促進牙槽骨的再生,為臨床牙周炎治療提供新思路。