2021年部分卷區高考試題道題深度分析展示
山東省2021年普通高中學業水平等級考試第20題分析
[原題略]
一、解題思路
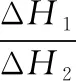

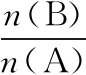
二、試題評價
1.試題情境
本題為學術探索情境,采用甲醇與異戊烯為原料高選擇性合成TAME工藝為載體,在復雜陌生研究對象及問題情境下,對化學反應中的能量變化、化學反應速率、化學平衡等重點知識進行了綜合性、創新性考查。
甲氧基-2-甲基丁烷(TAME)是隨著汽油調和技術發展而出現的油品添加劑,可以達到降低成本、節約石油資源的目的。TAME因其以甲醇與異戊烯合成價格較低,且抗暴效果、環保和安全性能均優于其他同類產品,成為市場應用潛力巨大的汽柴油添加劑,齊魯石化公司開發的相關聯產工藝和產量在國內均處于領先。本題情境的選擇體現了這一成熟的合成方法所具有的環境友好、經濟高效的特征。
TAME合成所采用的C5叔碳烯烴,是催化裂化得到的輕汽油中含量最多的烯烴,其同分異構體中,2-甲基-1-丁烯和2-甲基-2-丁烯用于本題中TAME的合成,且得到產物相同;其他異構體3-甲基-1-丁烯和直鏈烯烴則無醚化活性。所以,本題引導學生在解答過程中體會合成路徑的高選擇性優勢。
在《碳五叔碳烯烴乙醇醚化研究進展》一文中,選取的合成反應和圖像(見表1及圖1)與本題高度相似,是命題的文獻依據。
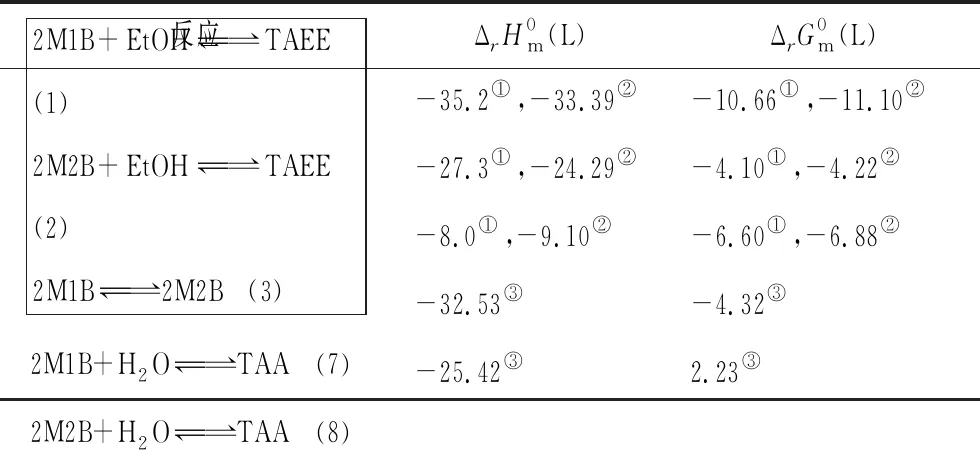
表1 反應的標準摩爾焓變及Gibbs自由能變(298.15 K)

圖1 2M1B及2M2B醚化、水合、異構化反應的平衡常數
2.必備知識
一是化學語言與概念,主要涉及蓋斯定律、平衡常數、化學反應速率等基本概念;二是反應變化與規律,主要包括化學反應的吸放熱,外界條件對平衡移動、化學反應速率的影響,化學平衡常數的計算等。
3.關鍵能力
一是理解與辨析能力,要求能夠從題給信息中提取有效信息,應用反應熱、化學反應速率和化學平衡等基本知識解決本題設置的實際問題;二是分析與推測能力,要求能夠根據題干描述,判斷變化的外界因素,進一步判斷平衡移動方向;三是歸納與論證能力,要求能夠從圖像、圖示中提取信息,結合所學知識對反應熱大小比較、平衡常數Kx的計算、反應方向進行綜合分析判斷。
三、教學啟示
第20題是試卷的最后一題,學生沒有足夠時間進行充分的審題和思考,同時,題目依托陌生情境,數形結合,頗具難度,使本題得分較低。破解新情境試題,需要考生在掌握必備知識的基礎上,具備信息加工能力、分析歸納能力和邏輯推理能力。因此,在復習時倡導學生展開讓學習真正發生的“深度學習”。綜合運用知識和方法創造性地解決問題時深度學習更容易發生,其特征是注重批判理解、強調信息整合、促進知識建構、注意遷移運用、面向問題解決并提倡主動學習和終身學習,其核心特征是高階思維,發展高階思維有助于促進深度學習。據此,筆者認為可以從以下幾個途徑更好的進行新高考備考:
1.回歸知識本源,重視知識形成
在深入學習《普通高中化學課程標準(2017年版2020年修訂)》(以下簡稱《課程標準》)的同時,教師在日常教學中不能忽視教材和教參的閱讀和使用。教材編寫組專家在用教材中的史料、實驗、概念呈現對《課程標準》的解讀。本次等級考試題中多個情境素材都是脫胎于教材的史料、課后習題、教參分析。因此,教師應深度挖掘教材和教參中的知識延伸,配合變式訓練,促進學生知識的全面建構。根據學科特點,知識形成的過程遠比結論更重要。高中化學課堂可選取科學探究、圖像圖譜辨識、化工流程分析、有機合成路線等設計核心任務,在任務導向下開展項目學習、合作學習、實驗探究,從單一知識點,到真實復雜情境下的問題解決,逐步提升學生學習能力和學科素養。
2.促進知識結構化,構建思維模型
高考注重考查必備知識,幫助學生形成知識結構化是一輪復習的重點,也是后續形成模型、提升核心素養的必須。例如,Kc、Kp、Kx是常見的幾種化學平衡常數,在以往的全國高考卷和各地高考卷中都有呈現。但這幾種化學平衡常數各自計算表達式又略有不同,計算時不同的反應還可能因系數、恒容、恒壓關系存在簡化計算,這些都需要學生在日常積累中形成經驗、劃歸能力。再比如,比較速率大小的常見方法應梳理到位,c-t圖像中,同一點的v正、v逆如何比較,不同點的v正、v逆如何比較、宏觀速率如何比較等等。結構化知識才能進一步形成知識模型、思維模型,胸有成竹方有能力走出誤區。
3.重視情境創設,提升關鍵能力
情境類試題是高考命題的趨勢,通過情境考查化學原理和方法在生產實踐中的應用。2021年山東省學業水平等級考試大量出現新情境,學生反饋的難點主要是審題入題困難,在“與數學知識關聯辨識模型、提取圖表信息”“獲取關鍵內容與有關已學知識進行整合”顯得應對不足。建議后期備考過程中,教師應關注當今世界的科學研究熱點,增加情境分析的專門指導,配合基于科技文獻的閱讀訓練和原創題編制,在各種新情境中,訓練審題、分析、作答的各個細節,從知識獲取、實踐操作和思維認知不同維度提升學生的學科關鍵能力。
【作者單位、姓名】山東省青島第十七中學 趙嶸
2021年全國甲卷第28題分析
[原題略]
1.試題分析
(1)28題情境素材源自十四五期間的我國力爭實現的“2030年前實現碳達峰,2060年前實現碳中和的目標”政府工作報告。題干中給出用氫氣與溫室氣體二氧化碳反應制備甲醇的反應原理,向考生普及用化學方法減少二氧化碳來實現碳中和的技術手段,展示我國科學家在綠色發展和清潔能源開發利用方面的創新成果,彰顯我國在應對全球氣候變化問題的責任與擔當,最后回歸到用化學反應原理知識來解決情境問題。
(2)根據《中國高考評價體系》中“一核四層四翼”的基本框架,28題在知識獲取能力群方面主要考查信息搜索能力、閱讀理解能力和信息理解能力,如28題(1)提供合成甲醇的反應焓及分步反應快慢信息,讓學生獲取反應能量變化的基本信息,并判斷物質等溫和等壓下甲醇物質的量分數的變化曲線;在實踐操作能力群方面通過數據圖的形式向學生提供豐富的信息,讓學生通過化學反應原理分析數據曲線代表的物理量之間的關系,考查學生語言表達能力、數據處理能力、信息轉化能力,如(2)②對應等壓過程的曲線的判斷理由;在思維認知能力群方面主要考查歸納概括能力、演繹推理能力和批判性思維能力。
(3)28題(1)密切關注《課程標準》中的學業要求和中學教學實際,通過圖像方式提供豐富的數據信息,深入考查學生信息整理能力,如三個相關反應的判斷并說明理由,落實了宏觀辨識與微觀探析素養。28題(2)落實變化觀念與平衡思想、證據推理與模型認知等學科素養。在“宏觀-微觀-符號-曲線”上考查到位,考查要求上難度有所降低,如(2)①二氧化碳加氫制甲醇的總反應平衡常數要求學生給出Kp表達式,體現試題的基礎性、應用性。
(4)本題考查知識點有蓋斯定律、化學反應的活化能、焓變、反應條件選擇、平衡思想等。
(5)本題聚焦基礎化學理論和化學工程技術,注重選取碳中和真實情境,弘揚學科核心價值,創新呈現形式,優化設問方式,聚焦學科核心素養,突出考查關鍵能力,踐行中國高考評價體系。
(6)對適合學生認知特點的化學學科基本反應原理的考查,轉變呈現方式和考查思路,使考生能由淺入深、由表及里地分析和解決問題,鼓勵學生理性學習,引導減少死記硬背和“機械刷題”現象,充分發揮高考命題積極導向作用。
2.試題解析


根據蓋斯定律可知,①+②可得二氧化碳加氫制甲醇的總反應:

ΔH=ΔH1+ΔH2=(+41 kJ·mol-1)+(-90 kJ·mol-1)=-49 kJ·mol-1;該反應總反應為放熱反應,因此生成物總能量低于反應物總能量,反應①為慢反應,則反應①的活化能高于反應②,同時反應①的反應物總能量低于生成物總能量,反應②的反應物總能量高于生成物總能量,因此示意圖中能體現反應能量變化的是A項,故答案為-49;A。ΔH1為正值,ΔH2和ΔH為負值,反應①的活化能大于反應②的。

②該反應正向為放熱反應,升高溫度時平衡逆向移動,體系中x(CH3OH)=0.1將減小,因此圖中對應等壓過程的曲線是b;理由:總反應ΔH<0,升高溫度時平衡向逆反應方向移動,甲醇的物質的量分數變小。本題亦可以采用反證,等溫情況下,增大壓強平衡向體積減小方向移動,即正向移動,則x(CH3OH)增大,符合a曲線,即等溫選a,等壓則選b。
③設起始n(CO2)=1 mol,n(H2)=3 mol,則

起始(mol) 1 3 0 0
轉化(mol)x3xxx
平衡(mol) 1-x3-3xxx

【作者單位、姓名】貴州省黔西第一中學 史光源
2021年河北省普通高中學業水平選擇性考試13題分析
[原題略]
1.試題素材來源
本題引入大學教材中速率方程表達式來創新命題,以溶液中發生的競爭反應為載體,在復雜、陌生的研究對象及問題情境下,體現對圖像的識別、競爭反應中平均速率、濃度及轉化率的計算、活化能與化學反應速率的關系等知識的基礎性、綜合性和創新性的考查。
2.考查的關鍵能力
本題考查的關鍵能力側重于三個方面:一是理解與辨析能力,要求能夠從題干、題圖中提取有效信息,解決關于平均反應速率計算的實際問題;二是分析與推測能力,要求能夠根據反應速率與化學計量數、濃度的關系以及速率方程表達式解決競爭反應中物質濃度之比及轉化率計算的實際問題;三是歸納與論證能力,要求根據題給信息,推斷出競爭反應中反應速率的大小并結合所學知識對活化能的大小進行分析判斷。
3.考查的化學學科核心素養
本題考查的學科素養側重于兩個方面,一是變化觀念,要求能夠認識化學變化是有一定速率的,能多角度、動態的分析溶液中物質的濃度和轉化率的變化;二是證據推理與模型認知,能根據題給信息判斷競爭反應速率的快慢,并對活化能越大,反應速率越慢的理論模型及化學反應速率的定義表達式的計算模型進行應用。
4.亮點及創新點分析
(1)引入大學教材中速率方程表達式來創新命題。
(2)選擇題中首次引入了競爭反應,并要求進行競爭反應中物質平均反應速率和轉化率的計算。
5.命題思想及解題思路
A項:考查化學反應速率的定義表達式計算模型應用。

綜上所述,相關說法錯誤的只有A,故本題選A。
化學復習教學要吻合命題趨勢,既要全面夯實基礎,又要根據測試熱點引導學生梳理必備知識、建構思維模型,形成結構化、可視化的解題思路,同時還要提升獲取、整合信息的能力,最終轉化為問題解決的關鍵能力。
【作者單位、姓名】河北省石家莊市鹿泉區第一中學 趙均娜 魏利巍
2021年廣東省普通高中學業水平選擇性考試第17題
[原題略]
【試題分析】(1)1962年高考開始明確考查實驗室制備氯氣的化學方程式的書寫,之后經常作為識記內容進行反復考查。它之所以作為重點識記內容,主要是因為它是初中化學氣體制備系列裝置和原理的延伸,也是氣體制備知識的收官典型。
(2)根據化學方程式可知,制取的氯氣中混有氯化氫、水蒸氣,氯氣有毒,必須進行尾氣處理,因此使用飽和食鹽水吸收氯化氫氣體,濃硫酸除去水蒸氣,最后用NaOH溶液吸收尾氣,因此接口連接順序為c-d-b-a-e。
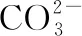
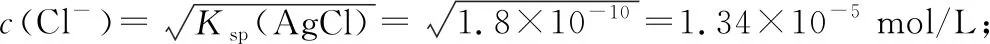
⑥從猜想b的結果逆推,要判斷AgCl在水中的溶解度隨溫度這個因素的變化情況,可以控制相同測試溫度,比較不同溫度的飽和溶液的電導率。相同測試溫度下,如果高溫飽和溶液電導率比低溫的飽和溶液高,則可以得出結論:隨著溫度的升高,氯化銀飽和溶液的離子濃度越高,故可得猜想b的溶解度隨著溫度的升高而升高的結論。
所以可以設計試樣Ⅰ在45℃下測試與實驗3比較;設計試樣Ⅱ在45℃下測試與實驗3比較。故答案為45℃;Ⅱ;45℃;⑦猜想b成立的判斷依據是A3>B2>B1。
1.素材來源、命題角度
本題挖掘化學史作為背景,融合新信息“電導率”,考查了實驗基礎和比較實驗設計的綜合能力。本題前面的問題都比較常規,難點在(4)。2007年人教版教材《選修4 化學反應原理》多處探究實驗使用了控制變量的研究方法。2018年北京初中階段“控制變量”思想成為考查的核心角度。確實,學生在初中階段,三種金屬活潑性比較的探究實驗,已經奠定了這類思想方法的基礎。2019年人教版教材必修的氧化還原反應探究實驗,也是三種強弱的比較。
2.映射課程標準、考查能力、素養
《課程標準》的學業水平質量指出,“4-3……能運用變量控制的方法探究并確定合適的反應條件,安全、順利地完成實驗;能用數據、圖表、符號等描述實驗證據并據此進行分析推理形成結論……”考查了學生獲取信息、運用新的信息解決問題的能力,邏輯分析能力,體現了運用科學思維方法解決實際問題的智慧,通過科學探究,考查了證據推理與模型認知的化學學科核心素養。
3.創新點、亮點
大題一般都是組合的,有些問題屬于識記層次的,有些問題是有區分選拔功能的。然而剝開“電導率”這層新衣服,不難發現,這個問題不算新問題,運用的方法,也有章可循,源于初中金屬活動性順序比較,深化在化學反應速率的影響因素,如果平時踏實學習的話,是可以深諳這類變量控制題目的思維模型的。
當然,壓在考生頭上的一座大山是現學現用的能力。這里出現的文獻資料,提供一個對于學生來講比較陌生的概念:電導率。然后解讀信息,可以發現,“溫度、濃度”屬于兩個自變量,“電導率、溶解度”屬于因變量,兩個因變量的情況,還是比較新鮮的表述。猜想a含糊,理解猜想b就存在障礙,猜想b的驗證思想,已經揭示了這類A>B>C的實驗模型。我們需要把新信息拆解,套入既有的熟悉的比較探究實驗的原型,這類問題就可迎刃而解。
前面說到學業質量水平的表述,“能用數據、圖表、符號等描述實驗證據并據此進行分析推理形成結論”,在此處有沒有考查呢?其實是有的。我們作圖3來理解(4)的實驗設計。
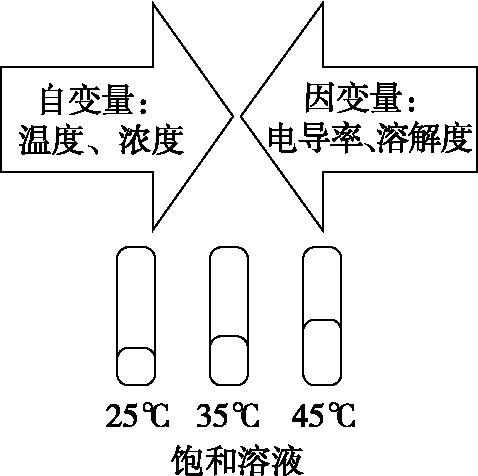
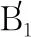
4.變式、同源試題復習建議
通過分析,不難發現,這類比較實驗探究題,屬于實驗設計能力的考查重點,深入考查了同學們的邏輯思維能力。所以,平時的新課學習,需要加強化學學科思維方法的原型辨認練習,以不變的“變量控制設計思想”應付萬變的情景。復習階段,需要把同類型的教材比較探究實驗(比如金屬性比較、氧化還原性比較、影響反應速率、化學平衡的因素等)進行梳理,列表分類別比較,求同求異,以求深入理解設計原理。嘗試自行根據實驗目的設計整個方案,遇到這類給出一半方案的試題,自然胸有成竹,也可準確評價別人的實驗方案。
5.小結
高考化學定位是選拔性考試,要篩選出具有運用信息解決問題能力的人才和建立了良好的思維方法習慣的人才。所以,針對高考的復習,不僅要有一定的題量,更加要深入理解、對標《課程標準》要求,對知識和技能、素養和智慧加以磨煉,守得云開見天明。

