中孕期母血產前篩查的室內質控結果室間比對分析
張 穎,段紅蕾,李照俠,朱雨捷,李 潔
南京大學醫學院附屬鼓樓醫院產前診斷中心,江蘇南京 210008
中孕期母血清學篩查主要通過檢測母血清中甲胎蛋白(AFP)、游離人絨毛膜促性腺激素(Freeβ-hCG)水平,同時結合孕婦年齡、體質量、采血孕周等妊娠相關信息,評估胎兒21-三體、18-三體、開放性神經管畸形的患病風險[1-2]。實驗室對AFP、Freeβ-hCG指標檢測的準確性,將直接影響篩查結論及后續的臨床處理,嚴格的室內質量控制(簡稱質控)管理和室間質評是高質量產前篩查工作中的重要環節[3]。為更好評估實驗室檢測的精密度和準確度,在已有室內質控和室間質評的基礎上,江蘇省在全省范圍內開展孕中期母血清學篩查數據室內質控室間比對工作。
1 資料與方法
1.1數據采集 在江蘇省產前篩查質控數據平臺上,收集2018年9月至2019年8月33家檢測單位上報的中孕期母血清學產前篩查的AFP、Freeβ-hCG質控數據9 632個。
1.2質控品 各實驗室統一使用相同批號的AFP/Freeβ-hCG質控(U2180501,杭州寶榮)。每套質控品包括高、中、低3個水平。
1.3檢測方法 各家實驗室將統一批號的質控品和標本同時采用時間分辨免疫熒光法進行檢測。各檢測單位按照Levey-Jennings質控標準根據檢測結果完成室內質控后,將質控品測定數據及儀器型號上傳至江蘇省產前篩查質控數據分析平臺。
1.4試劑與儀器 檢測儀器及試劑均由美國PerkinElmer公司生產。33家檢測單位中,21家單位(A1~A21)使用1235型儀器,4家單位(S1~S4)使用1420型儀器,8家單位(D1~D8)使用DX型儀器。
1.5評價指標 根據國家標準《臨床實驗室室間質評要求》制訂評定標準[4]。
1.5.1精密度評價 變異系數(CV)=標準差/均值。變異系數指數(CVI)=某個實驗室標準差/所屬儀器分組標準差。判定標準:CV<5.0% 且CVI≤1.0,為合格;CV<5.0%且CVI>1.0,為假陽性;CV>5.0%且CVI>1.0為真陽性。CV的合格需結合CVI值進行綜合分析。
1.5.2結果一致性評價 總誤差(TE)=|單個實驗室均值-所屬儀器分組均值|+2×單個實驗室標準差。允許總誤差(TEa)設定為實驗室所屬儀器分組均值的30%。
標準差指數(SDI)=(單個實驗室均值-所屬儀器分組均值)/所屬儀器分組標準差。判定標準:TE≤TEa且|SDI|≤2.0為合格,TE≤TEa且|SDI|≤1.0為良好,TE≤TEa但|SDI|>2.0或TE>TEa均為不合格。
1.5.3準確度和精密度綜合評價 臨界系統誤差(ΔSEc)= (所屬儀器分組TEa-|單個實驗室均值-所屬儀器分組均值|)/單個實驗室標準差-1.65,ΔSEc用于準確度和精密度的綜合性評判,測量在5.0%以上結果超出TEa界限之前均值偏移的標準差個數。 判定標準:ΔSEc>2.0為合格。如ΔSEc≤2.0,需重新制訂實驗室的質控規則。
1.6統計學處理 采用R軟件(4.0.2版本),統計AFP和Freeβ-hCG低值、中值及高值質控品的測定個數、均值、標準差、CV、SDI、CVI、TE和ΔSEc等參數,并采用ggplot2包分別繪制AFP和Freeβ-hCG指標的CV值分布直方圖,以及CVI和SDI的尤敦圖。
1.6.1納入標準 因各實驗室標本量不同導致實驗次數不相同,納入同一質控品批號使用頻次≥10次的數據。
1.6.2剔除標準 根據Grubbs檢驗法的臨界值表剔除極端異常值:G=|單個實驗室測定值-單個實驗室均值|/單個實驗室標準差。剔除超過本組均值±3標準差的質控數據。
2 結 果
2.133家實驗室的精密度測定分析 AFP檢測的精密度測定合格率為97.0%(32/33,圖1),不合格率為3.0%;Freeβ-hCG檢測的精密度合格率78.8% (26/33),不合格率為21.2%。其中編號S1的實驗室中AFP和Freeβ-hCG的3個水平精密度均不合格,均CV>5%。Freeβ-hCG測定中發現,共7家實驗室Freeβ-hCG質控結果不合格,其中S1實驗室3個水平質控結果均不合格,D7、D8、A4實驗室分別有2個水平質控結果不合格,D2、D6、A13實驗室各有1個水平質控數據不合格, 且CV均>5%(圖2)。
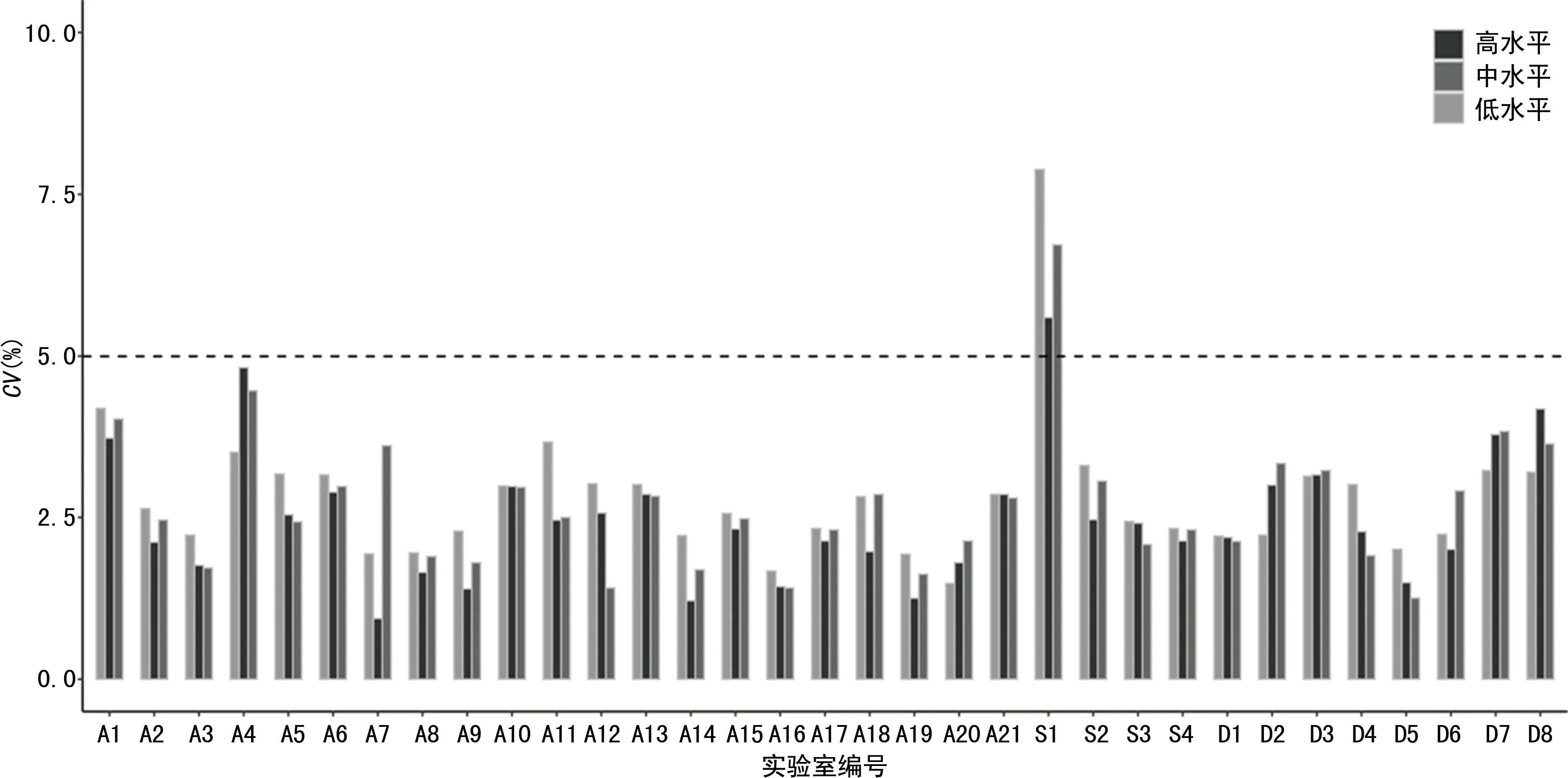
圖1 33家實驗室AFP檢測的CV分布圖

圖2 33家實驗室Freeβ-hCG檢測的CV分布圖
2.233家實驗室測定結果的一致性分析 33家實驗室AFP和Freeβ-hCG檢測均為TE≤TEa且|SDI|≤2.0,AFP和Freeβ-hCG檢測一致性合格率為100.0%。其中23家實驗室AFP測定TE≤TEa且|SDI|≤1.0,實驗室一致性測定良好率為69.7%(23/33,圖3);Freeβ-hCG檢測的實驗室一致性測定良好率為81.8%(27/33,圖4)。

圖3 33 家實驗室AFP檢測的CVI與SDI分布尤敦圖

圖4 33 家實驗室Freeβ-hCG檢測的CVI與SDI分布尤敦圖
2.33種儀器測定的精密度分布 剔除138個數據,納入9 494個質控數據。1420型儀器組質控剔除率(3.19%)高于1235型儀器組(1.24%)和DX型儀器組(1.65%),差異有統計學意義(χ2=26.20,P<0.001);3組儀器間,AFP的CVI合格率差異無統計學意義(χ2=2.36,P=0.308);Free β-hCG的CVI合格率比較:DX型儀器組低于1235型和1420型儀器組,差異有統計學意義(χ2=6.94,P=0.031)。
各儀器組的SDI和TE都符合基本要求。1235型儀器組和DX型儀器組ΔSEc達標率100%(29/29);1420型儀器組ΔSEc有1家實驗室(S1)不達標。見表1。

表1 3種儀器測定AFP和Freeβ-hCG的精密度分布

續表1 3種儀器測定AFP和Freeβ-hCG的精密度分布
3 討 論
質量管理是實驗室管理的核心,搞好質量管理也是實現實驗室標準化、規范化和科學化管理的關鍵。實驗室可采用室內質控來評價檢測結果的精密度,但較難評價準確度;采用室間質評可進一步評估檢測的準確度,但頻次相對較低。本次是對2018年9月至2019年8月江蘇省33家產前篩查實驗室使用相同批號的質控品,并將室內質控結果實時上傳做室間質量比對,可高頻率同時監測評價實驗室檢測的精密度和準確度,較好地彌補了室內質控和室間質評的局限性[5]。
CV是常用的精密度評價指標,本研究中AFP和Freeβ-hCG指標CV不合格率分別為3.0%和21.2%。CV不達標,說明實驗室檢測穩定性差,隨機誤差大。實驗室環境、儀器狀態、加樣量是否準確等因素均會影響檢測的精密度。CVI被用來評價相同儀器組內各實驗室檢測的相對精密度。CVI的假陽性或假陰性評估,需要與該組的組CV來比對:組CV比較小,那么可能出現單家實驗室CVI假陽性,反之組CV很大,則可能出現單家實驗室CVI假陰性。使用1235型儀器的實驗室中有7家(A1、A4、A5、A7、A10、A11、A13)、使用DX型儀器的實驗室中有5家(D2、D3、D4、D7、D8)都出現CVI假陽性,這是其組內均值較低造成的。因此在分析單家實驗室CV時需結合組內CVI。Freeβ-hCG指標檢測CV值較大,可能與Freeβ-hCG指標更易受溫度等因素影響有關[6]。有研究表明,溫度升高可導致Freeβ-hCG假性增高,進而導致21-三體假陽性率增加;反之增加漏診風險。
TE是總誤差,含精密度和準確度;SDI被用來評價相同儀器組內各實驗室檢測的相對準確度。A11、A12、A16、S1實驗室SDI雖達標,但檢測值相對本組均值偏離較大,需警惕。以A11實驗室為例,AFP指標偏低會引起21-三體和18-三體陽性率升高,導致開放性神經管畸形陽性率降低。A12實驗室AFP和Freeβ-hCG指標均偏高,導致增加18-三體漏診風險。建議上述實驗室通過對儀器的加樣針進行校準,調整標本處理流程等方式降低系統誤差,同時評價所在地區人群分布中位數來決定是否需要調整中位數方程[7],降低與同組實驗室的差異。
除S1實驗室外,本次各家實驗室ΔSEc均達標,說明使用的質控規則和方法以及設定測定的質控品個數符合質量控制規范標準。
儀器分組結果顯示,在不考慮S1實驗室的情況下,3種技術平臺均具有較好的一致性。在精密度方面,1235型儀器組優于1420型儀器組和DX型儀器組。1420型時間分辨熒光分析儀屬于半自動化機器,需要手工加樣,孵育的時間和溫度誤差可能容易對檢測穩定性產生影響。DX型與1235型雖然都是全自動儀器,1235型每批次實驗均進行定標,而DX型用戶大多采用定期定標校準方式,如果儀器狀態改變卻未及時定標校準,可能對檢測結果造成影響,所以實驗室應定期對儀器做維護,及時發現問題;同時DX型投入臨床使用時間相對于1235型較短,數據量較少,目前使用定期定標的方法是否需要調整,有待于進一步積累數據。
綜上所述,本次實驗的室內質控結果室間比對顯示,除S1實驗室外,其他實驗的精密度檢測均合格,同一檢測平臺的檢驗結果也具有較好的一致性,但不同實驗室、不同檢測平臺的精密度尚存在一定差異,可通過SOP固化流程、人員培訓熟練操作、儀器維護與保養、設備更新和性能增高等措施來改進。該方法可以發現無室間質評檢測項目在同一檢測平臺的報告結果中存在的質量問題、檢驗結果的不一致性,有利于提高檢驗結果的可比性。

