Ag@硅氧倍半聚合物的合成及其對對硝基苯酚的催化還原性能
吳洪花 祖鳳華 付 山 董曉龍 李素云 義建軍 郝海軍*, 徐慶紅*,
(1北京化工大學化學學院,北京 100029)
(2中國石油天然氣股份有限公司石油化工研究院,北京 102206)
對硝基苯酚(4?NP)是一種重要的化工原料,作為中間體被廣泛地應用于染料、農藥、醫藥等合成中。但4?NP同時也是一種劇毒化合物,對人體肝臟和腎臟以及神經系統會造成損害[1?4],如果其不能被妥善處理,進入自然界后會對生態環境安全和人類身體健康造成嚴重威脅。為了消除4?NP對環境和人體安全的危害,學術界探索并發展了許多去除環境中4?NP的方法,其中主要有物理、生物和化學3種方法[5]。
物理去除4?NP的方法主要有吸附、萃取和膜分離等。吸附法[6?9]僅僅是轉移了4?NP,并未完全消除其危害,且吸附劑再生是一個較為突出的問題。萃取法[10?12]則存在萃取劑使用量大且萃取劑容易殘留而引發二次污染問題。膜分離法[13?16]存在的對膜材料要求高等問題也限制了其大規模應用。生物法[17?20]主要通過利用微生物將 4?NP 降解為 CO2和NH3等相對危害較低的小分子,具有二次污染小、成本較低的獨特優勢。但微生物對環境要求相對較高,易受4?NP的毒性影響而死亡,且微生物整體降解效率偏低,降解過程所需時間長。目前化學法成為去除溶液中4?NP的主要方法。
化學法去除溶液中4?NP主要有氧化和還原2種方法。氧化法是利用過氧化氫、臭氧、高錳酸鉀和 Fenton 試劑等[21?24]高效氧化劑對 4?NP進行化學氧化降解,具有綠色、高效等優點,但該方法同時具有成本高、反應條件苛刻等缺點。利用還原劑將4?NP還原為4?氨基苯酚(4?AP)是還原法在廢水處理中的應用。該方法具有變廢為寶的獨特優勢,還原產物4?AP不僅是目前應用廣泛的一種精細有機化工中間體,具有很高的產品附加值[25],而且非常符合綠色環保理念。還原法將4?NP還原為4?AP所用的催化劑通常需要負載在載體上。目前所用的載體主要有聚乙烯醇海綿、碳材料、金屬氫氧化物等,催化劑主要有鉑、銠、鉍等貴金屬的納米粒子[26?28]。銀納米粒子(Ag NPs)以其高效的催化還原性能始終受到人們的廣泛關注[29?33],尤其是粒徑小、高度分散(在載體表面)的 Ag NPs。
我們以易合成得到的含多配位基微孔硅氧倍半聚合物為主體材料,將Ag+與聚合物骨架先配位后還原得到Ag NPs高度分散的Ag@硅氧倍半聚合物復合物,并以此復合物作為催化劑將4?NP還原為4?AP。研究結果表明,復合物中銀負載量(質量分數)約為13.66%,在水溶液中25℃、6 min內可將4?NP完全還原為4?AP,而且7次循環使用后依然保持95%以上的催化活性,表現出優異的催化還原性能。
1 實驗部分
1.1 試劑與儀器
氨丙基三乙氧基硅烷((CH3CH2O)3SiCH2CH2CH2NH2,99%)、草酰氯(C2O2Cl2,98%)購自麥克林公司,P123(聚環氧乙烷-聚環氧丙烷-聚環氧乙烷三嵌段共聚物)、對硝基苯酚(99%)、檸檬酸鈉(99%)、硝酸銀(99%)、硼氫化鈉(99%)購自北京化工廠,濃鹽酸(HCl,36.7%)、無水乙醇(99.7%)、二氯甲烷(98%)購自國藥集團,三乙胺(99.5%)購自阿拉丁公司。實驗所用試劑均為分析純,全部實驗用水均為脫氧去離子水。
利用核磁共振波譜儀(400 MHz,Chloroform?d,AVANCEⅢ,瑞士,布魯克Bruker)和質譜(MS,Agilent Q?TOF6540)對合成樣品進行純度分析;利用能量色散X射線光譜儀(EDS,S?4700 Hitachi,日本)對合成的復合催化劑進行組成分析;利用Bruker Vector?22紅外光譜分析儀(德國布魯克光譜儀器公司制造)對合成產物中鍵合情況以及某些官能團的存在進行分析,待測樣品用KBr稀釋(嚴格控制樣品與KBr質量比為1∶100),測試波長范圍為400~4 000 cm-1,儀器分辨率為 2 cm-1;利用 TecnaiG220S?TWIN透射電子顯微鏡(TEM,美國FEI公司制造)對樣品的形貌及內部結構進行觀測,儀器工作電壓為200 kV;利用JEM?2010掃描電子顯微鏡(SEM,日本電子株式會社制造)對催化劑樣品形貌進行分析,儀器工作電壓為200 kV;利用X射線光電子能譜儀(XPS,日本島津公司)采集樣品的電子能譜,儀器的校準峰為C1s(284.6 eV);利用UV?3600紫外可見光譜分光光譜儀(日本島津公司制造)對樣品的紫外吸收進行分析(測試波長范圍為200~800 cm-1,儀器分辨率為2 cm-1)。
1.2 Ag@硅氧倍半聚合物(復合催化劑)的制備
將無水二氯甲烷(15 mL)、三乙胺(3.7 mL,27 mmol)和氨丙基三乙氧基硅烷(6 mL,27 mmol)分別加入50 mL干燥的三頸燒瓶中。保持混合液溫度為0℃下,向燒瓶內部逐滴加入含草酰氯的二氯甲烷溶液(1.0 mL,13.6 mmol)。滴加完成后,反應混合物在室溫下攪拌4 h,然后旋蒸除去溶劑得到硅氧倍半聚合物前驅體。前驅體的1H NMR及MS信息(CDCl3,400 MHz)δ:7.56(s,J=6.9 Hz,2H),3.80(q,J=7 Hz,12H),3.32(t,J=6.7 Hz,4H),1.67(m,J=7.7 Hz,4H),1.22(t,J=7.1 Hz,18H),0.64(t,J=8.3 Hz,4H);13C NMR(CDCl3,400 MHz)δ:159.81,58.47,42.02,22.81,18.28,7.15。 MS(ESI+)(M+1):m/zC20H44N2O8Si2計 算 值 :497.275 1,實測值:497.275 1。
硅氧倍半聚合物的合成[34]:向100 mL三頸燒瓶中依次加入脫氧去離子水(47.80 mL,2.66 mol)、無水乙醇(1.8 mL,26 mmol)和P123(1.0 g,1.74×10-4mol),混合物在室溫下劇烈攪拌2 h后升溫至80℃,然后將適量的、新合成的硅氧倍半聚合物前驅體逐滴加入到上述混合物中并不間斷攪拌2 h,將混合物轉移至反應釜中于100℃反應24 h。上述反應混合物經過萃取除去未參與反應的P123后,真空干燥6 h,得到硅氧倍半聚合物。
將0.8 g硅氧倍半聚合物和1.5 g AgNO3置于250 mL三口燒瓶中,并用100 mL脫氧去離子水溶解。在不間斷攪拌下,將上述混合體系在70℃持續加熱8 h,然后離心分離(5 000 r·min-1),棄去上清液,固體產物用脫氧去離子水洗滌若干次。然后將固體產物轉移至含有100 mL脫氧去離子水的燒瓶中,在98℃油浴持續加熱、攪拌條件下,將100 mL濃度為0.05 mol·L-1的檸檬酸鈉溶液逐滴加入上述固液混合物中。滴加完畢后立即停止反應,將混合物離心分離(5 000 r·min-1),棄去上清液,固體用脫氧去離子水洗滌數次,70℃真空干燥12 h。
以上所有實驗過程均在氮氣保護下進行。
1.3 催化劑催化性能測試
在常溫下,4?NP飽和溶液呈淡黃色,并在317 nm處有紫外特征吸收。當向其溶液中加入NaBH4溶液后,溶液為堿性,4?NP將以陰離子形態存在于溶液中。4?NP的特征吸收峰從317 nm紅移至400 nm,此時溶液顏色為亮黃色[35?36]。向 4?NP 和NaBH4的混合溶液中加入催化劑之后,通過比較溶液在400 nm處及317 nm處(4?AP的特征吸收)的吸光度值,可判定4?NP被還原的程度[37]。
分別配制濃度為0.1 mmol·L-1的4?NP溶液及濃度為0.5 mol·L-1的NaBH4溶液。配制過程全部用脫氧去離子水溶解固體樣品。量取2.5 mL 4?NP溶液于比色皿中,并向其中加入0.5 mL新配制的NaBH4溶液,在250~500 nm波長范圍內測液體的吸光度。然后向比色皿溶液中加入3 mg催化劑,自催化劑加入后每隔3 min測定液體的吸光度,比較溶液的吸光度隨反應時間的變化關系。上述反應過程需要控制一定的反應溫度。
2 結果與討論
2.1 合成產物的結構表征
SEM照片(圖1A)顯示,所合成的硅氧倍半聚合物外形不規則,尺寸分布在100~500 nm之間,TEM照片(圖1B)進一步證明了合成產物微形貌的不規則性。另外,圖1C顯示材料內部有大量蠕蟲狀孔的存在,孔徑大約為1.3 nm。圖1D為Ag@硅氧倍半聚合物的高分辨TEM照片。由圖可知,在硅氧烷聚合物表面高度分散著大量粒徑約為15 nm的Ag NPs,其晶格間距約為0.237 nm(圖1E),與文獻報道的結果[38]相一致。某些納米粒子粒徑較大,說明發生了團聚現象。在固載過程中,Ag+除了以配位態被固載于硅氧倍半聚合物孔道內部及外表面以外,硅氧倍半聚合物的外表面還存在部分吸附態Ag+,這部分Ag+被還原時發生了局部區域團聚現象。

圖1 (A)硅氧倍半聚合物的SEM照片;(B)硅氧倍半聚合物的TEM照片;(C)Ag@硅氧倍半聚合物的高分辨TEM局部放大照片;(D)Ag NPs的高分辨TEM照片;(E)單個Ag納米粒子的晶格照片;(F)硅氧倍半聚合物的EDS元素含量分析Fig.1 (A)SEM image of silsequioxanes;(B)TEM image of silsequioxanes;(C)High resolution TEM magnified local image of Ag@silsequioxanes;(D)High resolution TEM image of Ag NPs amplified locally;(E)Lattice photos of single Ag nanoparticle;(F)Analysis of elemental contents in Ag@silsequioxanes by EDS
EDS譜圖表明Ag@硅氧倍半聚合物復合催化劑中N與Si的原子比約為1∶1(圖1F),這與合成聚合物單體中二者的理論比相一致;復合催化劑中銀的負載量(質量分數)約為13.66%。
硅氧倍半聚合物及Ag@硅氧倍半聚合物的紅外光譜圖如圖2所示。從圖中可以發現,二者紅外吸收光譜基本一致。二者骨架中的碳氫振動(νC—H)及 Si—O—Si骨 架振動(νSi—O—Si)吸 收分別出現 在2 940 及 1 120 cm-1處,羰基振動(νC=O)吸收出現在1 661和1 686 cm-1處,亞氨基振動(νN—H)吸收出現在3 419和3 438 cm-1處。Ag與硅氧倍半聚合物骨架間的配位作用使亞氨基和羰基吸收發生了一定程度的紅移。
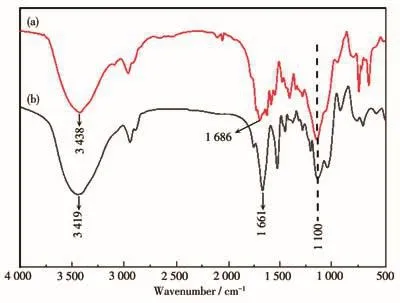
圖2 硅氧倍半聚合物(a)和Ag@硅氧倍半聚合物(b)的紅外光譜圖Fig.2 FTIR spectra of silsequioxanes(a)and Ag@silsequioxanes(b)
為了進一步證明硅氧倍半聚合物骨架上亞氨基和羰基與Ag元素之間配位關系的存在,對硅氧倍半聚合物、Ag+@硅氧倍半聚合物以及Ag@硅氧倍半聚合物進行了XPS測試,結果如圖3所示。由圖3可以看到,與硅氧倍半聚合物相比,Ag+@硅氧倍半聚合物中的N1s及O1s電子結合能發生了明顯變化。N1s的2種電子結合能分別從硅氧倍半聚合物中的399.1 eV(N—H結合態)和399.6 eV(N—C結合態)升高至399.3和399.9 eV(Ag+@硅氧倍半聚合物中);O1s的2處電子結合能分別從531.0 eV(O=C)和531.9 eV(O—Si)(硅氧倍半聚合物中)升高至531.3和532.1 eV(Ag+@硅氧倍半聚合物中)。而Ag@硅氧倍半聚合物相比于Ag+@硅氧倍半聚合物,N1s及O1s的電子結合能下降至399.2和400.0 eV(表1),接近硅氧倍半聚合物中N1s及O1s的電子結合能。上述結果表明,在Ag+@硅氧倍半聚合物中,硅氧倍半聚合物骨架上的O和N兩種元素受到了強烈的外界力作用,而這種外力作用只可能來自元素間的配位作用。這種配位、還原作用亦可以被Ag3d(圖3C)電子結合能在AgNO3、Ag+@硅氧倍半聚合物及Ag@硅氧倍半聚合物中的變化所證明。Ag+@硅氧倍半聚合物中Ag3d結合能相比于AgNO3中的結合能增加了約0.5 eV;而在Ag@硅氧倍半聚合物中,Ag3d結合能與銀原子中Ag3d的電子結合能367.7 eV一致[39],說明Ag+完全被還原為0價。以上產物中的N1s、O1s和Ag3d電子結合能數值列于表1中。
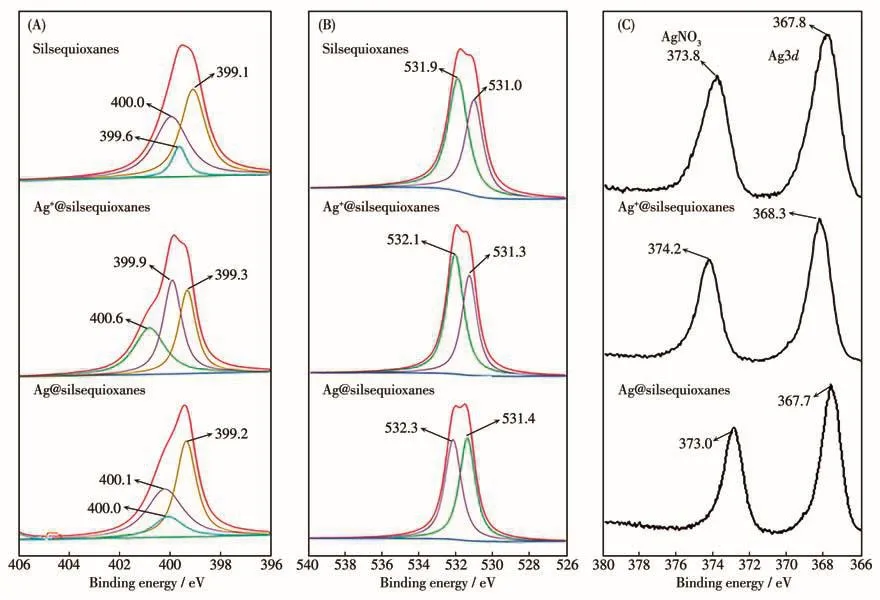
圖3 硅氧倍半聚合物、Ag+@硅氧倍半聚合物和Ag@硅氧倍半聚合物中的N1s(A)、O1s(B)、Ag3d(C)XPS譜圖Fig.3 XPS spectra of N1s(A),O1s(B),and Ag3d(C)in silsequioxanes,Ag+@silsequioxanes and Ag@silsequioxanes
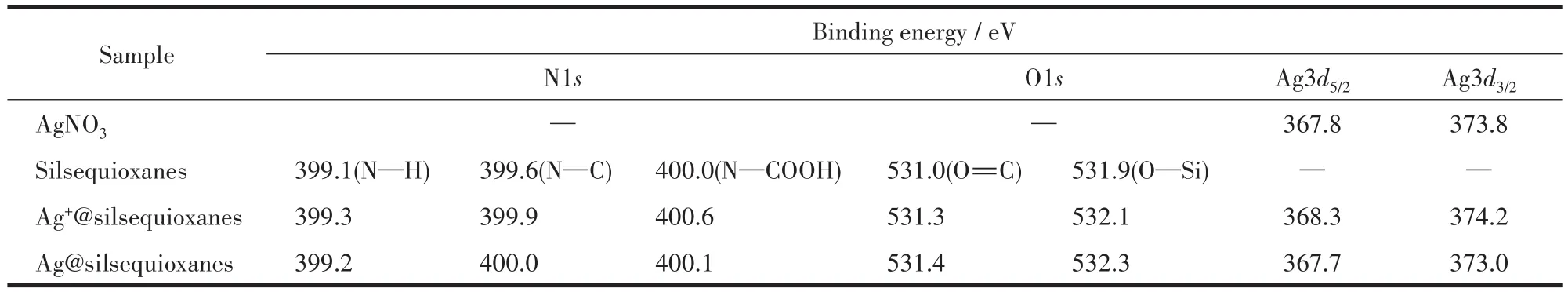
表1 樣品中某些元素的電子結合能Table 1 Binding energies of N1s,O1s and Ag3d in the samples
2.2 合成的負載型催化劑在4-NP還原反應中的催化活性探究
單質銀具有良好的催化還原活性,但銀的催化效率與銀原子聚集體粒徑大小有直接關系。顆粒粒徑越小,銀原子被暴露的程度越大,銀的催化活性提升得越高。將Ag NPs高度分散在硅氧倍半聚合物載體上,其目的就是要避免單質銀團聚現象的發生,獲得高度分散的小粒徑支撐型Ag NPs,提高銀的催化還原活性。首先,在常溫常壓下,分別向2個干燥的容器中加入20 mL 4?NP飽和溶液和5 mL配制的 NaBH4溶液(0.5 mol·L-1),然后再分別向 2個體系中加入等量的(3.0 mg)Ag@硅氧倍半聚合物和硅氧倍半聚合物。相同反應條件下2個反應體系的紫外可見光譜如圖4A和4B所示。結果發現,硅氧倍半聚合物在15 min內對4?NP無任何催化活性,溶液吸光度有所下降是硅氧倍半聚合物吸附性導致的;但對于加入Ag@硅氧倍半聚合物的體系,當反應進行到3 min時,有97%的4?NP被還原為4?AP,反應進行到6 min時,反應物幾乎完全被還原,催化劑的催化活性高達 33.0 g4?AP·gAg-1。Ag@硅氧倍半聚合物對4?NP的催化還原效果亦可以通過溶液前后顏色的變化看出(圖4D),在復合催化劑Ag@硅氧倍半聚合物的催化下,4?NP與NaBH4混合溶液在3 min內迅速從亮黃色變為無色(4?AP在水中的顏色)。對于載體來說,其本身對4?NP還原為4?AP不具有催化活性,這可以從圖4B中可以清楚地看出,說明擔載型復合催化劑的催化活性僅來自負載在載體硅氧倍半聚合物表面上的Ag NPs。進一步研究表明,不加入任何催化劑的情況下(空白實驗),NaBH4不能將4?NP還原為4?AP(圖4C)。
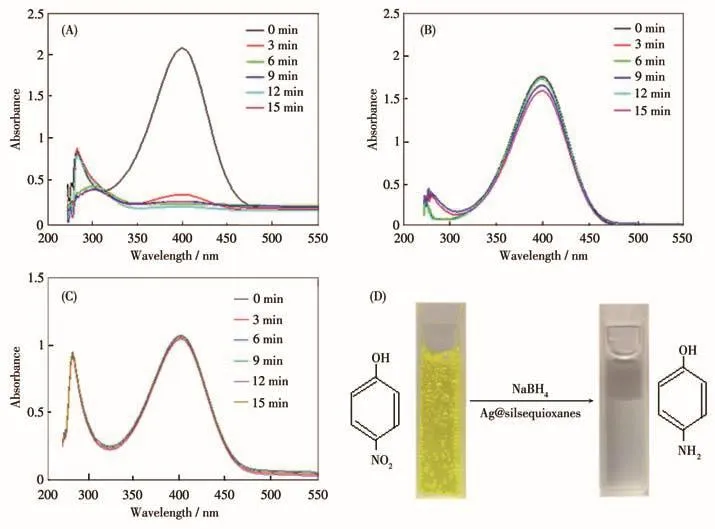
圖4 常溫常壓條件下,混合溶液(20 mL 4?NP飽和溶液和5 mL 0.5 mol·L-1NaBH4溶液)在加入3.0 mg Ag@硅氧倍半聚合物(A)、硅氧倍半聚合物(B)以及不加任何其他物質(C)后一定時間間隔下的紫外可見光譜圖;4?NP和NaBH4混合溶液在Ag@硅氧倍半聚合物加入前后顏色變化情況(D)Fig.4 UV?Vis spectra of mixed solution(20 mL 4?NP saturated solution and 5 mL NaBH4solution with a concentration of 0.5 mol·L-1)after adding Ag@silsequioxanes(A),silsequioxanes(B)and no additives(C)in a certain time interval at normal temperature and pressure;Color change of the solution before and after adding Ag@silsequioxanes for 6 min(D)
不同催化劑加入量(常溫常壓)對催化性能的影響如圖5所示。研究發現,3 mg復合催化劑在6 min內即可將底物完全催化還原。以3 mg復合催化劑和6 min為基本反應條件,在不同反應溫度下研究發現,在25℃環境中,Ag@硅氧倍半聚合物即可將4?NP完全催化還原為4?AP(圖 6),說明升高溫度對該催化反應幾乎沒有影響。
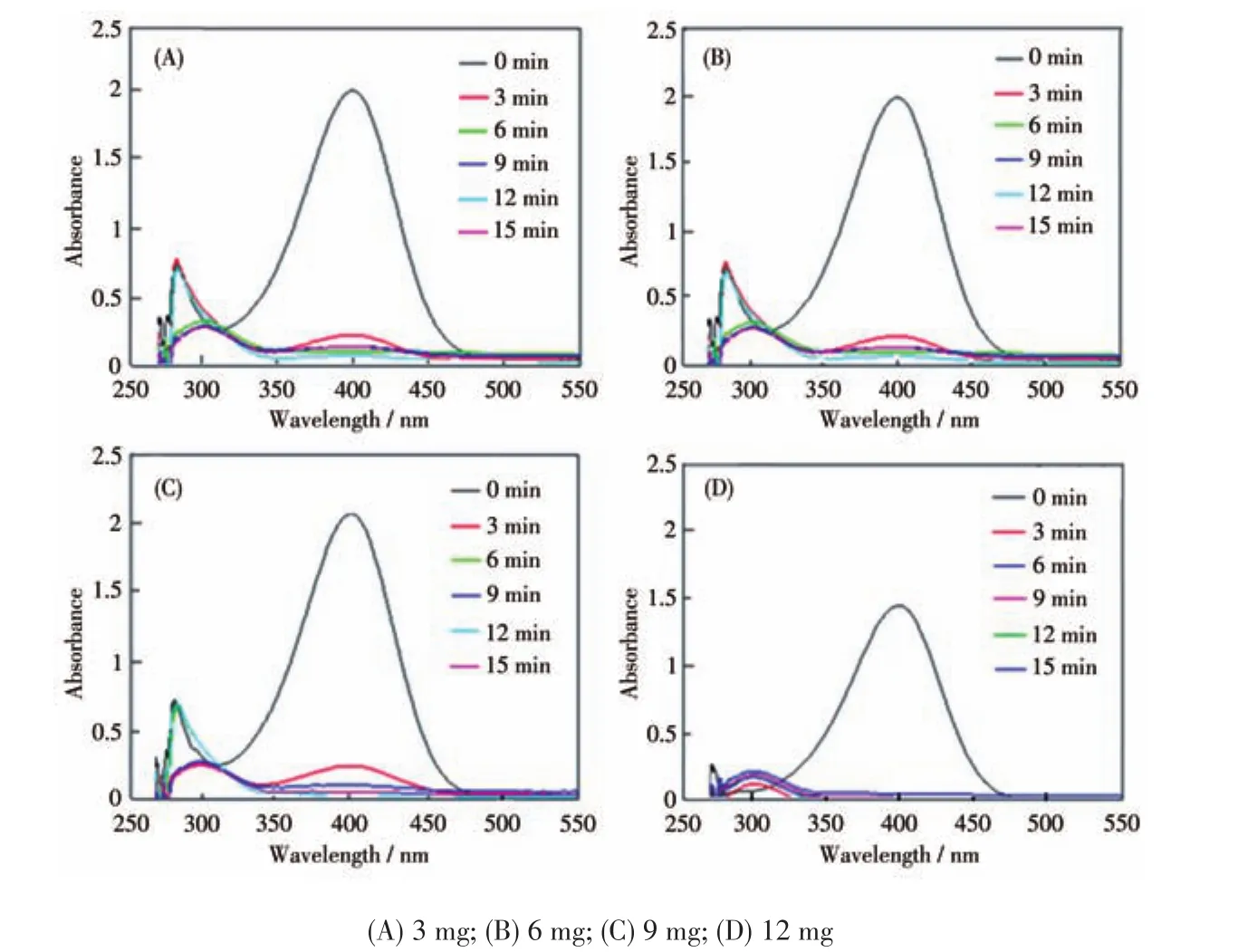
圖5 常溫常壓條件下,混合溶液(20 mL 4?NP飽和溶液和5 mL 0.5 mol·L-1NaBH4溶液)在加入不同質量的Ag@硅氧倍半聚合物后一定時間間隔下的紫外可見光譜圖Fig.5 UV?Vis spectra of mixed solution(20 mL 4?NP saturated solution and 5 mL NaBH4solution with a concentration of 0.5 mol·L-1)after adding Ag@silsequioxanes with different masses in a certain time interval at normal temperature and pressure

圖6 不同溫度下,混合溶液(20 mL 4?NP飽和溶液和5 mL 0.5 mol·L-1NaBH4溶液)在加入3 mg Ag@硅氧倍半聚合物6 min后的紫外可見光譜圖Fig.6 UV?Vis spectra of mixed solution(20 mL 4?NP saturated solution and 5 mL NaBH4solution with a concentration of 0.5 mol·L-1)after adding 3 mg of Ag@silsequioxanes in 6 min at different temperatures
催化劑的可重復利用性是關乎其應用的重要指標,可以以多次使用后催化底物的轉化率對其進行評價。底物轉換率(η)用公式η=(A0+At1-At2)/(A0+At1)表示,其中,A0為溶液的初始吸光度,At1與At2分別代表前一次及后一次循環實驗后溶液的吸光度。研究發現,Ag@硅氧倍半聚合物經過7次循環使用后,4?AP的轉換率保持在95%以上;但第8次循環使用時,4?AP轉換率開始明顯下降,大約80%,如直方圖7所示。因此,該負載型催化劑對4?NP還原為4?AP的反應具有一定的結構和活性穩定性。
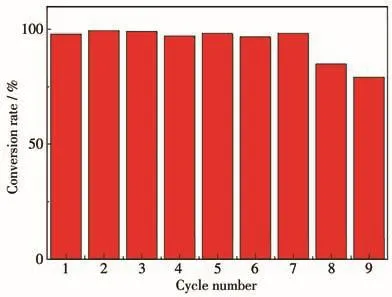
圖7 Ag@硅氧倍半聚合物循環使用催化性能穩定性直方圖Fig.7 Stability histogram of catalytic performance of Ag@silsequioxanes for recycling
2.3 硅氧倍半聚合物結構對Ag納米顆粒負載效果的影響
為了檢驗硅氧倍半聚合物中亞氨基和羰基官能團對Ag NPs負載作用的影響,將結構上不含亞氨基和羰基官能團的硅氧烷1,6?雙(三甲氧基硅基)己烷前驅體作為對比,并將其在酸性條件下聚合得到的硅氧倍半聚合物為載體進行Ag NPs負載,研究了其催化性能(該硅氧倍半聚合物的合成及1H核磁共振表征結果詳見Supporting information)。研究結果表明,Ag在1,6?雙(三甲氧基硅基)己烷聚合物表面上的負載量(質量分數)為6.40%(圖8A),遠低于Ag@硅氧倍半聚合物的13.66%,其將4?NP徹底還原為4?AP至少需要12 min,而相同條件下聚合物鏈上含亞氨基和羰基官能團的Ag@硅氧倍半聚合物只需要6 min(圖8B)。這種差異性可能來自2個方面:其一,Ag NPs在不含亞氨基和羰基載體表面進行的僅僅是物理負載,負載量較少;其二,簡單的物理負載造成Ag NPs在載體表面上發生團聚,銀傳輸電子路徑不通暢,導致催化效率低。
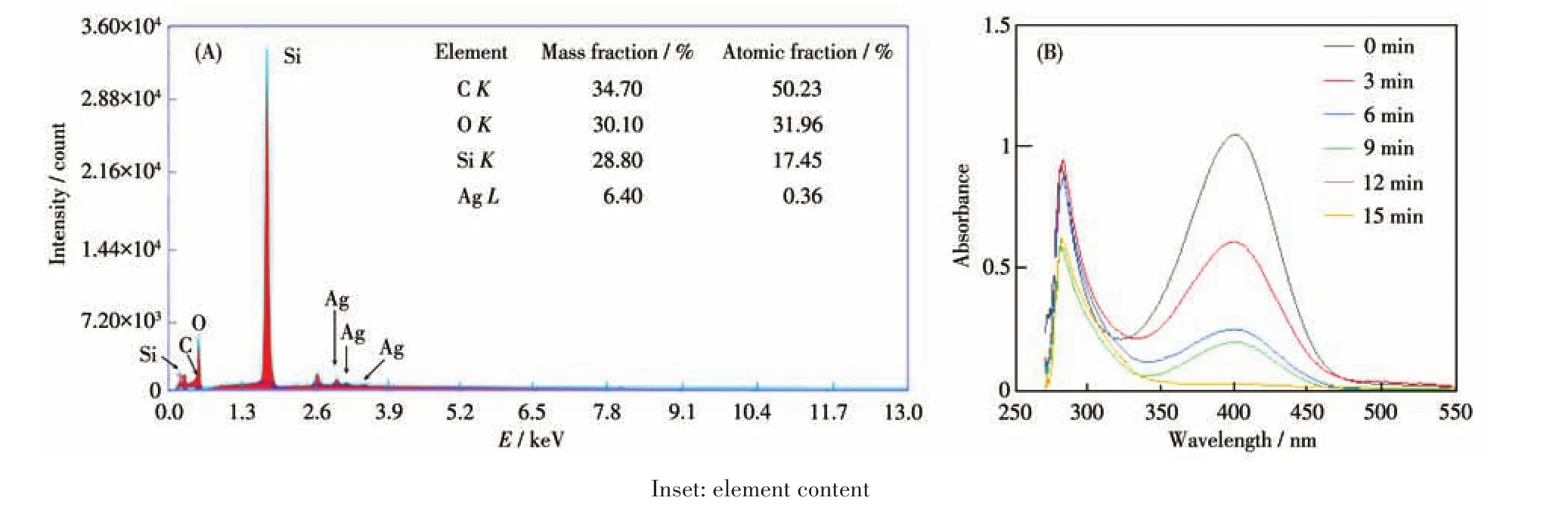
圖8 Ag@1,6?雙(三甲氧基硅基)己烷聚合物的EDS譜圖(A)和Ag@1,6?雙(三甲氧基硅基)己烷聚合物催化還原產物的紫外可見光譜圖(B)Fig.8 EDS spectrum of Ag@6?bis(trimethoxysilyl)silsequioxanes(A)and UV absorption spectra of the products catalyzed by Ag@6?bis(trimethoxysilyl)silsequioxanes(B)
2.4 Ag@硅氧倍半聚合物在4-NP還原反應中的催化原理
經過查閱相關文獻[40?41],Ag@硅氧倍半聚合物對4?NP的催化還原可能通過以下途徑完成。一方面,Ag NPs首先吸附BH4-,BH4-失去電子并通過Ag原子快速轉移給4?NP,大大降低了反應能壘;另一方面,電子的快速轉移相應地增加了Ag NPs表面的電勢差,進而增加了Ag NPs對NaBH4和4?NP的吸附能力,導致局部反應物濃度增加,加大了反應物碰撞幾率,使反應速率加快。此外,由于Ag NPs均勻地分布于載體表面,有效地避免了團聚現象發生,催化活性中心暴露程度增大,使復合催化劑表現出優異的催化性能[41]。反應原理如圖9所示。

圖9 Ag@硅氧倍半聚合物的催化反應原理Fig.9 Catalytic reaction principle of Ag@silsequioxanes
3 結 論
以氨丙基三乙氧基硅烷和草酰氯為原料,合成得到含亞氨基和羰基官能團的硅氧倍半聚合物,并成功地實現了負載型復合催化劑Ag@硅氧倍半聚合物的合成,該催化劑中的Ag NPs(平均直徑約為15 nm)高度分散在硅氧倍半聚合物表面。負載型催化劑在4?NP還原為4?AP反應中顯示出較高的催化活性。在常溫常壓下,復合催化劑的最高活性達到33.0 g4?AP·gAg-1。此外,該負載型催化劑具有良好的可重復使用性,經過7次循環使用,底物的轉換率保持在95%以上,具有高效、綠色等環境友好特性。
Supporting information is available at http://www.wjhxxb.cn
- 無機化學學報的其它文章
- Mn-Based Coordination Polymer:Facile Synthesis,Structure and Application in Glucose Electrochemical Sensing
- Preparation of Dehydrated Ni-Fe Hydrotalcite-like Compounds as an Eco-Friendly Catalyst for Highly Selective Acetalization of Biomass-Derived Furfural
- Synthesis,Structure Regulation and Characterization of Cadmium(Ⅱ)Complexes Based on Imidazole Carboxylic Acid Ligands
- Difunctional Effects of Organo-Modified T-Type Zeolite Membranes for Dewatering from Organic Solution
- Controlling Distribution of Gold Nanoparticles in Au@ZIF-8 Core-Shell Structures for Sensing Fluorescent Molecules with Photoluminescence
- Structures and Luminescence Property of Two Co(Ⅱ) and Cd(Ⅱ)Supramolecular Coordination Networks Created via Synergistic Effect of Coordination Bonds and Secondary Interactions

