金屬氧化物及氫氧化物去除水中氟離子的研究進展
楊 辰,謝友友,左景欒,琚宜文,琚麗婷,鄭建中
(1. 中國科學院大學 資源與環境學院,北京 100049;2. 中聯煤層氣有限責任公司,北京 100015;3. 中國科學院大學 地球與行星科學學院計算地球動力學重點實驗室,北京 100049)
氟是人體必需的微量元素之一,攝入適量的氟對人體骨骼、神經、生殖系統的發育具有重要作用,但過量攝入會導致氟中毒,危害人體健康[1]。人體中氟的主要來源之一是飲用水[2],世界衛生組織規定飲用水中F-的質量濃度應小于1.5 mg/L[3]。水中氟污染主要來自電鍍、玻璃及水泥生產、半導體制造、鋼鐵及鋁冶煉等行業[4]。
目前,去除水中氟離子的技術主要有沉淀法[5-6]、離子交換法[7-8]、膜分離法[9]、電滲析法[10]和吸附法[11]等。其中,吸附法除氟技術工藝成熟,操作方便,簡單高效,受到廣泛的關注[12]。對吸附劑的研究主要集中在金屬氧化物及氫氧化物、碳基吸附劑、離子交換樹脂、天然吸附劑等[13]。金屬氧化物及氫氧化物對氟離子具有較高的親和能力和吸附容量[14],主要包括鋁基、鐵基、稀土類、層狀雙金屬氫氧化物及其他金屬(包括鈣、鎂、鈦、鋯等)氧化物及氫氧化物。這類材料也常用于對天然吸附劑[15]、活性炭[16]等的修飾,以改善其除氟效果,是目前研究最多的除氟吸附劑之一。
本文綜述了金屬氧化物及氫氧化物除氟吸附材料的研究進展,介紹了吸附劑的吸附性能、吸附反應機理及改性方法,并在此基礎上探討了該類吸附材料的研究方向,為水中F-的吸附處理研究提供參考。
1 鋁基吸附劑
活性氧化鋁吸附F-的相關研究可追溯到1934年,是截至目前研究最為廣泛的氟吸附材料之一[17]。活性氧化鋁比表面積大(50~300 m2/g)、化學穩定性好并存在大量的晶格缺陷,具有較強的吸附能力,對氟的吸附量在1~20 mg/g[18-19]。活性氧化鋁除氟的過程是通過靜電吸附作用將F-吸附到氧化鋁表面,然后F-與氧化鋁中的羥基發生配體交換作用來實現的[20-21]。
溶液pH對除氟效果的影響較為顯著:酸性條件下,活性氧化鋁表面帶正電,有利于靜電吸附F-;然而,pH過低會促進AlF2+、AlF+絡合物的形成,影響水中F-的去除效果;pH 5~7范圍內除氟效果較好;堿性條件下,活性氧化鋁除氟效果較差,這主要是因為堿性條件下,材料荷負電,與F-產生靜電排斥作用,同時,OH-與F-產生競爭吸附[19,22]。其反應機理如下:
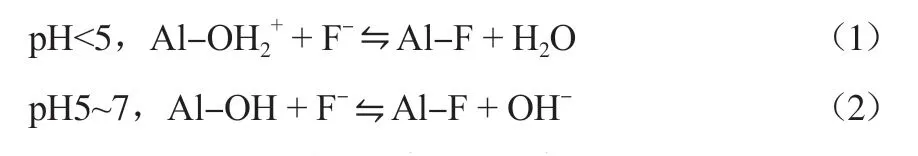
活性氧化鋁除氟效率的提高可以通過以下兩個途徑:增加表面活性位點的密度以及增加吸附劑的比表面積。考慮到氧化鋁除氟主要是通過F-與OH-交換完成的,增加表面活性位點的密度會促進氟的去除。GONG等[23]研究了表面酸堿度不同的氧化鋁的除氟性能,發現酸性氧化鋁除氟效率更高,這是因為其表面帶有更多正電荷且具有更多陰離子交換位點。此外,增加吸附劑的比表面積也是一種能有效提高活性氧化鋁除氟效果的手段。YANG等[24]采用異丙氧基鋁(Al(O-i-Pr)3)作為前驅體制備了比表面積為339 m2/g的高度有序的氧化鋁,對F-的吸附量可達135 mg/g,且吸附量在20 min內迅速增加。HUANG等[25]同時采用這兩種方式提高氧化鋁除氟能力,一方面采用空心管狀結構提高比表面積,另一方面使用H2O2將材料表面羥基化增加活性位點,材料的F-最大吸附量達600~800 mg/g。活性氧化鋁還可與碳質材料(如碳納米管等)以及其他金屬氧化物及氫氧化物吸附劑(如Fe3O4等)結合,提高吸附劑的比表面積[26]。然而采用鋁基吸附劑常有鋁離子溶出[18],可能對人體健康產生影響,還會導致處理后水的pH和總溶解固體量升高,使后續處理的難度加大[27]。
2 鐵基吸附劑
鐵基吸附劑主要包括鐵(氫)氧化物[28]和鐵礦石(紅土[29]和施威特曼石(Fe8O8(OH)6SO4)[30]等)。鐵氧化物表面含有不飽和配位點[31],與水中的OH-、H2O發生配合,使表面帶有具有反應活性的OH基團。鐵氧化物吸附氟的過程主要是通過F-與其表面的OH基團相互作用進行的[32]。其反應機理如下:
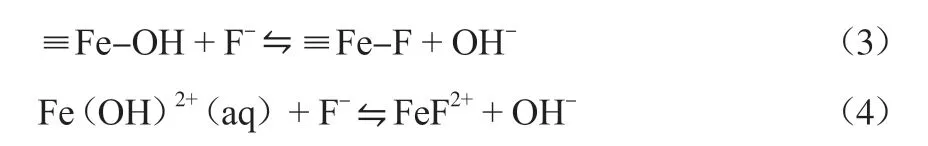
對鐵基吸附劑的研究主要集中在對鐵(氫)氧化物及鐵礦石吸附性能的研究。KUMAR等[28]研究發現,粒狀氫氧化鐵在pH為6~7時對F-的最大吸附量為7 mg/g。不僅鐵(氫)氧化物能去除水中F-,鐵礦石也有較好的除氟效果。施威特曼石在較低pH條件下能穩定存在,常被用于去除酸性廢水中的氟化物[30]。楊小洪等[33]對比了幾種鐵礦石的除氟效率大小,結果為:水鐵礦>磁鐵礦>針鐵礦>赤鐵礦。其中磁鐵礦因帶有磁性易于磁性分離回收而常被用作載體,廣泛應用于去除污染物的研究。ZHAO等[34]將Fe3O4納米顆粒與Al(OH)3結合,在pH為6.5時吸附量為88.48 mg/g,表現出較好的除氟能力。該材料可通過施加外部磁場快速從溶液中分離。GOSWAMI等[35]對合成的磁性施威特曼石的研究表明,該吸附劑對F-的吸附量為17.24 mg/g,且具有良好的再生性能。
近年來,研究者們還通過回收含鐵廢料中的鐵氧化物,將其資源化用于水中氟的去除。HUANG等[36]將芬頓反應副產物中的鐵氧化物廢料煅燒后用于水中氟的去除,300 ℃左右煅燒脫羥基形成的材料比表面積達124.7 m2/g,對氟化物的吸附量達27 mg/g。PEPPER等[37]利用鋁土礦殘渣(赤泥)合成的氧化鐵基吸附劑(β-FeOOH)對F-的最大吸附量為11.4 mg/g。
鐵基吸附劑對氟的吸附量較高,而且由于其某些形態具有磁性使得吸附材料易于從水中磁性分離,故常將其用于與其他吸附材料復合以進一步提高吸附性能并回收吸附材料,減少二次污染。
3 稀土類吸附劑
稀土金屬氧化物的水合物能有效去除水中F-[38-39]。NA等[39]對氫氧化鑭的除氟性能進行了研究:在pH為7.5時達到最大吸附量,為242.2 mg/g;當pH>10時吸附量為24.8 mg/g,其反應機理為:
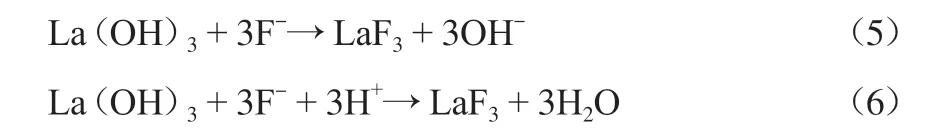
由于鑭成本較高,研究者們通常采用載體負載鑭以提高鑭的利用率來降低使用成本[40-42]。KAMBLE等[40]研究發現,載鑭殼聚糖吸附劑除氟性能優異,共存離子和Cl-等離子的存在對F-去除效果影響較小,而和的影響較大。這是因為和的存在使溶液pH升高,且和與吸附材料的親和力比F-更強[41]。FANG等[43]使用載鑭樹脂在pH為4.5~8.0范圍內去除氟化物,發現中性pH條件下強酸性吸附劑比弱酸性吸附劑的除氟效率更高,其大小順序為:Amberlite 200CTNa 樹脂>磷酸化交聯橙渣凝膠>Amberlite IR124 樹脂>皂化橙渣凝膠≥交聯果膠凝膠≥Diaion WK11 樹脂。對鑭改性活性炭除氟性能的研究顯示,在初始氟化物質量濃度為20 mg/L時,鑭改性活性炭的吸附量為9.96 mg/g,氟化物濃度會顯著影響改性活性炭的氟化物吸附能力[44]。
除鑭之外的稀土金屬氧化物同樣表現出較好的除氟效果。RAICHUR等[38]研究了多種稀土金屬氧化物的混合物對F-的吸附性能,稀土氧化物混合物對F-的最大吸附量為196.08 mg/g,其動力學過程非常迅速,在pH 6.5、吸附劑加入量4 g/L、F-質量濃度50~150 mg/L的條件下,5~10 min內可去除90%的氟化物,20 min左右可達到吸附平衡。盡管稀土元素除氟性能較好,但因其成本較高,研究者們常將稀土元素負載到各種載體上以提高其利用率。PAUDYAL等[45]將4種稀土金屬離子Sm(Ⅲ)、La(Ⅲ)、Ho(Ⅲ)和Sc(Ⅲ)負載到橘子廢渣上,在pH 4時,質量濃度為6 g/L的載La(Ⅲ)材料和質量濃度為15 g/L的載Sm(Ⅲ)材料可將氟化物質量濃度從15.24 mg/L降至0.8 mg/L。LIANG等[46]比較了載鑭及載混合稀土元素的磁性殼聚糖對氟化物的吸附性能,發現兩種材料都是較為理想的氟化物吸附材料且吸附性能相差不大,但是載混合稀土元素的磁性殼聚糖較為經濟實用。
稀土金屬氧化物及其氫氧化物除氟效果好但成本較高,將其負載于其他吸附劑上既可以降低成本,又可以使吸附量維持在較高水平,并且對F-有較高的選擇性,是目前研究較多、發展前景較好的吸附材料。
4 層狀雙金屬氫氧化物
層狀雙金屬氫氧化物是水滑石和類水滑石化合物的總稱,這類化合物經過煅燒轉化為金屬氧化物后,將其加入到含有陰離子的溶液中,又能部分恢復至原有的層狀結構,這種現象被稱為層狀雙金屬氫氧化物的“記憶效應”[47]。
層狀雙金屬氫氧化物的吸附性能與其結構中的金屬種類以及比例有關。Lü等[48]研究了煅燒過的Mg-Al-CO3層狀雙金屬氫氧化物去除F-的效果及其影響因素,結果顯示,500 ℃下煅燒的材料吸附性能最好,反應經過6 h達到平衡。共存離子會降低除氟效果,其影響大小順序為:。研究發現,煅燒過的Mg-Al層狀雙金屬氫氧化物的吸附量大于煅燒過的Zn-Al和Ni-Al層狀雙金屬氫氧化物,且Mg與Al摩爾比為2時效果最好,最大吸附量為213.22 mg/g,其反應機理為:
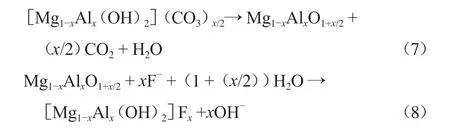
Lü等[49]進一步研究了未煅燒過的Mg-Al-CO3層狀雙金屬氫氧化物對高濃度F-的去除效果,結果顯示,最大吸附量可達319.8 mg/g,在pH為6.0~10.0的范圍內,吸附量隨著溶液pH的升高而減小,共存離子對除氟效果具有抑制作用,其影響大小順序為:。層間陰離子為和Cl-的Mg-Al層狀雙金屬氫氧化物均表現出良好的再生性能[50]。此外,Zn-Al[51]、Li-Al[52]、Co-Al[53]、Li-Al-La[54]等層狀雙金屬氫氧化物的除氟效果亦得到關注。
層狀雙金屬氫氧化物因其獨特的結構特性表現出良好的除氟性能,然而目前研制的層狀雙金屬氫氧化物多為納米級粉體,在現場應用方面受到一定的限制。
5 其他金屬吸附劑
鈣[55]、鎂[56]、鈦[57]、鋯[58-59]等金屬對F-均具有較好的親和力,因此,也常被用于水中F-的去除。
對鈣基吸附劑的研究早期集中在含鈣礦石[60]及其改性材料的除氟性能上。研究表明,生石灰的除氟機理為Ca(OH)2+ 2F-→ CaF2(s) + 2OH-。近年來,鈣基吸附劑的除氟研究主要集中于含鈣生物質[61-62]及含鈣納米吸附劑[55]的制備等方面。CHAUDHARY等[55]利用超聲輔助化學法合成了氫氧化鈣納米棒,該材料在pH為6.5時對F-的吸附量為(450±10)mg/g,加入量為2 g/L的氫氧化鈣納米棒材料對F-初始質量濃度為73 mg/L電鍍工業廢水的F-去除率為91.7%。
針對氧化鎂除氟性能的研究主要集中于提升氧化鎂吸附材料的比表面積,如制備介孔氧化鎂[56]和納米氧化鎂[63]等。NAGAPPA等[56]以硝酸鎂為氧化劑,甘氨酸為燃料,通過燃燒法制備了介孔氧化鎂納米晶,可去除氟化鈉標準溶液中97%的氟化物及管井水中75%的氟化物,而新制備、除氟再生后以及商品級氧化鎂粉末的氟化物去除率分別為97%、76%和17%。
二氧化鈦具有無毒、穩定和高光催化活性等特征,是常用于處理環境污染物的高效材料。BABAEIVELNI等[57]研究了二氧化鈦對F-的吸附性能,結果表明,反應3 h達到吸附平衡,溶液pH是影響除氟效果的主要因素,F-去除率隨溶液pH升高而下降,pH為2~5范圍內吸附量較大。其反應機理為pH<7時,pH>7時,≡Ti(OH)4(n-1)H2OOH-Na+F-+ H+。
鋯基材料也可用于F-的吸附去除,因為水合形式的四價鋯可以生成帶有豐富OH-和H2O的四核及八核物質,OH-和H2O能參與氟的取代[64]。其可能的除氟反應機理為pH<7.5時,≡Zr(OH)2+ F-(OH)F+OH-;pH>7.5時,≡Zr(OH)2·nH2O+·(n-1)H2OOH-Na+F-+H+[59]。DOU等[58]研究了水合氧化鋯在pH4和7時的氟化物吸附量,分別為124 mg/g和68 mg/g,該吸附劑通過帶電表面與氟化物之間的靜電作用以及表面羥基與F-交換去除氟化物。
近年來,鈣、鎂、鈦、鋯等其他金屬氧化物及氫氧化物吸附材料的改性也主要向增大比表面積、增加表面活性基團等方向發展。此外,亦有部分研究關注于將多種金屬氧化物復合或與其他具有除氟能力的吸附劑復合以提高吸附量,Fe-La-Ce[65]、Y-Zr-Al[66]等三金屬復合吸附劑也展示出良好的吸附性能。
6 結語
金屬氧化物及氫氧化物對氟離子具有較強的親和能力,是具有潛力的除氟材料之一,進一步的研究方向包括:
a)充分利用單一組分金屬氧化物及氫氧化物的優勢,開展對高效、高選擇性、易再生復合材料的研究,可進一步提高材料對水中氟離子的去除性能,及其對復雜水質條件的適應能力。
b)目前對金屬氧化物及氫氧化物的研究大多停留在實驗研究階段,需加強材料對實際廢水除氟效果的評價。
c)目前的研究多集中在材料吸附性能的評價,需加強對材料再生技術的研究,以節約資源,降低處理成本。

