高效液相色譜法測定伊格列凈片劑的含量
黃佳雯,梁佳威,顏亮,鄭楓
(1.中國藥科大學,江蘇南京 211198;2,南京卡文迪許生物工程技術有限公司,江蘇南京 210033)
伊格列凈(Ipraliflozin)是C-芳基葡糖苷類結構的高選擇性人體鈉-葡萄糖協同轉運蛋白2(SGLT2)口服活性抑制劑,通過選擇性的抑制腎臟近曲小管上皮細胞膜管腔側的鈉-葡萄糖協同轉運蛋白2(SGLT2),減少葡萄糖重吸收并促進尿糖排泄,進而降低血糖,同時可減重和降壓[1]。該藥已于2019 年在美國上市,但未在國內上市,目前未見各國藥典對本品的收載及進口注冊標準[2]。本研究旨在為仿制藥伊格列凈的含量測定提供科學性的方法依據及分析技術,保障藥品的安全性。
1 實驗部分
1.1 儀器和試劑
高效液相色譜儀:Agilent 1200,Agilent 色譜工作站。
伊格列凈L-脯氨酸(自制對照品,99.7%)、雜質IMP01(自制對照品,99.5%)、雜質IMP02(自制對照品,99.9%)、雜質IMP03(自制對照品,99.0%)、雜質IMP04(自制對照品,99.5%)、雜質IMP05(自制對照品,99.5%)、雜質IMP06(自制對照品,99.9%)、雜質IMP07(自制對照品,99.7%)、雜質IMP08(自制對照品,99.8%)、磷酸(分析純,上海阿拉丁生化科技股份有限公司)、甲醇(色譜純,默克)。
2 方法與結果
2.1 色譜條件
儀器:高效液相色譜儀;色譜柱:Waters Symmetry Shield RP18(3.5μm,3.0×50mm);流動相:0.05%磷酸-甲醇(65:35);檢測波長:230nm;流速:1.2mL/min;進樣體積:20μL。
系統適用性:取伊格列凈適量,用流動相溶解并定量稀釋制成每1mL 中約含伊格列凈(C21H21FO5S)50μg 的溶液,在擬定色譜條件下,精密量取20μL 注入液相色譜儀,記錄色譜圖色譜柱的理論塔板數大于2000,拖尾因子小于2.0。
具體試驗操作:取伊格列凈20 片,精密稱定,研細,精密稱取適量(約相當于伊格列凈25mg),置50mL 量瓶中,加流動相適量,超聲10min 使伊格列凈L-脯氨酸溶解,放冷,用流動相稀釋至刻度,搖勻,離心,取上清液濾過,精密量取續濾液5mL,置50mL 量瓶中,用流動相稀釋至刻度,搖勻,作為供試溶液,精密量取20μL注入液相色譜儀,記錄色譜圖;另取伊格列凈L-脯氨酸對照品,精密稱定,加流動相溶解并釋制成每1mL 中約含伊格列凈(C21H21FO5S)50μg的溶液,同法測定。按外標法以峰面積計算,并將結果乘以0.7784,即得。
試驗結果判定:含伊格列凈(C21H21FO5S)應為標示量的90.0%~110.0%。
2.2 輔料干擾試驗
考察在此色譜條件下空白輔料對檢測的影響。按處方量分別稱取空白輔料及伊格列凈L-脯氨酸適量,用流動相制成空白輔料溶液、原料溶液及原輔料混合溶液,精密量取20μL,注入液相色譜儀,記錄色譜圖。測定結果見表1。結果表明,空白輔料不干擾檢測。
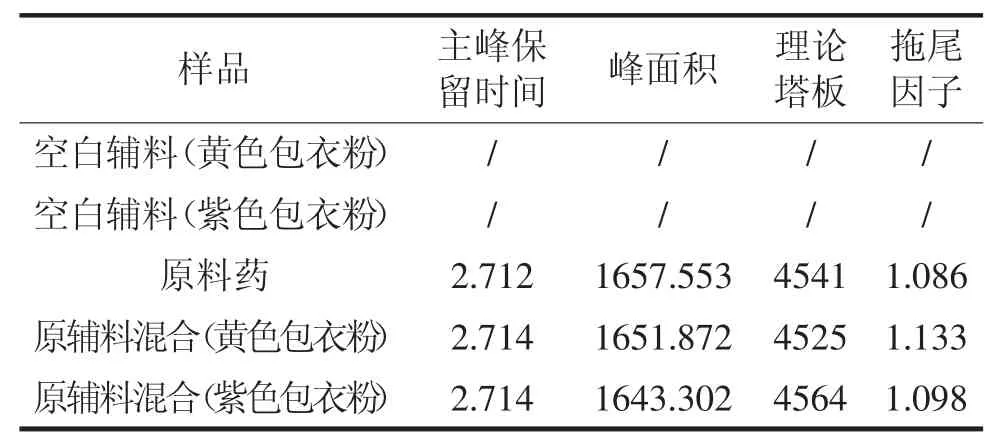
表1 輔料干擾試驗結果
2.3 專屬性試驗
取伊格列凈L-脯氨酸樣品及伊格列凈中可能存在的雜質IMP01、IMP02、IMP03、IMP04、IMP05、IMP06、IMP07、IMP08 適量,用甲醇溶解并用流動相定量稀釋制成每1mL 中約50μg 的溶液分別量取20μL,注入色譜儀,記錄色譜圖;并將伊格列凈L-脯氨酸溶液與各雜質溶液混合進樣,記錄色譜圖。結果見表2 和圖1。
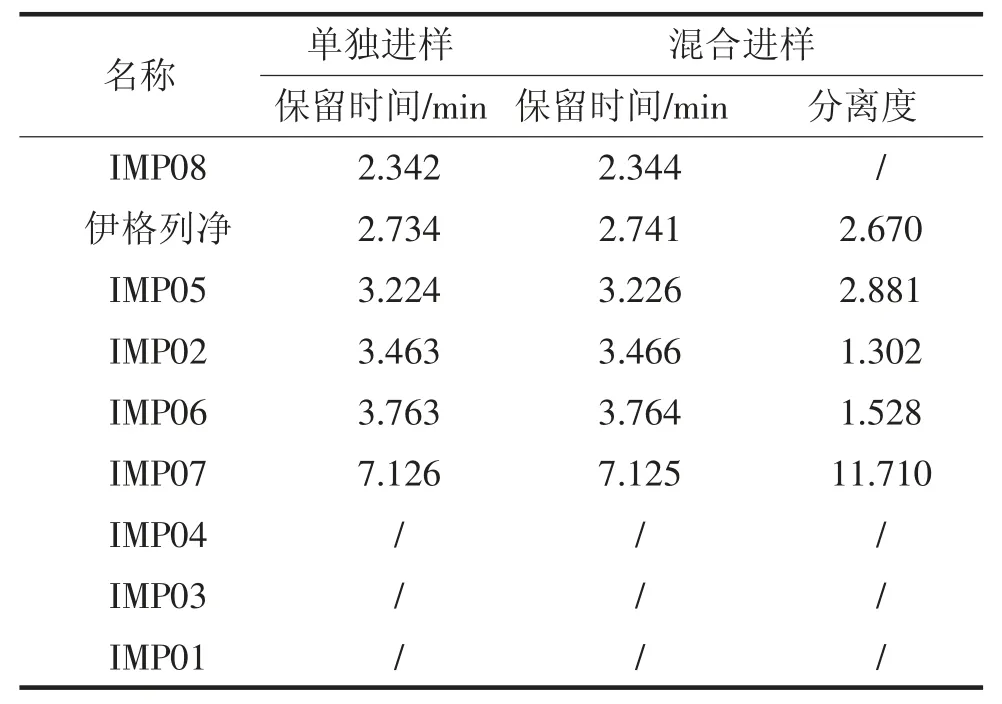
表2 專屬性試驗結果
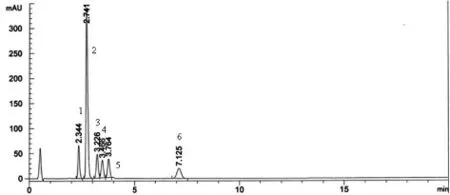
圖1 伊格列凈L-脯氨酸專屬性結果
結果表明:在擬定色譜條件下,伊格列凈L-脯氨酸主峰與雜質分離良好。雜質IMP01、IMP03、IMP04 極性與伊格列凈L-脯氨酸差異較大,在該條件不能洗脫出來,并不干擾伊格列凈L-脯氨酸測定。
2.4 進樣精密度試驗
取伊格列凈L-脯氨酸對照品溶液,按照擬定色譜條件,連續進樣6 次,記錄色譜圖。計算結果得到連續6 次進樣伊格列凈L-脯氨酸峰面積的RSD 為0.2%,表明進樣精密度良好。
2.5 溶液穩定性試驗
取伊格列凈L-脯氨酸對照品溶液,按照擬定色譜條件,在0h、1h、2h、4h、6h、8h、12h、24h進樣,記錄色譜圖。計算結果得到0~24h 內伊格列凈L-脯氨酸峰面積的RSD 為0.1%,表明伊格列凈L-脯氨酸對照品溶液在24h 內穩定性良好。
取伊格列凈L-脯氨酸片劑樣品適量,用流動相溶解并定量稀釋制成每1mL 約含伊格列凈 (C21H21FO5S)50μg 的溶液。按照擬定色譜條件,在0h、1h、2h、4h、6h、8h、12h、24h 進樣。計算結果得到0~24h 內伊格列凈L-脯氨酸峰面積的RSD 為0.2%,表明伊格列凈L-脯氨酸片劑樣品溶液在24h 內穩定性良好。
2.6 線性試驗
取伊格列凈L-脯氨酸對照品適量,用流動相溶解并定量稀釋制成每1mL 約含伊格列凈(C21H21FO5S)10~100μg 的系列標準溶液。按照色譜條件,分別精密量取20μL,注入液相色譜儀,記錄色譜圖,以濃度C(μg/mL)為橫坐標,峰面積A 為縱坐標,進行線性回歸,并計算回歸方程和相關系數。結果見表3 和圖2。結果表明伊格列凈在10.06~100.56μg/mL 范圍峰面積與濃度呈良好的線性關系。
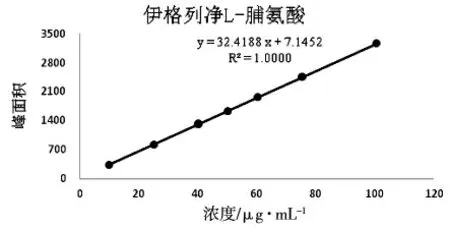
圖2 伊格列凈L-脯氨酸標準曲線
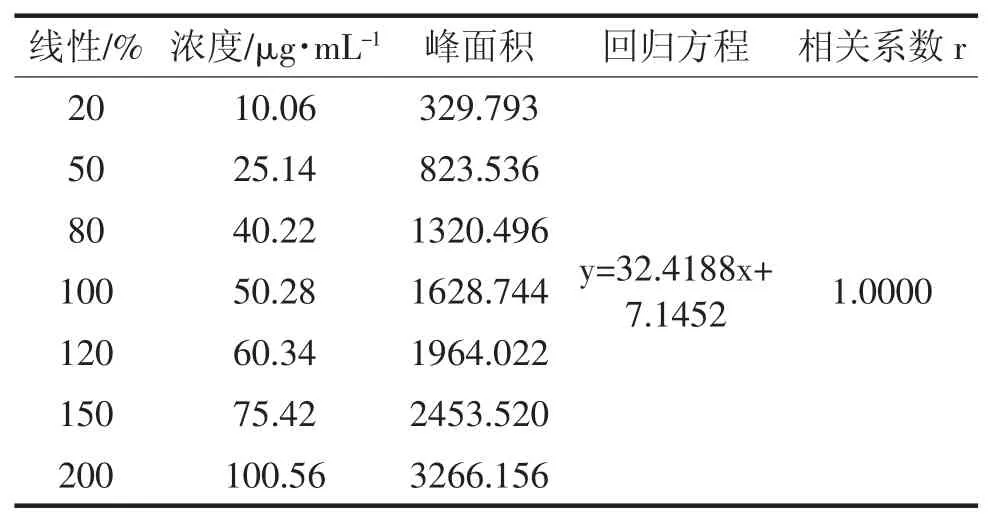
表3 線性試驗結果
2.7 準確度試驗
精密稱取伊格列凈L-脯氨酸對照品適量,約含伊格列凈(C21H21FO5S) 分別為40mg,50mg,60mg 置100mL 量瓶中,再分別加入空白輔料307mg,加流動相適量,超聲10 min 使伊格列凈溶解并稀釋至刻度,搖勻,濾過,精密移取續濾液5mL 置50mL 容量瓶中,用流動相稀釋至刻度,搖勻,作為供試溶液(每個質量分數配置3 份樣品)。另取伊格列凈L-脯氨酸對照品適量,定量制成每1mL 中約含伊格列凈 (C21H21FO5S)50μg的溶液作為對照溶液。照含量測定項下的方法操作,記錄色譜圖,計算測得量,根據測得量和加入量計算回收率。結果表明伊格列凈L-脯氨酸的總平均回收率為99.9%,RSD 為0.3%。數據見表4。
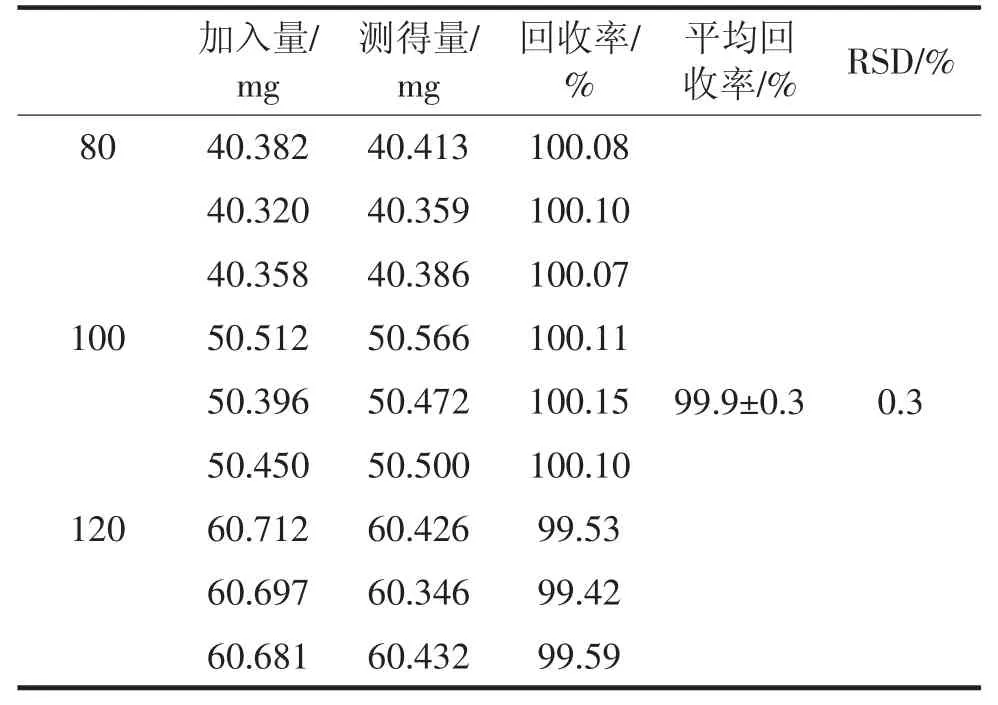
表4 準確度試驗結果(n=9)
2.8 耐用性試驗
取伊格列凈L-脯氨酸工作對照品適量,用流動相溶解并定量稀釋制成每1mL 約含伊格列凈 (C21H21FO5S)50μg 的溶液,作為對照品溶液;另取伊格列凈L-脯氨酸樣品適量,用流動相溶解并定量稀釋制成每1mL 約含伊格列凈(C21H21FO5S)50μg 的溶液,作為供試品溶液。在擬定色譜條件基礎上,分別考察柱溫±5°C,流動相比例±5%,流速±0.2mL/min,選用不同色譜柱對檢測的影響。結果表明,各條件下伊格列凈的精密度均符合要求,RSD ≤5%。
2.9 樣品測定
取三批伊格列凈片,按照“2.1”項下配制供試品溶液,按照擬定色譜條件進樣分析,記錄色譜圖,測定伊格列凈量。結果表明:三批供試品伊格列凈含量均為標示量的90.0%~110.0%。
3 討論
3.1 色譜柱的選擇
根據伊格列凈L-脯氨酸的理化性質,經優化后篩選出專屬性佳,精密度及準確度均符合規定且簡便快捷的等度條件,作為含量檢測方法。
有機相的比例對分離度影響較大,為了保證檢測條件的適用性,且為了保證藥品的質量及使用安全,最終采用流動相為0.05%磷酸-甲醇(65∶35) 方法本品進行含量的檢查。對比了Waters Symmetry Shield RP18 柱與Waters Symmetry C18 柱兩根50mm 短柱,兩種色譜柱均適合,主峰拖尾因子都在1.2 左右,就理論板數比較,Waters Symmetry Shield RP18 柱略優。選擇以十八烷基硅烷鍵合硅膠為填充劑的色譜柱,以0.05%磷酸-甲醇(65∶35)為流動相,能有效的檢測本品含量。
3.2 超聲時間的選擇
取伊格列凈片,精密稱定,研細,精密稱取適量(約相當于伊格列凈25mg),置50mL 量瓶中,加流動相適量,分別超聲1min、2min、5min、10min、15min 后,放冷,用流動相稀釋至刻度,搖勻,離心,取上清液濾過,精密量取續濾液5mL置50mL 量瓶中,用流動相稀釋至刻度,搖勻,作為供試溶液。精密量取20μL 注入液相色譜儀,記錄色譜圖;另取伊格列凈L-脯氨酸對照品,精密稱定,用流動相溶解并定量稀釋制成每1mL 中約含伊格列凈(C21H21FO5S)50μg 的溶液,同法測定。按外標法以峰面積計算,即得。結果見表5。

表5 超聲時間對含量測定的影響
結論:超聲2~5min 樣品即可提取完全。為了確保每次提取完全,因此,我們選擇超聲10min 做為溶劑提取時間。
3.3 濾膜的選擇
樣品溶液:取伊格列凈片,精密稱定,研細,精密稱取適量(約相當于伊格列凈25mg),置50mL 量瓶中,加流動相適量,超聲10min 后,冷卻至室溫,用流動相定容至刻度搖勻。
離心:取上述樣品溶液離心后取上層溶液。
取上述樣品溶液分別用美國PALL 的有機濾膜過濾,棄去初濾液1mL、3mL、5mL,取續濾液,作為樣品PALL-棄1mL、PALL-棄3mL、PALL-棄5mL。
取上述樣品溶液分別用江蘇酷拓的有機濾膜過濾,棄去初濾液1mL、3mL、5mL,取續濾液,作為樣品酷拓-棄1mL、酷拓-棄3mL、酷拓-棄5mL。
取上述樣品溶液分別用TITAN 的有機濾膜過濾,棄去初濾液1mL、3mL、5mL,取續濾液,作為樣品TITAN-棄1mL、TITAN-棄3mL、TITAN-棄5mL。
精密量取空白溶液、系統適用性溶液、離心樣品溶液及各個過濾樣品溶液各20 μL,分別注入液相色譜儀,記錄色譜圖;考察濾膜對伊格列凈的吸附情況。結果見表6。
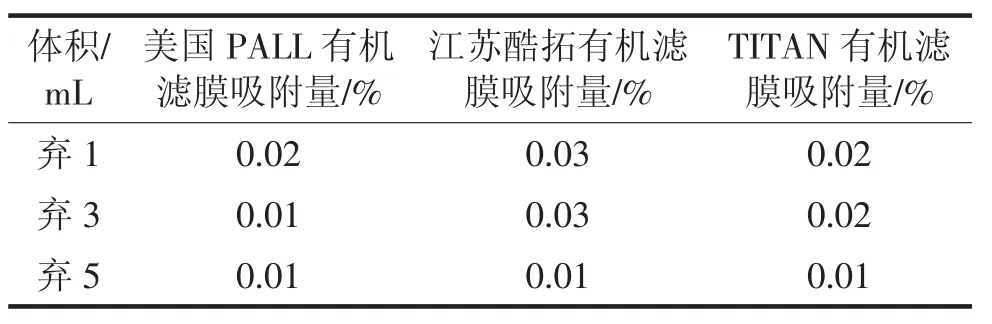
表6 濾膜吸附試驗結果
結論:由表6 可知美國PALL 有機濾膜、江蘇酷拓有機濾膜、TITAN 有機濾膜對伊格列凈的吸附量均在2%以內,因此認定以上三種濾膜對伊格列凈無吸附。

