補陽還五湯對局灶性腦缺血大鼠血液流變學及NLRP3/Caspase-1炎性反應的影響*
邵 樂 佘 顏 鄧國倩 胡哲銓 易 健 劉 林 郭 純 郭志華△ 吳其標
(1.湖南中醫(yī)藥大學第一附屬醫(yī)院,湖南 長沙 410007;2.湖南中醫(yī)藥大學,湖南 長沙410208;3.澳門科技大學,澳門 999078)
缺血性腦卒中是嚴重危害人類生命健康的重大心腦血管疾病之一,數(shù)據(jù)表明,全世界每年新增腦卒中患者約1 690萬人[1]。我國缺血性腦卒中患病率為1 762.77/1萬[2]。體內(nèi)存在促炎-抗炎平衡系統(tǒng),腦缺血后的炎癥失衡是導致神經(jīng)細胞損傷的重要原因[3],抑制腦缺血后炎癥反應是治療腦卒中的主要干預靶點[4]。缺血性腦卒中具有“虛、瘀”的中醫(yī)病機特點,補陽還五湯為治療氣虛血瘀型腦缺血的經(jīng)典名方。前期研究發(fā)現(xiàn),局灶性腦缺血模型大鼠中白細胞介素-1β(IL-1β)、MCP-1、MIP-1α等炎癥相關指標升高,存在明顯的炎癥穩(wěn)態(tài)失衡,本研究通過觀察補陽還五湯對MCAO大鼠大鼠血液流變學及NLRP3、Caspase-1的影響,進一步揭示其抗腦缺血炎癥反應機制。
1 材料與方法
1.1 實驗動物 SPF級雄性SD大鼠100只,體質量(200±20)g,湖南斯萊克景達實驗動物技術有限公司提供,合格證號:SCXK(湘)2012-0002。動物實驗經(jīng)湖南中醫(yī)藥大學第一附屬醫(yī)院實驗動物倫理委員會批準。
1.2 藥物與試劑 補陽還五湯組方:生黃芪120 g,當歸尾6 g,赤芍4.5 g,地龍3 g,川芎3 g,桃仁3 g,紅花3 g;由湖南中醫(yī)藥第一附屬醫(yī)院中藥房提供,按《中國藥典》相關要求制備煎煮液(2 g/mL),冷藏備用。所有藥材均符合藥典標準。鹽酸米諾環(huán)素膠囊(瀚暉制藥有限公司,批號:20091011)。NLRP3、Caspase-1、兔IgG即用型SABC免疫組化試劑盒、IL-1β、IL-18 ELISA測定試劑盒(武漢博士德生物工程有限公司)。
1.3 實驗儀器 全自動型血流變分析儀(北京賽科希德科技發(fā)展有限公司,SA-6000),多功能酶標儀(美國Perkinelmer公司,Enspire),石蠟切片機(英國Shando公司,F(xiàn)inesse 325型),Bx51光學顯微鏡及IPP6.0圖像分析系統(tǒng)(日本Olympus公司)。
1.4 模型制備 參照Longa與Knaga報道的方法[5-6],采用大腦中動脈線栓法(MCAO)建立永久局灶性腦缺血大鼠模型。假手術組僅切開皮膚、分離頸總動脈后縫合。大鼠清醒后2 h參照文獻[7]進行5級神經(jīng)功能評分,分值在1~3分者入組。
1.5 分組及給藥 大鼠隨機分為假手術組、模型組、補陽還五湯組、米諾環(huán)素組,并分為1、3、7、14、28 d,共5個觀察時間點,每組每個時間點各5只。各組造模后1 d后開始給藥,根據(jù)動物-人體表面積換算法,補陽還五湯組及米諾環(huán)素組給藥劑量為分別為3.15 g/kg、17.81 mg/kg,假手術組和模型組給予等體積生理鹽水灌胃,每日1次,每組給藥體積均為10 mL/kg。
1.6 標本采集與檢測 1)血液流變學指標:大鼠以10%水合氯醛(3.0 mL/kg)麻醉后,用1%肝素真空抗凝采血管經(jīng)腹主動脈取血4 mL,并將已取好的大鼠血液放入SA-6000全自動型血流變分析儀,檢測全血黏度、紅細胞聚集指數(shù)。2)腦組織NLRP3、Caspase-1表達:大鼠以10%水合氯醛(3.0 mL/kg)麻醉后,動物斷頭處死后,取各組大鼠腦組織,采用4%多聚甲醛固定,并經(jīng)脫水、包埋、切片、封片等處理后,采用免疫組化法檢測NLRP3、Caspase-1的陽性表達,按試劑盒具體步驟進行操作。每張組織切片隨機觀察5個高倍鏡視野(400倍),計算平均光密度值。3)血清IL-1β、IL-18含量檢測:大鼠以10%水合氯醛(3.0 mL/kg)麻醉后,經(jīng)腹主動脈取血4 mL,3 000 r/min離心15 min,取血清置-80℃冰箱中保存待測。采用ELISA法測定血清IL-1β、IL-18含量,嚴格按試劑盒說明書操作。
1.7 統(tǒng)計學處理 應用SPSS21.0統(tǒng)計軟件。計量資料以(±s)表示。組間比較若滿足正態(tài)性檢驗、方差齊性,則使用方差分析,若不符合正態(tài)分布、方差齊性,采用非參數(shù)檢驗進行統(tǒng)計處理;組與組之間兩兩比較可采用LSD法。P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 各組大鼠全血黏度及紅細胞聚集指數(shù)比較 見表1。與假手術組比較,模型組各時間點及補陽還五湯1 d組、米諾環(huán)素1 d組大鼠血液黏度顯著上升,差異具有統(tǒng)計學意義(P<0.05)。用藥3 d后MCAO大鼠血液黏度值開始下降,用藥7 d后各組與模型組比較,差異具有統(tǒng)計學意義(P<0.05)。與米諾環(huán)素組比較,補陽還五湯組各時間點比較無差異(P>0.05)。補陽還五湯各時間點組內(nèi)比較,用藥7 d后大鼠全血黏度值下降明顯,補陽還五湯組7、14、28 d時與1 d時比較差異具有統(tǒng)計學意義(P<0.05)。
表1 各組大鼠血液黏度及紅細胞聚集指數(shù)比較(±s)

表1 各組大鼠血液黏度及紅細胞聚集指數(shù)比較(±s)
注:與假手術組同時間比較,*P<0.05,**P<0.01;與模型組同時間比較,▲P<0.05,▲▲P<0.01;與本組1 d時比較,★P<0.05,★★P<0.01;與本組3 d時比較,#P<0.05,##P<0.01。下同。
images/BZ_33_1248_2010_2252_2143.png6.08±2.02 8.40±1.37*8.27±1.10*8.50±0.29*8.37±1.55*8.59±1.16*8.58±0.71*7.72±0.55 7.35±0.84▲★6.96±0.70▲★6.50±1.01▲★★8.49±2.41*7.46±1.33 7.09±0.75▲6.54±0.88▲5.93±1.31▲-米諾環(huán)素組(n=5)假手術組模型組(n=5)1 d 3 d 7 d 14 d 28 d 1 d 3 d 7 d 14 d 28 d 1 d 3 d 7 d 14 d 28 d補陽還五湯組(n=5)5.23±0.49 6.32±0.82*6.06±0.65*6.19±0.63*6.48±0.91*6.37±0.84*6.43±0.57*5.95±0.40 5.76±0.29▲★5.62±0.55▲★5.43±0.55▲★5.90±0.83*5.80±0.55 5.37±0.36▲5.29±0.65▲5.19±0.69▲5.86±0.51 7.33±1.18*7.83±0.92*7.43±0.75*7.88±1.28*7.56±1.34*7.35±0.66*6.87±0.51 6.92±0.52▲6.31±0.78▲★6.06±0.82▲★6.77±0.70*6.54±0.52 6.16±0.50▲6.06±0.40▲5.57±0.85▲14.35±2.28 18.88±3.49*18.58±2.75*18.12±2.70*18.67±3.49*18.63±3.69*18.71±1.92*17.09±2.33 16.71±1.51▲★16.01±1.75▲★15.34±1.73▲★16.74±2.80*16.29±2.35 15.85±1.75▲14.09±1.19▲13.38±1.67▲38.06±3.42 44.31±5.18*45.42±4.66*46.78±6.21*47.78±5.87*46.41±7.73*47.89±3.73*43.26±4.45 42.78±4.61▲★41.24±5.87▲★40.82±5.68▲★45.12±3.82*41.94±3.49 40.51±4.65▲38.09±3.35▲37.50±3.52▲5.82±0.57 7.11±0.72*6.98±0.69*6.89±0.14*7.32±1.16*7.23±0.59*7.24±0.41*6.68±0.56 6.45±0.64▲★6.34±0.71▲★6.10±0.52▲★7.77±1.15*7.05±0.81 6.15±0.51▲6.05±0.66▲5.67±0.85▲
2.2 各組大鼠腦組織CA1區(qū)NLRP3表達的比較 見表2,圖1。假手術組大鼠腦組織海馬CA1區(qū)有少量NLRP3表達,模型組與用藥組腦缺血損傷后NLRP3表達增加,并在1 d達到高峰,3、7、14、28 d呈下降趨勢,但仍明顯高于假手術組(P<0.05)。用藥后,與模型組比較,補陽還五湯組及米諾環(huán)素組各時間點的NLRP3表達均有所下降,差異有統(tǒng)計學意義(P<0.05)。與米諾環(huán)素組比較,補陽還五湯組各時間點比較無明顯差異(P>0.05)。補陽還五湯各時間點組內(nèi)比較,用藥7 d后大鼠NLRP3表達下降明顯,補陽還五湯組7、14、28 d與1 d時比較差異具有統(tǒng)計學意義(P<0.05)。
表2 各組大鼠腦組織海馬CA1區(qū)NLRP3表達的比較(平均光密度值,×10-3,±s)
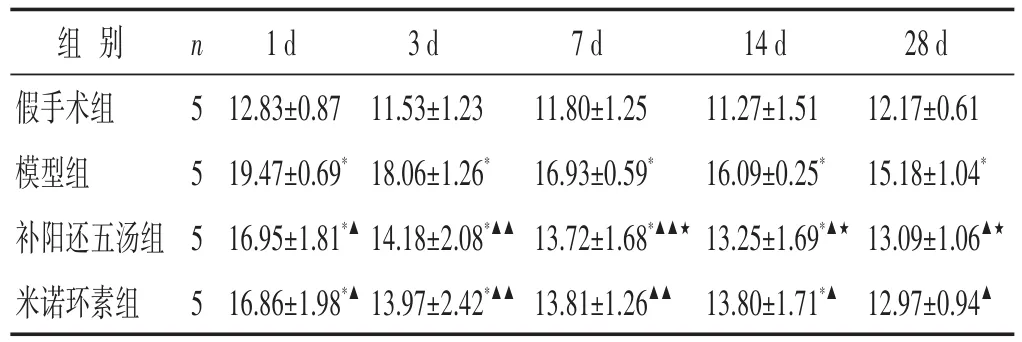
表2 各組大鼠腦組織海馬CA1區(qū)NLRP3表達的比較(平均光密度值,×10-3,±s)
組別假手術組模型組補陽還五湯組米諾環(huán)素組n 5 5 5 5 1 d 12.83±0.87 19.47±0.69*16.95±1.81*▲16.86±1.98*▲3 d 11.53±1.23 18.06±1.26*14.18±2.08*▲▲13.97±2.42*▲▲7 d 11.80±1.25 16.93±0.59*13.72±1.68*▲▲★13.81±1.26▲▲14 d 11.27±1.51 16.09±0.25*13.25±1.69*▲★13.80±1.71*▲28 d 12.17±0.61 15.18±1.04*13.09±1.06▲★12.97±0.94▲
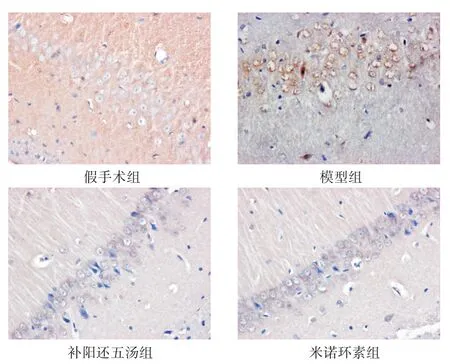
圖1 各組大鼠7 d時腦組織海馬CA1區(qū)NLRP3表達(DAB染色,400倍)
2.3 各組大鼠腦組織海馬CA1區(qū)Caspase-1表達的比較 見表3,圖2。假手術組大鼠腦組織有少量Cas?pase-1表達,模型組與用藥組腦缺血損傷后大鼠腦組織Caspase-1表達增加,并在3 d達到高峰,7、14、28 d呈下降趨勢,但仍顯著高于假手術組(P<0.01)。從用藥7 d后始,米諾環(huán)素組Caspase-1表達有所下降,與模型組比較差異均具有統(tǒng)計學意義(P<0.05或P<0.01)。與米諾環(huán)素組比較,補陽還五湯組各時間點比較差異無統(tǒng)計學意義(P>0.05)。補陽還五湯組內(nèi)各時間點比較,用藥7 d后Caspase-1表達下降明顯,補陽還五湯組28 d時與1、3 d時比較差異具有統(tǒng)計學意義(P<0.05)。
表3 各組大鼠腦組織海馬CA1區(qū)Caspase-1表達的比較(平均光密度值,×10-3,±s)
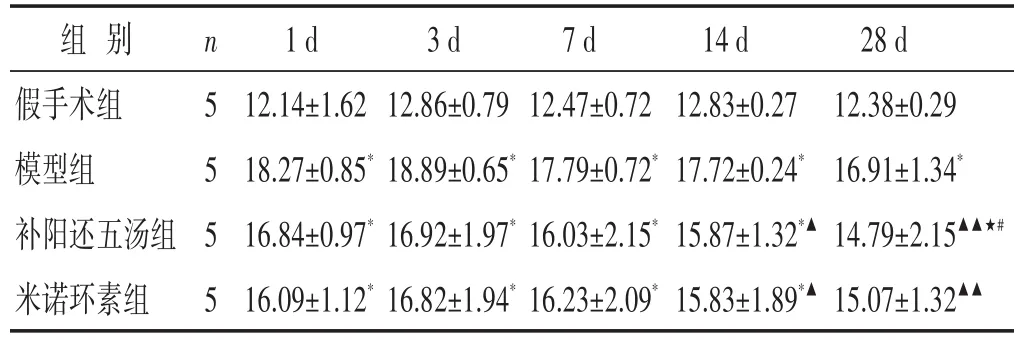
表3 各組大鼠腦組織海馬CA1區(qū)Caspase-1表達的比較(平均光密度值,×10-3,±s)
組別假手術組模型組補陽還五湯組米諾環(huán)素組n 5 5 5 5 1 d 12.14±1.62 18.27±0.85*16.84±0.97*16.09±1.12*3 d 12.86±0.79 18.89±0.65*16.92±1.97*16.82±1.94*7 d 12.47±0.72 17.79±0.72*16.03±2.15*16.23±2.09*14 d 12.83±0.27 17.72±0.24*15.87±1.32*▲15.83±1.89*▲28 d 12.38±0.29 16.91±1.34*14.79±2.15▲▲★#15.07±1.32▲▲

圖2 各組大鼠7 d時腦組織海馬CA1區(qū)Caspase-1表達(DAB染色,400倍)
2.4 各組大鼠血清IL-1β含量的比較 見表4。腦缺血損傷后,血清IL-1β含量上升明顯,并在3 d達到高峰,7、14、28 d呈下降趨勢,與假手術組比較,各組各時間點差異有統(tǒng)計學意義(P<0.05或P<0.01)。與模型組比較,用藥7 d后起,補陽還五湯組及米諾環(huán)素組血清IL-1β含量明顯下降,差異具有統(tǒng)計學意義(P<0.05或P<0.01)。與米諾環(huán)素組比較,補陽還五湯組各時間點比較無明顯差異(P>0.05)。補陽還五湯組內(nèi)各時間點比較,用藥7 d后IL-1β表達下降明顯,補陽還五湯組28 d時與3 d時比較差異具有統(tǒng)計學意義(P<0.05)。
表4 各組大鼠血清IL-1β含量的比較(pg/mL,±s)
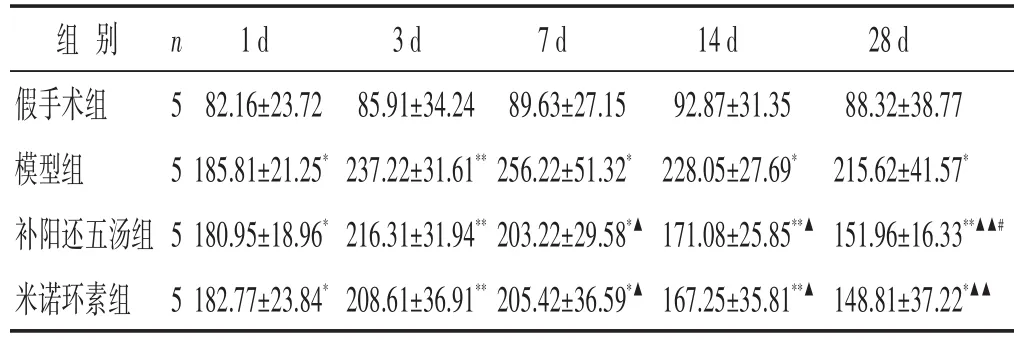
表4 各組大鼠血清IL-1β含量的比較(pg/mL,±s)
組別假手術組模型組補陽還五湯組米諾環(huán)素組n 5 5 5 5 1 d 82.16±23.72 185.81±21.25*180.95±18.96*182.77±23.84*3 d 85.91±34.24 237.22±31.61**216.31±31.94**208.61±36.91**7 d 89.63±27.15 256.22±51.32*203.22±29.58*▲205.42±36.59*▲14 d 92.87±31.35 228.05±27.69*171.08±25.85**▲167.25±35.81**▲28 d 88.32±38.77 215.62±41.57*151.96±16.33**▲▲#148.81±37.22*▲▲
2.5 各組大鼠血清IL-18含量的比較 見表5。腦缺血損傷后,血清IL-18明顯上升,術后1 d即達到高峰,隨后呈下降趨勢,與假手術組比較,模型組各時間點及用藥組1、3、7 d差異具有統(tǒng)計學意義(P<0.05或P<0.01)。與模型組比較,用藥1d后起,補陽還五湯組及米諾環(huán)素組血清IL-18含量明顯下降,差異具有統(tǒng)計學意義(P<0.05或P<0.01)。與米諾環(huán)素組比較,補陽還五湯組各時間點比較無明顯差異(P>0.05)。補陽還五湯各時間點組內(nèi)比較,用藥7 d后大鼠IL-18表達下降明顯,補陽還五湯組14、28 d時與1 d時比較差異具有統(tǒng)計學意義(P<0.05)。
表5 各組大鼠血清IL-18含量的比較(pg/mL,±s)
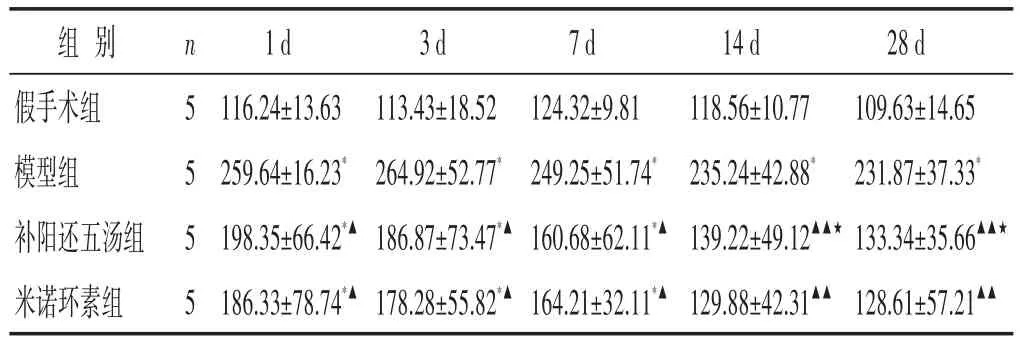
表5 各組大鼠血清IL-18含量的比較(pg/mL,±s)
images/BZ_35_165_1164_1169_1231.png假手術組模型組補陽還五湯組米諾環(huán)素組5 5 5 5 116.24±13.63 259.64±16.23*198.35±66.42*▲186.33±78.74*▲113.43±18.52 264.92±52.77*186.87±73.47*▲178.28±55.82*▲124.32±9.81 249.25±51.74*160.68±62.11*▲164.21±32.11*▲118.56±10.77 235.24±42.88*139.22±49.12▲▲★129.88±42.31▲▲109.63±14.65 231.87±37.33*133.34±35.66▲▲★128.61±57.21▲▲
3 討 論
缺血性腦卒中屬中醫(yī)學“中風”范疇,其病位在腦,為本虛標實之證,本虛為正氣虛損,標實為瘀阻腦絡,具有“虛、瘀”的基本病機狀態(tài),氣虛血瘀是其發(fā)病的關鍵。人到中年,臟腑功能減退,五臟皆虛,此為正氣虛損。氣機升降失調(diào),“氣為血之帥”,氣虛推動無力,血行遲緩,阻滯于脈絡,則成血瘀,瘀停于腦,此為瘀阻腦絡。從現(xiàn)代醫(yī)學角度研究發(fā)現(xiàn),血瘀證主要表現(xiàn)為血液流變學異常、血流動力學改變[8]、血栓形成[9]及動脈管腔狹窄[10],而這正是缺血性腦卒中的基本病理基礎,隨著現(xiàn)代醫(yī)學的發(fā)展,研究發(fā)現(xiàn),炎癥和血瘀證在疾病過程及治療上密切相關,血瘀證在某些細胞因子、臨床治療及動物模型方面與炎癥存在著密不可分的聯(lián)系[11-12],因此我們認為,腦缺血再灌注的“虛、瘀”中醫(yī)病機狀態(tài)與神經(jīng)炎性損傷密切相關。
NLRP3炎癥小體屬于機體內(nèi)識別模式受體(PPRs)NLR樣受體,主要在免疫炎癥細胞中表達,在免疫炎癥反應中起重要作用[13]。NLRP3炎癥小體由NLRP3、接頭蛋白ASC和前體Caspase-1組成。ASC為NLRP3炎性小體的一種重要接頭蛋白,連接上游NLRP3及下游前體Caspase-1。Caspase-1為NLRP3炎性小體的效應蛋白,其前體Caspase-1本身無催化活性,生理情況下,以無活性的形式位于靜息細胞的胞漿中,NLRP3炎癥小體激活后,前體Caspase-1可通過自身催化激活,激活后可促成IL-1β、IL-18等炎癥因子的活化[14]。本研究結果也證實,腦缺血損傷大鼠在缺血后1 d即出現(xiàn)NLRP3升高并達到峰值,Caspase-1的表達在腦缺血后3 d達到峰值,進一步證實了MCAO大鼠中存在NLRP3炎癥小體活化,其活化過程與文獻研究一致。
補陽還五湯是治療氣虛血瘀型腦缺血的經(jīng)典名方,臨床療效獨特[15-16],該方重用生黃芪補氣,令氣旺血行,瘀去絡通,為君藥。當歸尾長于活血,是為有化瘀而不傷血之妙,為臣藥。川芎、赤芍、桃仁、紅花助當歸尾活血祛瘀;地龍通經(jīng)活絡,均為佐藥。全方共奏益氣活血,通經(jīng)活絡之功。課題組前期研究發(fā)現(xiàn),其藥效物質主要來源為黃芪、川芎當中的川芎嗪、阿魏酸、芒柄花苷、毛蕊異黃酮、芒柄花素、洋川芎內(nèi)酯A、蒿本內(nèi)酯。而黃芪為治氣虛要藥,川芎為血中之氣藥,表明補陽還五湯對“虛、瘀”狀態(tài)的缺血性腦卒中療效確切。前期藥效學實驗表明補陽還五湯可改善MCAO大鼠神經(jīng)功能缺損癥狀,其作用機制與抗炎癥反應、抗氧化應激損傷等有關[17-19]。證實了補陽還五湯可通過多靶點、多環(huán)節(jié)、多效應途徑有效防治腦缺血。本實驗結果也證實,補陽還五湯可有效改善MCAO大鼠血液流變學指標,抑制NLRP3、Caspase-1表達,減輕炎癥反應,因此,我們推測,NLRP3炎癥小體的過度活化是腦缺血炎性損傷加重的重要因素,補陽還五湯可能是通過抑制NLRP3、Caspase-1表達,從而減輕腦缺血后炎癥反應,發(fā)揮抗腦缺血損傷的作用。

