碳材料在金屬化合物固態儲氫中的應用
劉 夢,陸 林,邱景義,陳俊紅,趙鵬程
(1.軍事科學院防化研究院先進化學蓄電技術與材料北京市重點實驗室,北京 100191;2.北京科技大學材料科學與工程學院,北京 100083)
燃料電池技術正在我國迅速推廣應用,至2020 年7 月,燃料電池汽車已超過7 200 輛,并建成加氫站約80 座。然而,我國燃料電池-氫能產業仍面臨核心技術和關鍵零部件缺失等突出問題,氫氣的安全、經濟和高效儲運仍是主要技術障礙。常見的儲氫技術主要有高壓儲氫、低溫液化儲氫和固態儲氫等[1]。固態儲氫在能源效率、存儲密度和安全性等方面具有明顯的優勢,其中最具代表性的是金屬化合物儲氫材料,但熱力學穩定、動力學釋放氫緩慢和循環可逆性差等問題限制了它們的實際應用。近年來的研究表明,碳材料在金屬化合物儲氫材料的開發中發揮越來越重要的作用。本文主要從納米結構約束、催化劑和添加劑的角度闡述了碳材料對金屬化合物固態儲氫材料熱力學和動力學的影響,并討論了相關作用機制。
1 納米結構約束
1.1 鎂基金屬氫化物
氫化鎂(MgH2)由于成本低和理論質量儲氫容量高(質量分數7.6%)被認為是最有前途的金屬化合物儲氫材料之一,納米結構約束被認為是改善金屬化合物儲氫性能的有效方法,碳材料因結構可設計性強成為納米結構約束的重要材構有序的MgH2,載量可達75%(質量分數)。生成復合材料的脫氫峰值溫度為247 ℃,比純MgH2低121 ℃。Mg 對空氣中的氧氣非常敏感,一旦被氧化就將失去儲氫性能。為此,如圖1 所示,Chen 等[4]采用甲烷等離子體金屬反應法制備了碳然而它的應用受到脫氫溫度高和動力學釋放緩慢的限制[2]。料。Xia 等[3]利用溶劑熱法制備了在石墨烯上分散良好且結封裝的Mg。復合材料在300 ℃下10 min 內可吸收4.8%(質量分數)H2,并在350 ℃下20 min 內解吸出5.0% (質量分數)的H2。該方法為制備空氣中穩定的納米尺寸儲氫材料提供了一種新的技術方案。
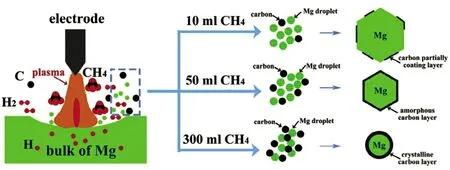
圖1 Mg@C的制備工藝原理圖[4]
1.2 金屬硼氫化物
硼氫化鋰(LiBH4)和硼氫化鈉(NaBH4)具有較高的理論質量儲氫容量(18.5%和10.8%,質量分數),但可逆性差,納米化也是改進其儲氫性能的有效方法。如圖2 所示,Lai 等[5]采用浸漬法將金屬硼氫化物約束在碳納米孔球體內。最近,Chong 等[6]使用濕化學方法將NaBH4封裝在“石墨烯包裹層”中。NaBH4均勻分布在石墨烯表面并被單層石墨烯片包裹,這種形態限制了復合材料相的分離和團聚,最大化脫氫/加氫能力并防止脫氫產物的逸出。封裝在“石墨烯包裹層”中的NaBH4可在350 ℃時釋放7.0%(質量分數)的H2并在6 個循環中表現出穩定的可逆性。
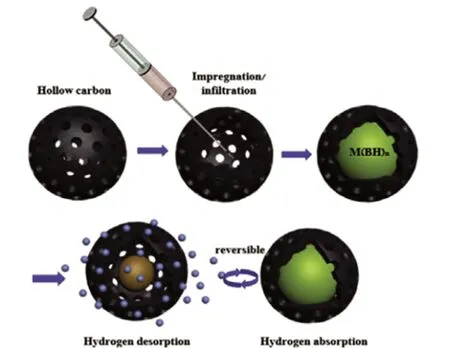
圖2 浸漬法制備M(BH4)n-HCN 的示意圖[5]
1.3 金屬鋁氫化物
鋁氫化鈉(NaAlH4)因具有良好的熱力學性質和可觀的理論質量儲氫容量(7.4%,質量分數)成為研究最多的金屬復合氫化物,但釋放和吸收動力學緩慢限制了其應用。Nielsen等[7]將NaAlH4熔體滲透到碳氣凝膠中,NaAlH4形成在納米多孔骨架中,顯著改善了NaAlH4的氫脫附動力學,最大氫釋放速率溫度從252 ℃降至162 ℃。Gao 等[8]也通過熔體滲透法將NaAlH4約束在更小的納米孔碳材料中,可使其吸附動力學得到改善并影響熱力學。之后,Palm 等[9]用溶液浸漬法將NaAlH4沉積在高微孔碳材料上,實現在環境溫度(>23 ℃)下開始釋放H2。
2 催化劑
2.1 鎂基金屬氫化物
大量實驗證明,添加催化劑也是降低MgH2運行溫度和改善脫氫動力學的一種有效手段。碳自身獨特的電子性質(如離域π 鍵)以及C 原子與H 原子間的相互作用,使碳對各種儲氫材料表現出催化作用。Imamura 等[10]首次將石墨碳(G)作為催化劑研究了對Mg 脫氫/吸氫性能的影響。在苯存在的情況下機械研磨Mg/G,發現G 對氫分子具有催化活性。之后的研究表明,即使沒有苯,碳也可以發揮催化作用。Liu 等[11]研究發現石墨烯納米片與MgH2球磨可以提供更多的活性催化位點,有利于H2的吸附和解離。碳納米管(CNT)和碳氣凝膠(CA)也被證實具有催化作用,對增強儲氫能力和改善動力學非常有效。如圖3 所示,Peng 等[12]制得的Mg@CA 表現出增強的氫化和脫氫速率。
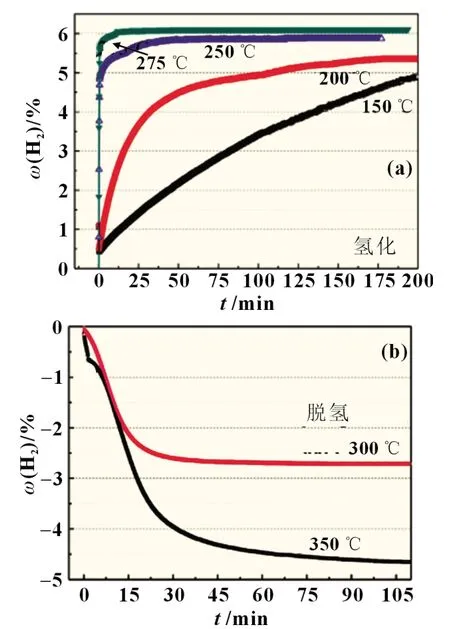
圖3 Mg@CA在不同溫度下的(a)氫化和(b)脫氫曲線[12]
2.2 金屬硼氫化物
機械研磨法在制備復合材料過程中會降解碳納米結構而影響其催化作用,該問題可通過使用溶劑制備技術得到解決。因此,Han 等[13]采用一步溶劑法合成了Mg(BH4)2-CNTs復合材料,CNTs 載量為50%(質量分數)時復合材料在76 ℃就開始釋放氫。如圖4(a)所示,在峰值釋放溫度117 ℃時,10 min 內可以從樣品中脫出3.79%(質量分數)的H2。Jiang 等[14]研究了微量CNTs 摻雜對Mg(BH4)2性能的影響。如圖4(b)所示,CNTs 載量為5%(質量分數)時顯示出最佳的脫氫動力學且脫氫活化能遠低于純Mg(BH4)2,即少量的CNT 催化劑也可以顯著增強動力學。
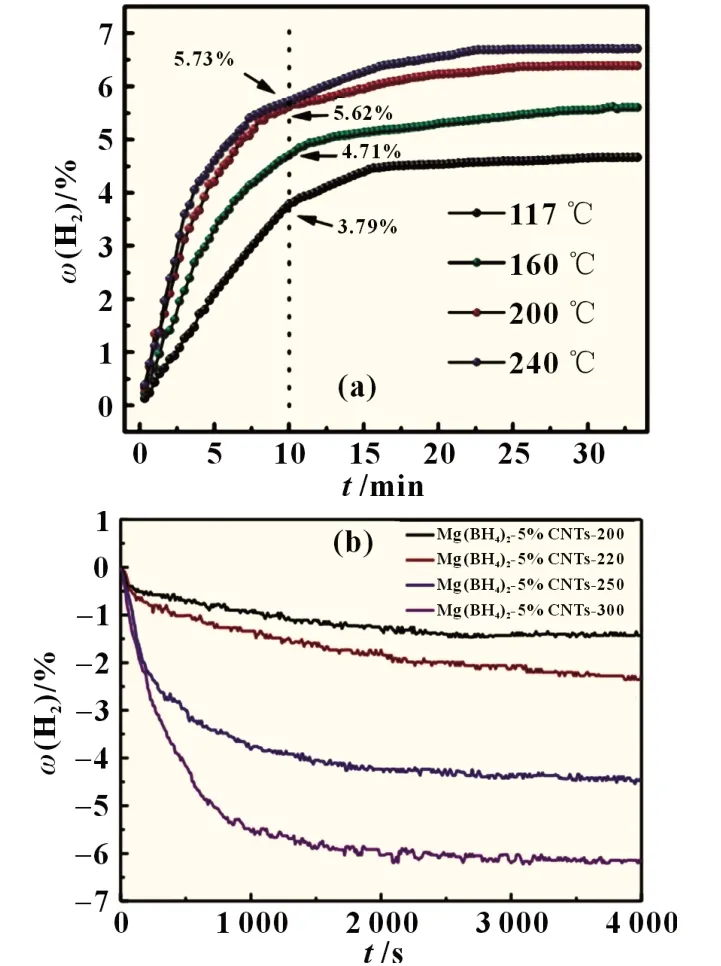
圖4 (a)含50%(質量分數)CNTs的Mg(BH4)2的氫解吸曲線[13]和(b)含5%(質量分數)CNTs的Mg(BH4)2的脫氫動力學曲線[14]
2.3 金屬鋁氫化物
類似的,Berseth 等[15]使用溶劑制備技術將NaAlH4和碳結合,發現與CNT 和G 相比,富勒烯是NaAlH4的最佳催化劑。DFT 計算發現不同碳的電子親和能隨曲率的增大而增大,曲率的增加會使去除氫原子的能量減少。作者還用碳的電負性解釋了催化作用,NaAlH4中的鍵在Na+和AlH4-之間是離子性的,而在Al 和H 之間是共價的。電負性碳的存在會影響Na 將電子提供給AlH4-,因此削弱了Al-H 鍵,更易于氫的釋放和吸收。
3 添加劑
3.1 鎂基金屬氫化物
壓實鎂基金屬氫化物的氫滲透性受到阻礙,導致脫氫/再氫化動力學緩慢,并且循環中應變的存在會導致壓實鎂基金屬氫化物的破裂和分解。研究表明,摻入碳添加劑可以提高機械穩定性、導熱性和氣體擴散性。Chaise 等[16]將膨脹天然石墨(ENG)與鎂基金屬氫化物壓實成圓片,加入ENG 后顯著提高壓實圓片的徑向導熱率且導熱率隨ENG 含量線性增加。Yan 等[17]研究了ENG 含量和壓片壓力對Mg(NH2)2-2 LiH-0.07 KOH 性能的影響,發現隨著壓實壓力的增加,第一個吸附循環的氫解吸動力學下降,而從第二個吸附循環開始,無論壓實壓力如何變化,均表現出相似的氫解吸動力學和容量。最近,Liu 等[18]將竹形碳納米管作為載體用于MgH2的自組裝,通過高壓致密化后的復合材料獲得高達65.90 g/L 的體積容量且性能無明顯退化,特殊結構的CNTs 與致密化的結合為提高儲氫密度提供了一個新的視角。
3.2 金屬硼氫化
Sitthiwet 等[19]采用熔融滲透法將LiBH4約束在浸漬有氧化鈦的活性炭納米纖維(ACNF-Ti)中并將其壓實成片。壓實LiBH4-ACNF-Ti 的脫氫溫度保持在352~359 ℃,遠低于壓實的純LiBH4,且復合材料可實現在脫氫/再加氫循環過程中的機械穩定性。為進一步改善儲氫性能,Thiangviriya 等[20]將ACNF 應用于壓實的2 LiBH4-MgH2中。如圖5 所示,摻入量為30%(質量分數)時,壓實樣品的起始脫氫溫度從350 ℃降低至300 ℃,氫釋放量從理論容量的55%升高至87%,且壓片在循環過程中保持機械穩定性。

圖5 2 Li-MH和2 Li-MH-ACNF脫氫期間的(a)同步DSC-TG-MS 曲線和(b)壓實試樣及其再氫化后的照片[20]
3.3 金屬鋁氫化物
Pohlmann 等[21]通過混合25%(質量分數)的ENG,使NaAlH4的導熱系數從不到1 W/(m·K)提高到38 W/(m·K)。與松散粉體相比,壓實NaAlH4的體積儲氫容量從19 g/L 增加到59 g/L。此外,ENG 在壓實過程中可充當潤滑劑并作為金屬鋁氫化物粉體的結合劑。之后,Plerdsranoy 等[22]首次提出將LiAlH4-LiBH4壓實在ACNF 中,將研磨后的粉體在976 MPa下壓實得到圓片樣品。相比研磨的LiAlH4-LiBH4,壓實樣品的脫氫溫度降低了85 ℃,氫釋放量從理論比容量的65%提高到80%。此外,LiAlH4-LiBH4的活化能顯著降低且體積儲氫容量從32.5 g/L提高到53.3 g/L。ACNF 的曲率和連接的多孔結構使壓實樣品具有優異的氫滲透性,它還可以充當壓實樣品的增強骨架,保證循環過程中的機械穩定性。
4 結論與展望
本文主要討論了碳材料對典型金屬化合物儲氫材料性能的增強作用,分別從納米結構約束、催化劑和添加劑的角度介紹了碳的作用機制:
(1)納米結構約束:碳材料結構的強可設計性可有效納米約束金屬化合物,使氫以更快的速度釋放出來。
(2)催化劑:碳材料獨特的電子性質可以改善金屬化合物的電子相互作用,從而降低氫的解吸能。
(3)添加劑:碳材料的高導熱性可顯著增強循環過程中的脫氫動力學。
綜上所述,碳材料具有強結構設計性、獨特的電子性質和高導熱性,是提高金屬化合物儲氫性能的理想復合材料。其中,碳材料作為催化劑的作用機制仍存在爭議,還需進行系統的研究。

