CYP3A4基因多態性對羥考酮抑制腰椎手術后疼痛的影響
丁勝楊,徐曉曉,吳周全
(1.大連醫科大學 研究生院,遼寧 大連 116044;2.南京醫科大學附屬常州市第二人民醫院 麻醉科,江蘇 常州 213003)
羥考酮是屬于阿片μ和κ阿片受體激動劑的一種半合成蒂巴因衍生物[1]。因其較好的鎮痛效果和較小的不良反應,在麻醉臨床工作中常常被用于術后鎮痛[2]。但羥考酮有著極大的個體差異,不同患者的有效鎮痛劑量可在10~1 040 mg·d-1之間波動[3]。細胞色素P450 3A4酶(CYP3A4)是阿片類藥物的主要代謝途徑,CYP3A4的多態性由40多對等位基因決定,其中CYP3A4*1G基因突變會導致酶系產生功能性改變,這也是導致阿片類藥物代謝差異性的主要因素[4]。本課題組擬通過研究CYP3A4基因多態性對羥考酮抑制術后疼痛的影響,探討個體化差異對羥考酮藥效的影響,為臨床實施個體化用藥提供理論依據。
1 資料與方法
1.1 一般資料
本研究經南京醫科大學附屬常州市第二人民醫院倫理委員會批準(批準號:[2018]YK003-01),患者均簽署知情同意書。選擇2019年1月至2020年3月在南京醫科大學附屬常州市第二人民醫院行全麻下腰椎手術患者150例,根據基因型分成3組:野生純合子(AA)組(CYP3A4*1/*1,n=80),突變雜合子(GA)組(CYP3A4*1/*1G,n=60),突變純合子(GG)組(CYP3A4*1G/*1G,n=10)。患者納入標準:全麻下行腰椎手術的患者。排除標準:(1)肝炎患者或嚴重肝腎功能損害患者;(2)有長期服藥史的患者;(3)不能配合實驗的患者;(4)有嚴重精神疾病史的患者;(5)對麻醉藥物使用禁忌患者;(6)術前服用過CYP3A4酶誘導劑、抑制劑或對肝功能有嚴重損害藥物的患者。
1.2 麻醉方法
患者入室后按慣例行心電監測。麻醉誘導:咪達唑侖0.05 mg·kg-1,丙泊酚初始血漿靶濃度為3 μg·ml-1,根據患者腦電雙頻指數(BIS)的變化調整丙泊酚靶濃度,待BIS降至75以下時靜脈注射羅庫溴銨0.6 mg·kg-1、舒芬太尼0.8 μg·kg-1,待BIS降至50以下后進行氣管插管,所有患者均由同一麻醉醫師行氣管插管。術中采用七氟烷、瑞芬太尼、丙泊酚維持麻醉,并使患者BIS在 40~60之間,間斷靜脈注射順式阿曲庫銨0.1 mg·kg-1維持肌松。手術結束前30 min左右給予靜脈推注羥考酮(萌蒂制藥有限公司,批號BJ9415)5 mg,同時予以自控靜脈鎮痛(PICA)(鎮痛泵配方:羥考酮25 mg、0.9%氯化鈉溶液共100 ml,背景劑量2 ml·h-1,單次自控劑量4 ml,鎖定時間15 min)。手術完成后待患者自主呼吸完全恢復、呼之能應、脫氧觀察5 min SpO2維持在95%以上時拔除氣管導管。
1.3 基因檢測方法
基因檢測方法采用焦磷酸測序法,于術前2~3 d 抽取受試者靜脈血4 ml,置于乙二胺四乙酸(EDTA)抗凝管中。提取外周血基因全組DNA后采用聚合酶鏈反應(PCR)對目的基因進行擴增,取30 μl PCR擴增產物加入3 μl結合了抗生素蛋白鏈菌素的磁珠和37 μl結合緩沖液進行孵育。將磁珠在清洗液中清洗使標記生物素與未標記生物素的DNA單鏈互相分離,加入測序引物再次孵育冷卻至室溫后,加入適當劑量的反應酶、底物、dNTP等進行反應,由焦磷酸測序儀讀取分析結果,對DNA鏈進行多態性分析。
1.4 痛閾值測定
采用神經肌肉刺激儀(SD-V,蘇州)測定患者的痛閾值。測定的部位選在左手無名指第1指肚、左側臍旁3 cm和左側頸部胸鎖乳突肌中點,局部用酒精消毒后固定電極,兩個電極相距1 cm,痛閾檢測電流頻率為20 Hz,疏密波,刺激強度(1~65)從1開始,每3 s增加1,直至病人主訴測試部位出現不能忍受的疼痛感覺時,記錄此時的刺激強度即為病人該部位的皮膚痛閾值。最后取3個部位痛閾值的平均值即為患者的痛閾值。本試驗痛閾值測定于術前進行。
1.5 觀察指標
主要觀察指標:不同時間點疼痛強度數字評估量表(NRS)評分、術中鎮痛藥物使用量、羥考酮總使用量、鎮痛泵按壓次數;次要觀察指標:血漿皮質醇(Cor)濃度、不良反應發生率。
1.6 統計學處理
使用SPSS 23.0統計軟件分析數據,正態分布的計量資料以均數±標準差表示,組間比較采用單因素方差分析;計數資料的比較采用χ2檢驗。P<0.05 為差異具有統計學意義。
2 結 果
2.1 一般情況
在納入試驗的患者中AA組80例,GA組60例,GG組10 例,CYP3A4*1G 等位基因突變頻率為26.7%,等位基因分布符合Hardy-weinberg平衡(χ2=0.12,P>0.05),說明本組研究人群中 CYP3A4*1G 基因型分布已經達到遺傳平衡,具有群體代表性。3組患者年齡、體重、ASA分級、痛閾值等一般資料比較差異無統計學意義(P>0.05),見表1。
2.2 各組NRS評分和血漿Cor濃度的比較
各組間NRS評分和血漿Cor濃度的比較采用重復測量方差分析,球形檢驗顯示P<0.5,不符合球形性,采用Greenhouse-Geisser校正。與AA組比較,GA和GG組患者各時間點的疼痛強度NRS評分降低(P<0.05)。各組血漿Cor濃度隨時間的延長逐漸下降,在T3時濃度最低(P<0.05);隨著時間的延長,與AA組比較,GA和GG組下降幅度更大,其中GG組下降幅度最大(P<0.05)。見表2。
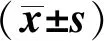
表2 各組間不同時間點NRS評分和血漿Cor濃度的比較
2.3 3組術中鎮痛藥物使用量的比較
3組患者術中均使用舒芬太尼及瑞芬太尼鎮痛,方差齊檢驗顯示P>0.05,進一步采用LSD法對各組間舒芬太尼及瑞芬太尼的用量進行兩兩比較,結果表明3組術中鎮痛藥物使用量的差異無統計學意義(P>0.05),見表3。
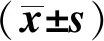
表3 3組術中鎮痛藥物使用量的比較 μg
2.4 3組羥考酮使用量及不良反應的比較
3組患者術后均使用羥考酮鎮痛,方差齊性檢驗顯示P>0.05,進一步采用LSD法對各組間24 h內羥考酮總使用量及按壓次數進行兩兩比較。與AA組比較,GA和GG組患者鎮痛泵按壓次數和無效按壓次數減少,相應的羥考酮的使用量也減少,且GG組減少最明顯(P<0.05)。3組間惡心嘔吐和呼吸抑制發生率的差異均無統計學意義(P>0.05)。見表4、5。
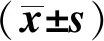
表4 3組24 h內羥考酮總使用量及鎮痛泵按壓次數比較
2.5 3組患者TWA- MAP和TWA- HR的比較
3組患者TWA-MAP和TWA-HR的比較方差齊性檢驗顯示P<0.05,因此采用Games-Howell檢驗,結果顯示,與AA組比較,GG和GA組患者TWA-MAP和TWA-HR降低(P<0.05),但GA組與GG組之間的差異無統計學意義(P>0.05),見表6。
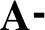
表6 3組患者TW MAP和TW HR的比較
3 討 論
腰椎手術后疼痛主要來自兩個方面:一方面是手術區域結構的傷害,如顯露對椎旁肌肉的廣泛剝離等引起局部及血漿中致痛物質如乳酸、前列腺素等水平升高,刺激外周感受器產生外周性疼痛;另一方面是術中對神經根的牽拉和激惹可直接刺激中樞神經系統引起中樞性疼痛[5-6]。個體化用藥是一種新興的醫學模式,根據不同個體特有的遺傳學特點,制定適合個體遺傳特點的治療方案,或針對遺傳變異的不同開發個體化藥物的醫學模式[7]。個體化用藥可通過預測特異性或過表達靶點,預估藥物效應和劑量。在腰椎手術中依據基因型對患者術后鎮痛藥物的選擇及藥物劑量的控制實行個體化管理,同時降低不良反應的發生率。
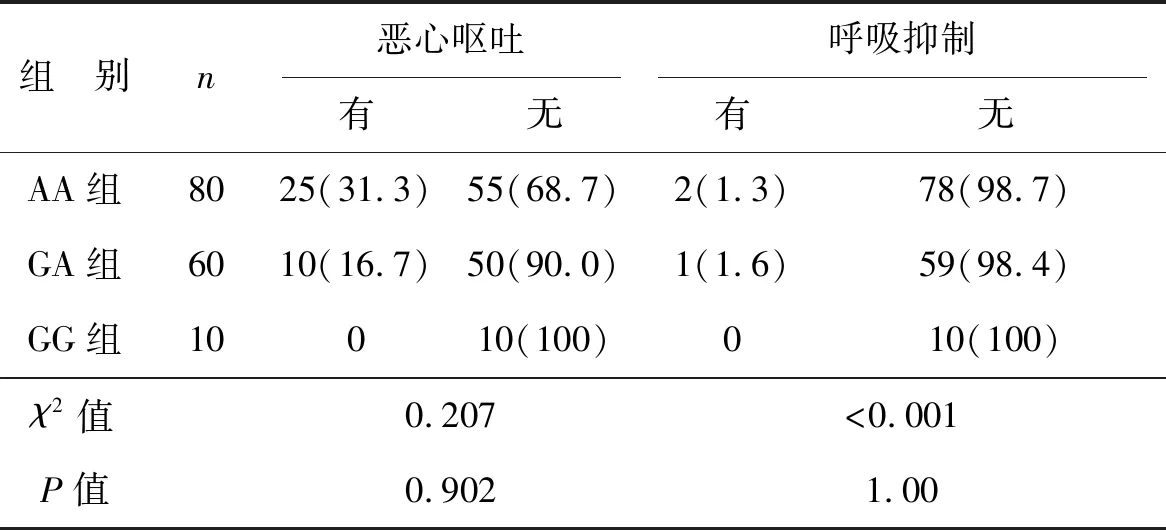
表5 3組患者不良反應發生情況的比較
羥考酮PICA可安全有效地減輕中、大型手術后疼痛[8],已有的臨床研究認為羥考酮具有相當于嗎啡的超強鎮痛作用[9],且與嗎啡相比較具有更加安全的特點,主要表現為惡心、嘔吐、呼吸抑制的發生率低[10],但是研究發現個體基因的不同與羥考酮術后鎮痛用量相關[11]。羥考酮主要是經CYP3A4和CYP2D6在肝臟和腸壁進行代謝,其中CYP2D6僅對羥考酮的代謝有影響,但對鎮痛效果及不良反應發生率的影響尚無確切結論;CYP3A4是羥考酮代謝的主要途徑,Liukas等[12]用克拉霉素抑制CYP3A4后,羥考酮鎮痛效果有所增強。攜帶*1G等位基因個體體內CYP3A4酶活性降低,這是依據基因分型對羥考酮術后鎮痛個體化用藥的理論基礎。本研究考察了不同基因型患者術后不同時間點的NRS疼痛評分、PCIA的按壓次數和羥考酮的使用量,結果發現GA組患者的疼痛評分最低,PCIA的按壓次數最少,因此羥考酮總使用量也最少。這與Ren等[13]經Meta分析得出攜帶*1G等位基因的個體在術后24 h內需要的鎮痛藥物少于野生型*1/*1基因型的個體的結論一致[13]。此外血漿Cor濃度是應激反應的重要指標,在本試驗中,3組患者術后血漿Cor的濃度均逐漸下降,但是攜帶*1G等位基因的個體血漿Cor的濃度下降更加明顯,而且下降的趨勢與NRS評分的趨勢基本一致,因此根據患者基因型合理調整用藥劑量,進行個體化用藥,可以更好地優化術后鎮痛效果,減輕術后應激。
羥考酮主要的不良反應有血流動力學抑制、惡心嘔吐、呼吸抑制等,我們對惡心嘔吐及呼吸抑制發生情況進行分析,發現3組患者惡心嘔吐發生率無明顯差異,這與Ren等[13]攜帶*1G等位基因的患者惡心嘔吐發生率較低的研究結果不符,原因可能與我們收集的樣本量較少或者人種間差異有關。3組患者呼吸抑制的發生率無明顯差異,研究中患者發生呼吸抑制的主要表現為呼吸變淺,但呼吸頻率未受影響,給予呼喚或輕拍刺激后均可維持呼吸,且5~10 min內可恢復正常,這可能與羥考酮本身的呼呼抑制較輕有關。TWA-MAP和TWA-HR主要反映考察時間內患者MAP和HR的整體水平,在一定程度上反映羥考酮術后鎮痛效果及對循環系統的影響。我們對3組患者的TWA-MAP和TWA-HR進行分析,其中AA組個體的MAP偏高,特別是HR偏快,認為可能與術后的疼痛應激有關;攜帶*1G等位基因個體的MAP則相對偏低,HR偏慢,但均在正常范圍之內,可能是與羥考酮提供了良好的術后鎮痛有關。
綜上所述,CYP3A4基因多態性對羥考酮抑制術后疼痛有顯著影響,羥考酮對基因型為CYP3A4*1G/*1G的患者術后鎮痛效果最好,基因型為CYP3A4*1/*1G的效果稍次,基因型為CYP3A4*1/*1的效果最弱。因此通過個體化臨床用藥,根據遺傳學特點差異性來決定臨床用量,可以有效改善術后患者麻醉鎮痛的有效性和持續性,減少不良反應,進一步提高患者術后麻醉的滿意度。

