竹節參總皂苷通過調節miR-181a/PPARα通路改善非酒精性脂肪性肝病的作用
羅 悅, 劉小慧, 魏承亮, 段 麗, 劉朝奇, 賀海波, 蔡三金*
(1.三峽大學醫學院,湖北 宜昌 443002;2.三峽大學生物與制藥學院,湖北 宜昌 443002)
隨著生活方式的改變,非酒精性脂肪性肝病(NAFLD)全球發病率高達25%,為肝細胞癌的主要病因之一[1-2]。“多重打擊”假說指出,肝細胞脂質過度積累和肝細胞炎癥環境是導致肝細胞損傷、激活肝細胞死亡、促進星狀細胞活化、纖維基質沉積的重要因素[3-4]。
miRNA是一類長度約為22個核苷酸的非編碼單鏈RNA分子,可以通過靶向mRNA并抑制其翻譯或促進其降解在轉錄后水平調節基因表達。有研究指出,miR-181a在NAFLD患者、高脂飲食小鼠及ob/ob小鼠的血液和肝臟中高度表達,并在NAFLD中作用顯著[5]。
過氧化物酶體增殖物激活受體α(peroxisome proliferator activated receptor α,PPARα)是一種配體誘導的轉錄因子,在能量代謝、肝功能、炎癥、細胞周期改變和嚙齒動物肝癌發生中起關鍵作用[6]。有研究報道,敲除肝細胞特異性PPARα基因導致小鼠肝臟和全身脂肪酸動態平衡受損,可見PPARα與NAFLD發展密切相關[7]。
目前,臨床上仍缺乏針對治療NAFLD的公認藥物[8]。竹節參PanaxjaponicusC.A.Meyer是五加科人參屬多年生草本植物,具有散瘀止血、消腫止痛、止咳祛痰、補虛強壯的功效,竹節參總皂苷是其主要活性成分[9],具有減輕腸道炎癥反應、改善小鼠脂肪性肝病作用[10-11]。本研究利用高脂飲食建立NAFLD小鼠,并使用不同劑量竹節參總皂苷干預,為相關防治提供新的思路。
1 材料
1.1 動物 SPF級雄性BALB/c小鼠40只,飼養于三峽大學實驗動物中心[動物生產許可證號SCXK(鄂) 2017-0012]。所有操作都遵循倫理委員會相關動物使用和保護規定,倫理審查表編號2013090B。
1.2 試劑及藥物 竹節參購于恩施竹節參種植基地,經湖北省天然產物研究與開發重點實驗室汪鋆植教授鑒定為正品。竹節參總皂苷采用醇提法提取,大孔樹脂吸附法純化[12]。丙氨酸氨基轉移酶(ALT)試劑盒、甘油三酯(TG)試劑盒均購于中生北控生物科技有限公司;PrimeScriptTMRT reagent Kit with gDNA Eraser(Prefect Real Time)(日本TaKaRa公司,貨號RR047A);Green Taq Mix(南京諾唯贊生物科技有限公司,P131-03);抗體TLR4(美國Santa Cruz公司,貨號SC-293072)、p-STAT1(美國Cell Signaling公司,貨號8826)、β-actin(美國Cell Signaling公司,貨號4970L)。引物由生工生物工程(上海)股份有限公司合成。其余試劑均為分析純。
1.3 儀器 PowerPas Basic電泳儀(美國Bio-Rad公司);核酸蛋白分析儀(美國Beckman公司); Gene Genius凝膠分析系統(英國Syngene公司);Step One Plus 實時定量PCR儀(美國Applied Biosystem公司);梯度PCR儀(美國Applied Biosystem公司);Gel Logic-200凝膠成像分析系統(美國Kodak公司);全波長酶標儀(美國 Thermo公司)。
2 方法
2.1 分組及給藥 將小鼠隨機分為正常飲食組、模型組、竹節參總皂苷低劑量組、竹節參總皂苷高劑量組,除正常飲食組外(標準飼料喂養)其他3組給予華阜康公司高脂飼料(H10060)喂養,同時竹節參總皂苷組灌胃不同劑量藥物(15、45 mg/kg,溶于生理鹽水),正常飲食組予等量的生理鹽水灌胃,飼養19周,每2 d記錄1次體質量。
2.2 標本采集 將喂養19周后的小鼠稱定質量,腹腔注射10%水合氯醛麻醉,取血,血液靜置于37 ℃下1 h,3 000 r/min離心10 min,收集血清。小鼠脫頸椎處死,切取肝臟,生理鹽水沖洗并稱質量,切取肝大葉中部長度、厚度適中部分置于包埋夾中,多聚甲醛固定,剩余新鮮肝臟組織置于1.5 mL離心管中,在-80 ℃下保存。
2.3 小鼠血清ALT活性檢測 新鮮小鼠血清使用多功能酶標儀檢測ALT活性,具體方法參照試劑盒說明書。
2.4 小鼠肝臟組織TG水平檢測 稱取小鼠新鮮肝臟50 mg,浸于1 mL無水乙醇,置于1.5 mL離心管中,充分研磨后室溫抽提24 h,5 000 r/min離心5 min,收集上層澄清抽提液,使用多功能酶標儀檢測TG水平。
2.5 小鼠肝臟組織HE染色 小鼠肝組織固定完成后修整大小,乙醇梯度脫水,石蠟包埋,切片(厚度4 μm),常規HE染色,在顯微鏡下觀察。
2.6 RT-PCR與RT-qPCR檢測SREBP-1c、ChREBP、IL-1β、TNFα、miR-181a、PPARαmRNA表達 稱取小鼠新鮮肝臟50 mg至1.5 mL EP管中,使用Trizol充分裂解并提取總RNA,電泳檢測RNA完整性,逆轉錄試劑盒逆轉獲得cDNA,RT-PCR技術驗證引物,2%瓊脂糖凝膠電泳(內參β-actin),成像系統中拍攝分析。miR-181a以U6作為內參,在實時定量PCR儀中擴增并測量繪制擴增曲線,反應體系為5 μL SYBR Green,2.4 μL RNase-free water,0.4 μL引物(濃度為10 μmol/L),2 μL cDNA(逆轉后稀釋10倍),0.2 μL ROX。反應結束后讀取CT值,計算2-ΔΔCT,引物序列見表1。

表1 引物序列
2.7 Western blot法檢測p-STAT、TLR4蛋白表達 稱取小鼠肝臟組織適量,加入RIPA蛋白裂解液充分勻漿后,在4 ℃下提取30 min后,12 000 r/min離心10 min,收集上清為組織總蛋白,應用BCA蛋白定量法檢測蛋白濃度,加入蛋白上樣緩沖液,制備滅活樣品。經SDS-PAGE凝膠電泳分離后,按照蛋白分子大小切取相應凝膠片段,采用濕法轉膜將蛋白條帶轉移至PVDF膜上,經牛奶封閉、孵育一抗、洗膜、孵育二抗、洗膜等步驟后,X光片顯影,掃描圖像,Image J軟件分析蛋白表達。
3 結果
3.1 竹節參總皂苷對高脂飲食小鼠體質量及肝質量指數的影響 小鼠給予高脂飼料喂養19周后,體質量及肝質量指數較正常組升高(P<0.05,P<0.01);經竹節參總皂苷藥物干預后,小鼠體質量及肝質量指數下降(P<0.05,P<0.01),見表2。
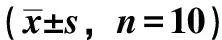
表2 竹節參總皂苷對高脂飲食小鼠體質量及肝質量指數的影響
3.2 竹節參總皂苷對高脂飲食小鼠血液中ALT活性及肝組織TG水平的影響 小鼠給予19周高脂飼料喂養后,血液中ALT活性及肝組織TG水平升高,與正常組比較具有顯著差異(P<0.05);與模型組比較,竹節參總皂苷低、高劑量干預后,血清中ALT活性及肝組織TG水平降低(P<0.05),見圖1。
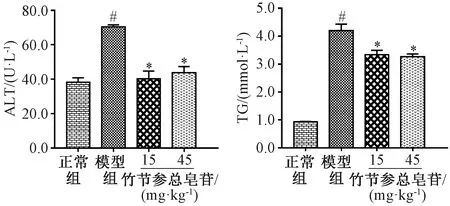
注:與正常組比較,#P<0.05;與模型組比較,*P<0.05。圖1 竹節參總皂苷對高脂飲食小鼠血液中ALT及肝組織TG的影響
3.3 竹節參總皂苷改善高脂飲食小鼠肝組織病理變化 小鼠給予高脂飼料喂養19周后,肝小葉結構不完整,肝臟細胞腫脹、變圓,排列不規則,可見彌漫性的脂質空泡,并有融合現象,伴隨炎性細胞浸潤,結合“3.1”“3.2”項下結果證明模型構建成功[13];經竹節參總皂苷干預后,肝組織病理變化改善明顯,肝索排列較整齊,脂肪空泡明顯減少,肝組織炎癥浸潤現象輕微,見圖2。
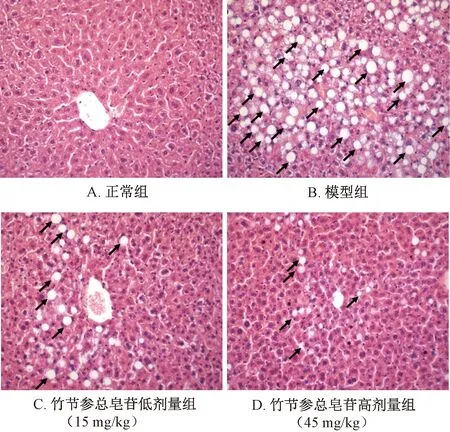
注:黑色剪頭指示脂質空泡位置。圖2 高脂飲食小鼠肝組織HE染色(×200)
3.4 竹節參總皂苷調節高脂飲食小鼠肝臟脂質代謝相關基因的表達 與正常組比較,模型組小鼠肝臟組織中脂質代謝相關基因SREBP-1c、ChREBPmRNA表達升高(P<0.05),高脂飲食引起小鼠肝臟脂質代謝紊亂;竹節參總皂苷干預后SREBP-1c、ChREBPmRNA表達降低(P<0.05),見圖3。
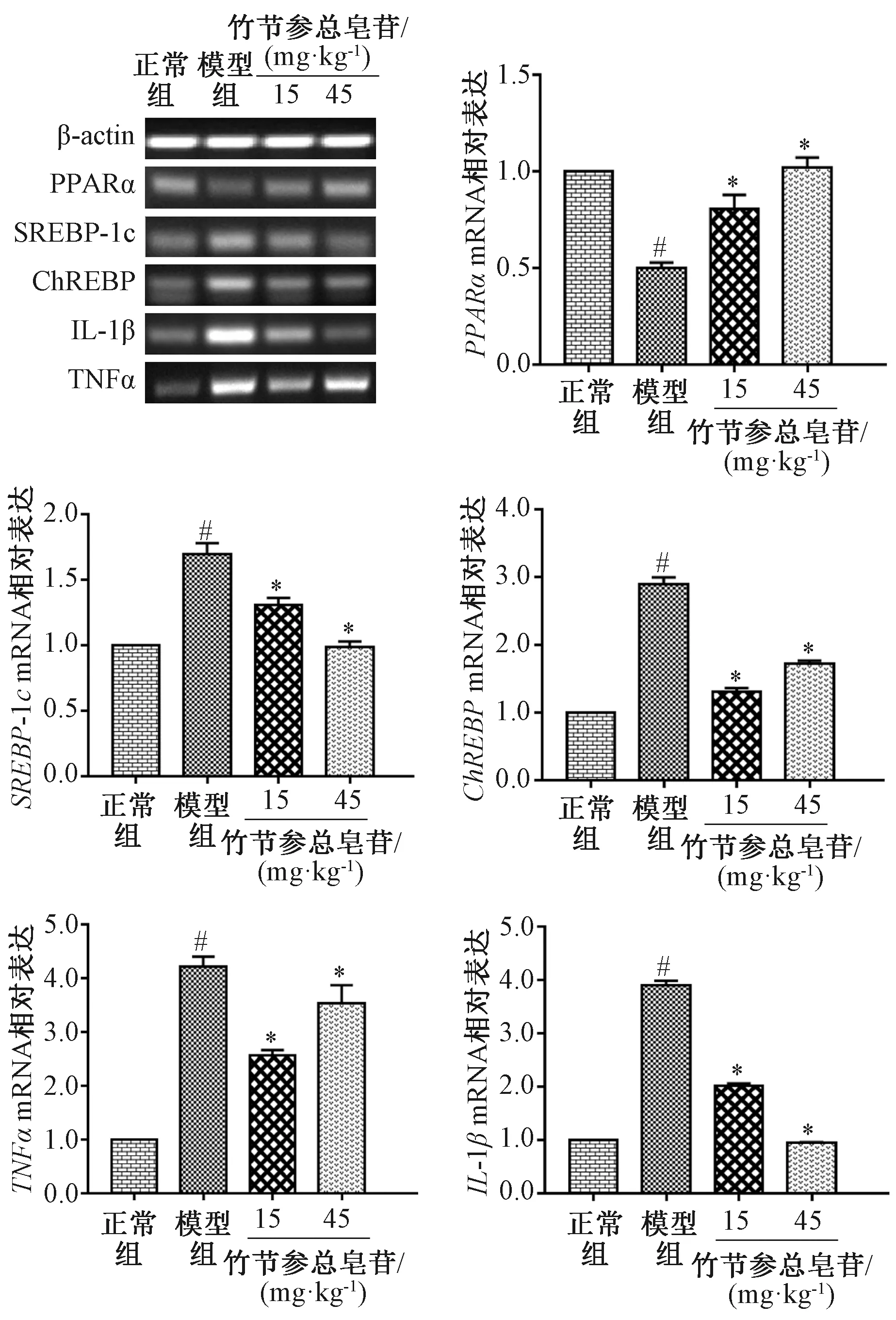
注:與正常組比較,#P<0.05;與模型組比較,*P<0.05。圖3 竹節參總皂苷對高脂飲食小鼠肝組織中脂質代謝及炎癥相關基因表達的影響
3.5 竹節參總皂苷調節高脂飲食小鼠肝臟組織炎癥相關基因及蛋白表達 小鼠高脂飼料喂養19周后,肝臟組織中TLR4、p-STAT1蛋白表達升高,見圖4;TNFα、IL-1βmRNA表達也較正常飲食組高(P<0.05),見圖3;低、高劑量竹節參總皂苷干預后,上述指標均有所下降,并趨于正常水平。
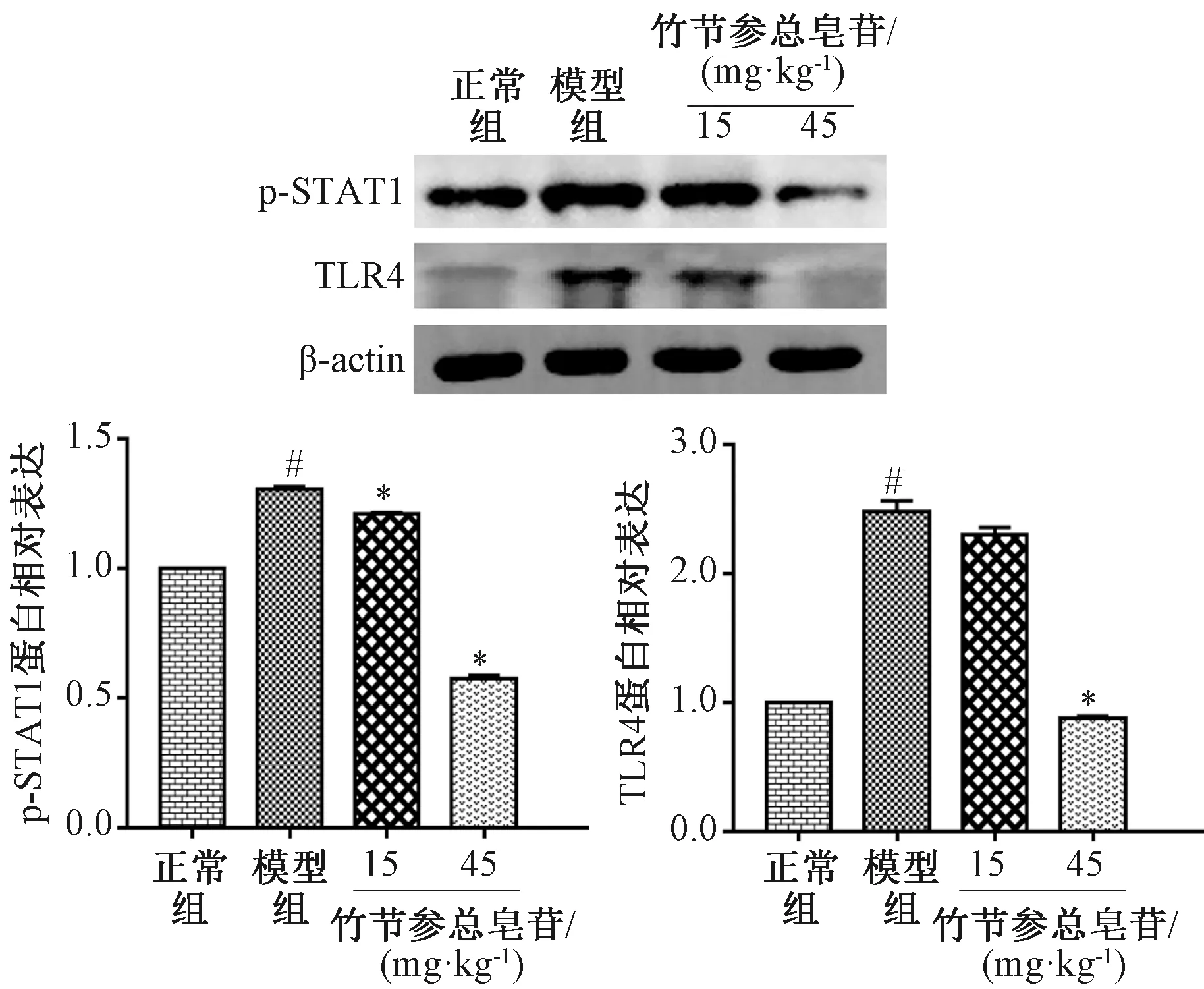
注:與正常組比較,#P<0.05;與模型組比較,*P<0.05。圖4 竹節參總皂苷對高脂飲食小鼠肝臟組織中炎癥相關蛋白表達的影響
3.6 竹節參總皂苷調節高脂飲食小鼠肝臟組織miR-181a及PPARα基因表達PPARα基因表達在小鼠肝組織中下降(P<0.05),而經竹節參總皂苷干預后升高,并趨于正常組水平,見圖3。同時,PPARα可作為miR-181a的靶蛋白,見圖5。模型組miR-181a基因表達較正常組升高,竹節參總皂苷干預后其表達呈下降趨勢(P<0.05),見圖6。

圖5 miR-181a和PPARα 3′UTR之間預測堿基配對
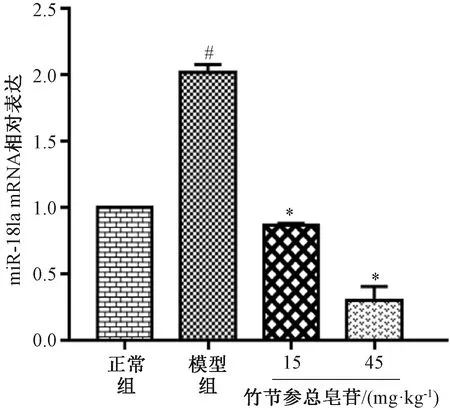
注:與正常組比較,#P<0.05;與模型組比較,*P<0.05。圖6 竹節參總皂苷對高脂飲食小鼠肝臟組織中miR-181a基因表達的影響
4 討論
miRNAs通過參與轉錄后調控干擾目標基因的表達,miRNA-181a是其中的一員,可調節基因表達所引起的肝臟代謝紊亂及應激激活途徑,從而影響NAFLD及其向疾病更嚴重階段的發展[14]。NAFLD患者及動物中顯著上調的miR-181a可損害肝臟葡萄糖、脂質平衡,而miR-181a可直接靶向PPARα,激活TLR4/NF-κB途徑,調節炎癥反應[15-16]。本實驗證實,NAFLD發生發展與miR-181a/PPARα信號通路相關,而竹節參總皂苷可通過調控該信號通路對NAFLD起到干預作用。
PPARα可同時參與NAFLD脂質代謝及炎癥反應的調節過程[17],通過LXR途徑調節SREBP-1c、ChREBP水平[18-19],調控乙酰輔酶a羧化酶(acetyl-CoA carboxylase,ACC)和脂肪酸合成酶(fatty acid synthase,FAS)活性[20-21],干預肝臟脂肪酸催化合成。抑制PPARα表達時,肝臟儲存過量的脂肪酸,破壞其生理適應機制,引起活性氧形成、內質網應激、肝細胞功能障礙和損傷,導致脂毒性炎癥發生[22]。脂毒性應激時Toll樣受體4(toll-like receptor 4,TLR4)被激活,一方面通過MyD88依賴途徑激活NF-κB誘導炎癥介質IL-1β、TNFα的釋放[23];另一方面通過MyD88和TRIF依賴性信號誘導STAT1在Ser727處的快速磷酸化,并形成同源二聚體進一步遷移到細胞核中驅動下游炎癥途徑,激化炎性反應[24-25],而PPARα可抑制TLR4表達來減輕炎癥水平[26]。本實驗結果顯示,竹節參總皂苷可能通過調節PPARα/SREBP-1c、ChREBP的脂毒性及PPARα/TLR4/STAT1的炎癥反應信號通路,達到改善NAFLD的作用。
綜上所述,miR-181a/PPARα及其介導的SREBP-1c、ChREBP及TLR4/STAT1信號通路促進NAFLD的發生與發展,而竹節參總皂苷可通過調控上述信號通路對NAFLD起到治療作用,為相關防治提供了新方向。

