基于網絡藥理學探討北沙參干預糖尿病的分子機制
古軍霞, 孫會改, 李 陽, 鄭玉光, 鄭 倩, 嚴玉平, 韓曉偉
(河北中醫學院,河北省中藥炮制技術創新中心,河北 石家莊 050200)
糖尿病是全世界最主要的慢性非傳染病之一,近年來發病率呈上升趨勢[1]。中醫認為,糖尿病是“氣陰兩虛,氣虛血瘀”之癥[2],基于多項臨床研究[3-4]、名老中醫經驗總結[5-6]及數據挖掘結果顯示[7-8],它主要分為肺胃陰虛熱盛、肝腎陰虛、氣陰兩虛、陰陽兩虛等7類,臨床治則清熱養陰、溫陽補腎、祛濕化痰、益氣健脾、活血化瘀。北沙參為陰虛及氣陰兩虛型處方的核心藥物之一[9-10],臨床上常用于治療肺熱燥咳、勞嗽痰血、胃陰不足、熱病傷津、咽干口渴等癥[11],含聚炔類、苯丙素類、黃酮類、甾體類、萜類、多糖類等成分[12-14],具有免疫調節、抗腫瘤、抗炎、抗氧化、保肝等作用[15-19],但關于它治療糖尿病的研究還較少。臨床報道,北沙參生脈散可以治療氣陰兩虛型的糖尿病,療效明顯[20],但分子機理尚不清楚。
本研究以北沙參8種主要成分為基礎,利用網絡藥理學構建成分-靶點-通路-疾病網絡,探討干預糖尿病的多成分、多靶點、多通路的作用機制,為相關研究奠定基礎。
1 材料和方法
1.1 活性成分與中藥靶點的篩選 活性成分從TCMSP數據庫 (http://lsp.nwu.edu.cn/tcmsp.php)獲取,以關鍵詞“北沙參”得到相關信息。以口服生物利用度(OB)、類藥性(DL)為標準,篩選出同時滿足OB≥30%、DL≥0.18及對應的靶點。
1.2 糖尿病靶點篩選與預測 把“Diabetes Mellitus”關鍵詞輸入NCBI(https://www.ncbi.nlm.nih.gov/)GEO數據庫中檢索糖尿病患者高通量數據,下載了以GPL22448 Phalanx Human lncRNA One Array v1_mRNA為平臺,來源包括糖尿病患者與正常人的基因芯片數據集GSE95849,得到糖尿病的差異表達基因。
1.3 蛋白相互作用網絡構建與分析 將蛋白靶點導入String數據庫(https://string-db.org/),限定物種為人, 進行蛋白互作分析,選取0.7的高置信度并保存結果,從而確保數據的可靠性。利用Cytoscape軟件將導出文件中的node1、node2和combined score信息導入并繪制相互作用網絡。節點(node)大小表示度值(Degree)的大小,邊(edge)的粗細表示combined score的大小。
1.4 生物過程與通路分析 運用cluster Profiler對與糖尿病相關的“活性成分-潛在靶點”網絡中的蛋白分別進行GO功能富集分析及KEGG信號通路分析,從而獲得顯著富集的基因功能和信號通路。
1.5 成分-靶點-通路-疾病網絡構建 在Excel表中將58種成分的預測靶點和通路分析構建“藥材-藥效成分”“藥效成分-靶點”“靶點-通路”“通路-疾病”之間的相互關系,以藥材、藥效成分、靶點蛋白、通路和疾病為5類節點,它們之間有相互關系的分別用邊相連, 采用Cytoscape 3.6.1軟件的關聯 (Merge) 功能構建北沙參-成分-靶點-通路-疾病網絡模型。
1.6 分子對接 采用Systems Dock Web Site(http://systemsdock.unit.oist.jp/iddp/home/index)對蛋白相互作用網絡中度值靠前的4個靶點與北沙參主要藥效成分進行分子對接驗證。以二甲雙胍(Metformin)為對照,整理對接結果中的docking score并分析。
2 結果
2.1 活性成分 活性成分共8種,見表1。

表1 北沙參中活性成分
2.2 作用靶點篩選(差異基因) 從GEO下載并導出平臺文件和矩陣文件,對數據進行注釋,將探針名稱轉換為基因名稱,并且將正常組和實驗組數據進行分組,原始數據以P<0.05為條件進行過濾后,選取糖尿病組織/正常組織上、下調差異倍數>1.51作為選取條件,共得到5 817個疾病靶點及熱圖(圖1)、火山圖(圖2)。取北沙參活性成分作用靶點和糖尿病相關靶點的交集,共獲得58個靶點。
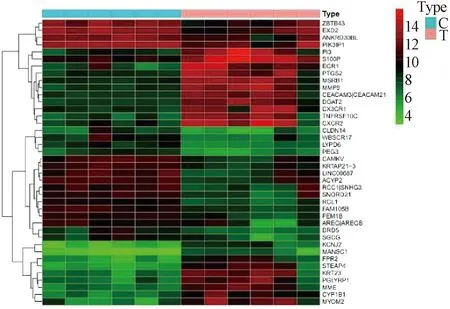
圖1 GEO數據庫差異熱圖

圖2 GEO數據庫差異火山圖
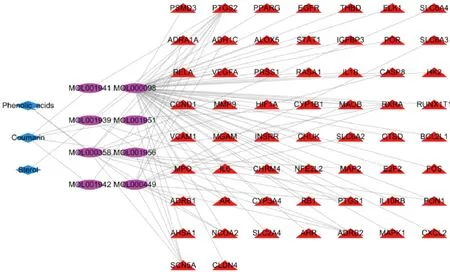
圖3 活性成分調控網絡圖
2.3 活性成分-作用靶點網絡 “藥物-成分-疾病-靶點”網絡圖見圖3,有61個節點、81條邊,紅色三角表示靶點基因(共58個),玫紅橢圓表示北沙參中的8種活性成分,藍色菱形為北沙參3種主要成分[甾醇類(Sterol)、香豆素類(Coumarin)和酚酸類(Phenolic Acids)];度值最高的活性成分為槲皮素(Quercetin),其次為豆甾醇(Stigmasterol)、β-谷甾醇(beta-Sitosterol)。
2.4 蛋白相互作用網絡與關鍵靶點
2.4.1 PPI蛋白互作網絡 北沙參可與3 320個靶點產生直接或間接作用,不同靶點之間聯系達82 802種。
2.4.2 關鍵靶點 采用Bisogenet插件,以Degree>81、Betweenness≥400為條件,對蛋白互作網絡節點進行拓撲結構分析,發現關鍵靶點56個,見表2,篩選策略見圖4。
2.5 GO、KEGG富集分析 GO富集分析見圖5,分子功能集中在RNA聚合酶Ⅱ特異性DNA結合轉錄因子(RNA polymerase Ⅱ-specific DNA-binding transcription factor binding)、DNA結合轉錄因子(DNA-binding transcription factor binding)、核激素受體結合(nuclear hormone receptor binding)等,生物過程集中在響應營養水平(response to nutrient levels)、響應氧化應激反應(response to oxidative stress)、響應抗生素(response to antibiotic)、細胞響應化學脅迫(cellular response to chemical stress)、細胞響應細菌源的分子(cellular response to molecule of bacterial origin),細胞組成集中在膜區域(membrane region)、膜筏板(membrane raft)和膜微區(membrane microdomain)、轉錄調節復合體(transcription regulator complex)和內腔囊泡(vesicle lumen)。
KEGG富集分析見圖6,58個潛在靶點基因所涉及到的通路共有168條,前10條分別為內分泌抵抗(Endocrine resistance)、NF-kappa B信號通路(NF-kappa B signaling pathway)、HIF-1信號通路(HIF-1 signaling pathway)、細胞凋亡(Apoptosis)、細胞衰老(Cellular senescence)、Ras信號通路(Ras signaling pathway)、MAPK信號通路(MAPK signaling pathway)、FoxO信號通路(FoxO signaling pathway)、PI3K-Akt信號通路(PI3K-Akt signaling pathway)、P53信號通路(P53 signaling pathway)。
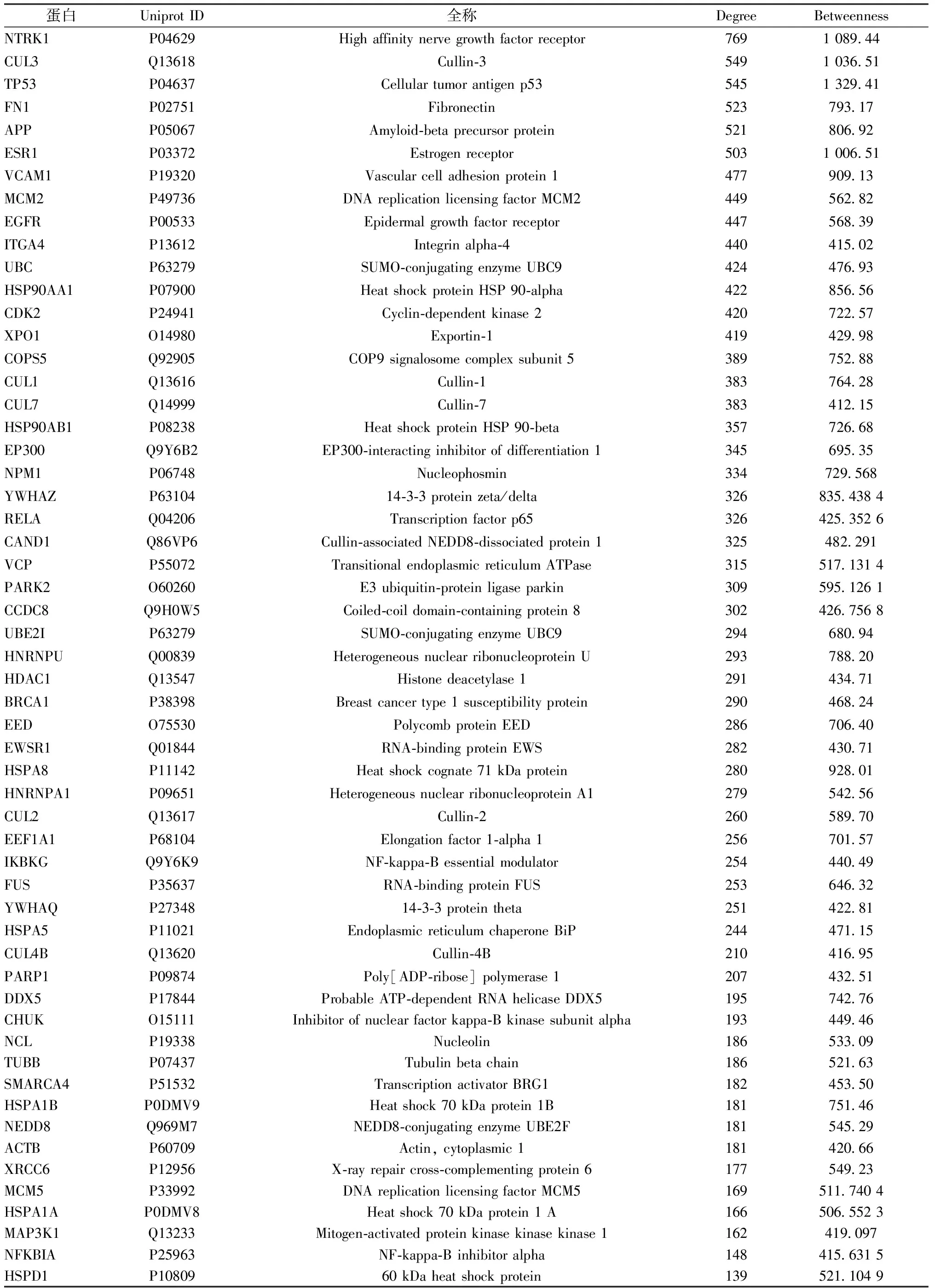
表2 PPI蛋白互作網絡關鍵靶點

圖4 核心靶點篩選策略示意圖

圖5 GO富集分析
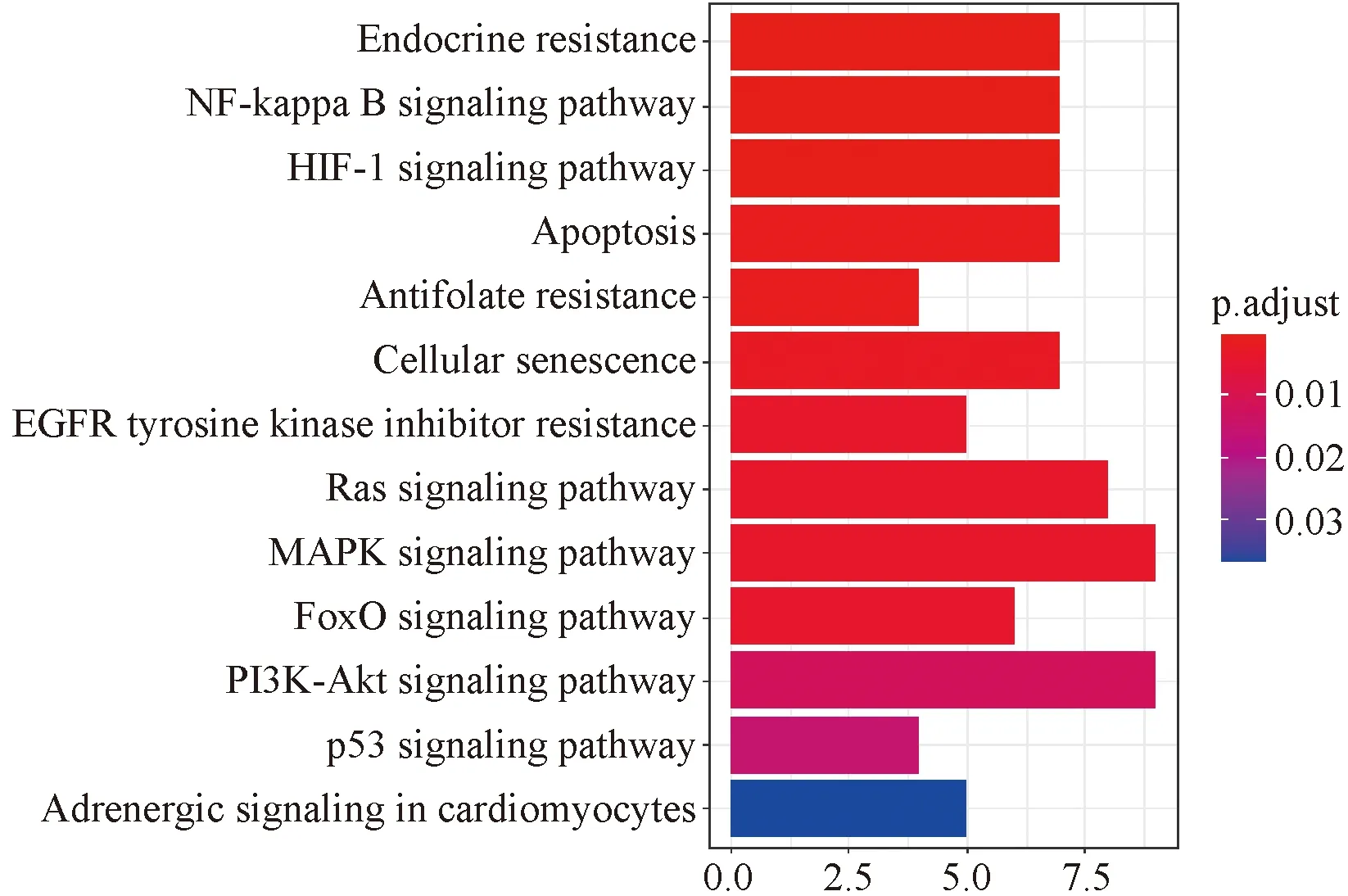
圖6 KEGG富集分析
2.6 KEGG網絡 網絡見圖7,藍色代表通路,紅色代表靶點,可知北沙參作用于金屬基質蛋白MMP-9、血管細胞黏附分子VCAM1、B型單胺氧化酶MAOB、絲裂原活化蛋白MAPK、血清高遷移率族蛋白IL1B、緊密連接蛋白CLDN4等多個靶點,通過NF-kappa B信號通路、HIF-1信號通路、Ras信號通路、MAPK信號通路、FoxO信號通路、PI3K-Akt信號通路、P53信號通路等進行協同調控來干預糖尿病。另外,節點面積越大,干預影響越大。
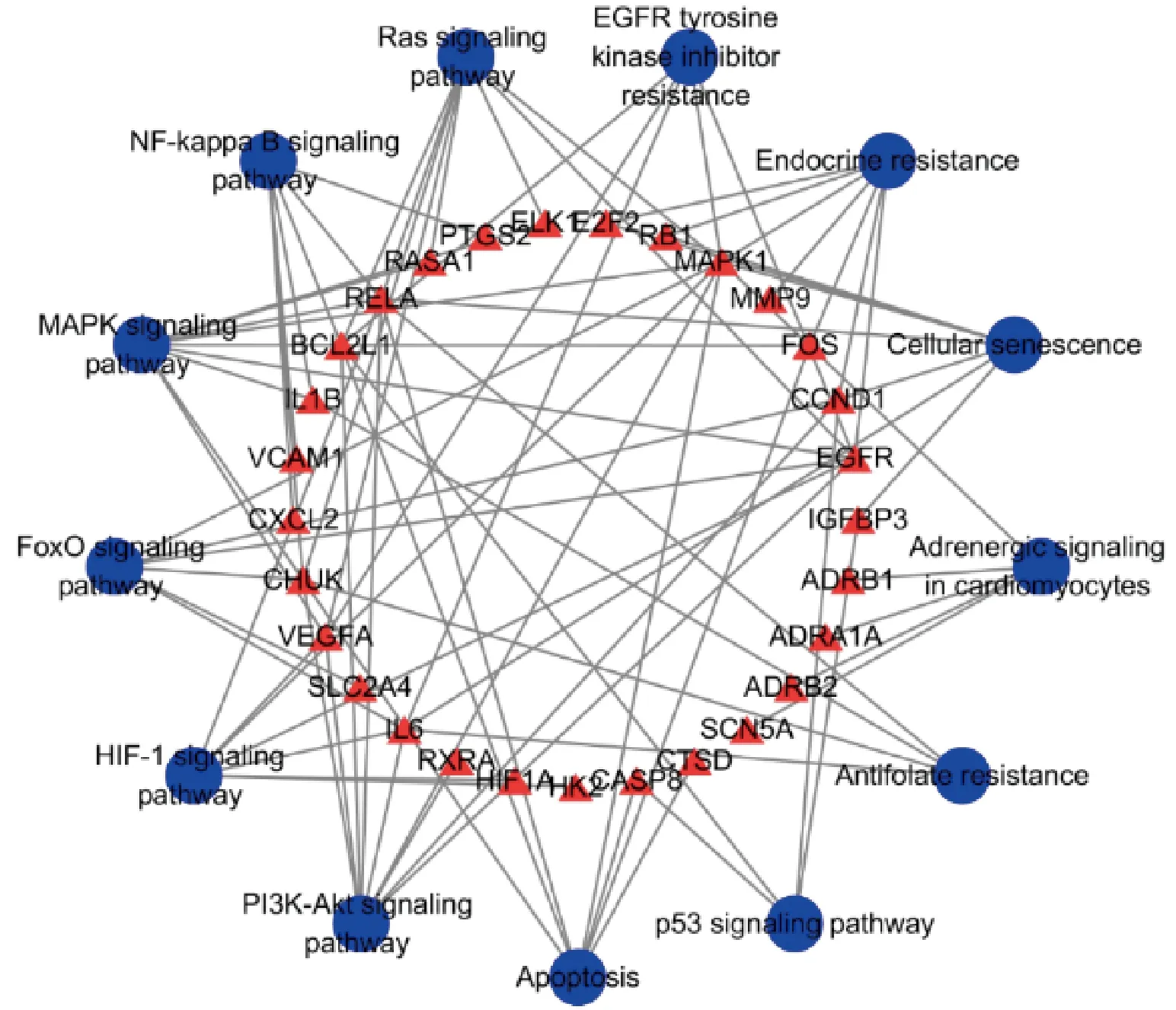
圖7 藥物-成分-靶點-通路-疾病網絡
2.7 活性成分與糖尿病關鍵靶點的分子對接 在KEGG信號通路中選取4個關鍵靶點作為靶點蛋白,分別是MAPK1、IL1B、NCOA2和PTGS1,代號(PDB ID)分別為4DEP、4IZ5、4p6x和1cqe,與主要活性成分進行分子對接,見圖8,與靶點蛋白的氫鍵結合力見表3。
槲皮素通過殘基ASP-337、THR-181、ALA-26和TYR-62與MAPK1蛋白質分子對接,VAL-233與IL1B蛋白質分子對接,ARG-558、GLY-547、GLU-748與NCOA2蛋白質分子對接,GLY-66、CYS-57和CYS-59與PTGS1蛋白質分子對接。豆甾醇與MAPK1之間無氫鍵,沒有分子對接,通過殘基NAG-403與IL1B蛋白質分子對接,VAL-538與NCOA2蛋白質分子對接,LYS-253、GLU-268與PTGS1蛋白質分子對接。β-谷甾醇與MAPK1之間無氫鍵,沒有分子對接,通過殘基ASN-229與IL1B蛋白質分子對接,ARG-558與NCOA2蛋白質分子對接,LEU-494與PTGS1蛋白質分子對接。前胡內酯通過殘基NAG-403和SER-213與IL1B蛋白質分子對接,LYS-151、ADP-900、GLU-33與MAPK1蛋白質分子對接,ARG-614、GLU-537與NCOA2蛋白質分子對接,GLY-214與PTGS1蛋白質分子對接。別異歐前胡內酯通過殘基TYR-310、AGR-308、ALA-325與IL1B蛋白質分子對接,ASP-30、GLU-12與MAPK1蛋白質分子對接,LYS-743、GLU-748與NCOA2蛋白質分子對接,ASP-497、ILE-498、GLN-479與PTGS1蛋白質分子對接。佛手素通過殘基NAG-403與IL1B蛋白質分子對接,THR-190與MAPK1蛋白質分子對接,ASP-549、ARG-558與NCOA2蛋白質分子對接,HIS-442、ARG-179與PTGS1蛋白質分子對接。異歐前胡素通過殘基ILE225與IL1B蛋白質分子對接,ARG-67、TYR-187、JYR-30與MAPK1蛋白質分子對接,GLY-547和ARG-558與NCOA2蛋白質分子對接,GLU-347與PTGS1蛋白質分子對接。異珊瑚菜素通過殘基GLU-217、VAL-233與IL1B蛋白質分子對接,LYS-117與MAPK1蛋白質分子對接,GLY-547、ARG-558、ASP-549與NCOA2蛋白質分子對接,PRO-514、SER-516、HIS-90與PTGS1蛋白質分子對接。

圖8 活性成分與靶點分子對接模型

表3 活性成分與靶點蛋白的氫鍵結合力
3 討論
本研究發現,北沙參8種活性成分有5 817個疾病靶點,其中58個與糖尿病的治療相關;可與3 320個疾病靶點產生直接或間接作用,不同靶點之間的相互聯系達82 802種,體現了其多成分、多靶點干預糖尿病的特點。
北沙參發揮治療糖尿病作用的成分可能為香豆素類、酚酸類和甾醇類。研究表明,香豆素類對小鼠2型糖尿病具有一定干預作用,對2型糖尿病相關的生化指標和組織病理具有一定的改善作用,其機制可能通過激活Akt或AMPK磷酸化下游底物,促進GLUT4轉位和葡萄糖轉運[21];酚酸類雖然不能直接降低血糖,但能夠顯著改善大鼠血管黏稠度,改善血脂代謝,從而降低糖尿病腎病的發病概率[22];甾醇類化合物可通過減弱自由基誘導的糖毒素來改善高血糖狀態,從而改善胰島素功能[23]。
PPI蛋白互作篩選出56個關鍵靶點,度值最高的是MAPK、IL1B、PTGS1、NCOA2。MAPK可通過激活外源胰島素從而調節胰島素水平來治療妊娠期糖尿病[24];IL1B能刺激胰島素分泌、增強胰島素的活性和促進葡萄糖轉運到胞漿,從而達到降低血糖的作用[25];NCOA2在脂肪代謝和糖代謝平衡方面有重要的作用,其多態性與2型糖尿病的發生相關[26];PTGS1與炎癥相關,糖尿病患者機體處于低度炎癥狀態,其程度與血糖高低呈正相關[27-28],四者能與北沙參活性成分進行分子對接,是其治療糖尿病的核心靶點。
KEGG富集表明,上述靶點主要集中在NF-kappa B信號通路、HIF-1信號通路、Ras信號通路、MAPK信號通路、FoxO信號通路、PI3K-Akt信號通路、P53信號通路等168條信號通路。在糖尿病的治療過程中,MAPK信號通路是與炎癥相關的信號通路;HIF-1是缺氧誘導因子,也是參與細胞應答缺氧基因的關鍵因子[29],通過調節葡萄糖轉運、控制糖酵解、促進糖異生從而影響葡萄糖穩態[30];脂肪酸、炎性因子和活性氧及相關靶蛋白可激活P53繼而導致胰島β細胞功能紊亂甚至凋亡[31],還可通過調節胰島素信號通路等多條途徑來干預胰島素抵抗[32]。由此可見,北沙參中的多種成分通過作用于多個靶點、調控多個信號通路來改善糖尿病及其并發癥。
綜上所述,本研究利用網絡藥理學初步闡述了北沙參干預糖尿病的潛在活性成分、作用靶點、發揮藥效的關鍵生物學通路,從分子水平揭示了可能機制。但上述結果只是預測,還需要通過藥理實驗作進一步驗證。

