血清IL-6、DD水平在預測高血壓患者腦出血風險中的作用
胡 兵,李 改,張會敏
(1.南陽市南石醫院檢驗科,河南 南陽 473000;2.新鄉醫學院,河南 新鄉 453003)
高血壓可誘發多種疾病,并可導致腦實質出血,即高血壓性腦出血(hypertensive intracerebral hemorrhage,HICH)。HICH屬臨床危重癥,約占所有類型腦出血的70%,有較高致殘率和致死率,預后不良[1]。探究HICH發生風險預測指標對降低HICH發生率有重要意義。有研究發現,HICH發病過程復雜,涉及炎癥、氧化應激、纖溶系統異常、細胞凋亡等多種機制[2-3]。白細胞介素-6(interleukin-6,IL-6)參與內皮細胞活化、黏附分子表達、炎癥細胞募集,與血壓水平有相關性[4]。D-二聚體(D-dimer,DD)是特異性纖維蛋白降解產物,其異常增加提示纖溶系統激活,參與腦血管疾病進展[5]。目前,臨床對血清IL-6、DD的研究多圍繞其與HICH病情嚴重程度開展,鮮有這2項指標預測高血壓患者發生腦出血風險的報道。本研究通過對400例高血壓患者進行5年隨訪,了解其腦出血發生情況,分析血清IL-6、DD在預測腦出血發生風險中的作用。
1 材料和方法
1.1 研究對象
選取2014年6月—2015年6月南陽市南石醫院400例高血壓患者,其中男215例、女185例,年齡(67.14±10.01)歲。納入標準:(1)符合《中國高血壓防治指南2010》[6]中的高血壓診斷標準;(2)入組前1個月未接受相關治療;(3)精神狀況、溝通能力正常,且同意配合隨訪。排除標準:(1)有腦出血發病史;(2)有外傷所致顱內出血史;(3)已出現嚴重高血壓并發癥;(4)合并惡性腫瘤;(5)精神異常。本研究獲南陽市南石醫院倫理委員會批準,所有患者均知情同意并簽署知情同意書。
1.2 方法
1.2.1 血清IL-6、DD檢測 采集所有患者靜脈血約5 mL,自然狀態放置20 min,分層后1 053×g離心15 min,收集血清。采用酶聯免疫吸附(enzyme-linked immunosorbent assay,ELISA)試驗測定血清IL-6、DD水平,嚴格根據試劑盒說明書操作,用Elx808自動酶標儀(美國BioTek公司)測定470 nm處吸光度值,根據標準曲線計算樣本中IL-6和DD水平。
1.2.2 腦出血診斷 對所有患者隨訪5年,參照《高血壓性腦出血》[7],根據電子計算機斷層掃描結果判斷是否發生HICH,包括出血性梗死和腦實質血腫。梗死灶邊緣發現點狀血或梗死灶中發現斑點狀、邊界模糊的高密度影為出血性梗死;梗死灶邊緣發現邊界清晰、均勻的高密度血腫,伴輕微或嚴重占位效應為腦實質血腫。按是否發生腦出血,將所有患者分為發生腦出血組和未發生腦出血組。
1.3 研究指標
統計所有患者一般資料并賦值,包括:年齡(連續變量)、性別(女=0,男=1)、體質量指數(body mass index,BMI)(連續變量)、吸煙(≥5支/d,且持續≥1年;否=0,是=1)、飲酒(酒精攝入量>30 g/周,且持續≥1年;否=0,是=1)、高鹽飲食(>8 g/d;否=0,是=1)、高脂飲食(每日脂肪熱量占比高于每日攝入總熱量的30%;否=0,是=1)、失眠(入睡潛伏期>30 min,夜間覺醒次數≥2次,早醒,睡眠質量降低,總睡眠時間<6.5 h,同時伴有日間功能障礙;無=0,有=1)、便秘[存在排便次數減少(每周<3次);排便困難;糞便呈干硬球狀,間或有排便不盡感,甚至需用手法輔助排便中2種及以上情況;無=0,有=1]、腦血管病家族史(無=0,有=1)、頸動脈粥樣硬化(彩色多普勒超聲檢查示頸動脈內膜中層厚度>1.0 mm;無=0,有=1)、腦微出血(磁共振成像檢查顯示T2WI上顯示低信號,存在圖像浮散效應;卵圓形或圓形;T2WI、T1WI圖像上無高信號表現;≥50%的低信號分布于腦實質;存在鈣化或鐵沉積、小血管留空影、海綿狀血管瘤等相似影像學表現;無=0,有=1)、糖尿病(煩渴多飲、多尿、多食、不明原因的體質量下降等典型糖尿病癥狀,餐后2 h血糖≥11.1 mmol/L,空腹≥7.0 mmol/L;無=0,有=1)、冠心病(心電圖出現有診斷意義Q波,或持續出現>1 d的演變損傷電流;無=0,有=1)、高脂血癥(三酰甘油>1.70 mmol/L,總膽固醇>5.72 mmol/L;無=0,有=1)、高尿酸血癥(血尿酸>420 μmol/L;無=0,有=1)、高血壓病程(連續變量)、高血壓分級[Ⅰ級:收縮壓為18.62~21.15 kPa(140~159 mmHg),舒張壓為11.97~13.17 kPa(90~99mmHg);Ⅱ級:收縮壓為21.28~23.81 kPa(160~179 mmHg ),舒張壓為13.30~14.50 kPa(100~109 mmHg);Ⅲ級:收縮壓>23.94 kPa(180 mmHg),舒張壓>14.63 kPa(110 mmHg);Ⅰ級=0,Ⅱ級=1,Ⅲ級=2]、服藥依從性(評價依據為Morisky服藥依從性量表[8],分數為0~8分,分數越高,表示服藥依從性越高;連續變量)、血清IL-6(連續變量)、血清DD(連續變量)。以上因素為自變量,以是否發生腦出血(否=0,是=1)為因變量,進行Logistic回歸分析。
1.4 統計學方法
采用SPSS 24.0軟件進行統計分析。呈正態分布的計量資料以±s表示,組間比較采用t檢驗。計數資料以例或率表示,組間比較采用χ2檢驗;采用Logistic回歸分析發生腦出血的危險因素。采用受試者工作特征(receiver operating characteristic,ROC)曲線評估血清IL-6、DD預測腦出血的效能。以P<0.05為差異有統計學意義。
2 結果
2.1 2組血清IL-6、DD水平及其他可能影響因素比較
經5年隨訪,400例高血壓患者失訪62例,完成隨訪的338例患者中,發生腦出血32例(9.47%)。發生腦出血組、未發生腦出血組年齡、性別、BMI、吸煙、飲酒、高鹽飲食、高脂飲食、失眠、便秘、腦血管病家族史、糖尿病、冠心病史、高脂血癥、高尿酸血癥、高血壓分級、服藥依從性比較,差異均無統計學意義(P>0.05);與未發生腦出血組比較,發生腦出血組頸動脈粥樣硬化、腦微出血所占比例及血清IL-6、DD水平較高(P<0.05),高血壓病程較長(P<0.05)。見表1。
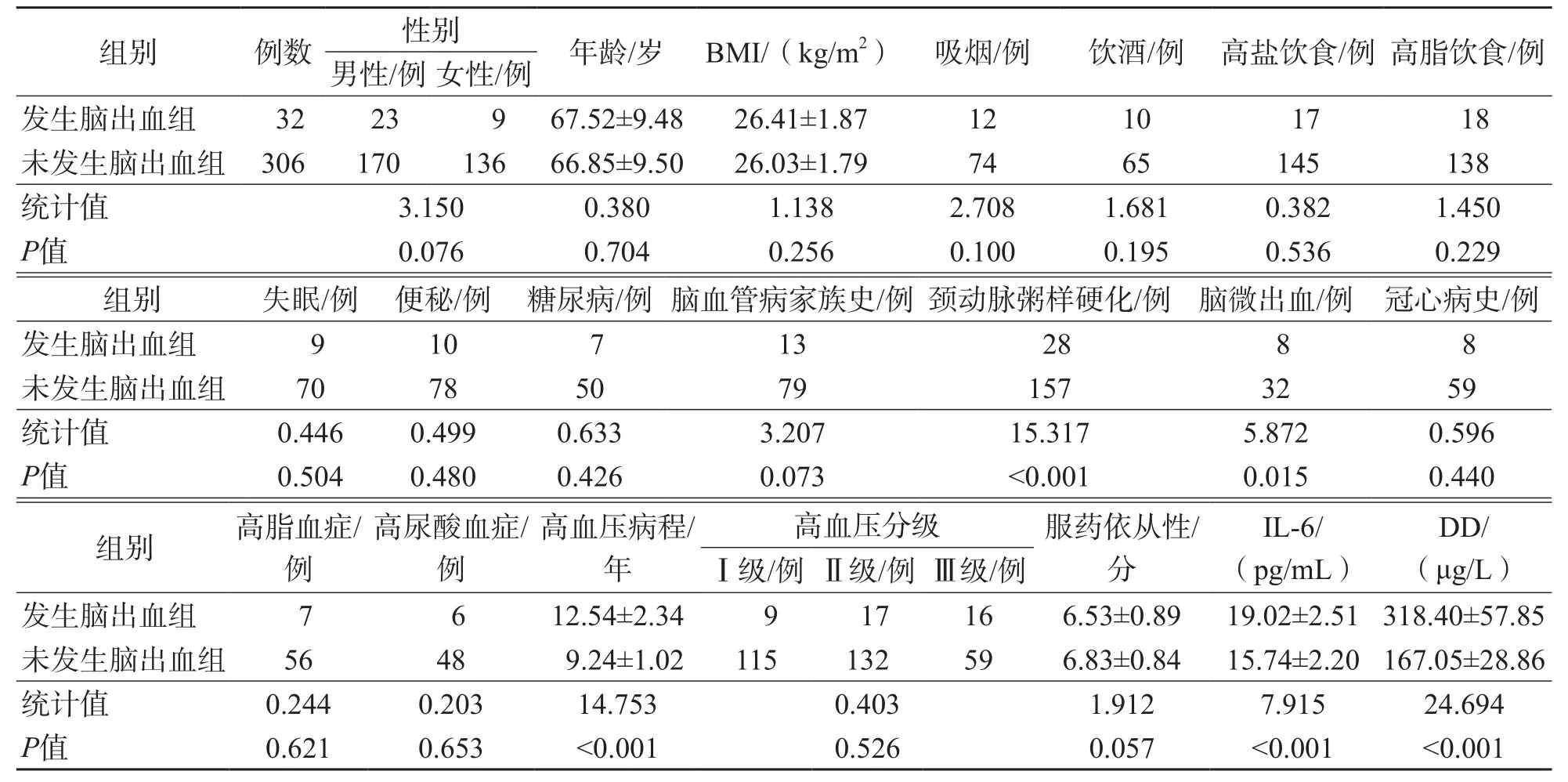
表1 2個組血清IL-6、DD水平及其他可能影響因素比較
2.2 高血壓患者發生腦出血的影響因素
Logistic回歸分析結果顯示,頸動脈粥樣硬化、腦微出血、高血壓病程、IL-6、DD均是高血壓患者發生腦出血的影響因素(P<0.05)。見表2。
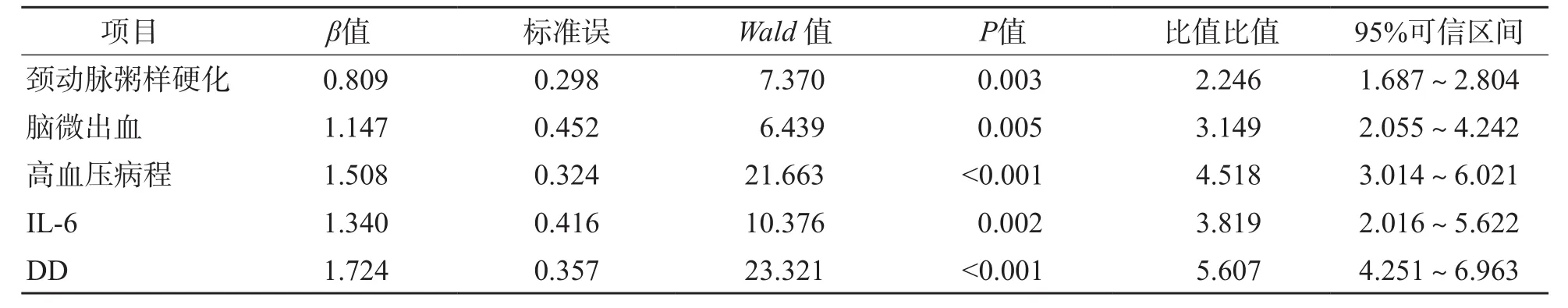
表2 高血壓患者發生腦出血的影響因素
2.3 血清IL-6、DD預測高血壓患者發生腦出血的效能
ROC曲線分析結果顯示,血清IL-6、DD預測高血壓患者發生腦出血的最佳臨界值分別為18.35 pg/mL、287.51 μg/L,2項指標單獨和聯合檢測預測高血壓患者發生腦出血的曲線下面積分別為0.706、0.731、0.795。見表3、圖1。

表3 血清IL-6、DD預測高血壓患者發生腦出血的效能
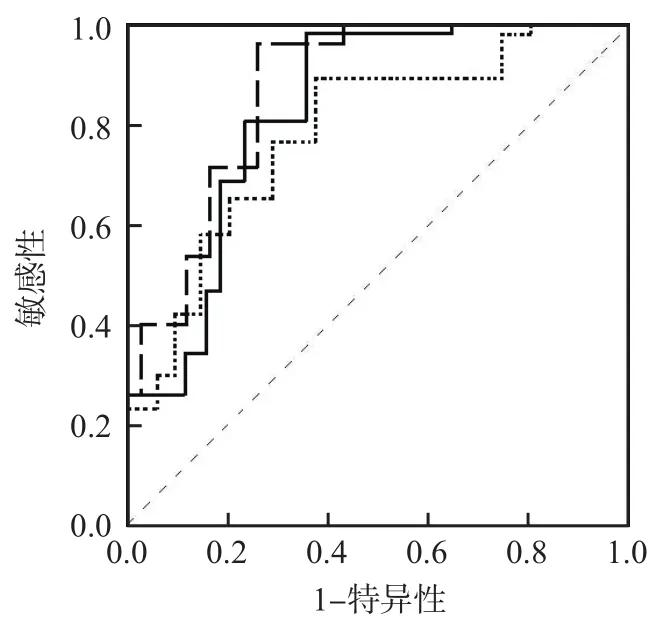
圖1 血清IL-6、DD預測高血壓患者發生腦出血的ROC曲線
3 討論
腦出血是非外傷性腦實質出血,占所有腦卒中的10%~20%[9]。高血壓是引發腦出血的常見基礎性疾病,HICH起病急、發展迅速、病情復雜,在及時采取有效治療措施同時,亟待探尋有效的實驗室指標預測HICH的發生風險,以制定針對性預防措施[10]。高血壓患者血壓驟升會導致腦動脈破裂,血腫占位效應、血腫形成可導致腦組織發生直接損傷或繼發性損傷,釋放血管活性物質導致顱內高壓、腦水腫、腦血流量、凝血纖溶系統改變;此外,血腫占位效應會激活周圍血管系統防御反應和全身系統炎癥反應,將已發生凋亡的細胞及細胞碎片清除[11-13]。因此,了解高血壓患者炎癥相關因子IL-6和凝血相關因子DD表達水平與腦出血發生的關系,對指導臨床預防HICH有重要意義。
本研究發現,發生腦出血組頸動脈粥樣硬化、腦微出血所占比例較未發生腦出血組高,血清IL-6、DD水平更高,高血壓病程更長;Logistic回歸分析結果顯示,上述指標均是發生腦出血的影響因素,提示除頸動脈粥樣硬化、腦微出血、高血壓病程等因素外,血清IL-6、DD水平異常也是腦出血發生的影響因素。頸動脈粥樣硬化與炎癥反應關系密切,粥樣斑塊中存在多種炎癥細胞,可能參與了腦出血進程,且斑塊可導致血管管腔因狹窄而發生結構性改變,減慢了局部血流,增加了腦出血的發生風險。腦微出血是以微小出血為主要表現的腦部微小血管病變。LEASURE等[14]發現,腦出血有級聯反應,即便僅有1處小血管破裂,也可能誘發臨近多處正常小血管破裂。長期高血壓會增加動脈血管壁厚度及僵硬度,并降低其順應性,導致動脈硬化和顱內小動脈破裂。IL-6是一種免疫及炎癥相關促炎細胞因子,其水平異常升高可活化巨噬細胞、內皮細胞、多型核細胞分泌內皮素-1樣免疫激活物,導致血管收縮,損傷神經系統,增加腦血管壁通透性,破壞血腦屏障,增加腦出血風險。有研究發現,神經元IL-6前體已發現存在于大腦、海馬神經元中,且作為分泌型信號分子,有較強的淋巴細胞趨化活性,介導免疫調節,參與HICH疾病進展[15]。DD是繼發性纖溶亢進特異性代謝產物,其水平異常升高是機體繼發性纖溶增強、高凝狀態的體現,易形成血栓傾向。此外,血清DD水平升高可誘導單核細胞合成并分泌IL-6、纖溶酶原激活抑制物等因子,引發凝血亢進,并增加血栓形成風險,使局部血管壁纖維蛋白沉積過多,進而導致管壁內膜增厚、硬化、甚至玻璃樣變。董蔚蔚等[16]發現,腦出血患者血清DD水平顯著上升,與血腫量、中線移位距離等顯著相關,且是預后不良的獨立危險因素,提示DD在腦出血發生、發展過程中有較高的參與度。
本研究ROC曲線分析結果顯示,血清IL-6、DD水平預測高血壓患者發生腦出血的最佳臨界值分別為18.35 pg/mL、287.51 μg/L,2項指標單獨及聯合預測高血壓患者發生腦出血的曲線下面積分別為0.706、0.731、0.795,提示2項指標聯合檢測預測效能高于單獨檢測。一般情況下,血清IL-6水平較穩定,有研究發現,IL-6除可以反映高血壓炎性程度外,同樣可作為高血壓腎病、高血壓心臟病的預測指標[17-19]。血清IL-6、DD聯合檢測可有效彌補IL-6特異性不足的缺陷,提高預測價值。此外,血液學指標檢測有簡單、快速的優勢,成本低,患者接受度也更高。臨床在治療高血壓時,需加強對血清IL-6、DD水平的監測,評估腦出血發生風險,及時調整治療策略,制定預防措施,以降低HICH的發生率。
綜上所述,血清IL-6、DD聯合檢測對高血壓患者發生腦出血有預測作用,可為臨床預防腦出血事件的發生提供參考。然而,本研究受到客觀條件限制,隨訪時間較短,難以掌握更長時間內高血壓患者腦出血發生情況,在今后的研究中將加以改進。

