個體化預測胃結直腸癌患者術后下肢靜脈栓塞的風險及列線圖模型的建立
李秀萍 葛智慧
下肢靜脈栓塞(lower deep venous thrombosis,LDVT)是臨床腫瘤外科術后嚴重的并發癥之一,多是由于惡性腫瘤、術中血管創傷、術后長期臥床休息等引起血液在血管內出現異常凝結,嚴重者血栓脫落可并發肺栓塞,危及生命[1]。LDVT不僅增加了患者的痛苦,同時也增加了治療難度[2]。胃結直腸癌(gastrocolorectal cancer,GC)是一種常見的消化道惡性腫瘤,近年來發病率不斷增加,與傳統外科切除手術相比,腹腔鏡微創治療技術憑借其創傷微小、出血較少、術后恢復時間較短等特點現逐漸得到GC患者與臨床醫師的廣泛認可[3]。然而隨著GC患者腔鏡手術的不斷增加,腹腔鏡術后LDVT等并發癥的報道也逐年增加,影響患者肢體基本功能的恢復,嚴重者可能引發腎衰竭等并發癥[4]。GC根治術后并發LDVT不僅降低了疾病的治療效果,增加了痛苦與治療費用,同時嚴重影響了患者預后,因此GC患者臨床資料中應注重LDVT的預防[5]。有關資料顯示,腫瘤分期、年齡、呼吸衰竭等因素可能會導致大腸癌患者血液凝集狀態發生改變,術后并發LDVT的概率明顯增加[6]。然而目前對于GC患者術后并發LDVT的危險因素研究較少,為此,本研究選取我院2018年1月至2020年11月收治的120例GC患者為研究對象,探討GC患者術后并發LDVT的危險因素并建立相應的列線圖預測模型,為患者預后提供依據。
1 資料與方法
1.1 研究對象
回顧性分析我院2018年1月至2020年11月收治的120例GC患者的病例資料,根據患者術后是否發生下肢靜脈栓塞將患者分為發生組(n=10)和未發生組(n=110)。下肢靜脈栓塞的診斷均由下肢深靜脈造影及多普勒超聲確診。納入標準:①經病理診斷為胃、結直腸癌的患者[7];②均行腹腔鏡下根治術;③患者術前肝腎功能無異常,凝血功能無異常;④入院后未進行預防性抗凝治療。排除標準:①GC為良性,不需行根治術治療的患者;②合并其他惡性腫瘤患者;③因故長期服用可影響凝血功能的藥物;④治療前已存在不同類型靜脈栓塞患者;⑤病理資料及回訪記錄不全患者。
1.2 觀察指標
調取并回顧性分析所有納入患者的一般資料,包括性別、年齡、BMI、高血壓史、高脂血史、糖尿病史、冠心病史、靜脈栓塞史、腫瘤分期、腫瘤壓迫、術中出血量、輸血、放化療史、溶栓治療史、臥床時間、血管過度暴露、術后止血藥應用、術中并發癥、靜脈穿刺次數、呼吸系統疾病及術中感染等信息。通過對比下肢靜脈栓塞發生組與未發生組患者以上指標的差異,分析其獨立風險因素。
1.3 統計學分析
所有患者數據應用SPSS 20.0軟件進行納入并統計分析,計數資料均用例數表示,采用卡方檢驗,P<0.05表示數據差異有統計學意義。采用Logistic回歸對獨立風險因素進行篩選,采用R(R3.6.0)軟件對篩選出的獨立危險因素建立列線圖模型,并應用rms程序包和Bootstrap法構建驗證集模型對列線圖預測模型進行驗證,計算一致性指數(C-index)、制作ROC曲線。
2 結果
2.1 兩組基本信息資料單因素分析
兩組患者中年齡、高血壓史、高脂血史、糖尿病史、冠心病史、靜脈栓塞史、腫瘤壓迫、術中出血量、輸血、溶栓治療史、臥床時間、血管過度暴露、術后止血藥應用、術中并發癥、靜脈穿刺次數及術中感染的數據差異有統計學意義(P<0.05),見表1。
2.2 多因素Logistic回歸分析結果
根據GC患者術后是否發生LDVT將患者分為發生組與未發生組,通過一般基本信息資料對比結果,對年齡、高血壓史、高脂血史、糖尿病史、冠心病史、靜脈栓塞史、腫瘤壓迫、術中出血量、輸血、溶栓治療史、臥床時間、血管過度暴露、術后止血藥應用、術中并發癥、靜脈穿刺次數及術中感染等數據作二元Logistic回歸分析,結果表明:年齡、高血壓史、糖尿病史、冠心病史、腫瘤壓迫、術中出血量、溶栓治療史、血管過度暴露、術后止血藥應用及術中并發癥的P值大于0.05,因此予以剔除,篩選出高脂血史(OR=2.924,95%CI:2580~8.730)、靜脈栓塞史(OR=2.041,95%CI:1.131~7.536)、輸血(OR=2.435,95%CI:1.152~4.845)、臥床時間(OR=1.382,95%CI:2.499~6.087)、靜脈穿刺次數(OR=1.495,95%CI:2.339~5.169)、術中感染(OR=3.024,95%CI:1.340~6.898)為胃結直腸癌患者術后是否發生LDVT的獨立危險因素,且數據差異具有統計學意義(P<0.05),見表2。
2.3 個體化預測GC患者術后下肢靜脈栓塞的風險模型的建立與驗證
本研究基于篩選出的獨立危險因素建立了預測GC患者術后發生下肢靜脈栓塞的列線圖模型。并通過將建模集原始數據重復抽樣1000次后(Bootstrap 法)對模型進行內部驗證,對比建模集與驗證集差異。
結果顯示:建模集和驗證集的C-index指數分別為0.837(95%CI:0.790~0.884)和0.828(95%CI:0.785~0.871);兩組的校正曲線均與標準曲線擬合較好,見圖1;兩組ROC曲線下面積(AUC)分別為0.837和0.828,見圖2,證明本次模型具有良好的預測精準度。
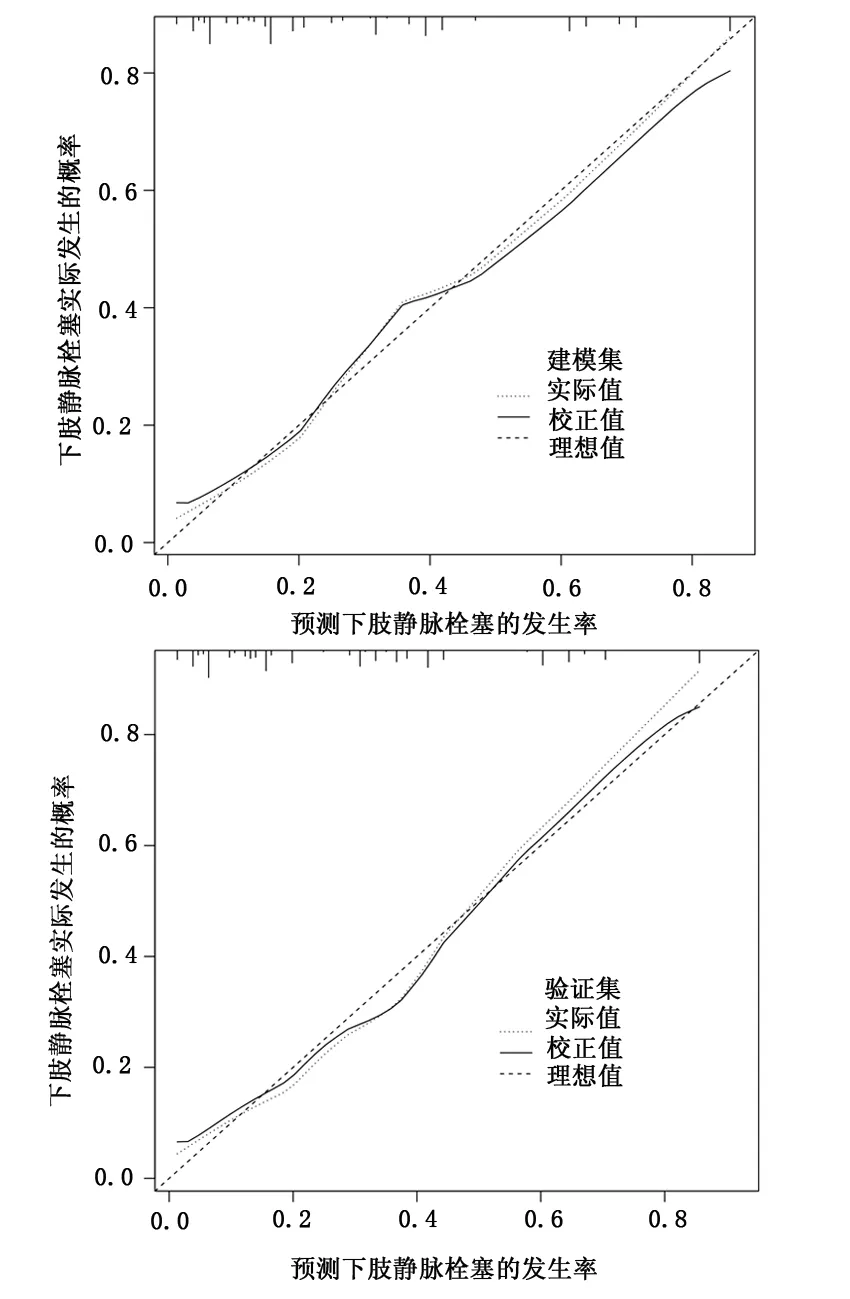
圖1 列線圖模型的校正曲線驗證
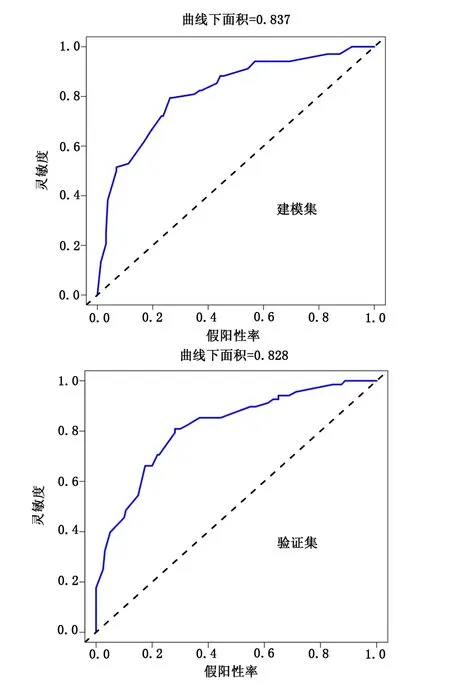
圖2 列線圖模型的ROC曲線驗證
3 討論
現代醫學研究發現,LDVT的發生主要與3大因素有關,即血液高凝集狀態、靜脈血管壁的損傷以及血液流變學狀態,近年來的研究結果逐漸證實LDVT的上述機制[8]。近年來腹腔鏡手術數量不斷增加,越來越多的GC患者選擇腹腔鏡手術治療,腹腔鏡手術雖創傷較小,但由于術中建立氣腹以及腹壓增加,使GC患者靜脈回流顯著減慢,增加了患者發生LDVT的風險,國內外文獻報道發生率高達36%,LDVT一旦發生可能危及生命[9]。我國LDVT的發生率雖低于西方發達國家,但生活方式的不斷改變也逐漸增加了LDVT的發生率,成為腫瘤外科患者健康殺手之一[10]。因此,分析并找出影響LDVT形成的危險因素并在早期干預,對降低LDVT發生率具有重要意義。
本研究采用單因素和多因素Logistic回歸分析法篩選出存在高脂血史、靜脈栓塞史、術中存在輸血、臥床時間≥10天、靜脈穿刺次數≥5次、存在術中感染為GC患者術后是否發生LDVT的獨立危險因素(P<0.05)。根據流行病學數據[11]統計,GC的發生人群多為高齡,患者自身合并高血壓、高血脂、心臟病等多種基礎病癥。老年患者的血管逐漸趨于老化,血管壁彈性較差,如若再患有高脂血癥,將使得血管中存在紅細胞、纖維蛋白及血小板異常聚集等情況,嚴重影響患者血液流通,極易引發靜脈栓塞的發生[12]。本研究中,高齡、高血壓等因素未納入獨立風險因素,可能與樣本量較小有關,后期需進一步加大樣本進行驗證,但高脂血癥普遍存在于發生組患者中(P<0.05),與以往研究結果一致。存在既往靜脈栓塞史,普遍被認為是GC患者發生LDVT的重要危險因素[13]。有數據顯示,LDVT患者中存在19%的患者存在靜脈栓塞史[14],其發生概率是無靜脈栓塞史患者的8倍,同時,5年內LDVT再發生率高達26%[15],對患者預后有著極其嚴重的影響。術中因出血過多等因素進行輸血,作為GC患者發生LDVT的獨立風險因素,可能與血庫中的存血顆粒及細胞碎片較多、血液粘稠度高有關[16],上述問題均會促進血管中血栓的形成,從而發生LDVT。GC患者治療后,常因限制行動而臥床時間長,有研究[17]指出,臥床時間越長,對患者下肢血液循環影響越重,血液常淤積在下肢,回流速度慢甚至無法回流,極易引發LDVT的發生。本研究中,臥床時間大于10天的患者發生LDVT幾率是臥床時間小于10天的2.328倍,與既往研究一致。患者在術后一段時間內禁止飲食,體液不斷減少,血液逐漸形成高凝狀態,同時,為供給患者營養,多次行靜脈穿刺,造成血管內壁的損害。有研究[18]顯示,多次的靜脈穿刺,極易損傷血管內皮,使膠原纖維和凝血因子暴露及釋放,從而促使血栓的形成。術中并發感染,同樣也是發生LDVT的危險因素。有隨機試驗結果[19]顯示,發生感染時,機體大量分泌炎性物質,激活瘤體細胞和單核細胞,使血液血流狀態發生改變,導致LDVT的發生。
基于以上篩選出的獨立危險因素,建立了預測GC患者發生LDVT的列線圖模型,同時為驗證預測模型的準確性,采用內部驗證的方式建立驗證集,對模型進行了進一步的預測效能檢驗,結果顯示建模集和驗證集的C-index指數分別為0.837(95%CI:0.790~0.884)和0.828(95%CI:0.785~0.871),兩組ROC曲線下面積(AUC)分別為0.837和0.828,校正曲線均與標準曲線擬合較好。因此本研究中構建的列線圖模型可清晰的反映GC患者發生LDVT的危險因子的影響程度,具有使用方便、直觀連續的優勢。患者及醫務工作者可根據列線圖中各項危險因素進行轉換,獲取各危險因素的相應賦分值并計算總分值,個體化預測GC患者發生LDVT的概率,進而指導臨床。
綜上所述,高脂血史、靜脈栓塞史、術中存在輸血、臥床時間≥10天、靜脈穿刺次數≥5次、存在術中感染為GC患者術后是否發生LDVT的獨立危險因素(P<0.05),基于危險因素建立的列線圖模型可有效預測和量化GC患者術后發生LDVT的風險,有助于改善GC患者的預后。本次研究的局限性在于:①單中心小樣本量的試驗,并沒有在多中心進行廣泛的臨床試驗,較為局限;②危險因素對GC患者術后發生LDVT的影響機制尚未完全明確,故本次護理模型尚需納入更大樣本、更明確的影響因子的研究予以進一步驗證。

