抑制PERK/e IF2α通路對七氟醚誘發POCD大鼠內質網應激和α-突觸核蛋白的影響
苗亞飛,楊木強,司馬靚杰,閆俊強
(1.河南科技大學第一附屬醫院麻醉科,河南 洛陽 471003;2.河南科技大學第一附屬醫院神經內科,河南 洛陽 471003)
雖然七氟醚是一種穩定、安全的麻醉誘導劑,但是最近研究發現七氟醚會損傷神經元,誘發術后認知功能障礙(Postoperative cognitive dysfunction,POCD),甚至導致永久性的神經功能損傷以及帕金森癥等[1],α-突觸核蛋白(α-Syn)是參與帕金森的重要蛋白,在POCD中也起著促進作用[2]。目前研究認為海馬神經元受損是患者神經功能、記憶力減退的重要原因,而由各種原因引起的氧化應激反應和炎性反應會誘發海馬神經元內質網應 激(Endoplasmic reticulum stress,ERS),進 而 導致神經元凋亡和功能障礙[3]。PERK/eIF2α通路是調節ERS的關鍵通路,并且有研究顯示麻醉會引起PERK水平的升高,并且抑制ERS反應可緩解麻醉小鼠的POCD,并抑制神經元細胞凋亡[4]。本文主要分析抑制PERK/eIF2α通路對七氟醚誘發大鼠POCD、內質網應激和α-Syn的影響。
1 材料與方法
1.1 材料和儀器 Sprague-Dawley(SD)大鼠(清潔級,雄性。20周,350~400 g,河南科技大學實驗中心)。七氟醚(Abbvie公司,美國)。PERK/eIF2α通路抑制劑GSK2606414(Selleck公司,美國)。110 SE型小動物麻醉機(Ohmeda公司,美國)。水迷宮視頻跟蹤分析系統(泰盟科技有限公司,中國)。TUNEL凋亡試劑盒(碧云天公司,中國)。anti-PERK、anti-eIF2α、anti-Caspase-3、anti-CHOP、anti-α-Syn(Abcam公司,美國)。PVDF膜(Bio-Rad公司,美國)。ECL試劑盒(Amersham,美國)。顯微鏡(Olympus,日本)。
1.2 分組、建模和干預方法 24只SD大鼠隨機分為對照組、七氟醚組和GSK2606414組(N=8)。七氟醚組和GSK2606414組參考文獻通過七氟醚建立SD大鼠POCD模型[5],主要步驟如下:SD大鼠禁食禁飲8 h后放置在連接麻醉機的大小為60 cm×30 cm×25 cm透明麻醉箱內,另一側通道連接連接氣體監測儀。七氟醚的麻醉濃度為2%,氧流量為3 L/min,連續4 h。對照組大鼠進行同樣的處理但不吸入七氟醚。GSK2606414組大鼠根據參考文獻[6]使用GSK2606414進行干預,在吸入七氟醚6 h前用GSK2606414灌胃,劑量為150 mg/kg,對照組和模型組給予等量的生理鹽水灌胃。吸入七氟醚后4 h進行水迷宮實驗和跳臺實驗,然后腹腔注射戊巴比妥(劑量為2 mL/kg,濃度為20 g/L)麻醉并處死大鼠,取出海馬體進行后續試驗。
1.3 Western blot檢測蛋白 在液氮下將海馬體研磨并用預冷的PBS緩沖液洗滌,裂解后萃取總蛋白,將蛋白樣本與角質酶II混合并進行SDSPAGE分離蛋白,經轉膜后封閉,在PDVF膜中加入anti-PERK、anti-eIF2α、anti-Caspase-3、anti-CHOP、anti-α-Syn(1:500稀釋)在4°C孵育過夜,然后加入1∶5 000稀釋的二抗(1 h,室溫)。ECL試劑盒可視化蛋白條帶,以GAPDH為內參對蛋白條帶的灰度進行定量。紋狀體中α-突觸核蛋白水平檢測方法與此相同。
1.4 水迷宮實驗和跳臺實驗檢測神經功能和學習能力 通過水迷宮視頻跟蹤[7]和跳臺實驗[8]檢測進行檢測。對于水迷宮實驗,逃避潛伏期越長、穿越平臺次數越低提示神經功能損傷越嚴重。對于跳臺實驗,學習期和實驗期錯誤次數越高、潛伏期越長提示學習能力越差。
1.5 TUNEL染色檢測凋亡 將海馬體組織固定并透化,根據試劑盒說明書進行操作,然后將其放置于TUNEL溶中,在37℃下孵育1 h。洗滌后加入Converter-POD溶液孵育30 min。之后依次進行顯色、DAPI染色細胞核,然后進行封片。通過檢測熒光反應計算凋亡率。
1.6 統計學處理 所有實驗設立3個平行實驗。數據以平均值±標準偏差(SD)表示。 統計分析使用SPSS 19軟件。 進行單因素方差分析,兩兩比較使用LSD-t檢驗。 統計學顯著性表示為P<0.05。
2 結果
2.1 GSK2606414對PERK/eIF2α通路的影響 七氟醚組的PERK和eIF2α水平顯著高于對照組(P<0.05),GSK2606414組的PERK和eIF2α水平顯著低于七氟醚組(P<0.05),提示GSK2606414可有效抑制PERK/eIF2α通路,見表1、圖1。
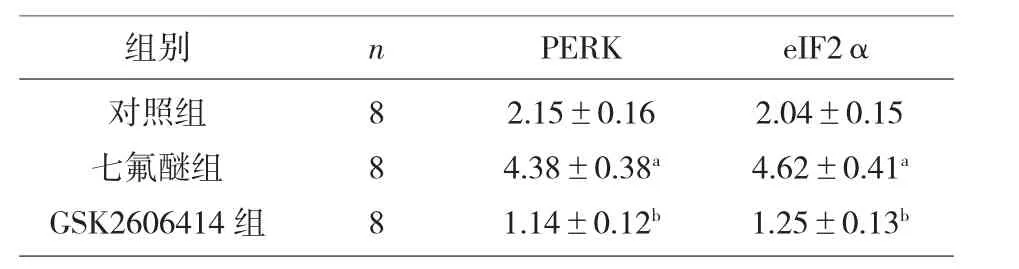
表1 各組PERK/e IF2α通路比較
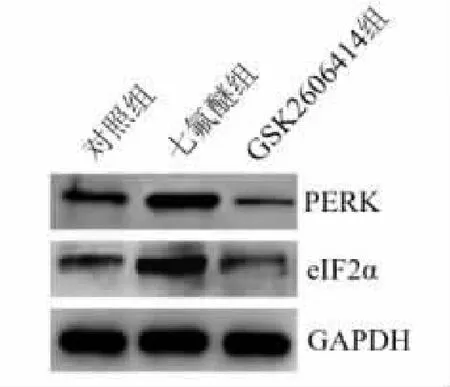
圖1 Westernblot檢測GSK2606414對PERK/e IF2α通路的影響
2.2 GSK2606414對神經功能和學習能力的影響與對照組比較,七氟醚組的逃避潛伏期、錯誤次數和潛伏期顯著升高而穿越平臺次數顯著降低(P<0.05),GSK2606414組的逃避潛伏期、錯誤次數和潛伏期顯著低于七氟醚組穿越平臺次數顯著高于七氟醚組(P<0.05),見表2。
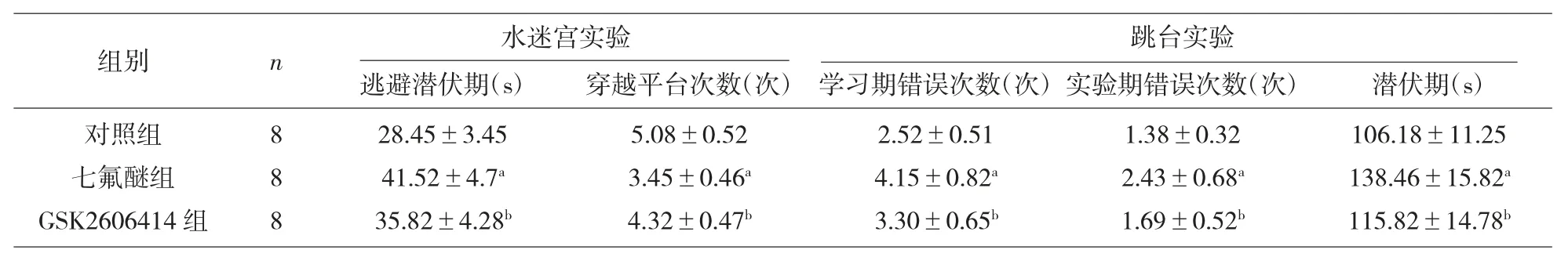
表2 各組水迷宮實驗結果和跳臺實驗結果比較
2.3 GSK2606414對海馬神經元凋亡的影響 如圖2,藍色熒光為細胞核,綠色熒光為凋亡細胞。對照組海馬神經元凋亡率為(1.25±0.35)%,七氟醚組的凋亡率為(16.23±2.85)%,顯著高于對照組,GSK26 06414組凋亡率為(7.83±1.68)%,顯著低于七氟醚組(P<0.05)。

圖2 TUNEL檢測GSK2606414對海馬神經元凋亡的影響
2.4 GSK2606414對內質網應激和α-Syn水平的影響 七氟醚組海馬體組織的CHOP、Caspase-3和α-Syn水平顯著高于對照組(P<0.05),GSK2606414組的CHOP、Caspase-3和α-Syn水平顯著低于七氟醚組(P<0.05),見表3、圖3。
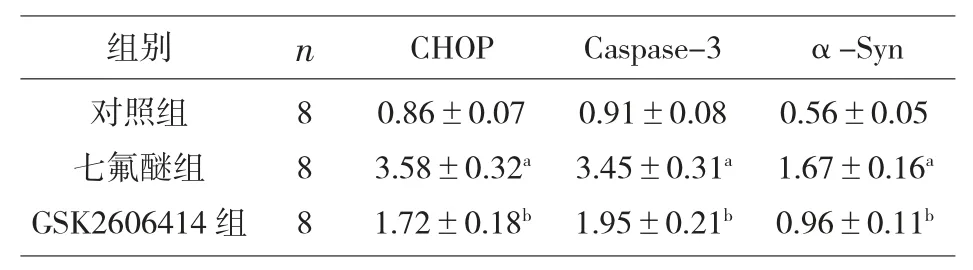
表3 各組內質網應激和α-S y n水平比較

圖3 Western blot檢測GSK2606414對內質網應激和α-Syn水平的影響
3 討論
近年來,外科手術得到了迅猛發展,患者對于手術安全性和舒適性的也要求提高,七氟醚具有快速誘導麻醉、對肝和腎功能影響小及穩定的血液動力學等特點,在麻醉中廣泛使用。但是過往研究已經發現了七氟醚在中樞神經系統中的作用,可能會出現POCD,甚至影響兒童的智力和記憶力,引起帕金森癥等,分析POCD的發病機制具有重要意義[9]。
海馬體神經元的損傷是引起術后認知功能障礙的主要原因,研究顯示七氟醚會引起海馬體神經元凋亡,從而引起POCD[10]。氧化應激反應在其中起著重要作用,研究顯示七氟醚可以通過調節氧化應激引起海馬體神經元凋亡[11]。PERK/eIF2α通路與氧化應激密切相關,研究顯示PERK/eIF2α通路的激活與POCD有關[12]。七氟醚也具有激活PERK/eIF2α通路的作用[13],據此我們推測七氟醚可能通過PERK/eIF2α通路參與POCD的發生。在本次研究中,我們通過吸入七氟醚建立大鼠POCD模型,然后通過GSK2606414抑制PERK/eIF2α通路。結果顯示模型組大鼠海馬體中PERK/eIF2α水平顯著升高,而GSK2606414可以顯著一直POCD大鼠的PERK/eIF2α通路。此外,七氟醚組的PERK/eIF2神經功能和學習能力降低,海馬體的細胞凋亡率,GSK2606414組神經功能和學習能力高于七氟醚組,海馬體的細胞凋亡率低于七氟醚組。這提示在七氟醚引起的POCD大鼠模型中,PERK/eIF2α通路被激活,而抑制PERK/eIF2α通路可以緩解七氟醚對海馬體凋亡和神經功能、學習能力的影響。
為進一步分析PERK/eIF2α通路在七氟醚引起的POCD大鼠模型中的作用機制,檢測了ERS和α-Syn的水平。PERK/eIF2α通路可以直接調節ERS,ERS是是細胞對外界壓力或損傷的早期或初始反應,并與神經元損傷或死亡有關,如阿爾茨海默癥、帕金森癥等,研究顯示了氧化應激引起的ERS與老年患者POCD[14]。而PERK/eIF2α通路的激活也會引起α-Syn的上調,也會參與ERS[15]。本次研究結果顯示與對照組比較,七氟醚組的α-Syn和質網應激標志蛋白CHOP、Caspase-3水平顯著升高,GSK2606414組α-Syn、CHOP、Caspase-3水平顯著低于七氟醚組。有研究顯示七氟醚會通過調節PERK/eIF2α通路引起超結構ER交替和ER應激活化,而ERS會促進CHOP、Caspase-3蛋白的升高,引起凋亡[16]。α-Syn與腦部神經元的損傷密切相關,研究顯示α-Syn可以倍七氟醚和PERK誘導,抑制ERK/eIF2α通路會減少α-Syn的表達保護腦神經[17-18]。本次研究結果顯示抑制PERK/eIF2α通路可以抑制七氟醚引起的海馬體ERS和α-Syn的表達。
綜上所述,七氟醚會引起PERK/eIF2α通路、ERS和α-Syn的上調,而抑制PERK/eIF2α通路會顯著抑制ERS和α-Syn的表達,緩解海馬體神經元的凋亡。但是關于吸入七氟醚通過PERK/eIF2α通路調節ERS和α-Syn的機制仍需要進一步研究。

