動態適形弧放射治療與容積旋轉調強放射治療在非小細胞肺癌立體定向放射治療中的劑量學差異
魏鵬,葉書成,劉衛東,楊君東,王夢雅,呂敏,王麗芳(通信作者)
1 濟寧醫學院附屬醫院腫瘤科(山東濟寧 272000);2 濟寧醫學院臨床醫學院(山東濟寧 272067)
肺癌是臨床上最常見的惡性腫瘤。我國每年新發肺癌病例已近80萬例,而死亡病例高達60余萬例,該病已成為我國發病率與病死率均最高的癌癥[1-2]。有研究顯示,約85%的肺癌為非小細胞肺癌[3]。臨床對早期非小細胞肺癌患者首選根治性手術治療,但對于不能手術或不愿手術的患者,放射治療則是標準的治療手段[4]。近年來,立體定向放射治療(stereotactic body radiation therapy,SBRT)已成為早期非小細胞肺癌患者的常用治療方法,可精確地消融腫瘤,同時最小化危及器官的損傷。目前,臨床主要采用容積旋轉調強放射治療(volumetric modulated arc therapy,VMAT)技術進行SBRT[5-7],但VMAT實施過程中多葉準直器、患者運動與機架角度等相互影響可導致治療精度的不確定性。近年來,動態適形弧放射治療(dynamic conformal arc therapy,DCAT)被廣泛用于各種腫瘤的治療中[8-10]。本研究選取15例非小細胞肺癌患者,比較了DCAT與VMAT在非小細胞肺癌SBRT中的劑量學差異,以期為非小細胞肺癌患者放射治療技術的臨床選擇提供參考。
1 資料與方法
1.1 一般資料
選取2016年1月至2020年1月于濟寧醫學院附屬醫院接受放射治療的15例非小細胞肺癌患者,其中男8例,女7例;年齡52~86歲,平均(68±11)歲;左側肺癌5例,右側肺癌10例;靶區體積5.46~76.11 cm3,平均(32.68±22.73)cm3;所有患者均經病理檢查確診,無縱隔淋巴結轉移。
1.2 方法
1.2.1 CT 模擬定位與靶區勾畫
所有患者均取仰臥位,雙手臂交叉抱肘放于額前,使用立體定向固定體架、真空負壓袋和腹壓板(腹壓板壓至腰肋三角下30 mm 左右)進行體位固定;在患者平靜呼吸下使用荷蘭飛利浦公司大孔徑CT 模擬定位機進行全時相(10個時相)四維CT 掃描,掃描范圍從環狀軟骨至第12胸椎,包括全胸廓的所有區域,掃描厚度和層間距均為3 mm,掃描結束后將CT 圖像以Dicom 格式傳輸至Monaco5.11.03治療計劃系統;最終由高年資放射治療醫師在肺窗下勾畫各時相的腫瘤靶區(gross target volume,GTV)并生成內靶區(internal target volume,ITV),將ITV 外放5 mm 生成計劃靶區(plan target volume,PTV),并勾畫雙肺、患側肺、健側肺、心臟、脊髓、肋骨、食管、大血管、氣管樹等危及器官。
1.2.2 計劃設計
采用瑞典醫科達公司Monaco5.11.03 治療計劃系統分別對15 例非小細胞肺癌患者進行DCAT 和VMAT 計劃設計,過程中使用醫科達Versa HD 直線加速器,射線能量選擇6 MV FFF,劑量率均為1400 MU/min。DCAT 計劃:以PTV 為治療等中心,治療角度為220°單弧照射,選擇可變劑量率與子野形狀優化等。VMAT 計劃:選擇與DCAT計劃相同的治療等中心,同樣的治療角度,雙弧照射。計算網格與統計不確定度選擇2 mm 和1%,PTV 與危及器官的優化參數均相同。PTV 的處方劑量為48 Gy/4 f,單次劑量為12 Gy。處方劑量覆蓋95%的靶區體積,90%的處方劑量至少覆蓋99%的靶區體積,危及器官劑量限制參考AAPM TG101號報告[11]。
1.3 計劃評估
對每例患者的DCAT計劃與VMAT計劃均采用下列參數進行評估:PTV 最大劑量(Dmax)、平均劑量(Dmean)、最小劑量(Dmin)、適形度指數(conformity index,CI)[12-13]和50%處方劑量線包圍的所有體積與PTV體積之比(R50%),R50%值越小越好,雙肺Dmean、V20(%)、V13.5(cm3)、V12.5(cm3)和V5(%),患側肺Dmean、V20(%)和V5(%),健側肺V5(%),其他各危及器官最大劑量Dmax,以及計劃計算時間、機器跳數、控制點數和出束時間等,其中C I=(T VPI)2/(TV×VPI)(TVPI為處方劑量線所包圍的靶體積,TV表示靶體積,VPI表示處方劑量線包圍的所有區域的體積,CI值的范圍為0~1,越接近1說明靶區適形度越好)。
1.4 統計學處理
2 結果
2.1 PTV 劑量分布
兩組計劃得到的PTV 劑量參數均能滿足臨床要求。兩組PTV 劑量比較,DCAT 計劃的Dmax與Dmean均高于VMAT 計劃,差異有統計學意義(P<0.05);DCAT 計劃靶區劑量的Dmin稍高于VMAT計劃,但差異無統計學意義(P>0.05);VMAT 計劃的CI、R50%均優于DCAT 計劃,差異有統計學意義(P<0.05),見表1。
表1 兩組計劃的PTV 劑量分布比較()

表1 兩組計劃的PTV 劑量分布比較()
注:DCAT 為動態適形弧放射治療,VMAT 為容積旋轉調強放射治療,PTV 為計劃靶區,CI 為適形度指數
2.2 危及器官劑量分布
兩組計劃得到的危及器官劑量參數均能滿足臨床要求。兩組危及器官劑量比較,DCAT 計劃的雙肺Dmean、V20、V13.5、V12.5均高于VMAT 計劃,患側肺的Dmean、V20、V5均高于VMAT 計劃,肋骨和氣管樹的Dmax均高于VMAT 計劃,差異有統計學意義(P<0.05),見表2。
表2 兩組計劃的危及器官劑量分布比較()

表2 兩組計劃的危及器官劑量分布比較()
注:DCAT 為動態適形弧放射治療,VMAT 為容積旋轉調強放射治療
2.3 計算時間、機器跳數、控制點數和出束時間
DCAT 計劃的計算時間、出束時間均短于VMAT 計劃,機器跳數、控制點數均低于VMAT 計劃,差異有統計學意義(P<0.05),見表3。
表3 兩組計劃計算時間、機器跳數、控制點數和出束時間比較()
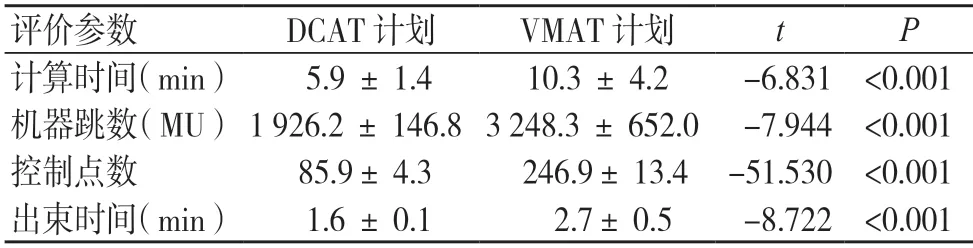
表3 兩組計劃計算時間、機器跳數、控制點數和出束時間比較()
注:DCAT 為動態適形弧放射治療,VMAT 為容積旋轉調強放射治療
3 討論
非小細胞肺癌患者行SBRT 時,通常靶區體積小、分次次數較少且單次劑量較大,不可避免地會導致治療時間較長。隨著VMAT 技術的引入,與傳統的調強適形放射治療(intensity modulated radiotherapy,IMRT)技術相比,治療時間明顯縮短。但由于需要大量的小子野來調制光束,VMAT實際治療過程中受多葉準直器運動、患者呼吸運動、機架旋轉與靶區之間復雜的相互影響可能會出現脫靶的情況[14]。因此,在患者實施治療前和治療過程中需要對VMAT 計劃進行較為嚴格的質量保證。
DCAT 將多葉準直器的適形能力與旋轉弧形射束相結合,從而產生適用于腫瘤靶區部位的持續改變的劑量分布。此技術可以使多葉準直器葉片在機架旋轉過程中不斷更新以適形靶區體積并同時保護靶區周邊危及器官。醫科達Monaco 治療計劃系統在傳統DCAT 基礎上增加了子野形狀優化和可變劑量率兩個選項。子野形狀優化是在子野進行初始排序后改進了子野形狀,以滿足靶區周圍危及器官的約束條件[15];且子野形狀優化增強了計劃質量,縮短了出束時間,減少了子野數量。可變劑量率是指允許機架旋轉速度和劑量率變化,在一定程度上增加了放射治療計劃的調制能力。
Moon 等[16]針對肝癌患者的SBRT 研究表明,DCAT 雖然在正常肝臟的V30、V20和V10明顯高于VMAT,但是兩種治療技術均能滿足放射治療腫瘤協作組(Radiation Therapy Oncology Group,RTOG)關于SBRT 的相關協議;DCAT 在計算時間、機器跳數和出束時間方面明顯優于VMAT,是VMAT 的一個有效替代方案。Stathakis 等[17]的研究也表明,DCAT 在肝癌和肺癌患者的SBRT 中可以獲得與VMAT 相似的劑量結果,同時在危及器官與靶區重疊區域DCAT 可以獲得更低的劑量。
本研究中,DCAT 計劃在危及器官劑量方面不優于VMAT 計劃,與Thaper 等[18]的研究結果相似。雖然在適形度和劑量梯度等方面DCAT 計劃不如VMAT 計劃,但是DCAT 計劃具有以下優勢:DCAT計劃可以抵消多葉準直器相互作用的影響,在整個治療過程中靶區都保持在治療射野內;DCAT 計劃在非均勻區域的計算敏感度比VMAT 小,在計算時間、機器跳數、控制點數和治療時間方面優于VMAT 計劃。本研究結果顯示,DCAT 計劃的平均出束時間比VMAT 計劃快1 min,而機器跳數和控制點的減小、治療時間的縮短可以更好地幫助患者保持治療體位和控制呼吸,從而提高治療的精度和患者的舒適度。因此,對于一些協調性差、呼吸控制困難或耐受能力有限的患者,應優先考慮采用DCAT。此外,更少的機器跳數和更短的治療時間可以減少多葉準直器的漏射劑量和直線加速器的負荷,降低直線加速器損耗,延長設備使用壽命。
綜上所述,對非小細胞肺癌患者采用DCAT 和VMAT 兩種技術進行SBRT,均能獲得比較滿意的靶區劑量分布,VMAT 計劃對于危及器官的保護更好,DCAT 計劃在計算時間、機器跳數、控制點數和出束時間方面更具優勢。

