卒中后認知障礙對數學計算-步行雙任務中步態自動化程度和跌倒風險的影響
認知障礙是卒中后常見的障礙類型之一,主要表現為額葉執行功能受限和注意力缺陷
。步行-認知的雙重任務執行是卒中患者回歸社區后需常面對的日常活動之一
,不同于健康人群,腦卒中者常通過過度占用執行功能和注意力來執行步行控制
。在當前認知資源容量的框架理論下,執行功能障礙和注意力缺陷可能是誘發步行不穩和跌倒發生的主要原因之一
。然而,認知障礙、雙任務下的步態表現和跌倒風險三者之間的關系依然尚未明確
。明確此關系對于理解認知障礙誘發跌倒的潛在機制具有重要意義,且可為雙重任務干預方案的設計提供理論指導。
中樞神經系統的步行控制可以看作為執行步行控制和節律化自動控制之間的平衡
。執行步行控制與前額葉的資源利用相關
,而節律自動化控制則涉及基底核
。研究發現,不同認知任務影響步態表現和跌倒風險的機制并不相同
。前人研究的雙重任務設計較多集中在與前額葉、語言中樞以及感覺-運動皮層介導的認知任務層面上
,而對于涉及空間記憶的數學計算卻關注較少。研究顯示,基底核不僅與節律化自動控制有關,還同時介導數學計算
。此外研究表明,集中注意學習可以激活右側基底核
,這可能說明注意力缺陷也會間接影響基底核的功能發揮。因此,設計數學計算的認知任務可能對于理解雙任務下的步行自動化控制和跌倒風險程度具有重要意義。然而,較為遺憾的是,前人研究中步態時空參數的評估并不能反映與基底核相關的步態自動化控制
。此外,采用質心和壓力的距離或夾角來評估跌倒風險,忽略了支撐面和步行速度的影響
。因此,本研究通過設計步行-數學計算的雙任務,采用步態變異性和步態穩度量化評估步行自動化程度和跌倒風險,旨在探討卒中后認知障礙對數學計算-步行雙任務中步行自動化程度和跌倒風險的影響。
1 資料與方法
1.1 一般資料 于2019年6月~10月間在上海市虹口江灣醫院及其周邊社區,共招募腦卒中受試者31名。診斷標準:符合《各類腦血管疾病診斷要點》腦卒中診斷標準,并經CT或MRI檢查證實。納入標準:年齡50歲~ 75歲,性別不限;首次發病,且病程>6個月;無佩戴各類輔助步行或矯形器具;可自主步行20m。排除標準:伴有其他神經系統疾病或嚴重內科疾病者;患有肌骨類型疾病或其他疾病,并導致下肢不對稱及肌骨損傷者;視力或聽力障礙者;已參加任何臨床研究者;接受系統化的認知功能訓練者。由一名經驗豐富的康復治療師,采用MoCA認知評估量表(Montreal Cognitive Assessment, MoCA)對受試者進行認知功能評定
,根據認知功能評估結果分為認知障礙組(
=14,MoCA<26)和無認知障礙組(
=17,MoCA≥26)。此外,評估受試者下肢功能(Fugl-Meyer Assessment,FMA)和Berg平衡功能。兩組受試者基線特征見表1。本研究經醫院倫理委員會批準,且受試者知情同意。
早期生長反應因子1(EGR-1)是一種早期生長反應基因,屬于轉錄因子鋅指蛋白家族成員。它可以在幾分鐘內激活一系列信號通路,其活性在數小時內即衰退。滲透壓改變、熱休克、缺氧、DNA損傷、輻射損傷等應激都會刺激EGR-1的表達。EGR-1通過多種通路調節細胞的增殖、分化和凋亡。但是,目前關于EGR-1在卵巢癌中的發生、發展中起到什么樣的作用還未有明確的報道。本研究運用免疫組化的方式檢測EGR-1蛋白在卵巢癌的表達情況,探討EGR-1在卵巢癌的發生、發展的過程中的作用與意義。

1.2 方法
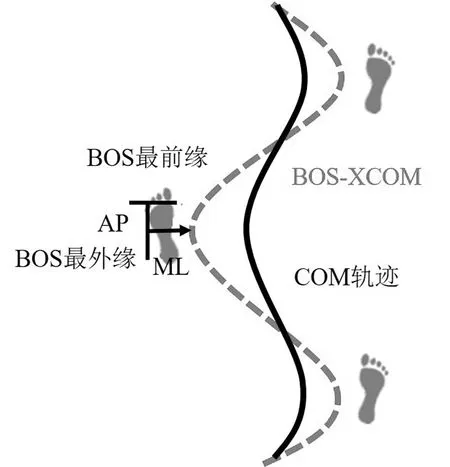
在雙重任務中,跌倒風險和步行自動化控制息息相關
。本文研究結果顯示,認知障礙組內外側動態穩度顯著低于無認知障礙組。這與前人關于遺傳性痙攣、腦卒中等領域的研究結果相一致
。以往針對神經病變人群步行策略的研究認為,腦卒中步態表現的改變不僅僅是因為運動功能的受限,也有可能是其根據自身功能而選擇慢速平穩的應對策略有關
。盡管我們并未發現前后方向的不穩增大,但這并不意味著認知障礙對前后方向的動態穩度沒有影響,原因在于步速的降低和雙支撐的延長使得動態穩度趨于正常。然而,認知障礙組在步行腳跟觸底時,內外側跌倒風險依然較大,這提示在康復干預中應著重于內外側平衡的訓練。
2.2 兩組患者并發癥發生率對比 對照組腎結石患者并發癥發生率為2.00%,觀察組患者為20.00%,觀察組患者并發癥發生率顯著增高,兩組比較有統計學意義(P<0.05,表2)。
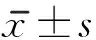
2 結果
卒中后認知障礙影響步態生物力學變化和誘發跌倒的潛在機制,持續引發神經康復領域研究人員的重點關注
。與前人研究側重點不同的是,本研究著眼于涉及基底核的數學計算-步行雙重任務,并明確了卒中后認知障礙對數學計算-步行雙重任務中步行自動化程度和跌倒風險的影響。結果發現,與無障礙組相比,認知障礙組具有顯著更低的步速、更大的雙支撐期比例、更大的步速變異性及更低的內外側動態穩度。這可能說明在可影響基底核的雙重任務中,執行功能障礙和注意力缺陷進一步降低了步行自動化模式和增加了跌倒風險。
在健、患側肢體腳跟觸地時,認知障礙組的內外側動態穩度顯著小于無認知障礙組(
<0.05),前后方向動態穩度2組間比較差異無統計學意義。見表4。
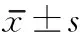
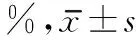
其次,需要建設目標,通過運用云計算、移動互聯網、大數據分析等先進技術,建設出符合院校發展的數字化環境,從而實現規范高效的管理,并且可以為學校管理者作出決策提供強有力的依據,為全校的老師和學生提供更加便捷的信息服務系統,科學地提高學校的信息化水平,實現學校轉型發展[3]。
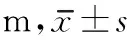
3 討論
2組步態時空參數的比較。與無認知障礙組相比,認知障礙組具有顯著較小的步速和較大的雙支撐期(
<0.05);其余步態參數指標無統計學差異。見表2。2組步態參數變異性比較,認知障礙組的步速變異性顯著大于無認知障礙組(
<0.05);其余步態參數變異性指標未見統計學差異。見表3。
步態控制主要依賴于前額葉-紋狀體網絡,此網絡涉及執行功能
。其中,紋狀體是基底節環路的輸入層,主要參與步行程序性和節律自動化的過程,而前額葉主要是在復雜的步行條件下補充自動化
。步態參數變異性與步行自動化控制程度的負相關關系已得到大量研究證實
。在本研究中,我們發現認知障礙組的步速變異性顯著更大,這可能說明執行功能障礙對步行自動化模式產生顯著的負面影響。研究發現,與青年相比,健康老年人和腦卒中患者在步行任務中均表現出前額葉的過度激活,且腦卒中患者前額葉過度激活程度大于健康老年人
。目前認為,這種前額葉過度激活的現象是為了補償中樞病變后步行自動化模式的匱乏,用以補充自動化和執行步行控制
。較為有趣的是,我們發現,伴有執行功能障礙和注意力缺陷的卒中者在數學計算-步行雙重任務中步速的顯著降低。其可能的原因是,由于腦卒中患者隨意性控制下降及本體感覺障礙,平衡調節和維持需要更高的集中注意力才能完成
,這從一定層面上解釋了步速降低、雙支撐延長及步速變異性增大的部分原因。
1.2.1 生物力學測試方案 50個反光Marker依據Vicon動作捕捉方案依次粘貼于身體骨性標志處。采用三維紅外運動捕捉系統(Vicon Motion Systems, T40, UK)和三維測力臺(AMTI, OR6-GT1000, USA)同步采集步態中的運動學和動力學參數,采樣頻率分別為100 Hz和1000 Hz。在本研究中,認知-步行雙重任務測試要求受試者一邊步行,一邊進行10—3的連續遞減計算
。其中,要求受試者以自我選擇速度進行步態測試,在正式測試前,要求受試者完成5次步態預測試,以充分熟悉實驗場地和實驗意圖。正式實驗采集3次成功的數據用以后續數據處理分析。
優先注意資源的限制和環境需求導致機體在面對不同認知任務時,出現不同的應對策略
。Patel等
的研究評估添加不同類型認知任務的效果,結果發現連續減法中認知消耗最高。與本研究結果較為不一致的是,上述研究發現數學計算的介入并沒有顯著降低步態表現,其認為這是步行自動化的結果。造成這種結果不一致的原因可能歸因于受試者的不同,健康老年人在腦功能、步態表現和認知資源容量上均優于腦卒中患者
。這也可能暗示在臨床康復中設計雙重任務干預類型時,應根據患者認知水平和功能水平進行選擇。
水體沉積物是水體營養元素的重要蓄積庫,是水體營養鹽的緩沖劑,維持水中營養鹽平衡,在水體缺乏營養時,水生生物的生長主要是靠沉積物釋放的營養鹽維持調節。磷是造成水質富營養化的關鍵性的限制性因素之一[1]。城市河流閘控滯流,水力流通性差,造成大量沉積物淤積,內源負荷累積。城市河流沉積物磷的沉積物-水界面交換和輸送研究具有重要意義。
本研究存在著一些限制:①本研究采用MoCA量表對受試者認知功能中的各項能力進行了評估,但并未進一步分析MoCA分項得分,尤其是執行功能、注意力與步態變異性及動態穩度的相關性;②我們基于前人研究結果,在前言和討論部分進行了腦功能和步態控制的相關討論,但并沒有進行雙重任務下的腦功能評估。未來研究可在此基礎上,通過納入涉及不同腦區的認知任務,采用近紅外技術明確不同認知雙重任務下的步態控制、跌倒風險與腦功能潛在關系。
綜上所述,卒中后執行功能障礙和注意力缺陷改變了雙重任務下的步行模式,對步態變異性和動態穩度產生顯著的負面影響。建議臨床康復治療中,應多設計包含運動控制和數學計算的雙重任務訓練,以期降低跌倒發生率。
[1] Graff-Radford J. Vascular Cognitive Impairment [J]. CONTINUUM Lifelong Learning in Neurology, 2019, 25 (1): 147-164.
[2] 王延延, 安丙辰,鄭潔皎. 腦卒中后認知障礙引起跌倒的機制研究進展 [J]. 中國康復理論與實踐, 2016, 22(11):1285-1288.
[3] 張陽,Pinter D. 年輕腦卒中患者認知功能障礙的發病率 [J]. 中國康復, 2019, 34(9):476-478.
[4] 朱玲玲,繩宇. 血管性輕度認知障礙老年人雙重任務行走下步態參數特征與跌倒的關系 [J]. 中國康復理論與實踐, 2020, 26(4):467-471.
[5] 葉明珠, 熊健, 王樂聰, 等. 老年認知障礙與跌倒的相關性研究進展 [J]. 中國康復, 2020, 35(07):383-386.
[6] Al-Yahya E, Johansen-Berg H, Kischka U, et al. Prefrontal cortex activation while walking under dual-task conditions in stroke: a multimodal imaging study [J]. Neurorehabilitation & Neural Repair, 2016, 30 (6): 591-599.
[7] Hawkins K A, Fox E J, Daly J J, et al. Prefrontal over-activation during walking in people with mobility deficits: Interpretation and functional implications [J]. Hum Mov Sci, 2018, 59(5): 46-55.
[8] 劉玉,李慶雯. 雙任務訓練在腦卒中患者下肢康復中的研究進展 [J]. 中國康復醫學雜志, 2020, 35(1):100-105.
[9] Tombu M, Jolicoeur P. All-or-none bottleneck versus capacity sharing accounts of the psychological refractory period phenomenon [J]. Psychol Res, 2002, 66 (4): 274-86.
[10]Yang L, Lam F M, Huang M, et al. Dual-task mobility among individuals with chronic stroke: changes in cognitive-motor interference patterns and relationship to difficulty level of mobility and cognitive tasks [J]. Eur J Phys Rehabil Med, 2017, 54 (4): 526-535.
[11]Clark D J. Automaticity of walking: functional significance, mechanisms, measurement and rehabilitation strategies [J]. Front Hum Neurosci, 2015, 9(2): 246-252.
[12]Maidan I, Nieuwhof F, Bernad-Elazari H, et al. The role of the frontal lobe in complex walking among patients with parkinson's disease and healthy older adults: an fNIRS study [J]. Neurorehabil Neural Repair, 2016, 30 (10): 963-971.
[13]Al-Yahya E, Dawes H, Smith L, et al. Cognitive motor interference while walking: a systematic review and meta-analysis [J]. Neuroscience & Biobehavioral Reviews, 2011, 35 (3): 715-728.
[14]Mink J W. The basal ganglia: focused selection and inhibition of competing motor programs [J]. Progress in Neurobiology, 1996, 50 (4): 381-425.
[15]黃彩平, 謝欲曉, 王思遠, 等. 步行-執行功能雙任務訓練對慢性腦卒中患者康復的研究進展 [J]. 中國康復醫學雜志, 2018, 33(8):988-992.
[16]Holden A, Wilman A, Wieler M, et al. Basal ganglia activation in Parkinson's disease [J]. Parkinsonism Relat Disord, 2006, 12 (2): 73-77.
[17]Patel P, Bhatt T. Task matters: influence of different cognitive tasks on cognitive-motor interference during dual-task walking in chronic stroke survivors [J]. Top Stroke Rehabil, 2014, 21 (4): 347-357.
[18]梁雷超, 黃靈燕, 伍勰, 等. 膝骨關節炎對女性老年人步行動態穩定性的影響 [J]. 體育科學, 2016, 36(03):61-66.
[19]張麗, 卞立, 陳煜, 等. 腦卒中后認知功能障礙的康復評估與治療進展 [J]. 中國康復, 2020, 35(12):660-663.
[20]Herman T, Mirelman A, Giladi N, et al. Executive control deficits as a prodrome to falls in healthy older adults: a prospective study linking thinking, walking, and falling [J]. J Gerontol A Biol Sci Med Sci, 2010, 65 (10): 1086-1092.
[21]Montero-Odasso M, Verghese J, Beauchet O, et al. Gait and cognition: a complementary approach to understanding brain function and the risk of falling [J]. J Am Geriatr Soc, 2012, 60 (11): 2127-2136.
[22]梁雷超, 呂嬌嬌, 黃靈燕, 等. 認知-姿勢控制雙任務在老年人跌倒研究中的應用進展 [J]. 中國康復理論與實踐, 2016, 22(11):1289-1293.
[23]van Vugt Y, Stinear J, Claire Davies T, et al. Postural stability during gait for adults with hereditary spastic paraparesis [J]. J Biomech, 2019, 88(11): 12-17.
[24]Hof A L, Gazendam M G, Sinke W E. The condition for dynamic stability [J]. J Biomech, 2005, 38 (1): 1-8.
[25]Cohen J A, Verghese J, Zwerling J L. Cognition and gait in older people [J]. Maturitas, 2016, 93(9): 73-77.
[26]Watson N L, Rosano C, Boudreau R M, et al. Executive function, memory, and gait speed decline in well-functioning older adults [J]. J Gerontol A Biol Sci Med Sci, 2010, 65 (10): 1093-1100.
[27]Annweiler C, Beauchet O, Bartha R, et al. Motor cortex and gait in mild cognitive impairment: a magnetic resonance spectroscopy and volumetric imaging study [J]. Brain, 2013, 136 (3): 859-871.
[28]Montero-Odasso M, Speechley M, Chertkow H, et al. Donepezil for gait and falls in mild cognitive impairment: a randomized controlled trial [J]. Eur J Neurol, 2019, 26 (4): 651-659.
[29]Hermand E, Tapie B, Dupuy O, et al. Prefrontal cortex activation during dual task with increasing cognitive load in subacute stroke patients: a pilot study [J]. Front Aging Neurosci, 2019, 11 (2): 160-166.
[30]Mihara M, Miyai I, Hatakenaka M, et al. Sustained prefrontal activation during ataxic gait: a compensatory mechanism for ataxic stroke[J]. Neuroimage, 2007, 37 (4): 1338-45.
[31]鐘琳曄, 劉喆, 常冬梅, 等. 探究恢復期腦卒中患者注意力缺陷與平衡控制及跌倒的關系 [J]. 中國康復理論與實踐, 2010, 16(12):1160-1163.
[32]王丹丹, 霍博雅. 腦卒中恢復期患者注意力缺陷與平衡功能、日常生活活動能力及跌倒的關系 [J]. 廣東醫學, 2012, 33(7):932-934.
[33]Chen N, Xiao X, Hu H, et al. Identify the alteration of balance control and risk of falling in stroke survivors during obstacle crossing based on kinematic analysis [J]. Front Neurol, 2019, 10(5): 813-826.
[34]Den Otter A R, Geurts A C, de Haart M, et al. Step characteristics during obstacle avoidance in hemiplegic stroke [J]. Exp Brain Res, 2005, 161 (2): 180-192.

