快速測定嬰幼兒配方乳粉中的維生素B1及B2
梁敏
(福建省產品質量檢驗研究院,國家加工食品質量監督檢驗中心,福州 350001)
0 引言
B族維生素是人體必需的營養元素,自身無法合成,須從外界攝入[1-3]。對于食物來源相對單一的嬰幼兒而言,嬰幼兒配方乳粉中維生素含量偏高或偏低均會對其生長發育帶來直接影響。我國對嬰幼兒配方食品中的維生素添加量均作出了強制性要求[4-5]。因此,對嬰幼兒配方乳粉中維生素含量進行快速準確的測定,對嬰幼兒的健康成長具有重要意義。
目前,食品中維生素B1、B2的測定依據是兩個獨立的標準[6-7],前處理均需采用高壓提取后過夜酶解的方式,成本高,且耗時長,方法重復性差,不利于高通量樣品的檢測;且市場上獲得的酶,大多本底含有維生素B1,需增加空白試驗,前處理及后期計算均較為繁瑣。故本研究參考標準方法,綜合文獻報道[8-11],對前處理條件進行系統優化,通過不斷測試,建立高效液相色譜法同時測定嬰幼兒配方乳粉中維生素B1、B2,方法快速準確,重復性高,實用性強,適用于奶粉常規檢測,也可為后續標準的修訂提供參考價值。
1 材料與方法
1.1 儀器與試劑
Waters e2695高效液相色譜儀(配備熒光檢測器),美國Waters公司;Ultimate XB-C18(150 mm×4.6 mm,5 μm)色譜柱,月旭科技股份有限公司;壓力蒸汽滅菌鍋,上海東亞壓力容器制造有限公司;Sartorius BSA 224S電子天平,賽多利斯科學儀器(北京)有限公司;高速臺式離心機,湖南湘儀實驗室儀器開發有限公司;IKA MS 3 basic單發渦旋振蕩器,上海滬粵明科學儀器有限公司;維生素B1(鹽酸硫胺素,≥99 %),美國Sigma公司;維生素B2(核黃素,≥98%),德國Dr公司;木瓜蛋白酶(酶活≥800 U/g),Aladdin-阿拉丁試劑(上海)有限公司;高峰淀粉酶(酶活≥3 700 U/g),CNM試劑;正丁醇(分析純)、甲醇(色譜純)、鹽酸(分析純,37%)、無水乙酸鈉(分析純)、鐵氰化鉀(分析純),上海滬試化工有限公司;氫氧化鉀(分析純),國藥集團化學試劑有限公司;除特殊說明外,其他試劑均為分析純,實驗用水均為超純水。
1.2 方法
1.2.1 標準溶液配置
維生素B1標準溶液:準確稱取50 mg維生素B1于50 mL容量瓶中,使用濃度為0.01 mol/L的鹽酸溶液溶解并定容,得質量濃度1.00 mg/mL標準儲備液,置于0~4℃冰箱保存;取標準儲備液用水逐級稀釋,得質量濃度分別為0.02,0.1,0.5,1.0,2.00 μg/mL的維生素B1系列標準溶液。
維生素B2標準溶液:準確稱取10 mg維生素B2于100 mL棕色容量瓶中,使用濃度0.1 mol/L鹽酸溶液溶解,沸水浴10 min,取出冷卻至室溫后定容,得0.10 mg/mL標準儲備液,置于0~4℃冰箱保存;取標準儲備液用水逐級稀釋,得質量濃度分別為0.02,0.1,0.5,2.0,2.00 μg/mL的維生素B2系列標準溶液。
1.2.2 樣品處理
稱取5.00 g樣品于100 mL具塞錐形瓶中,使用約60 mL溫水充分溶解樣品,加入1 mL鹽酸溶液(1+1),搖勻,加塞。將錐形瓶置于高壓滅菌鍋內,在121℃下保持30 min。水解結束后待冷卻,加入氫氧化鉀溶液(質量濃度150 g/L)約2 mL(調節溶液pH值約為5~6),樣品轉移至100 mL容量瓶,定容,搖勻,將樣品溶液用濾紙過濾至燒杯,清液備用。
維生素B2測定:取上述清液過0.45 μm濾膜,上機測試。
維生素B1測定:取上述清液400 μL至2.5 mL離心管,加入200 μL堿性鐵氰化鉀(1.0 g/L),渦旋混勻30 s,準確加入1.00 mL正丁醇,再次渦旋混勻30 s后,于16 000 r/min下離心1 min,取上層過0.22 μm有機濾膜,上機測試。另取400 μL標準溶液進行同步衍生。
1.2.3 液相色譜條件
流動相為濃度0.05 mol/L乙酸鈉:甲醇=65∶35;流速為1.0 mL/min;進樣量為10 μL;柱溫為35℃;維生素B1為激發波長375 nm,發射波長435 nm;維生素B2為激發波長462 nm,發射波長522 nm。
2 結果與分析
2.1 前處理條件的優化
2.1.1 酶解步驟的去除
國家標準中規定,食品中維生素B1、B2的測定均需要經過高壓水解,而后進行酶解(約16 h),耗時長,且經過多次轉移,目標化合物可能會出現不必要的損失或降解。乳粉中的維生素基本來自人為添加,部分以游離態形式存在,只有小部分被糖或蛋白質等化合包裹,同時,由于維生素B2的溶解性較差,因此考慮保留高壓水解過程。經過試驗表明,高壓水解后樣品中的大分子物質即可被破壞,從而釋放出維生素B1和B2。故本研究嘗試省略酶解步驟,并將B1和B2前處理進行合并,結果滿意,極大的降低了耗材成本和時間成本。
2.1.2 蛋白質的沉淀
張隆龍[10]等人做了相似研究,乳粉經過高壓后直接進行維生素B2的檢測及維生素B1的衍生化。試驗發現,只經過高壓水解后的樣品處于乳濁狀態,無法得到澄清溶液,對后期樣品的過濾造成困難,且測定結果重復性較差。故本研究采用調節溶液pH值的方式使蛋白質沉淀。奶粉中主要含乳清蛋白和酪蛋白[12],等電點在4.6~4.8之間,但由于乳粉基質各不相同,添加的金屬離子可使等電點出現不同程度的偏移,故堿的添加量也稍有不同。實驗結果表明,當氫氧化鉀溶液(質量濃度150 g/L)添加量為2 mL時,溶液pH值約為5~6,樣品基本能得到較好的沉淀效果。
2.1.3 維生素B1衍生條件的優化
在保證取樣具有代表性的情況下,本研究將待衍生試樣體積減少至400 μL,同比降低后期有毒有機試劑正丁醇的使用量,同時,由于衍生試樣的減少,可使樣液與衍生試劑在短時間內充分混勻,加快反應效率;選擇使用2.0 mL離心管進行衍生反應,加入正丁醇提取后可直接進行高速離心,有效降低了由多次轉移帶來的回收率損失。在該條件下對衍生劑的濃度進行優化,確定衍生劑質量濃度為1.0 g/L時,樣品衍生效果最佳。
2.2 方法學驗證
2.2.1 線性范圍、檢出限及定量限
將維生素B2系列標準工作液、維生素B1標準衍生液注入色譜儀,以對應得到響應值來繪制標準工作曲線,分別以3倍和10倍信噪比來進行計算檢出限及定量限。結果見表1,目標化合物在對應濃度范圍內的線性關系良好,檢出限及定量限均低于國家標準,滿足檢測要求。圖1為標準溶液色譜圖,維生素B1和B2分別在6 min和5 min之內出峰,單個樣品檢測時長控制在11 min,有利于樣品快速分析,同時可減少由維生素B1衍生物降解帶來的誤差[13]。
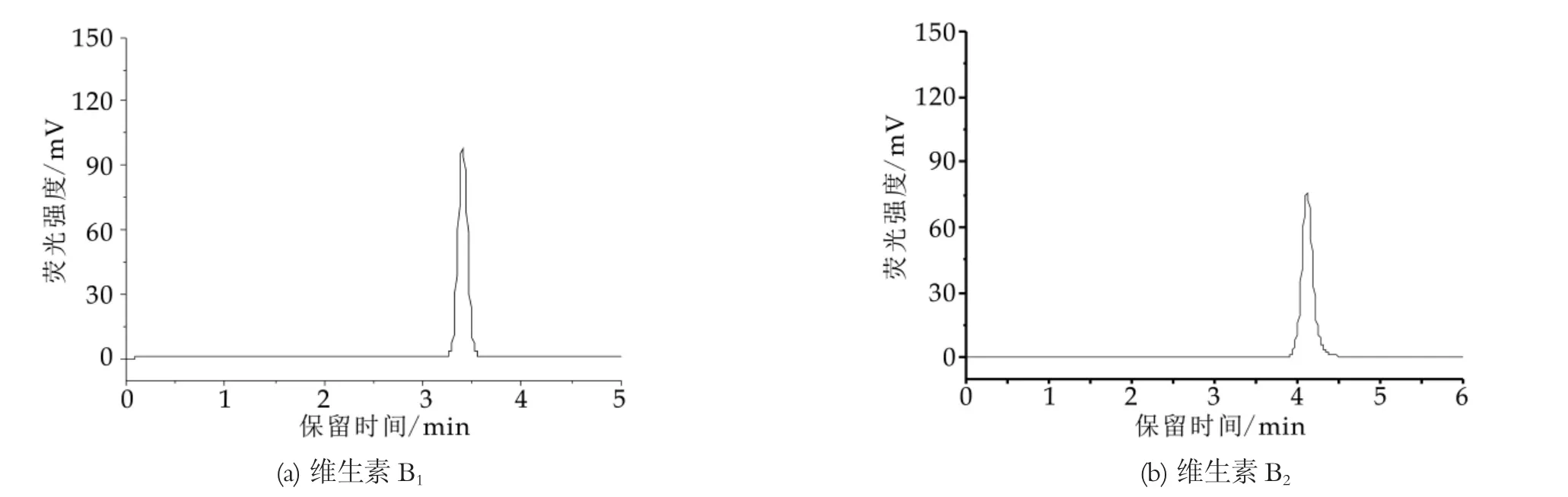
圖1 維生素B1和B2標準溶液色譜

表1 維生素B1和B2的回歸方程、相關系數、線性范圍、檢測限及定量限
2.2.2 精密度及回收率
隨機抽取一份乳粉樣品進行精密度試驗,采用本方法對樣品進行處理后進樣分析(n=6),連續測定3 d,得維生素B1、B2日內精密度分別為1.98%、1.23%,日間精密度分別為3.12%、2.87%,表明該方法精密度良好。
取6份不同品牌(A,B,C,D,E,F)的嬰幼兒配方乳粉,各添加適量標準溶液,得3個濃度水平加標試樣,按照本方法進行分析,每個添加水平平行測定3次。實驗結果如表2所示,維生素B1回收率在92.4%~100%之間,維生素B2回收率在93.0%~102%之間,符合檢測要求。
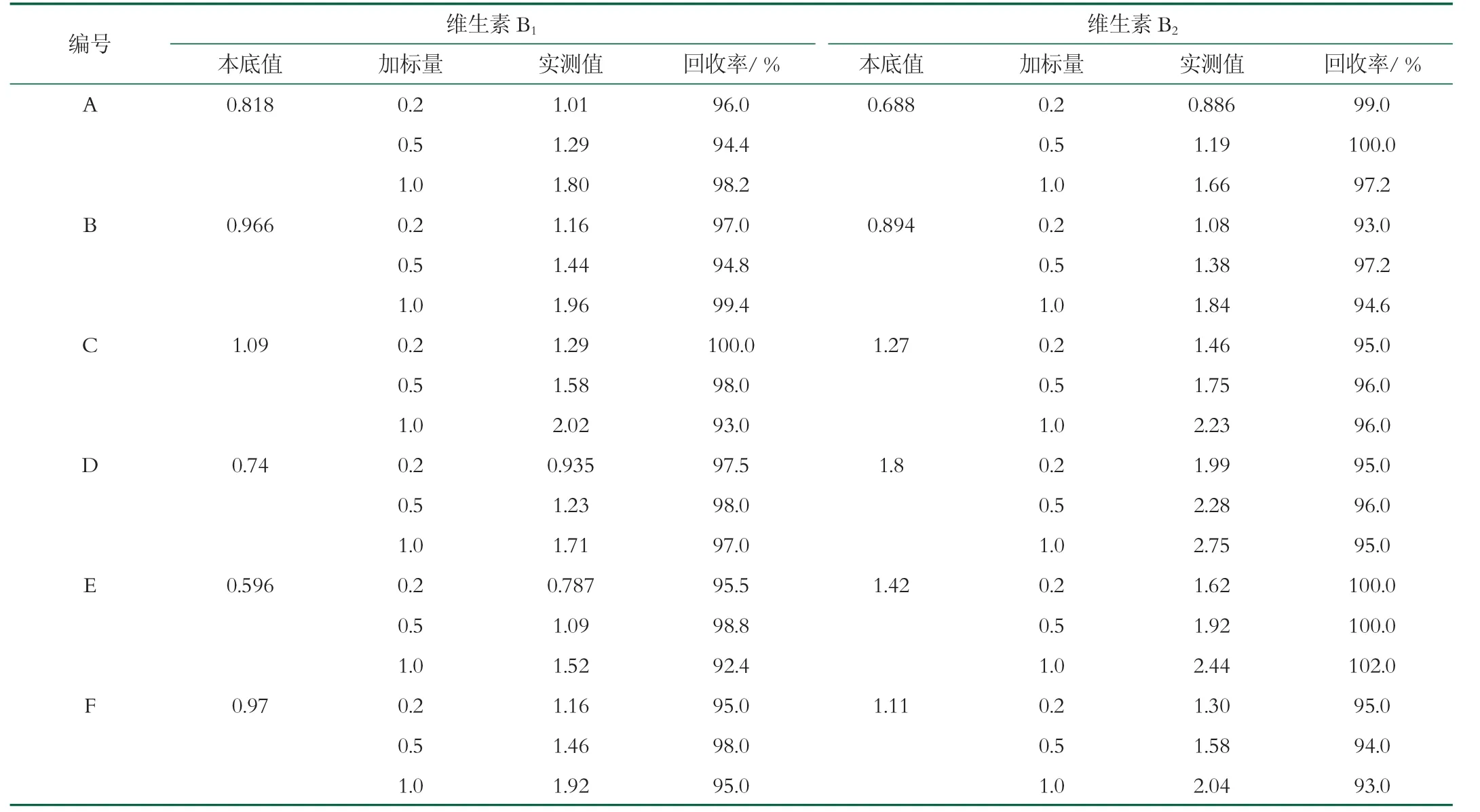
表2 6種嬰幼兒配方乳粉中維生素B1和B2加標回收率(n=3) mg/100g
2.3 實際樣品測定
隨機抽取20批次不同品牌及段位的奶粉,采用本方法及標準方法進行測定,每個樣品平行測定3次,取均值進行比較,含量統計見表3。結果顯示,部分乳粉中維生素B1、B2測定值高于標準方法,其原因可能為標準方法中酶解時間過長,目標化合物發生降解,同時表明該方法測定值更接近真實值;20批次乳粉測定值與標準方法測定值之間的相對誤差小于5.77%,表明該方法適用于嬰幼兒配方乳粉中維生素B1及B2的檢測。
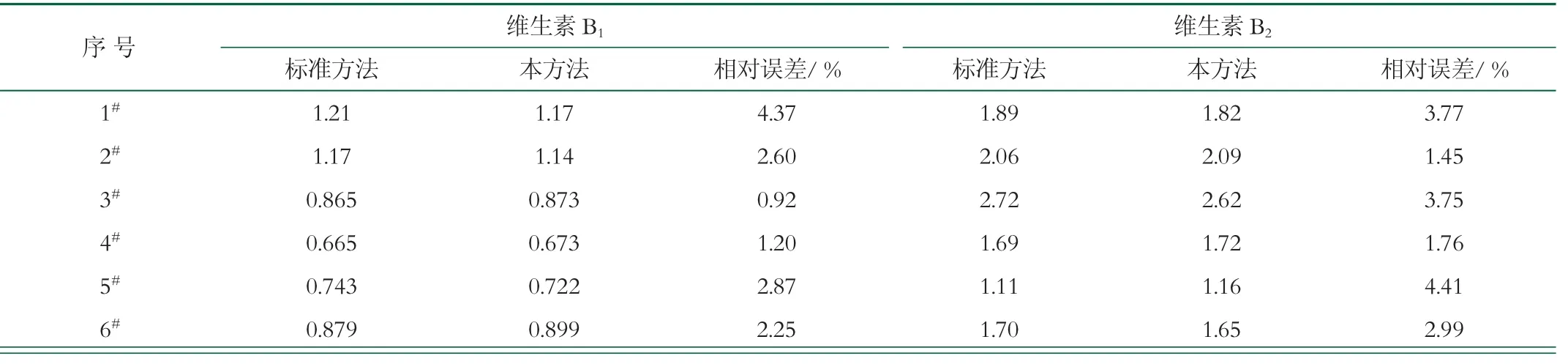
表3 不同方法測定20批次乳粉中維生素B1和B2測定結果比較(n=3) mg/100g
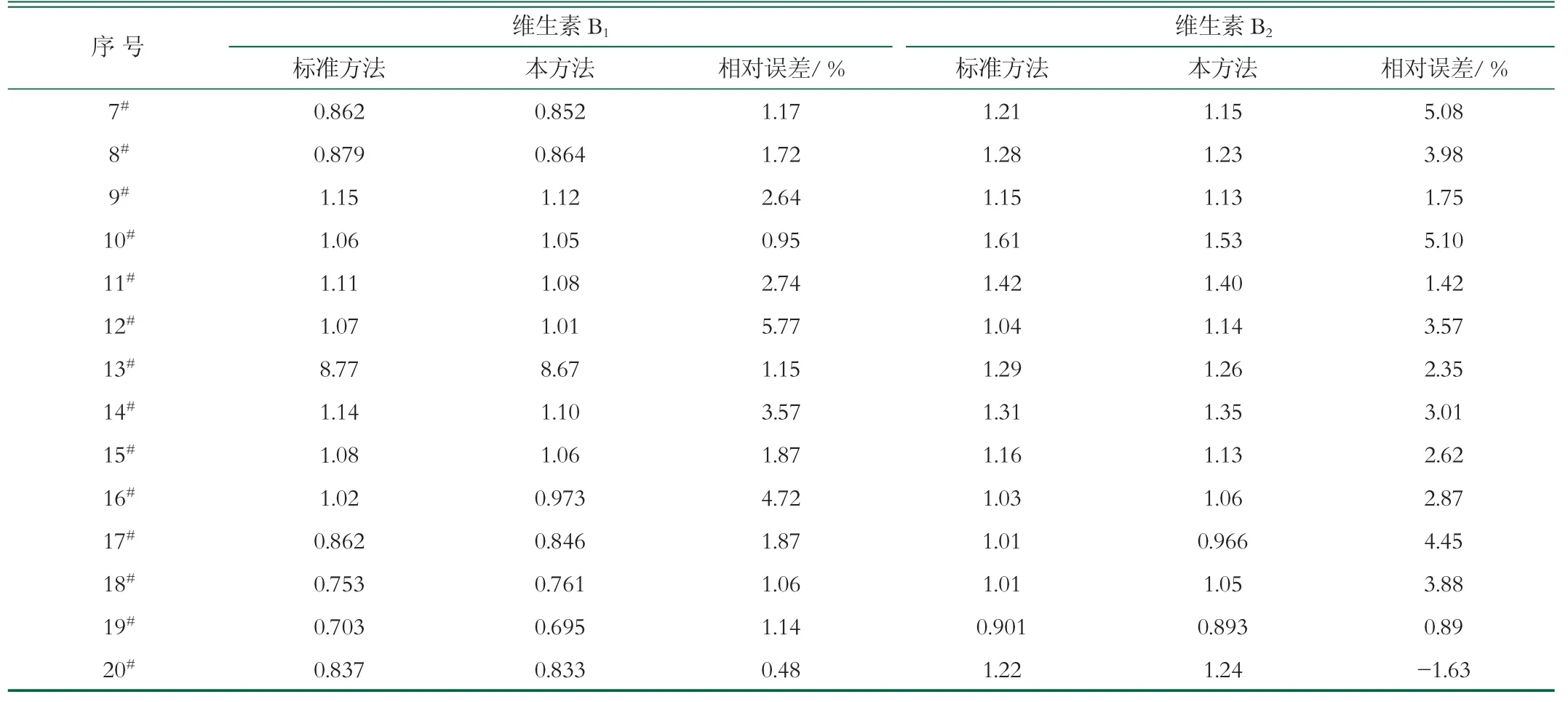
(續表3)
3 結論
目前,食品中維生素測定相關國家標準的建立大多是針對單一化合物,而嬰幼兒配方乳粉中一般會同時添加多種營養元素,采用標準方法進行測定,成本高,效率低。為提高檢測效率,多物質的聯測是該行業發展的重要方向之一。對于多維生素聯測的研究目前多使用液相色譜質譜串聯[14-20],儀器昂貴,對操作人員要求高,不利于作大規模推廣;且維生素結構多樣,對前處理的要求不同,復雜樣品基質的多維生素聯測,很大程度上只是單純縮短了檢測時間,難以保證樣品中目標化合物的提取效率,實用性不強;而直接采用高效液相色譜進行測定的多聯測研究,樣品也多集中在保健品、功能性飲料、營養強化劑[21-26]等相對簡單的基質。本研究基于目標化合物的理化性質以及樣品基質特性,建立高效液相色譜聯合熒光檢測器測定幼兒配方乳粉中維生素B1、B2的方法。通過大量數據表明,該方法快速,準確,可應用于嬰幼兒配方乳粉中維生素B1、B2的常規檢測,具有較強的現實意義和推廣價值。

