糖尿病視網膜病變早期診斷技術及其應用
尹玉如,趙博軍,2
0引言
糖尿病視網膜病變(diabetic retinopathy,DR)是糖尿病(diabetes mellitus,DM)嚴重的眼部并發癥,具有高發病率、高致盲率的特點。糖尿病視網膜病變早期防治研究組(Early Treatment Diabetic Retinopathy Study,ETDRS)研究表明,90.0% DR患者可通過對DR的早期診斷與及時有效的干預避免發生視力的嚴重下降,改善其視力預后[1],因此DR的篩查及早期診斷對患者的預后及治療效果有重要意義。隨著對神經血管單元(neurovascular unit,NVU)概念的提出及檢測手段的不斷更新,已有許多研究認為DR患者在病變早期,甚至是微血管受到損傷之前就已經發生了視網膜神經節細胞、膠質細胞等神經組織的退行性病變[2-4]。研究提示我們應將視網膜的神經級血管視為一個相互作用的整體,結合視網膜電生理功能、神經及血管組織的改變全面分析,從而實現對DR的早期診斷及治療。
根據ETDRS發布的糖尿病視網膜病變防治指南,DR被認為是一種DM引起的慢性進展性微血管病變,不同程度的微血管病變是DR診斷、分類及治療的主要依據[1]。臨床上針對DR的傳統檢查主要包括眼底鏡、眼底照相及熒光素眼底血管造影(fluorescein fundus angiography,FFA),這些檢查存在著一定的局限性。眼底鏡檢查及眼底照相只能定性地觀察視網膜形態學變化,而無法定量分析視網膜的厚度變化,具有主觀性強、無法發現早期病變等局限;FFA雖是目前DR診斷的金標準,但FFA不能分層成像、存在熒光素滲漏而影響對血管的觀察;同時FFA檢測時間較長且具有侵入性,對患者的全身情況有一定限制,不利于患者的依從性[5-6]。因此,手持式免散瞳視覺電生理診斷設備(RETeval)、光學相干斷層掃描(optical coherence tomography,OCT)及光學相干斷層掃描血管成像(optical coherence tomography angiography,OCTA)憑借其無創性、可量化性、掃描速度快、軸向分辨率高等優勢,近年來已成為DR的重要檢查。隨著技術的進步,人們對DR的認識逐漸加深。然而目前尚缺乏一種被廣泛認可的亞臨床期診斷指標,因此利用多種檢測手段對DR進行早期評估是最可靠的診斷方法。
1 RETeval的原理及優勢
視網膜電流圖(electroretinogram,ERG)是一種臨床廣泛使用的視網膜電生理功能檢測方法,其主要原理是通過記錄整個視網膜神經元對不同照度閃爍光刺激所引發的電位變化情況,對視網膜電生理功能進行評估,而視網膜電生理功能的改變一定程度上可以反映視網膜神經系統生理情況。ERG波形的主要參數包括隱式時間和振幅[7]。研究發現在DM患者中,ERG的隱式時間延長,振幅降低出現在特征性的微血管改變之前[8],因此認為ERG可作為DR篩查的檢測手段。然而傳統的ERG檢測過程繁瑣,檢查前需要對受檢者進行散瞳和局部麻醉,且檢測時長較長,不適合用于對DM患者進行篩查。
近年來,一種稱為RETeval的手持免散瞳便攜ERG記錄裝置被引入臨床,RETeval設備是一種便攜、非侵入、非散瞳的全視野視網膜電生理(ERG)檢測儀器。RETeval主要由紅外檢測系統、紅外敏感型攝像頭、皮膚電極片構成(圖1[9])。刺激閃光由RGB(紅色、綠色、藍色)組合而成,閃光包括兩個強度的照度,即16Td·s和32Td·s;頻率為28.3Hz;強度為3.0(cd·s)/m2;脈沖時間為1ms。檢測時將電極貼片與設備連接,皮膚電極貼片貼于受檢者下瞼下方約1cm處,由檢測者手持設備,將設備放置于待檢測眼前方,囑受檢者注視設備中作為引導的紅色固視燈,紅外攝像頭將受檢者瞳孔大小對不同閃爍光照度的反應進行攝像并分析,檢測過程約3min。RETeval對受檢者的檢測指標包括16Td·s和32Td·s照度下的視網膜電生理振幅、隱式時間及瞳孔面積,通過“DR評估”模式進行分析檢測結果得到一個綜合數據結果,即RETeval的“DR評估得分”,設定正常范圍為7.0~19.9分[9-10]。
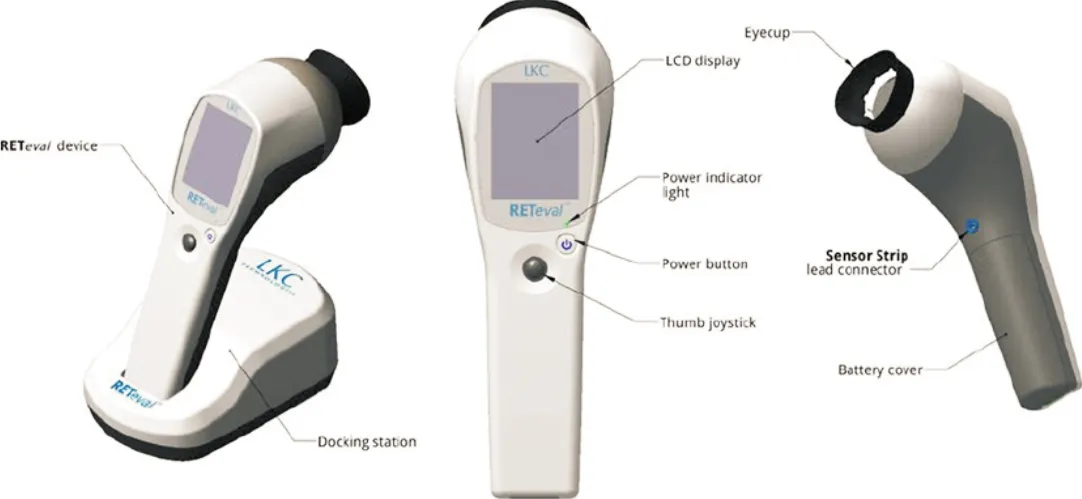
圖1 RETeval組成示意圖 RETeval主要由光照刺激發生器、記錄器、分析系統為一體的儀器及與受檢者相連的皮膚電極片組成。
2 OCT及OCTA的原理及優勢
OCT的出現徹底改變了玻璃體視網膜狀況的臨床評估和研究[11],現已被廣泛運用于臨床。OCT是基于光學技術和計算機圖像分析等技術,由低相干光源和 Michelson光纖干涉儀組成,利用低相干光源對眼內不同組織橫截面進行掃描的技術(圖2[12])。OCT通過光敏測量儀對干涉光進行探測轉化為數字,并經計算機處理生成圖形及數字,提供定性的視網膜三維斷層圖像、顯示視網膜各層結構,并可定量測量黃斑水腫厚度,視網膜、視網膜神經纖維層(retinal nerve fiber layer,RNFL)厚度等。
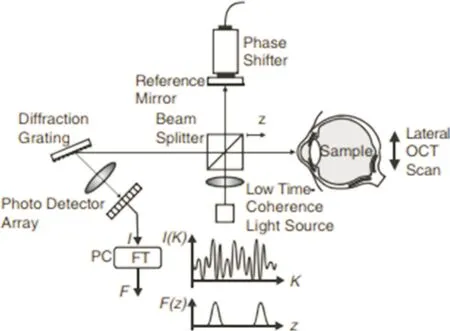
圖2 OCT原理示意圖。
近年來在OCT技術發展的基礎上,衍生出了OCTA。OCTA利用視網膜血管中流動的紅細胞與其周圍相對靜態組織所產生隨機干涉光譜的差別,通過對同一個部位進行連續多次掃描,對同一點多次OCT信號強度進行處理后構建出視網膜微血管網(圖3[12]),是一種無需造影劑的、非侵入性的血管成像技術[13]。OCTA可觀察視網膜及脈絡膜的血管形態、量化血流密度、顯示黃斑中心凹無血管區(foveal avascular zone,FAZ)的大小和形狀、形成的新生血管,同時還能對黃斑區視網膜各層結構進行分層、定量檢測視網膜各層厚度。

圖3 OCTA原理示意圖。
OCT及OCTA檢查在操作上無創、快捷、可重復性強,有利于提高患者依從性,可用于早期篩查,同時能直觀地觀察視網膜各層血管形態,提供血管及神經可量化的客觀數據,對DR的臨床診斷、隨訪、療效評價及相關研究有重要意義。OCT及OCTA檢查與FFA檢查的優勢及局限見表1。
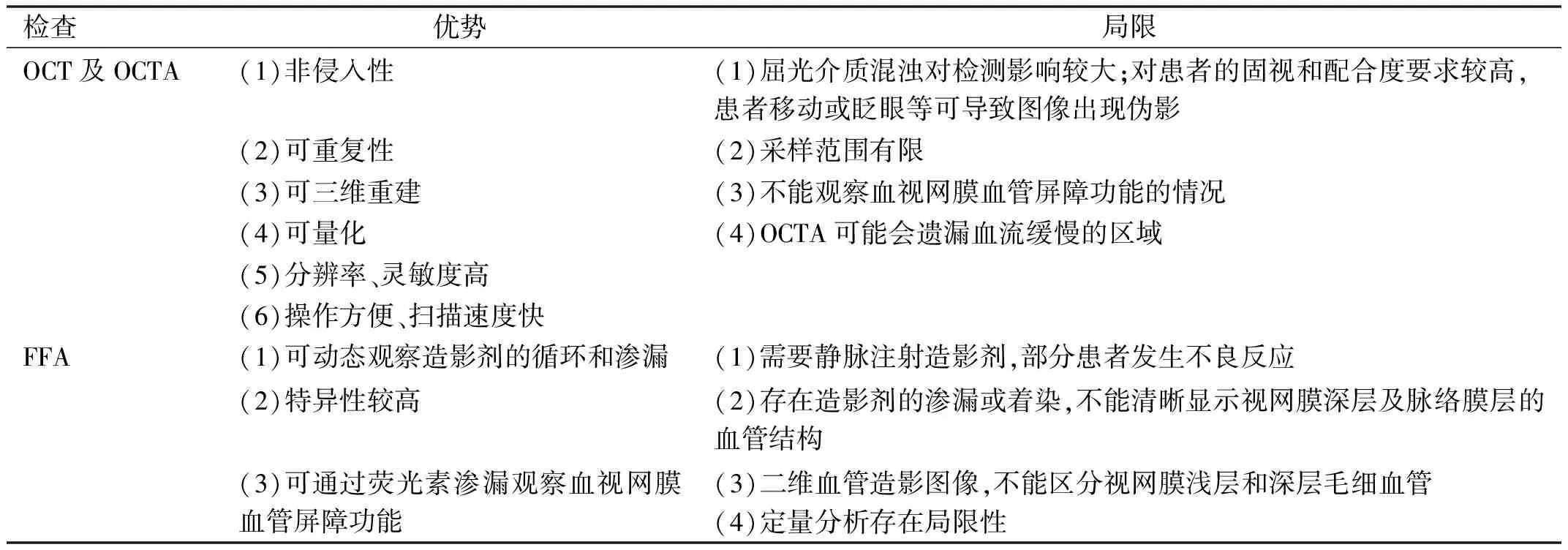
表1 OCT及OCTA檢查與FFA檢查的優勢及局限
3 RETeval在DR中的應用
RETeval是一種手持式的ERG檢測儀器,能對受檢者對光刺激產生的電信號振幅、隱式時間、閃爍ERG波形及瞳孔面積進行測量,并通過自帶程序對這些檢查結果進行實時分析,即時報告受檢者對應的“DR評估得分”,以達到評估視網膜的電生理功能的目的,進而反映視網膜神經組織的情況。
RETeval設備帶有“DR評估得分”,該程序可通過綜合分析受檢者振幅、隱式時間及瞳孔面積,得出一個綜合數據結果,作為“DR評估得分”(圖4)。Maa等[14]通過對5組視網膜病變嚴重程度不同的DM患者468例研究顯示,當“DR評估得分”的正常值設定為7.0~19.9分時,對DR檢測的靈敏度為83%,特異性為78%,陰性預測值達99%;Fukuo等[15]通過對118例不同嚴重程度DR患者進行RETeval檢測,結果表明,DR的嚴重程度與隱式時間和幅度之間存在顯著相關性;Al-Otaibi等[16]通過分析400例DM患者的RETeval檢測數據發現該裝置的靈敏度高達95.4%;Zeng等[17]發現“DR評估得分”與HbA1c的升高顯著相關。上述研究表明DM患者早期電生理功能即出現損傷,表現為振幅、隱式時間、閃爍ERG波形及瞳孔面積的改變。RETeval可通過對這些改變的檢測及定量分析視網膜電生理功能的損傷程度,間接提示視網膜尤其是視網膜神經節細胞的功能完整性情況。同時RETeval的檢測過程為非侵入性、免散瞳,對操作者的技術水平要求較低且能夠即時報告檢測結果。因此,RETeva可作為首選篩選工具為臨床DR篩查提供更快更準確的檢測信息,是適用于大規模DR篩查的新興檢測手段。然而,RETeval仍存在一定的局限性,如特異度較低、僅對電生理功能信息進行分析等。因此應將其與OCT、OCTA聯合應用,排除視神經等相關疾病的影響,客觀且全面地對視網膜情況進行評估。
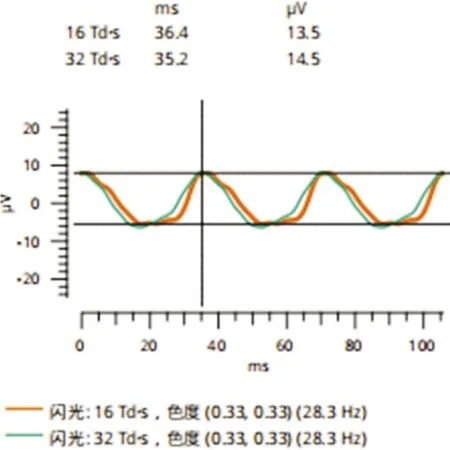
圖4 RETeval運用“DR評估程序”顯示的ERG波形 紅線:16Td·s照度下受檢者的隱式時間(ms)和振幅(μV);綠線:32Td·s照度下受檢者的隱式時間(ms)和振幅(μV)。
4 OCT及OCTA在DR中的應用
4.1OCT OCT問世以來已經成為臨床上針對DR患者黃斑區改變的重要檢測工具,其對黃斑水腫程度及范圍的檢測有利于對DR病程的判斷及治療效果的評價。同時,隨著技術的發展,臨床及科研工作者逐漸開始利用其對視網膜黃斑以外的病變進行研究,對視網膜各層的形態學檢查及定量的厚度檢測已經成為新的研究熱點。OCT對黃斑情況及視網膜各層厚度的檢測有利于DR的早期診斷及治療,同時也為視網膜神經退行性病變的研究提供了更多的信息和新的思路。
4.1.1糖尿病性黃斑水腫糖尿病性黃斑水腫(diabetic macular edema,DME)指黃斑區毛細血管滲漏所導致的黃斑中心2個視盤直徑范圍內的視網膜增厚,是發達國家影響DM患者視力的最主要原因。OCT能對黃斑的水腫范圍、水腫程度以及各層視網膜組織形態改變進行定性、定量分析[18]。
Arf等[19]回顧性評估了309例406眼DME患者的情況,發現囊樣水腫是DME最常見的類型,同時發現黃斑水腫程度與最佳矯正視力呈負相關;Boyer等[20]將1 048例DME患者分為3組,分別給予地塞米松(Dexamethasone,DEX)0.7、0.35mg和假性治療,應用OCT記錄了DEX植入后中央黃斑厚度(central macular retinal thickness,CRT)的變化情況,每3mo對治療后的DME患者進行1次OCT檢測,平均隨訪時間為24.9(中位數16)mo,發現DEX植入物劑量0.7mg組CRT平均降低的均值為-111.6μm,DEX植入物劑量0.35mg組為-107.9μm,DEX植入物0.7mg組和0.35mg組較假性治療組(-49.6μm)CRT平均降低的均值明顯較大(均P<0.001)。
OCT可定量檢測黃斑水腫的范圍及厚度,其可重復性為臨床橫向對比及縱向分析提供了可能,為DME治療方案的研究提供了重要工具。目前OCT已被廣泛運用于臨床及科研,已成為DME治療指南中推薦的檢查,運用OCT對DME進行人工智能的篩查及隨診已成為研究新熱點[21]。
4.1.2視網膜各層厚度研究發現,在眼底出現可見的微血管病變之前已經發生視網膜神經病變[22-25]。視網膜厚度可以間接反映神經節細胞及其軸突等的數量變化,因而通過檢測其厚度,可以間接反映細胞的活性,判斷視網膜的健康程度[22]。Park等[23]對無DR的2型DM患者與正常健康人群進行OCT檢測,發現與正常健康人群相比DM患者RNFL厚度明顯變薄,提示OCT可以檢測無DR的DM患者早期視網膜損傷情況;史強等[24]研究表明DM患者在發生DR前會出現RNFL變薄、視功能對比敏感度下降;尹玉如等[25]研究發現無DR的DM患者視盤周圍RNFL厚度顯著變薄,非增殖性糖尿病視網膜病(non-proliferative diabetic retinopathy,NPDR)組的RNFL厚度和放射狀視盤周圍毛細血管叢(radial peripapillary capillaries,RPC)血流密度顯著降低。因此利用OCT對視網膜各層厚度進行定量研究,可以間接反映視網膜神經組織的情況,具有早期診斷、早期防治的重要意義。
4.2OCTA OCTA現已成為對DR患者視網膜血管情況評估的重要檢查,廣泛運用于臨床,為DR的診斷及療效分析提供全面且可定量的信息。目前OCTA對DR的檢測主要集中于視網膜微血管改變,包括視網膜微血管瘤、視網膜新生血管(retinal neovascularization,RNV)及視網膜缺血情況,如FAZ面積及視網膜毛細血管密度等。OCTA可對無法在FFA上觀察到的RPC情況進行評估,并一定程度反映DR患者視網膜神經的早期病變,其對DR患者血管改變的評估不僅可以作為FFA的補充為診療提供更全面的信息,還有利于闡明DM對視網膜血管的影響,發現DR的早期病變,并為DR的治療提供更多思路。
4.2.1黃斑中心凹無血管區受DR影響,黃斑旁中心凹的血管組織異常代謝,引起FAZ的擴大及變形,這一改變也被認為是DR最早出現的臨床體征。有研究應用FFA與OCTA同時檢測DR患者的FAZ面積,發現兩者有較高的一致性,證明OCTA技術的可靠性[26]。Takase等[27]應用OCTA測量63例患者FAZ面積,得出表層血管網中FAZ面積在健康對照組、無DR的DM組、DR組中分別為0.25±0.06、0.37±0.07、0.38±0.11mm2,發現在眼底未出現臨床征象視網膜病變的DM患者中FAZ面積較健康對照組增加,表明即使在視網膜病變發生之前,糖尿病患者眼部就已經顯示出黃斑部的視網膜微循環損傷。提示OCTA可通過對FAZ面積的量化監測其改變,有助于對DR進行篩查及早期診斷,便于隨訪及療效評價。
4.2.2視網膜微動脈瘤根據DR診斷標準,視網膜微動脈瘤(retinal microaneurysms,RMAs)是DR早期形態學的特征性改變,RMAs是由于血管壁損傷后抗壓能力降低而導致的局部擴張。
Mendis等[28]運用FFA對10名健康受試者進行檢測,并對5只尸體眼進行組織學研究,對兩組中來自等效視網膜區域的毛細血管進行形態學和定量分析。在組織學標本中,淺表毛細血管網的密度顯著大于深層毛細血管網的密度,但僅30%的FFA圖像提供了與組織學相匹配的清晰毛細管圖像,FFA圖像中的毛細血管網絡密度始終低于組織學圖像,其提供的有關淺表毛細血管網絡的形態學信息不完整,而有關深層毛細血管網絡的信息則更少;Haritoglou等[29]研究發現RMAs與DME形成密切相關,RMAs可能是DME發生的預兆。由于OCTA不存在熒光素滲漏,RMAs的形態及大小較準確,其可作為FFA檢查的初步檢測,有利于完整、準確地觀察并量化RMAs病變。同時提示臨床可對RMAs進行監測從而提前預防DME的發生。
4.2.3視網膜新生血管RNV是由于缺氧、缺血、創傷和腫瘤等原因使得促血管生長因子與血管生成抑制因子之間的平衡被打破而出現的增殖性糖尿病視網膜病變(proliferative diabetic retinopathy,PDR)特征性體征,可導致玻璃體出血、視網膜脫離和視力喪失[30]。
Lee等[31]通過對8例DM患者的23處視網膜病變進行觀察,發現OCTA在觀察RNV時相對于FFA更為清晰且檢出率更高;Russell等[32]通過對PDR患者651眼的FFA及OCTA檢查結果進行回顧性分析發現,OCTA有利于觀察新生血管的細微變化,可顯示FFA無法顯示的病變。由于OCTA的分辨率較高,可檢測到FFA無法顯示的新生血管病變的細微變化,顯像清晰,可重復性強,檢出率高,在RNV的檢測及療效分析中有獨特優勢。
4.2.4視網膜毛細血管密度RPC是視盤區域特殊的毛細血管叢,具有血管較長、直及分支少等解剖特點,對高糖及缺血缺氧等病理刺激較敏感[33],OCTA可對無法在FFA上觀察到的RPC的情況進行評估,并一定程度反映DR患者視網膜神經的早期病變。Rabiolo等通過OCTA檢測
發現對照組(健康人群)、DM組的RPC血流密度分別為0.466±0.015、0.448±0.043(P<0.001),與正常對照組相比,沒有觀察到DR臨床指征的DM患者RPC灌注密度更低[34]。Cao等[35]研究發現RPC血管密度與RNFL厚度及最佳矯正視力呈負相關;李海東等[36]發現與健康體檢者比較,NDR組患眼平均及各象限RPC血流密度均降低。
目前臨床上OCTA主要運用RMAs、RNV等指標評價較晚期DR病變,而RPC主要用于青光眼、前部缺血性視神經病變等疾病中對于神經系統病變的檢測。近年來對RPC的研究提示在DR視網膜黃斑區發生微血管改變之前,RPC的血流灌注已經受到影響。OCTA提供的RPC情況,在沒有出現DR診斷指征的DM患者中視網膜的血流灌注已經出現了損傷,同時血流密度的改變與視網膜神經組織的損傷存在一定的相關性,提示RPC血流密度的改變可以在一定程度反映DM患者視網膜神經的早期病變。
5小結及展望
DR對神經及血管的損傷較難逆轉,如何實現DR早期診斷、早期治療是一項重要的社會課題。現階段實現DR的早期診斷仍有困難。一方面,昂貴的檢測費用以及現有技術手段限制了對DR的篩查,如臨床上的DR患者多合并有心臟、腎臟等方面的全身疾病,一部分患者不適合行FFA等檢查;眼底檢查等操作不可量化、對技術要求較好,不適用于基層醫院及內分泌等相關科室的篩查。另一方面,目前臨床對DR患者的檢測及診治主要針對于微血管損傷及視功能發生損害之后,視功能受到損害之前患者對眼底的檢查不夠重視。
OCT、OCTA以及RETeval等檢查方便快捷、非侵入、依從性高,其檢測結果可量化、結果解釋簡單,可全面、便捷地提供神經組織、血管組織、電生理功能等可定量信息(圖5)。在疾病診斷方面,這三種檢測手段可重復性強,檢測結果可量化,為未來AI診治及遠程診斷提供可能性;在治療方面,這三種檢測手段可以分別從神經、血流及視網膜電生理方面,以NVU作為整體反映DR患者視網膜的早期病理性改變,靈敏全面地在DM患者眼底出現不可逆病變之前,檢測高血糖對視網膜造成的損傷,在視網膜神經系統受到不可逆損傷前進行臨床干預。研究神經血管損傷及其與DR危險因素的相關性,為DR的早期診斷及治療提供了新的思路,對DR患者的預后改善具有重大意義。

圖5 DR病變過程及檢測手段。

