胸腺肽制劑的質量及安全風險分析
陳小英,楊亞婷,王嫦鶴,劉海靜*
1.陜西中醫藥大學,咸陽 712046;2.陜西省食品藥品檢驗研究院,西安 710065
胸腺為機體的重要淋巴細胞器官,是T細胞分化、發育、成熟的場所[1]。胸腺肽是從健康豬或小牛胸腺中提取的具有生物活性的多肽類混合物,相對分子質量小于10 000道爾頓[2],其中公認為胸腺肽的有效成分是由28個氨基酸組成的胸腺肽α1(Tα1)。我國從1973年開始研究胸腺肽,在20世紀80 年代末改進并簡化了胸腺組分5(TF5)的制備工藝,使制品的相對分子質量控制在10 000道爾頓以下[3]。胸腺肽制劑臨床上常用的劑型有腸溶片劑、腸溶膠囊和注射劑。胸腺肽能誘導淋巴細胞分化、增殖與成熟,增強巨噬細胞吞噬和抗原遞呈功能,提高白細胞介素應答水平,可以調節機體的免疫功能[4]。胸腺肽制劑常用于各種原發性或繼發性T細胞缺陷病、某些自身免疫性疾病、慢性疾病、乙型肝炎、各種細胞免疫功能低下的疾病以及腫瘤的輔助治療等。
1 國內現有的生產企業和批號
胸腺肽制劑市場需求量大,全國生產胸腺肽制劑的企業較多,通過在國家食品藥品監督管理局網查詢并統計,我國市場上現有的胸腺肽制劑生產企業和批準文號分別為75家和243個。見表1。
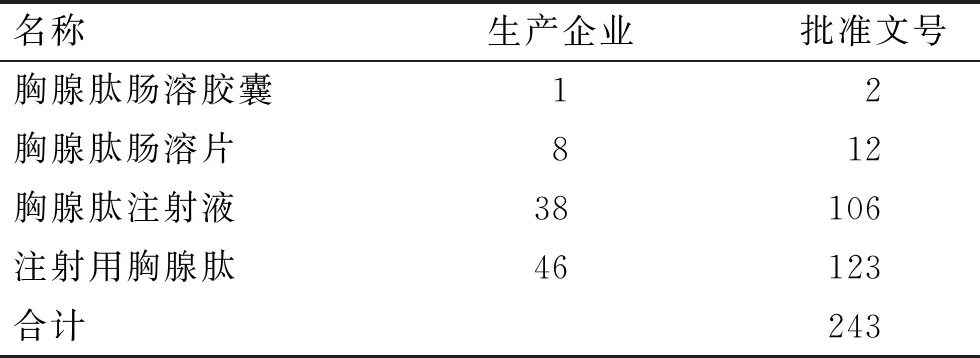
表1 胸腺肽制劑生產企業和批準文號
2 胸腺肽的生產工藝
目前國內生產的胸腺肽制劑是以健康豬或小牛胸腺為原料,提取高活性的多肽混合物。通過查閱文獻,胸腺肽提取主要有常規提取法、酸堿提取法和化學酶解法。
常規提取法:胸腺勻漿反復凍融,通過水浴解凍,離心沉淀,取上清液置于水浴中加熱80 ℃,調節pH值為中性,超濾,用滯留相對分子質量為1.0×104的超濾膜進行超濾,即得胸腺肽溶液[5-7]。
酸堿提取法:加鹽酸調節胸腺勻漿pH值至3.5,反復凍融3次,離心后調節pH值為6.5,超濾,用滯留相對分子質量為1.0×104的超濾膜進行超濾,即得胸腺肽溶液[5-7]。
化學酶解法:胸腺勻漿加入適當的木瓜蛋白酶水解,調節pH值為7.0,在37 ℃水浴中保溫數小時,加鹽酸調節pH值為3.5,水浴加熱,冷卻至室溫,用氫氧化鈉調節pH值為6.8,離心沉淀,超濾,用滯留相對分子質量為1.0×104的超濾膜進行超濾,即得胸腺肽溶液[8]。
常規提取法和酸堿提取法屬于物理提取方法,化學酶解法屬于化學提取方法。化學提取方法提取的多肽含量大于物理提取法,但是活性低于物理提取方法。物理提取法中,酸堿提取法的多肽含量和活性均大于常規提取法[5-8]。
3 胸腺肽注射劑現行標準及其存在的問題
胸腺肽制劑均屬于多組分生化藥,成分復雜。現行胸腺肽制劑的質量標準主要是化學藥品地方標準上升國家標準第16冊、新藥轉正標準第44冊和各企業標準,各標準中具體的檢驗項目見表2。胸腺肽制劑中的檢驗項目比較簡單,有效性和安全性指標未做出具體的規定。在現有標準中均缺少基原鑒定,無法控制藥品原料的動物來源。不同企業中胸腺肽生產工藝不同,導致胸腺肽特征圖譜差異較大,表明不同企業的胸腺肽制劑在質量中存在一定的差異,在質量標準中應添加胸腺肽專屬性鑒別項目,從而規范胸腺肽生產工藝,在一定程度上可以保證胸腺肽制劑的質量。
胸腺肽制劑的原料為健康豬或小牛胸腺,其原料的特殊性易受致病微生物、病菌等污染,人體過多攝入有害物質,可增加臨床不良反應風險。應高度關注胸腺肽制劑中生物胺含量、獸藥殘留、重金屬、病原微生物及病毒等安全性指標,對可能引起不良反應的因素進行控制,增強臨床用藥的安全性,保證廣大患者的利益。

表2 胸腺肽制劑的標準
4 胸腺肽制劑的不良反應
胸腺肽制劑中注射劑的不良反應報道較多, 2007~2013年胸腺肽注射劑的不良反應文獻有47篇,不良反應有101例[9]。2003~2011年共收到懷疑與胸腺肽注射劑有關的不良反應報告5 459例[10]。胸腺肽注射劑的不良反應主要有皮疹、心悸、發熱、惡心、胸悶、嘔吐、呼吸困難、支氣管哮喘、嚴重可導致過敏性休克等[11-12]。胸腺肽注射劑引起不良反應的主要原因為,注射劑具有高風險的特點[13-15],在臨床使用上引起的不良反應概率比傳統的口服劑型要高[16];胸腺肽是從動物臟器中提取的多肽混合物,在原料提取加工貯存過程中容易產生對人體有害的物質。
5 胸腺肽制劑存在的安全問題
胸腺肽溶液是從健康豬或小牛胸腺中提取的無菌溶液。動物胸腺來源復雜,組成不明確,動物健康狀況無法得到保證。胸腺肽制劑在原料和加工過程中易引入有害物質,比如生物胺、獸藥殘留、重金屬、致病微生物和病毒等。應控制這些有害物質,提高胸腺肽制劑的安全性,從而保證臨床用藥的可靠性。
5.1 生物胺
生物胺是一類具有生物活性的含氮的低相對分子質量有機化合物的總稱。生物胺主要包括腐胺、尸胺、精胺、亞精胺、酪胺、苯乙胺、組胺、色胺等[17]。生物胺常存在于動物類中藥或以動物為原料的生物藥品中。生物胺中組胺毒性最強,主要表現為頭疼、胸悶、腹瀉、心率增加、血壓下降、甚至休克;其次是酪胺可引起血壓升高、偏頭痛、呼吸困難;尸胺、腐胺可增加組胺和酪胺的毒性,尸胺、腐胺、精胺和亞精胺可與亞硝酸鹽反應產生亞硝胺致癌物質[18-19]。
動物源食品中檢測生物胺含量的方法比較成熟,常采用柱前衍生反相高效液相色譜法測定生物胺的含量[20-22]。在動物中藥材中生物胺的研究也比較普遍,比如對蜈蚣、鹿茸采用柱前衍生化的方法,使用高效液相色譜法(HPLC)測定生物胺的含量[23-24]。以動物為原料的生物制品中生物胺的測定也常用此方法,蘇喆等[25]對鹿瓜多肽注射劑中的生物胺應用柱前衍生化反相高效液相色譜法進行測定,該法專屬性、精密度、線性關系以及回收率等均良好。徐學平等[26]采用柱前衍生的方法對胸腺中的組胺進行測定,在胸腺中均可測出組胺。可以借鑒文獻中生物胺的測定方法,對胸腺肽制劑中生物胺的含量進行測定。
5.2 獸藥殘留
獸藥可用于預防和治療動物疾病,科學規范地使用獸藥,能有效預防動物疾病,促進動物生長,提高產量,改善動物質量。但是,一些飼養戶在經濟利益的驅使下,為了促進動物生長和提高產量,違規或過多地使用獸藥,使過多的獸藥殘留在動物體內[27]。獸藥殘留分為4類:抗生素類(四環素類、磺胺類、喹諾酮類、氯霉素等)[28];抗病毒類(美金剛、嗎啉胍、金剛烷胺、金剛乙胺等)[29];激素類(己烷雌酚、己烯雌酚、雌酮、雌二醇等)[30];抗寄生蟲類[31](苯并咪唑類藥物)。其中抗生素類占所有獸藥添加劑的60%,是最主要的獸藥殘留藥[32]。動物飼養過程中獸藥的濫用,導致在動物源食品和藥品中獸藥頻繁被檢出。胸腺肽原料來自健康豬或小牛胸腺,動物來源復雜,生產廠家對動物來源控制薄弱,缺乏統一的監管體系,未對胸腺中獸藥殘留進行控制。
獸藥殘留的檢測主要使用酶聯免疫吸附(ELISA)法、HPLC法、氣相色譜-質譜聯用法、液相色譜-四級桿-質譜法等[33]。超高效液相色譜-串聯質譜法具有高效、靈敏、快速、選擇性好等優勢,現廣泛應用于獸藥殘留檢測[34-35]。獸藥殘留越來越受到企業和個人的關注,對動物類中藥和以動物類為原料的中藥制劑中獸藥殘留進行檢測,比如檢測梅花鹿鹿茸中獸藥殘留[36];中藥膏劑中蜂蜜的獸藥殘留用高效液相色譜-串聯質譜法,該方法在相應的濃度范圍內線性關系良好[37]。胸腺肽制劑原料來源于健康豬或小牛胸腺,在動物生長過程中,養殖戶是否過量地使用獸藥或使用禁用獸藥,提高動物生產繁殖能力和產量,生產企業未對獸藥殘留進行檢測,無法確保原料安全。
5.3 重金屬
胸腺肽來自健康豬或小牛胸腺,動物是人工養殖,水、土壤、肥料的使用可能引入重金屬[38]。胸腺肽制劑在生產過程中會引進鋁、鉻、鐵、鋇等重金屬,胸腺肽注射劑內包材常采用玻璃包裝,會引入硼、鋁、硅等元素[39]。研究表明,重金屬對人體的代謝和正常的生理作用會造成明顯的損害,當體內重金屬過量時會嚴重危害人體健康[40]。
重金屬的檢測方法主要有原子吸收光譜法、紫外分光光度法、原子熒光光譜法、電感耦合等離子體質譜(ICP-MS)等[41],其中ICP-MS為重金屬常用的檢測方法,因其操作簡單、結果準確可靠[42-43]。ICP-MS廣泛用于動物類中藥材中重金屬的測定[44],李勇等[45]使用ICP-MS方法對地龍和水蛭中的重金屬及有害元素進行測定。胸腺肽注射劑臨床用法是皮下或肌肉注射、靜脈注射,不經過肝臟的首過效應,直接進入人體,微量的重金屬對人體都可能產生很大的危害。為了確保臨床安全性,應關注胸腺肽制劑中重金屬的含量。
5.4 病原微生物及病毒
動物在飼養過程中很容易被病原微生物污染,比如肉毒梭菌、沙門氏桿菌、巴氏桿菌[46]、布魯氏菌、副結核分枝桿菌等。檢測病原微生物的主要技術有病原學檢查、ELISA、膠體金免疫層析技術、聚合酶鏈式反應(PCR)檢測法、生物芯片技術等方法[47]。蔡珠明等[48]采用IS900-PCR分離鑒定得到3株牛型副結核分枝桿菌。何亞鵬等[49]采用多重PCR方法同時檢測豬種、牛種、羊種、綿羊種布魯氏菌,該方法因其特異性強、敏感度高、穩定性好的特點,可用于生物制品污染的布魯氏菌的快速檢測。
國際上現有對生物制品中病毒安全性控制的標準或指導原則主要有:生物技術產品的病毒安全性評價;日本藥典(JP17,所列生物技術/生物制品病毒安全的基本要求);美國藥典(USP41 1050,人源或動物源細胞系制備的生物技術產品的病毒安全性評價)等。各標準或指導原則雖然都具有科學性和規范性,但是均未涵蓋所有相關生物制品。目前國內現有的指導原則有:國家食品藥品監督管理總局(CFDA)發布的“血液制品去除/滅活病毒技術方法及驗證指導原則”;“生物組織提取制品和真核細胞表達制品的病毒安全性評價技術審評一般原則”。現行藥典未對生物制品中通用病毒進行相關的規定[50]。
6 展望
胸腺肽制劑屬于多肽類藥物,生物活性高和特異性強,但其穩定性差和半衰期短。胸腺肽制劑的生產工藝不同,使其有效性差異較大,導致臨床療效差異性大。胸腺肽制劑在臨床上得到廣泛的應用,但不良反應報道多,易出現呼吸困難、休克甚至死亡等嚴重不良反應,應引起高度重視。健康豬或小牛胸腺是胸腺肽制劑的原料,動物在飼養過程中易感染致病微生物和病毒,易攝入過多的重金屬,過多地使用獸藥。在生產和貯藏的過程中產生對人體有害的生物胺。生物胺、獸藥、重金屬、致病微生物等,都增加胸腺肽制劑在臨床上的安全風險,增加不良反應的概率。

