胺碘酮致甲狀腺功能異常的研究
王小菡,劉云兵
(1.川北醫學院臨床醫學系,四川南充 637100;2.綿陽市中心醫院心臟電生理中心,四川綿陽 621000)
20世紀60年代胺碘酮作為一種抗心絞痛藥物問世,隨后研究發現胺碘酮可有效抗心律失常[1]。當心動過速時,胺碘酮通過抑制K+通道,延長心肌動作電位時程及有效不應期來終止心動過速。另外,胺碘酮能非特異性阻斷α和β受體,擴張冠狀動脈與外周動脈,有效增加心臟供血與降低外周阻力,是目前公認的能有效降低心肌梗死患者病死率的藥物。胺碘酮在治療心律失常方面有明顯療效,但也有許多不良作用,可能累及皮膚、眼、肺、肝等[2]。研究發現,約20%的患者使用胺碘酮后會出現甲狀腺功能異常[3]。甲狀腺功能異常往往起病隱匿,癥狀輕微,導致不能被及時發現予以干預,因而臨床上使用胺碘酮應增加對甲狀腺功能的監測。本文將從胺碘酮致甲狀腺功能異常的具體機制、臨床分類、后續診療等方面進行綜述。
1 胺碘酮導致甲狀腺功能異常的發病機制
1.1 碘過量效應 胺碘酮是一種苯并呋喃的碘化衍生物,結構與甲狀腺激素相似。胺碘酮具有親脂性,常存在于脂肪等組織中,半衰期較長,在50~100 d。胺碘酮在CYP3A酶的作用下經氨基生物轉化生成去乙基胺碘酮(DEA),具有更長的半衰期,并在組織器官中積累。每200 mg胺碘酮含有75 mg有機碘,隨后在體內代謝成6 mg的有機碘,遠遠超過了正常人每日碘攝入量(0.15~0.30 mg),導致碘過量[4]。
在生理狀態下,當出現碘過量時,過量的碘競爭性抑制過氧化酶的活性并且抑制甲狀腺濾泡內溶酶體的釋放,減少酪氨酸碘化,抑制甲狀腺激素的合成和釋放,從而降低甲狀腺激素的水平,即Wolff-Chaikoff效應。然而這種效應是暫時的,多數機體很快適應使得甲狀腺激素代謝維持正常,促使血清三碘甲狀腺原氨酸(T3)、甲狀腺素(T4)和促甲狀腺激素(TSH)值恢復基線值[5]。這種現象稱為Wolff-Chaikoff效應的逃逸現象。當機體碘的有機化和激素合成未能恢復時,T3、T4持續性減少,容易引起甲狀腺功能減退。此外,人體攝入過量的碘會導致甲狀腺激素合成的增加,即Jod-Basedow效應。在潛在甲狀腺自主結節或潛在Graves病患者中,尤其生活在碘缺乏地區的患者中,暴露于過量碘環境可能發生甲狀腺功能亢進。
1.2 內在藥物效應 胺碘酮主要通過以下3種方式影響甲狀腺功能:①細胞毒性作用;②抑制脫碘酶活性;③抑制T3與其核受體結合[6]。
1.2.1 細胞毒性作用 多項研究證實胺碘酮及DEA對甲狀腺有直接的、劑量依賴性的細胞毒性作用,DEA對甲狀腺的細胞毒性甚至比胺碘酮更大。此外,研究發現胺碘酮可以通過破壞包涵體、明顯擴張的內質網等亞細胞器功能引起甲狀腺結構的明顯扭曲和細胞凋亡、壞死等,對甲狀腺有直接毒性作用,進而導致慢性甲狀腺炎。
1.2.2 抑制脫碘酶活性 在肝臟、腎臟等外周組織中,T4在5'-脫碘酶作用下脫碘生成T3。然而,胺碘酮可以作為甲狀腺激素類似物抑制促甲狀腺激素釋放激素和脫碘酶的活性,抑制T4向T3的脫碘轉化過程[7],導致低T3綜合征的發生,這給心臟病患者維持正常的心臟收縮功能帶來潛在的風險和挑戰。
1.2.3 抑制T3與其核受體結合 胺碘酮和DEA的化學結構與T3非常相似,抑制T3與其核受體結合,從而降低甲狀腺激素相關基因的表達和甲狀腺激素作用的發揮,見表1。
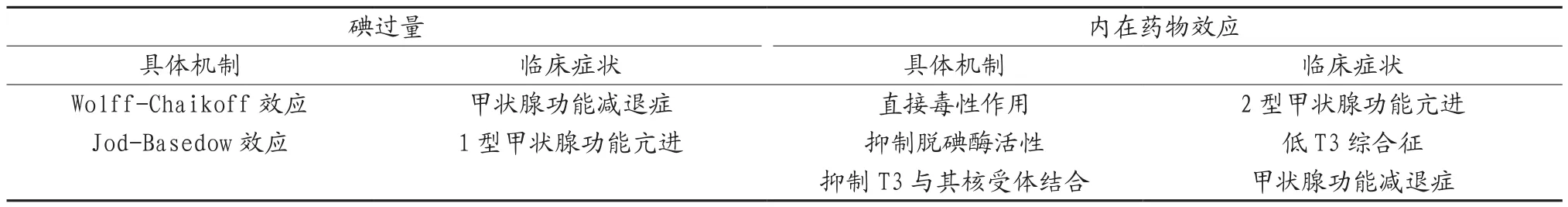
表1 胺碘酮引起甲狀腺功能異常機制
胺碘酮在上述機制的作用下影響甲狀腺激素的代謝,引起甲狀腺功能異常,包括胺碘酮引起的甲狀腺功能減退癥(amiodarone-induced hypothyroidism,AIH)、胺碘酮引起的甲狀腺功能亢進癥(amiodarone-induced thyrotoxicosis,AIT)。AIT又可以分為兩種亞型,即1型AIT和2型AIT。另外,AIT可能存在“混合”形式,即小部分患者可能同時具有以上兩種亞型的特征[8]。
2 胺碘酮引起的甲狀腺功能減退癥(AIH)
AIH常發生在甲狀腺功能正常或潛在甲狀腺功能異常的患者中[9]。流行病學研究發現,碘的攝入量的不同也會引起AIH發病率的差異。在碘攝入量充足的地區(如馬薩諸塞州伍斯特),AIH發生率為22%;相反,在碘攝入量較低的地區與國家(如意大利西托斯卡納)AIH的發生率僅為5%。除了碘攝入量,年齡、性別、橋本氏甲狀腺炎、產生甲狀腺自身抗體等也是AIH的危險因素。其中橋本氏甲狀腺炎是AIH發展和持續的最常見的危險因素,加上女性橋本氏甲狀腺炎的發病率是男性的7倍左右,使得女性AIH的發生率也明顯高于男性[10]。AIH的臨床表現與因其他原因引起的甲狀腺功能減退臨床表現無明顯差異,包括畏寒、皮膚干燥、疲勞、動作遲緩、注意力不集中等。
3 胺碘酮引起的甲狀腺功能亢進癥(AIT)
與大多數甲亢癥狀類似,胺碘酮也能引起心悸、出汗增多、體重減輕、手指震顫等典型癥狀。研究發現,AIT好發于老年人,臨床表現往往呈非典型,如食欲減退和抑郁狀態等,而且男性的發病率更高,約是女性的3倍左右[11]。兩種AIT的臨床表現相似,但是發生機制不同,因此臨床上需要進行鑒別診斷再對癥治療。1型AIT常發生在既往有甲狀腺基礎疾病的患者,如結節性甲狀腺腫、Graves病,特別是當患者平時碘的攝入量較低時或居住在碘缺乏地區時,使用胺碘酮后使機體處于碘過量狀態從而誘導甲狀腺激素合成和釋放過量,引起甲亢的發生。2型AIT較1型AIT更為常見,約有90%的AIT為2型AIT。與1型AIT不同的是,2型AIT在碘攝入量充足的地區更為普遍,且常發生在無潛在甲狀腺疾病的個體中[12]。2型AIT是一種破壞性甲狀腺炎,主要是由于胺碘酮的直接毒性引起甲狀腺濾泡細胞受損,使甲狀腺激素大量釋放。
盡管AIT各亞型臨床癥狀相似,但仍需要對兩種亞型AIT進行鑒別診斷,并予以不同的治療方案。目前常用的鑒別診斷方法如表2所示。
1型AIT常發生于既往有甲狀腺基礎疾病的患者,可以通過回顧病史及利用甲狀腺超聲和甲狀腺彩色血流多普勒超聲進行1型AIT和2型AIT的鑒別診斷。甲狀腺超聲顯示甲狀腺存在彌漫性或結節性甲狀腺腫及甲狀腺彩色血流多普勒超聲發現甲狀腺內血管形成正常或增加,則首先考慮為1型AIT;2型AIT由于甲狀腺破壞而顯示結構扭曲,在甲狀腺彩色血流多普勒超聲上顯示血管形成正常或血管減少,1型AIT顯示血管形成正常或增加[13]。核成像技術也常常用于兩種亞型AIT的鑒別診斷,常用的示蹤劑包括放射性碘(RAI)、99m锝-甲氧基異丁基異腈(MIBI),見表2。大多數2型AIT患者放射性碘攝取量通常較低[14]。有研究表明大多數1型AIT患者攝取[99mTc]-MIBI,相反,2型AIT患者不會攝取[99mTc]-MIBI[15]。1型AIT患者血清甲狀腺自身抗體陽性率較高,但少數2型AIT患者血清中也可檢測到甲狀腺自身抗體[16]。因此通過甲狀腺自身抗體的有無來區分1型和2型AIT并不十分可靠。除此之外,一些生化指標也可以作為鑒別診斷的方法。例如馬爾坎特斯等人在2019年發現血漿β-葡萄糖醛酸酶是一種在炎癥過程中釋放到細胞外液中的溶酶體酶,其在2型AIT患者中酶活性更高,因此血漿β-葡萄糖醛酸酶可較好區分1型AIT和2型AIT[17]。在鑒別診斷過程中當同時存在1型和2型特征時,這種情況可能是屬于混合型AIT,這使得診斷和治療都更加復雜。

表2 AIT-1和AIT-2的鑒別診斷方法
4 胺碘酮引起甲狀腺功能異常的治療
4.1 AIH的治療 胺碘酮引起的甲狀腺功能減退癥包括亞臨床AIH與AIH,其中亞臨床AIH沒有具體的癥狀,一般不需要用甲狀腺激素進行替代治療。AIH的治療方案是通過補充甲狀腺素來改善甲狀腺功能。目前臨床上常用左旋甲狀腺素(L-T4)與胺碘酮進行聯合治療。但是在初次使用L-T4時應從低劑量開始,根據患者的FT4、 FT3/總三碘甲腺原氨酸(TT3)和TSH水平及患者的心臟狀況逐步調整劑量,在給藥過程中監測患者的臨床表現及血清中TSH等水平[18]。
4.2 AIT的治療
4.2.1 1型AIT的治療 1型AIT是由于甲狀腺激素合成和分泌過多所導致,因此治療1型AIT最有效的方法是阻斷甲狀腺激素的合成與分泌。硫代酰胺藥物如甲巰咪唑、卡比咪唑、丙硫氧嘧啶通過抑制甲狀腺過氧化物酶,減少T3和T4的合成而發揮作用。此外丙硫氧嘧啶還可以抑制外周脫碘酶的活性,抑制T4向T3的轉化[19]。但是隨后研究發現丙硫氧嘧啶具有潛在的肝毒性[20],因而臨床上目前常用高劑量的甲巰咪唑(40~60 mg/d)進行治療。如果使用甲巰咪唑治療后3~4周后,患者甲狀腺功能仍亢進,可以通過聯合高氯酸鉀抑制鈉-碘同向轉運體,阻斷碘化物進入甲狀腺從而減少甲狀腺內碘存儲,以提高治療效果。值得注意的是,研究發現大劑量應用甲巰咪唑可能會引起骨髓抑制,因此需要每兩周檢測患者白細胞的水平。除抗甲狀腺藥物之外,鋰也可以抑制甲狀腺激素的分泌,但由于其不良反應較嚴重,因所以其臨床應用受到限制。患者是否能夠停用胺碘酮需要根據其心血管危險程度等方面進行綜合研判。目前認為患有危及生命的心律失常和預后不良的危重患者應繼續使用胺碘酮。綜合評估后可以停用胺碘酮的患者即使立即停藥,也需要繼續使用甲巰咪唑直到尿碘水平恢復正常。當患者可以停用胺碘酮并且尿碘水平恢復正常時,也可考慮用放射性碘治療甲狀腺毒癥。
4.2.2 2型AIT的治療 2型AIT的嚴重程度與甲狀腺損傷的程度密切相關,且該病通常具有自限性,可以自發性緩解[21]。當患者僅有輕微的甲狀腺功能亢進且心臟功能穩定時,可以不進行額外藥物干預,隨訪檢測甲狀腺功能即可。一旦患者表現出明顯的甲狀腺功能亢進時,或當由于潛在的心臟狀況而需要快速恢復甲狀腺功能正常時,應立即予糖皮質激素治療。糖皮質激素具有抗炎和膜穩定作用,可以減輕破壞性和炎癥反應。臨床上常用40~60 mg/d的潑尼松持續處理2~4周,隨后依據患者的臨床表現和實驗室生化指標在用藥后2~3個月內逐漸減少給藥劑量。
4.2.3 混合型AIT的治療 當抗甲狀腺藥物或糖皮質激素單獨治療不能改善甲狀腺功能亢進時,應考慮混合型AIT的可能。對混合型AIT,抗甲狀腺藥物與糖皮質激素為期兩周聯合治療可能是最有益的治療方案。在治療過程中仍要考慮大劑量甲巰咪唑可能引發的骨髓抑制等副作用的影響。
4.2.4 嚴重AIT的治療 對于藥物難治性病例,需要考慮其他治療方法。血漿置換法可以迅速清除循環中的碘和過量的甲狀腺激素,但是其成本高,并且只能發揮瞬時效應,因而一般在重度AIT患者甲狀腺全切除術前使用。當心功能進行性惡化或左心室射血分數(LVEF)降低,死亡風險增加或嚴重基礎心臟病或惡性心律失常,及對抗甲狀腺藥物或糖皮質激素治療無效的AIT患者可以考慮切除甲狀腺從而快速控制甲狀腺功能亢進[22]。
5 小結
胺碘酮是臨床上廣泛使用的抗心律失常藥物,但是由于其富含碘元素和具有細胞毒性作用等原因,在胺碘酮治療心律失常期間常常導致會甲狀腺功能異常。因此,用藥期間,需要密切監測患者的甲狀腺功能。當患者出現明顯的甲狀腺功能亢進或甲狀腺功能減退時,立即對患者心臟功能和甲狀腺功能進行評估,并予以適當的處理。值得注意的是,需要正確鑒別1型、2型或混合型AIT才能施行有效的治療。

