急性失代償性心力衰竭病人血漿組織蛋白酶S和血小板反應蛋白-1水平與預后的關系
劉婷婷,劉 麗,林文果,黃大崗
急性失代償性心力衰竭(acute decompensated heart failure,ADHF)是病人突然發生心臟收縮、舒張功能不全或心律失常等心臟功能障礙,并迅速達到高峰,以呼吸困難為突出表現的一類臨床綜合征[1]。組織蛋白酶(cathepsin,Cat)屬于半胱氨酸蛋白酶家族,Cat S是其中一種,作為靶標蛋白質參與多種疾病的發生及發展過程[2]。血小板反應蛋白-1(thrombospondin-1,TSP-1)是重要的細胞外基質糖蛋白,有多個功能區結合位點,可與不同受體結合參與機體生理、病理進程[3]。研究表明Cat S、TSP-1與心力衰竭密切相關[4],但與ADHF及其預后關系的報道較少。本研究旨在探討ADHF病人血漿Cat S和TSP-1水平及其與預后的關系。
1 資料與方法
1.1 臨床資料 選取2017年1月—2019年12月我院收治的165例ADHF病人為研究對象,年齡47~83歲。根據紐約心臟病協會(New York Heart Association,NYHA)標準進行心功能分級。納入標準:①符合《中國心力衰竭診斷和治療指南2014》中ADHF診斷標準[5];②NYHA心功能分級Ⅲ級或Ⅳ級;③年齡≤85歲。排除標準:①肥厚性心肌病;②存在心臟瓣膜病;③6個月內有心肌梗死史;④合并全身感染;⑤合并免疫缺陷;⑥合并嚴重肝、腎功能障礙;⑦合并惡性腫瘤;⑧臨床資料不完整。本研究通過醫院倫理委員會批準,研究對象均簽署知情同意書。
1.2 方法
1.2.1 左心室射血分數(left ventricular ejection fraction,LVEF)檢測 研究對象入院24 h內行超聲心動圖檢查,靜息狀態下取左側臥位,檢測記錄LVEF,儀器為飛利浦iEElite型心臟彩色多普勒超聲儀,探頭頻率為2.5~3.5 MHz。
1.2.2 血漿Cat S、TSP-1水平檢測 研究對象入院24 h內抽取5 mL空腹靜脈血。采用酶聯免疫吸附法(enzyme linked immunaosorbont assay,ELISA)檢測血漿Cat S、TSP-1水平,儀器為Thermo Scientific Varioskan LUX多功能酶標儀,試劑盒均購自武漢博士德生物工程公司,嚴格按照試劑盒說明書操作。另外,收集并記錄研究對象性別、年齡、體質指數(body mass index,BMI)。依據Cat S、TSP-1中位數10.43 μg/L、153.19 μg/L分為高水平組、低水平組。
1.2.3 隨訪 采用電話、門診、住院相結合的方式進行為期12個月的隨訪,隨訪起點為出院后第1天,每兩個月隨訪1次,以出現終點事件或隨訪期滿作為隨訪終點,所有病人均得到有效隨訪。終點事件為:因心力衰竭需再次入院治療或發生心源性死亡。根據是否發生終點事件將研究對象分為預后不良組(53例)與預后良好組(112例)。以病人出現終點事件的時間計算無進展生存期。

2 結 果
2.1 預后良好組與預后不良組臨床資料比較 預后良好組性別、BMI與預后不良組比較差異均無統計學意義(P>0.05);與預后良好組相比,預后不良組年齡、NYHA心功能分級Ⅳ級比例均較高(P<0.05),LVEF較低(P<0.05)。詳見表1。
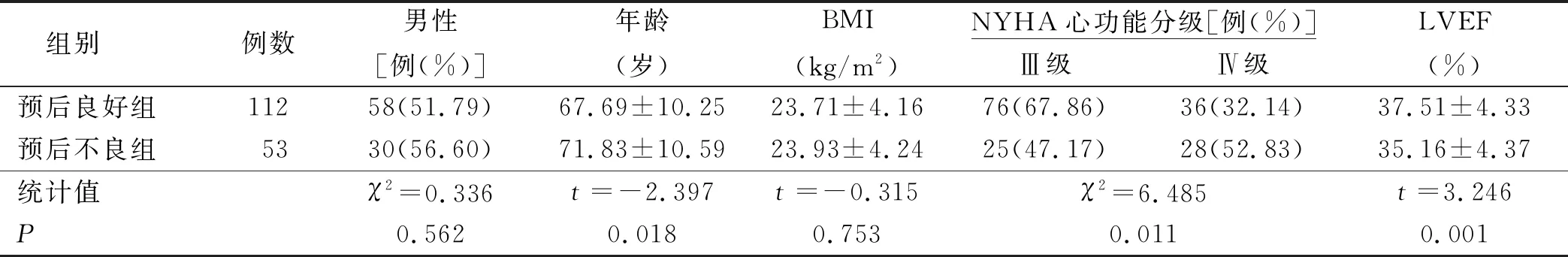
表1 預后良好組與預后不良組臨床資料比較
2.2 預后良好組與預后不良組血漿Cat S、TSP-1水平比較 與預后良好組比較,預后不良組血漿Cat S、TSP-1水平均較高(P<0.05)。詳見表2。
表2 兩組血漿Cat S、TSP-1水平比較(±s) 單位:μg/L
2.3 血漿Cat S、TSP-1與ADHF病人預后的關系 ADHF病人隨訪期內終點事件發生率為32.12%(53/165)。Cat S低水平組、Cat S高水平組終點事件發生率分別為22.89%、41.46%,無進展生存期平均值分別為11.451[95%CI(11.336,11.566)]個月、10.893[95%CI(10.729,11.057)]個月,Log-rank值為50.874,P<0.001。TSP-1低水平組、TSP-1高水平組終點事件發生率分別為20.48%、43.90%,無進展生存期平均值分別為11.512[95%CI(11.398,11.625)]個月、10.821[95%CI(10.657,10.985)]個月,Log-rank值為91.404,P<0.001。詳見圖1、圖2。
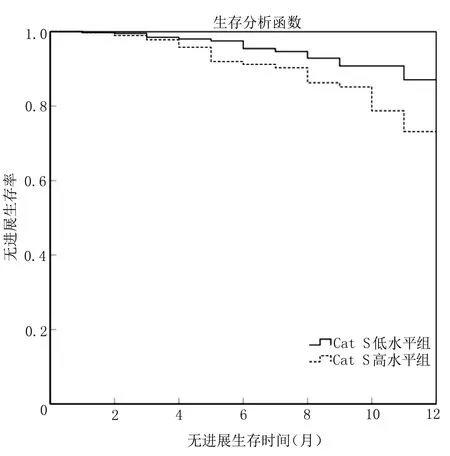
圖1 Cat S與ADHF病人預后發生終點事件的K-M曲線
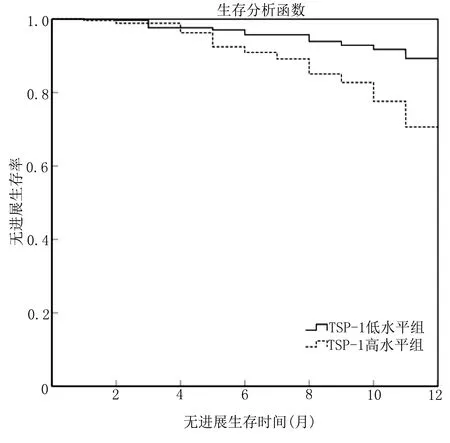
圖2 TSP-1與ADHF病人預后發生終點事件的K-M曲線
2.4 ADHF病人預后的影響因素分析 Cox單因素分析結果顯示,年齡、NYHA心功能分級、LVEF、Cat S、TSP-1差異均有統計學意義(P<0.05)。詳見表3。Cox多因素分析結果顯示,年齡、NYHA心功能分級、Cat S、TSP-1均是影響ADHF病人預后的獨立危險因素(P<0.05),LVEF是獨立保護因素(P<0.05)。詳見表4。
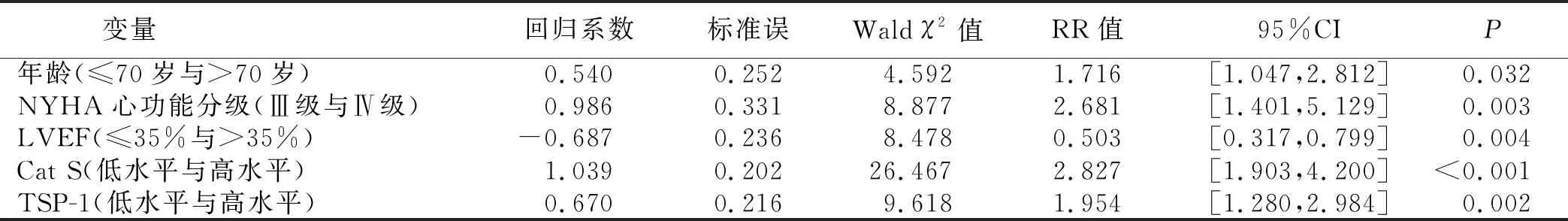
表3 影響ADHF病人預后的單因素分析結果
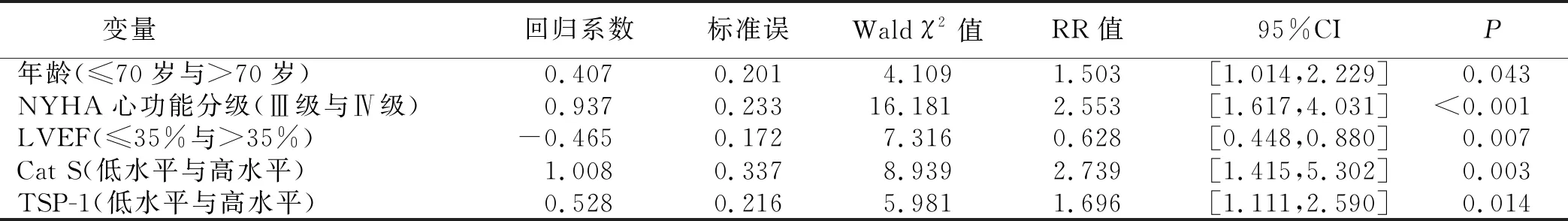
表4 影響ADHF病人預后的多因素分析結果
3 討 論
心力衰竭的發生及演變與心肌纖維化、炎癥反應、神經內分泌變化等多種生理、病理機制有關,是心血管疾病病人反復住院及死亡的重要原因之一。ADHF病人病死率高,預后狀況普遍較差,5年病死率可達60%以上[1]。本研究中終點事件發生率為32.12%,尋找能夠準確預測心力衰竭預后的生物標志物,以期改善病人預后狀況是臨床工作的重要課題[6]。
Cat是廣泛存在于溶酶體中的蛋白質水解酶,目前已在人體中發現15種Cat,Cat的異常表達與心血管疾病、腫瘤、骨質疏松癥等病理演變密切相關[7]。Cat S主要存在于機體淋巴結、脾臟及抗原呈遞細胞等器官或細胞中,可降解細胞外、細胞內基質及膠原纖維,對血管內皮細胞具有調控作用,與動脈粥樣硬化、心力衰竭等多種心血管疾病有關[8]。研究發現,敲除Cat S基因后,小鼠血管內皮細胞及血管平滑肌細胞增殖受到抑制,細胞外基質沉積,可減輕靜脈橋血管再狹窄程度,可能用于冠心病的治療[9]。TSP-1是一種血管生成抑制劑,可阻斷血管內皮細胞增殖、遷移,在細胞損傷應答過程中大量表達,其水平與冠狀動脈狹窄程度存在因果關系[10-11]。研究發現,與單純糖尿病病人相比,糖尿病合并冠心病及心力衰竭病人血漿Cat S、TSP-1水平均較高,可用于預測心功能,控制Cat S、TSP-1可能對預防糖尿病并發冠心病或心力衰竭具有積極意義[4]。本研究發現,與預后良好組相比,預后不良組血漿Cat S、TSP-1水平均較高,LVEF較低,提示Cat S、TSP-1與ADHF病人預后有關。分析原因為Cat S可降解細胞外基質,使纖維帽變薄,抗張強度降低,增加動脈粥樣硬化斑塊不穩定性,從而參與ADHF;TSP-1可黏附血小板,導致血管增大,并發揮抑制血管生成的作用,使ADHF病情進一步惡化。進一步研究發現,年齡、NYHA心功能分級、Cat S、TSP-1均是影響ADHF病人預后的獨立危險因素,LVEF是獨立保護因素,Cat S、TSP-1高水平提示預后不良,對合并危險因素的ADHF病人應重點監測,以預防不良預后的發生。
綜上所述,ADHF病人血漿高水平Cat S、TSP-1可能對預后產生不良影響,是ADHF病人預后不良的獨立危險因素,可能成為ADHF病人預后預測的潛在指標,臨床工作者可監測血漿Cat S、TSP-1水平,以便對預后恢復中的病人進行早期干預,以改善預后狀況,值得后續擴大樣本或進行多中心病例對照研究以論證結果。

