漆酶催化二氫楊梅素氧化聚合
劉曉玲,何承云,陳春剛,孫俊良,劉本國
(河南科技學院食品學院,河南 新鄉 453003)
類黃酮是自然界中廣泛存在的一大類酚類物質,具有抗氧化、抗炎、抗病毒、降血壓、降血糖和抗腫瘤等生物活性,是茶及眾多中草藥的活性成分[1-3]。但類黃酮的低水溶性和促氧化問題限制了其活性發揮和實際應用[4-5]。天然類黃酮聚合物,如茶黃素、原花色素和單寧等,具有比類黃酮單體更高的水溶性和生物活性[6-8]。這表明聚合反應能改善類黃酮的水溶性、減弱其促氧化性。類黃酮的聚合在食品加工中也廣泛存在,如葡萄酒中的兒茶素與乙醛的縮聚物對酒的風味和外觀有重要影響[9-10]。類黃酮的聚合可采用化學法和酶法。Geng Sheng等[11]采用化學法合成了兒茶素與甲醛酸的聚合物,Kim等[12]在乙醇溶劑中通過縮合反應生成了一系列兒茶酚-醛寡聚物。與兒茶素單體相比,這些衍生物均顯示出更高的清除超氧陰離子自由基能力和抑制人低密度脂蛋白氧化活性[13]。但化學聚合法存在區域選擇性差、毒副性殘留、原料損失大、產物收率低、環境不友好等諸多問題。漆酶是一種含銅的氧化還原酶,最早從紫膠漆樹的分泌物中發現,可催化多酚、多胺、木質素的氧化[14-15]。由于漆酶在催化作用的過程中主要生成產物是水,因此被認為是一種綠色型酶制劑受到國內外研究者的關注[16]。
2013年顯齒蛇葡萄葉被列入國家新食品原料。二氫楊梅素(圖1)為一種二氫黃酮醇類物質,是顯齒蛇葡萄葉的主要活性成分,含量可占干葉質量的20%以上,具有多種生物活性,已實現規模化生產[17-18]。但二氫楊梅素水溶性低、穩定性差的缺點限制了其在食品中的廣泛應用,課題組的前期研究也表明二氫楊梅素的α-葡萄糖苷酶抑制活性遠遜于顯齒蛇葡萄葉中的單寧組分[19]。已有研究表明類黃酮聚合物對黃嘌呤氧化酶和酪氨酸酶的抑制能力優于相應單體[20]。受此啟發,本研究擬以漆酶為催化劑,制備二氫楊梅素聚合物,系統考察反應時間、漆酶添加量、反應溫度、pH值等因素對產物顏色、α-葡萄糖苷酶抑制及抗氧化活性的影響,并運用波譜手段表征該衍生物結構。

圖1 二氫楊梅素的化學結構Fig. 1 Chemical structure of dihydromyricetin
1 材料與方法
1.1 材料與試劑
二氫楊梅素、阿卡波糖、溴化鉀(均為光譜級)上海阿拉丁生化科技股份有限公司;漆酶(來自漆樹)、α-葡萄糖苷酶(來自釀酒酵母)、對硝基苯-α-D-吡喃葡糖苷(p-nitrophenyl-α-D-glucopyranoside,pNP-G)、1,1-二苯基苦基苯肼(1,1-diphenyl-2-picrylhydrazyl radical,DPPH)、2,2’-聯氮雙(3-乙基苯并噻唑啉-6-磺酸)二銨鹽(2,2’-azinobis (3-ethylbenzothiazoline-6-sulfonic acid) diammonium salt,ABTS)美國Sigma-Aldrich公司;其他試劑均為分析純。
1.2 儀器與設備
CR-400色差計 日本美能達公司;TU-1810PC紫外-可見分光光度計 北京普析通用儀器有限公司;TENSOR27傅里葉變換紅外光譜儀、Avance 600 MHz核磁共振波譜儀 德國Bruker公司;7200型可見光分光光度計 尤尼柯(上海)儀器有限公司;GenPure UF/UV純水超純水系統 美國Thermo Scientific公司;ME104電子天平 梅特勒-托利多儀器(上海)有限公司;SHA-C水浴恒溫振蕩器 金壇市中大儀器廠;Alphal-2LD plus真空冷凍干燥機 德國Christ公司。
1.3 方法
1.3.1 二氫楊梅素的酶促修飾
將二氫楊梅素和漆酶溶于0.1 mmol/L pH 3.8~7.8磷酸緩沖液,在一定水浴溫度下(25~45 ℃),150 r/min振蕩反應指定時間(6~48 h),體系中二氫楊梅素質量濃度固定在2 mg/mL,漆酶濃度為1~9 U/mL,反應完畢后,冷凍48 h,而后冷凍干燥,得二氫楊梅素酶促衍生物。
1.3.2 色度測定
使用色差計對樣品進行色度分析,儀器用標準白板(L*=96.86,a*=-0.15,b*=1.87)校正后,測定二氫楊梅素酶促衍生物的色度,記錄L*、a*和b*值,重復測定5 次,取平均值。
1.3.3α-葡萄糖苷酶抑制能力測定
pNP-G作為底物時可被α-葡萄糖苷酶水解為黃色且在波長405 nm處有最大吸收的對硝基苯酚,其可反映α-葡萄糖苷酶活性。參照文獻[21]的方法,1 mL 0.2 U/mLα-葡萄糖苷酶溶液與0.5 mL不同濃度樣品在試管中混合,對照管用0.5 mL磷酸鹽緩沖液(0.1 mol/L,pH 6.8)代替樣品,在37 ℃水浴中反應10 min,隨后加入底物1.0 mL 1.0 mmol/L pNP-G溶液,反應20 min,最后迅速加入1 mL無水乙醇,終止反應,用超純水定容至5.0 mL,測定405 nm波長處的吸光度。樣品的α-葡萄糖苷酶抑制率效果用半抑制濃度(IC50)進行比較,抑制率計算如式(1)所示:

1.3.4 DPPH自由基清除力測定
參照文獻[22]的方法,將2.0 mL不同濃度樣品的乙醇溶液與2.0 mL 0.2 mmol/L DPPH-乙醇溶液在試管中充分混合,室溫下避光反應30 min,測定反應液在517 nm波長處吸光度(A樣品),用無水乙醇調零。各樣品不同濃度各設置一個空白管扣除樣品顏色對實驗的影響,即2.0 mL對應濃度的樣品溶液與2.0 mL乙醇溶液的混合,其吸光度為A空白。對照管為2.0 mL DPPH溶液與2.0 mL乙醇混合,其吸光度為A對照。DPPH自由基清除能力的計算如式(2)所示:

1.3.5 ABTS陽離子自由基清除力測定
參照文獻[23]的方法,將100 mL 7 mmol/L ABTS溶液與1.75 mL 2.45 mmol/L過硫酸鉀溶液均勻混合,避光反應12 h,得ABTS陽離子自由基母液。使用pH 7.4、0.05 mol/L的磷酸緩沖液對其進行稀釋,至其在734 nm波長處吸光度為0.7左右,得ABTS測試液。分別取1 mL不同濃度的樣品溶液,加入ABTS測試溶液2 mL,充分混勻,在室溫下反應10 min,測定其在734 nm波長處吸光度,ABTS陽離子自由基清除能力的計算如式(3)所示:

1.3.6 紫外光譜測定
將樣品溶于適量甲醇中,測定其在220~400 nm波長范圍內的紫外吸收光譜。
1.3.7 紅外光譜測定
將溴化鉀在烘箱中烘干,先以溴化鉀壓片作為背景進行校準,分別取少量樣品與溴化鉀混合并充分研磨,用壓片機10 MPa下壓片,用紅外光譜儀記錄其400~4 000 cm-1范圍內的紅外光譜。
1.3.8 核磁測定
稱取50 mg左右樣品溶于1 mL DMSO-D6,轉移到核磁管中,采用核磁共振波譜儀測定樣品的1H和13C核磁譜。所有操作在25 ℃進行。
1.4 數據處理
2 結果與分析
2.1 色度分析
漆酶在氧氣存在的情況下,可催化小分子芳香族化合物氧化生成活性自由基,從而引發其聚合生成高分子化合物。本研究利用漆酶的這一催化特性,將二氫楊梅素單體聚合生成有色聚合物,其可用作新型食用色素。25 ℃水中二氫楊梅素的溶解度約為0.28 mg/mL,而其有色聚合物在水中的溶解度可高達33.20 mg/mL,酶法修飾能顯著提高二氫楊梅素水溶性。同時,反應時間、漆酶濃度、反應溫度、pH值對產物顏色有顯著影響(圖2和表1)。當固定漆酶濃度5 U/mL、pH 5.8、反應溫度35 ℃時,隨著反應時間的延長(6~48 h),二氫楊梅素衍生物的亮度減少(L*值減小),產品均偏紅黃色(a*值和b*值均大于0),顏色差異不大(ΔE值接近);當pH 5.8、反應溫度35 ℃、反應時間36 h時,隨著漆酶濃度的增大(1~9 U/mL),衍生物的亮度、紅黃值均降低,樣品間的色差顯著增大;當漆酶濃度5 U/mL、pH 5.8、反應時間36 h,可發現較之其他因素,反應溫度(25~45 ℃)對樣品色度的影響較小;當漆酶濃度5 U/mL、反應時間36 h、反應溫度35 ℃時,pH值引起的樣品色度變化顯著高于其他因素。pH值為3.8和7.8時,酶促反應較難進行,樣品的色度指標與二氫楊梅素接近;pH值為4.8和6.8時,酶促反應雖能進行,但亮度值下降不大,顯著高于pH值為5.8時獲得的樣品,表明所用漆樹漆酶的最適催化pH值在5.8左右,而前人研究也表明漆酶催化木質素的最適反應pH值為6[24]。

圖2 反應時間(a)、漆酶濃度(b)、反應溫度(c)、pH值(d)對二氫楊梅素衍生物顏色的影響Fig. 2 Effects of reaction time (a), laccase concentration (b), reaction temperature (c) and pH (d) on the color of dihydromyricetin derivatives
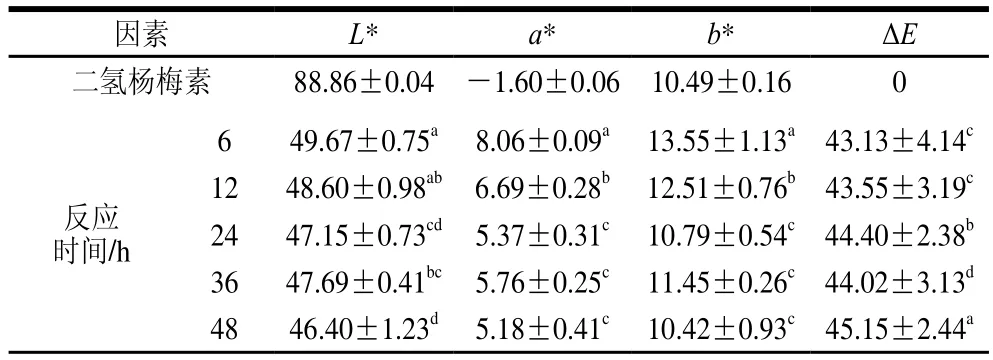
表1 二氫楊梅素衍生物的色度分析Table 1 Chroma analysis of dihydromyricetin derivatives
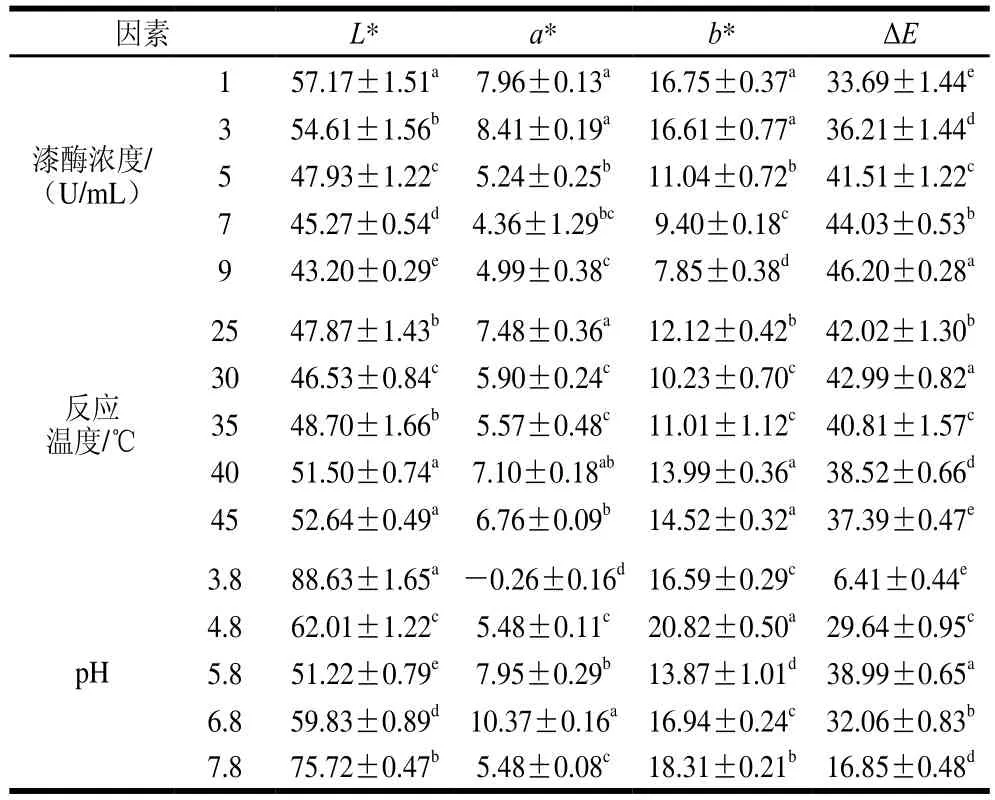
續表1
2.2 α-葡萄糖苷酶抑制活性
α-葡萄糖苷酶與糖尿病并發癥的發生有關,糖尿病治療藥物常以該酶為作用靶標,但這些藥物在應用中卻存在毒副作用大的問題[25-26]。最新研究表明天然類黃酮聚合物,如茶黃素、原花色素和單寧等,具有比類黃酮單體更高的生物活性[27-28],這提示可通過制備類黃酮聚合物的方式,提高類黃酮的α-葡萄糖苷酶抑制活性。本研究中,酶促反應條件不僅對二氫楊梅素衍生物顏色有顯著影響,對其生物活性也可能有重要影響。系統考察了反應時間、漆酶濃度、反應溫度、pH值對二氫楊梅素衍生物的α-葡萄糖苷酶抑制活性的影響。二氫楊梅素抑制α-葡萄糖苷酶的IC50值為85.95 μg/mL。如圖3所示,當固定漆酶濃度5 U/mL、pH 5.8、反應溫度35 ℃時,隨著反應時間的延長,樣品的IC50值逐漸降低,當反應時間為24 h,其基本保持恒定,反應時間的適當延長有利于產物酶抑制活性的提高。與之類似,漆酶濃度的適當增加亦可顯著提高產物活性,但當漆酶濃度超過5 U/mL時,繼續增加,產物的活性提高不明顯。反應溫度對產物活性的影響則呈現U型特征,在35 ℃條件下制得的衍生物抑制效果最佳(IC506.2 μg/mL)。當pH 3.8時,所得產物在200 μg/mL時的抑制率僅為4%,IC50因而未能測出,而pH 7.8時所得產物的IC50為45 μg/mL。這表明在上述pH值條件下,漆酶催化活性不高。而pH值為5.8和6.8時所得產物表現出較強的酶抑制活性,且二者IC50值接近。為了進一步考察漆酶修飾對二氫楊梅素活性和結構的影響,挑選在反應溫度35 ℃、pH 5.8、反應時間36 h,漆酶濃度分別為1、3、5 U/mL時獲得的二氫楊梅素衍生物(分別表示為U-1、U-3和U-5)為代表性樣品用于后續的抗氧化和結構表征。

圖3 反應時間(a)、漆酶濃度(b)、反應溫度(c)、pH值(d)對二氫楊梅素衍生物的α-葡萄糖苷酶抑制效果的影響Fig. 3 Effects of reaction time (a), laccase concentration (b), reaction temperature (c) and pH (d) on α-glucosidase inhibitory activity of dihydromyricetin derivatives
2.3 DPPH自由基清除能力
由圖4可知,二氫楊梅素及其衍生物(U-1、U-3、U-5)均表現出DPPH自由基清除能力,且呈量效關系,其IC50值依次為5.32、54.28、54.68、54.86 μg/mL,漆酶的氧化聚合導致了二氫楊梅素的抗氧化能力顯著降低。
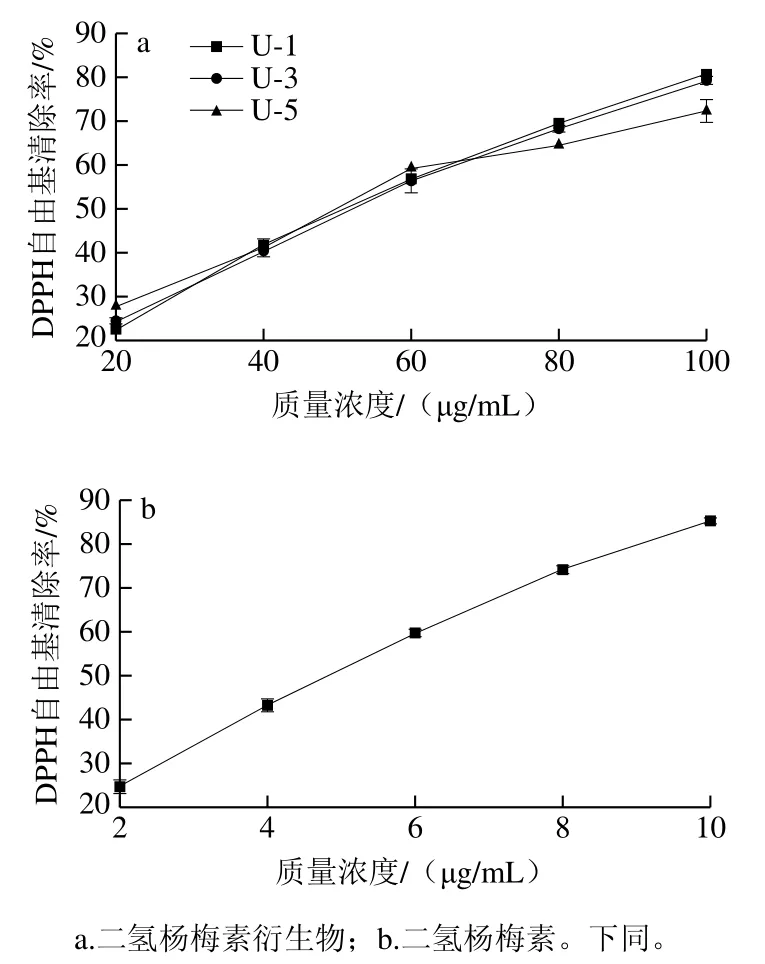
圖4 二氫楊梅素及其衍生物的DPPH自由基清除能力Fig. 4 DPPH radical scavenging activity of dihydromyricetin and its derivatives
2.4 ABTS陽離子自由基清除能力
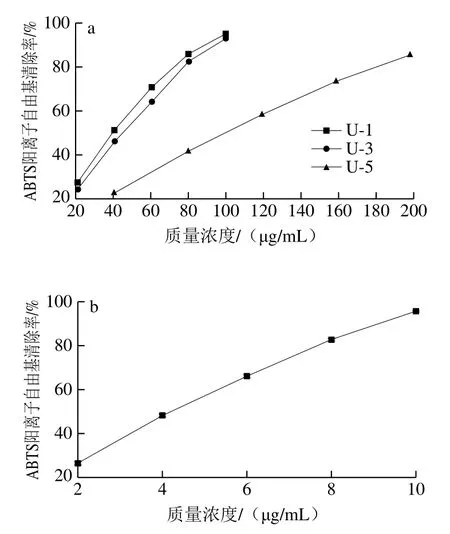
圖5 二氫楊梅素及其衍生物的ABTS陽離子自由基清除能力Fig. 5 ABTS radical cation scavenging activity of dihydromyricetin and its derivatives
如圖5所示,隨著樣品質量濃度的增大,其ABTS陽離子自由基清除能力呈線性上升,二氫楊梅素、U-1、U-3和U-5的IC50值分別為4.81、39.32、44.42、99.99 μg/mL。二氫楊梅素衍生物的活性均低于二氫楊梅素,并且其活性與制備時所用漆酶濃度呈反比關系。結合DPPH實驗結果,推測漆酶通過氧化二氫楊梅素上酚羥基形成聚合物,導致了衍生物抗氧化活性的降低。
2.5 二氫楊梅素衍生物的紫外光譜分析
紫外光譜在類黃酮結構測定中占有非常重要的地位,其可確定類黃酮骨架和羥基的取代位置。典型的類黃酮化合物的紫外圖譜上一般有2 個吸收帶,240~285 nm(帶II)和300~550 nm(帶I)。一般認為帶I主要與類黃酮B環上的肉桂酰生色基團有關,帶II與A環上的苯甲酰生色基團有關。如圖6所示,二氫楊梅素屬于二氫黃酮醇類物質,只有苯甲酰系統,因此主要體現帶II特征,帶I僅呈肩峰,其最大吸收峰位于在289 nm處。而U-1、U-3和U-5的紫外圖譜仍體現二氫楊梅素特征,證明二氫楊梅素骨架結構在衍生物中得到保留,但帶I的相對強度提高,且最大吸收峰發生了藍移,出現在了292 nm波長處,表明苯環上的酚羥基發生了取代。
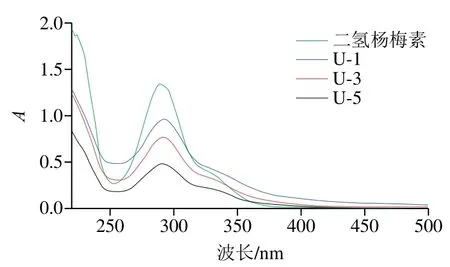
圖6 二氫楊梅素及其衍生物紫外圖譜Fig. 6 Ultraviolet spectra of dihydromyricetin and its derivatives
2.6 紅外光譜分析
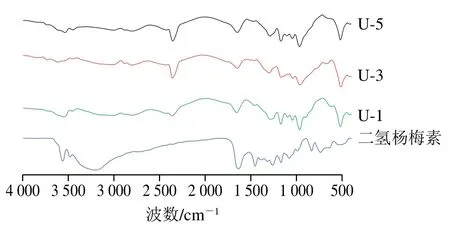
圖7 二氫楊梅素及其衍生物紅外圖譜Fig. 7 Infrared spectra of dihydromyricetin and its derivatives
波長在2~25 μm的中紅外光譜專屬性極強,能用來分析大多數化合物,反映化學反應過程中的基團變化情況。如圖7所示,二氫楊梅素具有3 213(酚羥基)、1 391(苯環)、1 630(羰基)、1 169(C—H伸縮振動)、1 081 cm-1(C—O伸縮振動)等特征吸收峰。酶促氧化聚合物后,二氫楊梅素的紅外圖譜發生了顯著變化:隨著漆酶濃度的增加,所得衍生物的酚羥基特征吸收峰強度逐漸降低,而C—O伸縮振動峰強度逐漸提高。這表明漆酶通過催化酚羥基氧化,而后以醚鍵相連,實現二氫楊梅素的聚合。Sun Xuejiao等[29]發現以鄰苯二酚為底物,采用漆酶催化其進行聚合反應,產物中鄰苯二酚單體結構單元以醚鍵相連接,這與本實驗結果一致。
2.7 核磁共振波譜分析
由于U-5衍生物的聚合度較大,其不能溶于測試溶劑,因此本研究僅對二氫楊梅素、U-1和U-3進行了核磁分析。二氫楊梅素的1H和13C核磁共振峰的歸屬解析如圖8、9所示,其與文獻報道一致[30]。U-1和U-3的核磁共振圖譜其仍然體現了二氫楊梅素的結構特性,但除C-5上所連酚羥基,其他的酚羥基信號與完全消失,這與紅外光譜結果相印證,表明這表明漆酶通過催化酚羥基氧化實現二氫楊梅素的聚合。
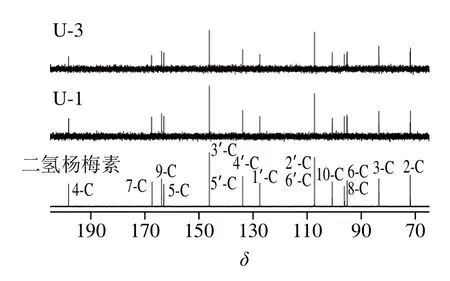
圖8 二氫楊梅素及其衍生物的13C核磁共振圖譜Fig. 8 13C-NMR spectra of dihydromyricetin and its derivatives
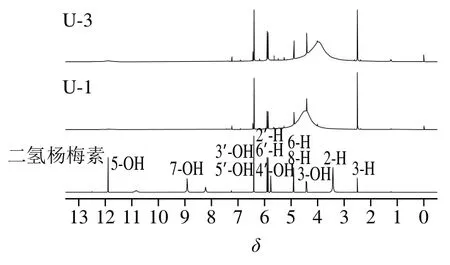
圖9 二氫楊梅素及其衍生物的1H核磁共振圖譜Fig. 9 1H-NMR spectra of dihydromyricetin and its derivatives
3 結 論
漆酶可用于二氫楊梅素的氧化聚合,反應時間、反應溫度、酶濃度和pH值對二氫楊梅素衍生物的顏色有規律性影響。修飾后,二氫楊梅素抑制α-葡萄糖苷酶的能力得到顯著提高,而DPPH自由基和ABTS陽離子自由基清除能力卻下降。波譜分析表明漆酶通過催化酚羥基氧化,而后以醚鍵連接,實現二氫楊梅素聚合。所得二氫楊梅素衍生物具有一定抗氧化活性和突出的α-葡萄糖苷酶抑制活性,可用作食品色素,或作為降糖因子用于糖尿病人特膳食品。本研究對促進二氫楊梅素在食品中的應用,推動新型功能性食品開發具有重要意義。

