FASTKD4在骨肉瘤組織中表達及對骨肉瘤細胞增殖和凋亡的影響
張香路,王 震,常 俊,馬廣文,黃 斐
骨肉瘤是惡性程度最高的腫瘤之一,好發于兒童和青少年,目前以手術治療和化學治療為主,復發率較高,預后往往不佳[1-3]。過去三十年來,骨肉瘤患者的預后并未改變,凸顯了臨床對新研究、新方法的需求[4]。腫瘤的發生、發展涉及多個基因、多個環節的調控異常,尋找有效的靶基因治療骨肉瘤可能會有效的改善其預后[5-6]。
Fas活化激酶結構域蛋白4 (fast kinase domain-containing protein4,FASTKD4)也被稱為細胞周期進程修復蛋白2(cell cycle progression restoration protein 2,CPR2)和轉化生長因子β調節蛋白4(transforming growth factor beta regulator 4 ,TBRG4),是一種線粒體蛋白,廣泛分布在整個線粒體基質中,能夠調節線粒體中RNA的表達[7]。FASTKD4在之前的研究報道中較少,2014年Wolf et al[8]首次通過MitoString測試發現FASKTD4是一種新的線粒體蛋白。隨后2017年Boehm et al[7]證實FASKTD4對線粒體能量代謝有著重要的調節作用,這也是首次證實FASTKD4可以通過影響線粒體,從而進一步干預腫瘤的發生發展。但是FASTKD4對骨肉瘤是否有影響,目前尚無研究。為了明確FASTKD4在骨肉瘤中的作用,該研究擬檢測FASTKD4在骨肉瘤組織和骨肉瘤細胞中的表達,并通過小干擾RNA沉默骨肉瘤細胞中的FASTKD4,觀察其對骨肉瘤細胞生物學的影響。
1 材料與方法
1.1 標本的采集收集2017—2019年安徽醫科大學第四附屬醫院30例骨肉瘤患者的股骨遠端骨肉瘤標本。通過免疫組化和qPCR檢測骨肉瘤組織和癌旁組織中FASTKD4的表達。
1.2 細胞系骨腫瘤細胞系Saos-2、HOS和成骨細胞株均購自中國科學院上海細胞庫。使用含10%胎牛血清、100 U/ml 青-鏈霉素的RPMI-1640培養基,并在37 ℃、5% CO2的環境中進行細胞培養。
1.3 免疫組化將骨肉瘤組織和癌旁組織切片進行福爾馬林固定和石蠟包埋后,切片(5 μm)進行免疫組化。用抗FASTKD4的一抗(兔抗,濃度1 ∶1 000,CST)4 ℃孵育過夜,重復洗滌后再用二抗孵育30 min。最后切片用DAPI染色,并用蘇木精復染。
1.4 shFASTKD4慢病毒的構建與轉染為了有效阻止FASTKD4的表達,本研究構建了靶向干擾FASTKD4的小干擾RNA small interfering RNA (shRNA) 慢病毒載體。方法如下:靶向干擾FASTKD4的shRNA的干擾序列為GTTCTTCAGCCTGGTACAT。被用于對照組的,加擾(scrambled) shRNA(shCtrl)的干擾序列為TTCTCCGAACGTGTCACGT。相關莖環結構的DNA oligo (oligonucleotides ) 被合成,并被植入pGV115-GFP慢病毒載體(上海吉凱基因醫學科技股份有限公司)。通過這個慢病毒表達系統來構建shFASTKD4和scrambled shRNA。為了進行慢病毒轉染,用6孔板培養Saos-2細胞,并根據MOI加入shFASTKD4和shCtrl慢病毒。轉染后 72 h左右,熒光顯微鏡觀察綠色熒光蛋白(green fluorescent protein,GFP)的表達情況。轉染120 h后,收集細胞進行qPCR和Western blot檢測敲減效率。
1.4.1RNA提取和qPCR檢測 按照說明書的方法,使用Trizol 裂解腫瘤組織、癌旁組織和腫瘤細胞并收集RNA。每個樣本取2.0 μg RNA在M-MLV逆轉錄酶和oligo dT作用下合成cDNA。使用SYBR Green Premix Ex Taq試劑進行qPCP實驗,并在ABI 7500 QPCR儀進行檢測。使用GAPDH做為內參。FASTKD4的正向引物為5′- CAGCTCACCTGGTAAAGCGAT-3′,反向引物為5′-GGGAGTAGATGCTCGTTCCTTC-3′ (194 bp);GAPDH的正向引物為 5′-TGACTTCAACAGCGACACCCA-3′,反向引物為5′-CACCCTGTTGCTGTAGCCAAA-3′(121 bp), 參考GAPDH的表達結果標準化FASTKD4的表達結果。用 DNA 相對拷貝數和相對表達量(2-ΔΔCt) 表示FASTKD4基因的相對表達量。
1.4.2Western blot檢測 為了檢測Saos-2細胞中FASTKD4的敲減效率,采用Western blot的方法檢測細胞中FASTKD4蛋白的表達水平。Saos-2細胞被轉染shFASTKD4和shCtrl慢病毒后培養72 h,然后用PBS洗滌,并用預冷的lysis buffer進行裂解。細胞裂解液在4 ℃,12 000 r/min離心15 min,收集上清液,并用BCA試劑盒檢測蛋白水平。40 mg的蛋白被8%~12%的SDS-PAGE溶解后轉移到 PVDF 膜上,然后用TBTS配制的5%的脫脂牛奶封閉PDVF膜1 h,一抗4 ℃孵育過夜,TBTS液洗滌3次后,二抗孵育室溫孵育1 h,使用ECL法顯影。
1.4.3細胞增殖實驗 通過高內涵篩選的方法檢測shFASTKD4和shCtrl慢病毒轉染的Saos-2細胞的增殖。將處于對數生長期并轉染shFASTKD4和shCtrl慢病毒的Saos-2細胞按2×103個/孔種植到96孔板中。在37 ℃、5% CO2環境中培養4 d,且每天用高內涵細胞分析儀CellomicsArrayScan VTI (Thermo) 檢測讀板一次并定量細胞數量,連續檢測讀板4 d,實驗重復3次。
除了高內涵篩選的方法,本研究還采用CCK-8試劑盒來檢測shFASTKD4和shCtrl慢病毒轉染的Saos-2細胞的增殖。按2×103個/孔將細胞種植到96孔板中,連續培養4 d。每天在每孔加入10 μl CCK-8溶液37 ℃孵育4 h,酶標儀ELx800 Absorbance Microplate Reader (BioTek Instruments,Winooski,VT,USA) 選擇490 nm檢測OD值,連續檢測4 d。所有實驗重復3次。
1.4.4細胞克隆形成實驗 將處于對數生長期的shFASTKD4和shCtrl慢病毒轉染的Saos-2細胞與基質膠混勻后,1×103個/孔將細胞種植到24孔板中,使用含有20 ng/ml EGF、10 ng/ml b-FGF、5 μg/ml胰島素和0.4% 胎牛血清的DMEM/F12培養液培養12 d,并在1、6、12 d時進行熒光拍照,每組實驗重復3次。并用熒光圖像分析軟件(PhenoRipper)測量克隆球直徑。
1.4.5細胞凋亡檢測 采用Annexin V-APC 凋亡試劑盒檢測細胞凋亡。將shFASTKD4和shCtrl慢病毒轉染的Saos-2細胞培養48 h后,收集細胞,并用PBS洗滌,用細胞染色液調整細胞濃度為1×106/ml,每100 μl細胞懸液加入 10 μl Annexin V-APC 染色,室溫避光 15 min。使用FACS Calibur 流式細胞儀檢測細胞凋亡,每組實驗重復3次。
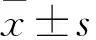
2 結果
2.1 FASTKD4在骨肉瘤組織和骨肉瘤細胞系中的表達分析采用免疫組化和qPCR的方法檢測FASTKD4在骨腫瘤組織中的表達情況,結果見圖1A、B,FASTKD4在骨肉瘤組織中呈高表達,而在癌旁組織中呈低表達,qPCR的結果也表明FASTKD4 mRNA在骨肉瘤組織中表達水平要高于癌旁組織,兩組之間差異有統計學意義(圖1C,t=10.86,P<0.05)。同時FASTKD4 mRNA在骨肉瘤細胞系Saos-2中表達最高,與HOS及成骨細胞比較差異有統計學意義(圖1D,t=19.72,P<0.05)。因此選擇Saos-2骨肉瘤細胞系進行后續實驗。
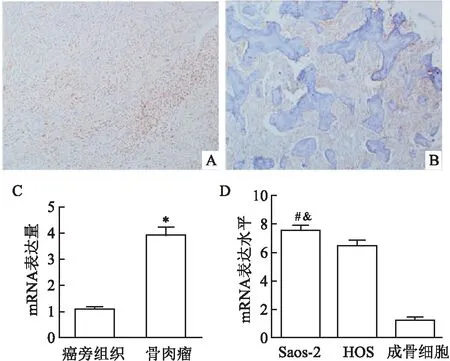
圖1 FASTKD4在骨肉瘤及癌旁組織中的表達
2.2 慢病毒介導的shRNA轉染骨腫瘤細胞抑制FASTKD4的表達為了評估慢病毒的敲減效率,Saos-2細胞被分別轉染shFASTKD4和shCtrl慢病毒載體。如圖2A~D所示,轉染72 h后,shFASTKD4和shCtrl組中超過80%的細胞GFP表達陽性。隨后,本研究用qPCR和Western blot的方法驗證FASTKD4的表達情況。如圖2E所示,與shCtrl組比較,shFASTKD4組中FASTKD4 mRNA的表達下降61%,兩組之間差異有統計學意義(t=12.45,P<0.05)。Western blot結果(圖2F)與qPCR一致,同樣顯示shFASTKD4組FASTKD4的蛋白表達水平低于shCtrl組。因此慢病毒介導的shRNA轉染有效的抑制了FASTKD4 mRNA和蛋白的表達。
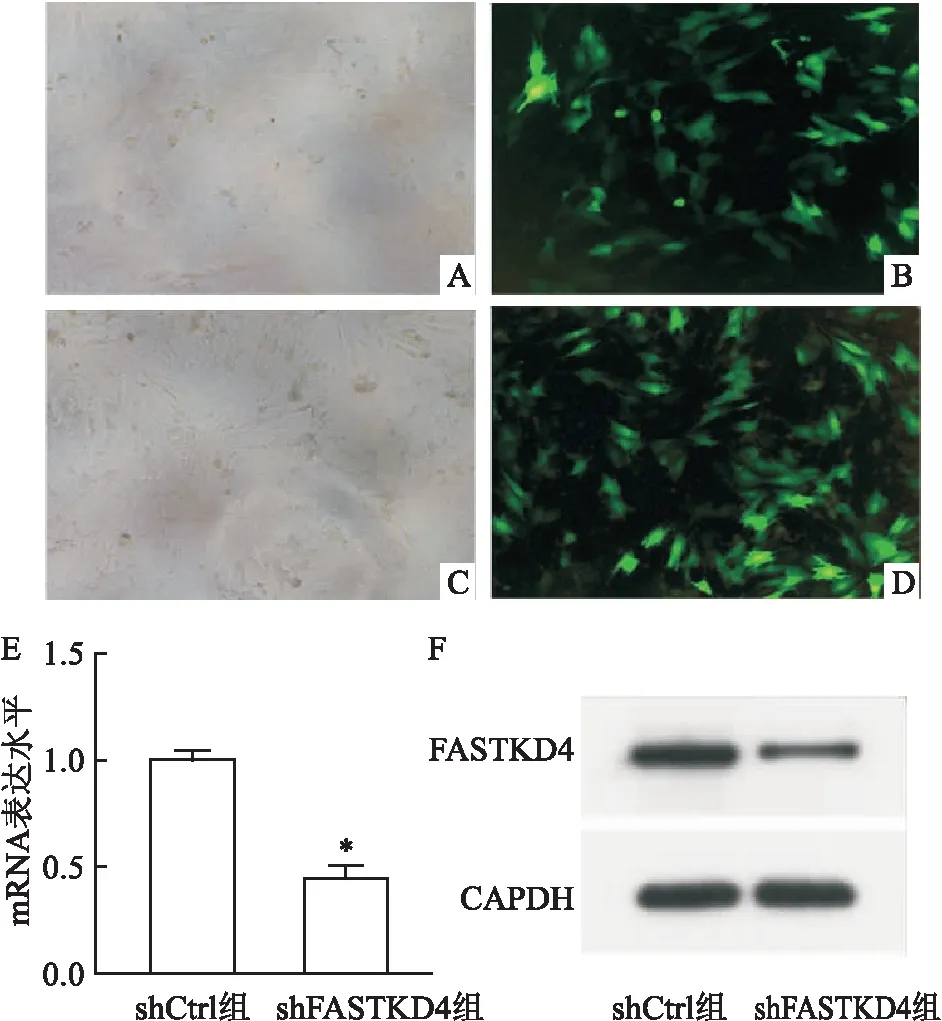
圖2 FASTKD4轉染效率及轉染后細胞中表達水平
2.3 FASTKD4敲除抑制骨肉瘤細胞增殖增殖是腫瘤細胞的一個重要特性,本研究通過高內涵篩選和CCK-8實驗分析了FASTKD4敲除后對骨肉瘤細胞增殖的影響。在高內涵檢測實驗中,轉染shFASTKD4和shCtrl的Saos-2細胞,被培養在96孔板中,并且通過CellomicsArrayScan VTI 連續觀察細胞4 d生長情況(圖3A)。如圖3B所示,與shCtrl組比較,shFASTKD4組中細胞增殖能力受到抑制。培養到第4天時,shCtrl組細胞增殖3.05倍,而shFASTKD4組中細胞增殖1.73倍,兩者之間差異有統計學意義(t=4.68,P<0.05)。課題組同時還用CCK-8實驗檢測了FASTKD4敲除對骨肉瘤細胞增殖能力的影響。如圖3C所示,CCK8結果同樣顯示了shFASTKD4組中細胞增殖能力低于shCtrl組,兩組之間差異有統計學意義(t=4.72,P<0.05)。

圖3 FASTKD4沉默后骨肉瘤細胞增殖能力檢測
2.4 FASTKD4敲除抑制骨肉瘤細胞克隆能力本研究通過基質膠成球實驗測定模擬體內三維情況下腫瘤細胞的克隆和成瘤能力。腫瘤細胞被接種在24孔板中,并在1、6、12 d時進行熒光拍照(圖4A)。如圖4B所示,在培養12 d shFASTKD4組中腫瘤細胞形成的克隆球直徑小于shCtrl組,兩組之間差異有統計學意義(t=14.87,P<0.05),表明FASTKD4敲除后抑制了腫瘤細胞的克隆形成能力。
圖4 FASTKD4沉默后骨肉瘤細胞克隆形成能力檢測
2.5 FASTKD4敲除誘導骨腫瘤細胞凋亡為了分析FASTKD4敲除對骨腫瘤細胞凋亡的影響,本實驗采用Annexin V-APC 單染法流式細胞儀檢測細胞凋亡(圖5A)。檢測結果顯示shCtrl組和shFASTKD4組細胞凋亡百分比分別為(2.36±0.11)%和(8.41±1.31)%(圖5B),兩組之間差異有統計學意義(t=7.97,P<0.05)。這表明FASTKD4敲除可以誘導骨腫瘤細胞的凋亡。
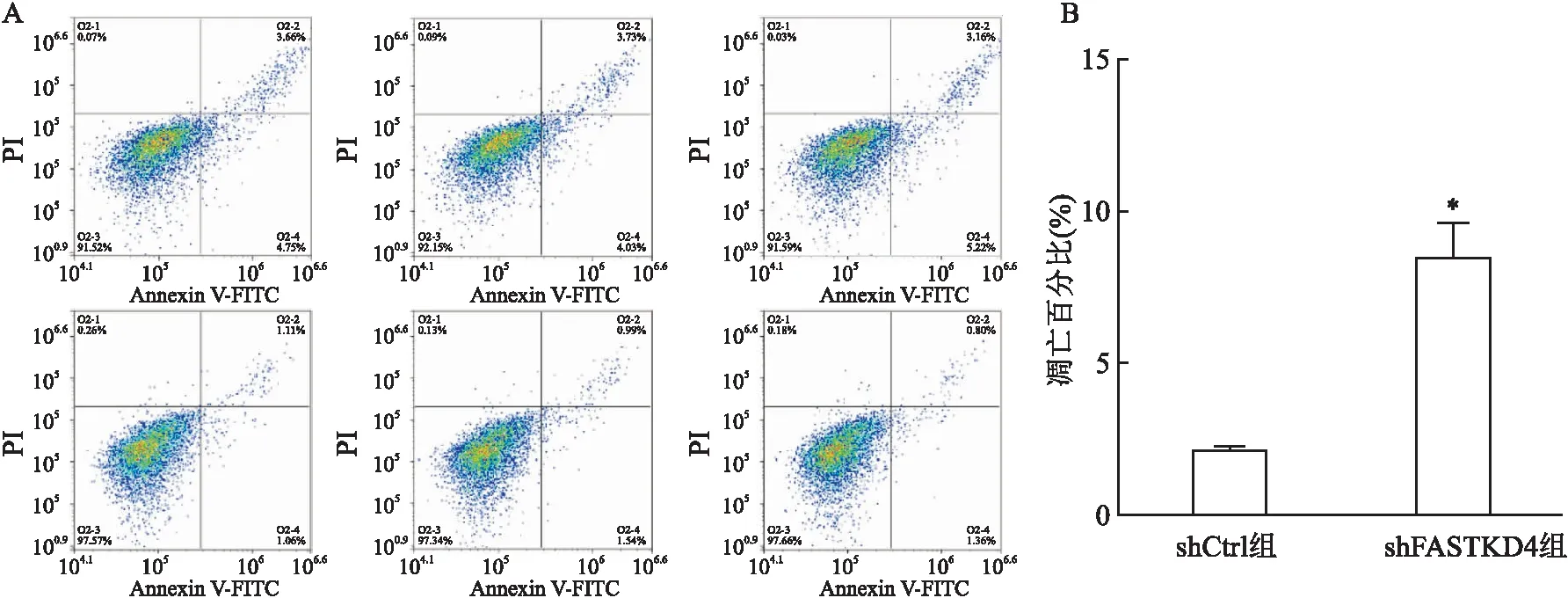
圖5 FASTKD4沉默后骨肉瘤細胞凋亡檢測
2.6 FASTKD4的敲除使骨肉瘤細胞中PI3K/AKT信號通路失活為了進一步探討FASTKD4在骨肉瘤中發生的分子機制,本課題組研究了PI3K/AKT信號通路,這是骨肉瘤中最常見的異常信號通路之一。通過Western blot檢測FASTKD4敲低對Saos-2細胞中p-PI3K、PI3K、p-AKT和AKT表達的影響。如圖6A、B所示,與shCtrl組比較,敲除FASTKD4下調了shFASTKD4組中p-PI3K和p-AKT蛋白的表達,兩組之間差異有統計學意義(t=26.42、24.98,均P<0.05),但在總的PI3K和AKT水平上未觀察到明顯差異。這些數據進一步說明,敲除FASTKD4使PI3K/AKT信號通路失活。
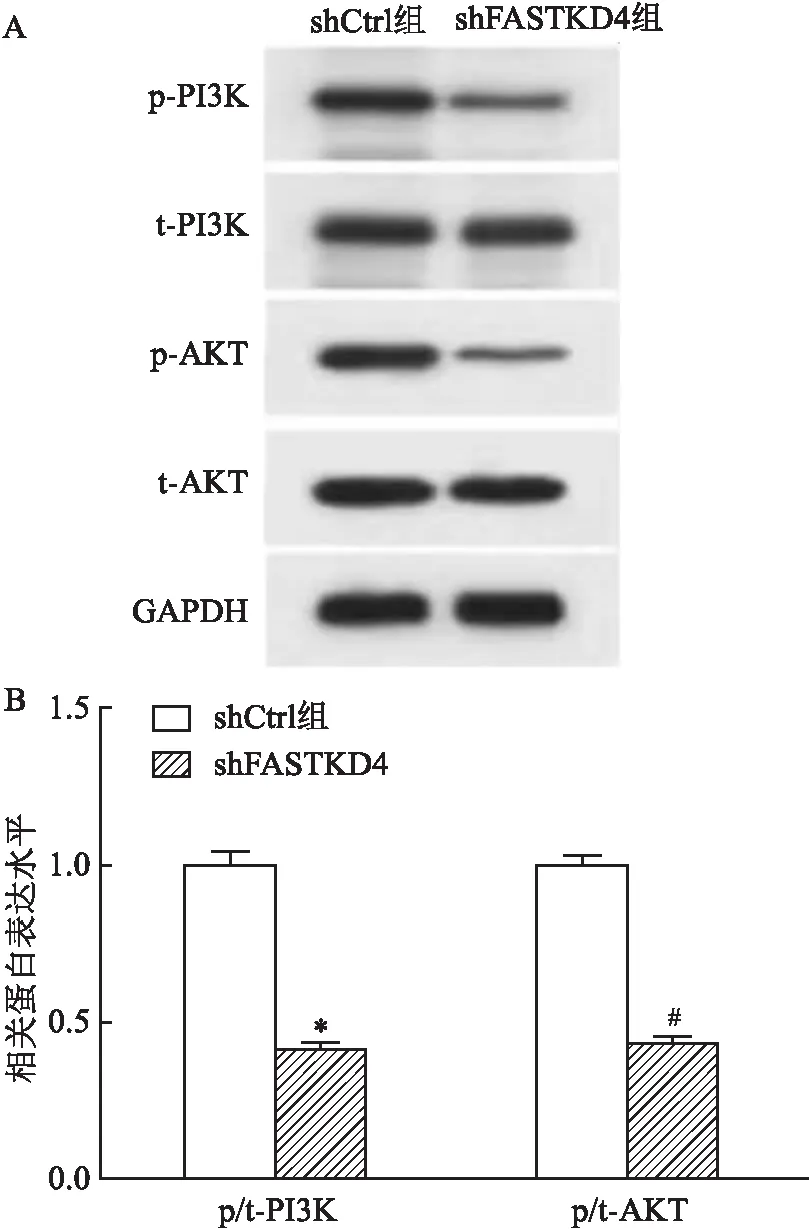
圖6 Western blot檢測Saos-2細胞中FASTKD4沉默對PI3K/AKT信號通路的影響
3 討論
隨著分子靶向治療技術的發展以及對骨肉瘤發生、發展機制研究的深入,目前骨肉瘤的分子靶向治療是臨床研究的一個熱點[9]。
腫瘤的發生、發展與腫瘤細胞的快速增殖和凋亡有關。作為與代謝和凋亡兩大癌癥標志相關的細胞器,線粒體正受到越來越多的關注。研究[7]表明腫瘤中抑癌基因的突變和癌基因的表達是通過作用線粒體來執行逃避凋亡和改變細胞代謝,進而促進癌細胞的生長。FASTKD4是線粒體基因中的一種,被認為是細胞周期相關基因,受到IL-2和JAK3的負調控。雖然FASKTD4與骨肉瘤之間的直接關系,目前尚無報道,但FASKTD4也已經被證實與多種腫瘤的發生有關,有研究[10]表明FASKTD4在肺癌組織中高表達,敲除FASKTD4后可以下調CAV1和RRM2,上調DDIT3來抑制肺癌細胞的增殖并促進凋亡。還有研究[11]發現FASKTD4在鱗狀細胞癌中發揮著重要作用,下調FASKTD4后,可以下調CAV-1并引起氧自由基的蓄積,同時抑制線粒體介導的凋亡反應。這也證實FASKTD4可以通過影響線粒體,在腫瘤的發生發展中發揮作用。因此本課題組推測FASTKD4可能也參與骨肉瘤的發生、發展。
本研究的結果表明在FASTKD4在骨腫瘤組織中表達顯著高于癌旁組織。在細胞實驗中,選擇了FASTKD4在骨腫瘤細胞中表達最高的Saos-2作為研究對象,通過細胞轉染小干擾RNA沉默FASTKD4的表達,qPCR和Western blot的結果證實了小干擾RNA沉默FASTKD4的有效性。FASTKD4沉默后的Saos-2細胞增殖的數量和克隆球直徑均小于對照組,而凋亡細胞的百分比高于對照組。這些結果表明FASTKD4沉默可以有效的抑制Saos-2細胞的增殖和克隆能力的形成,并促進Saos-2細胞的凋亡。本研究認為FASTKD4促進Saos-2細胞凋亡可能是導致細胞增殖受限的一個重要原因,這也與之前FASTKD4在其他腫瘤研究中的報道一致。
本研究評估了敲除FASTKD4對骨肉瘤細胞中PI3K/AKT信號通路的影響。結果顯示,敲除FASTKD4可抑制p-PI3K和p-AKT的表達水平,但在總的PI3K和AKT水平上未觀察到明顯差異,因此本研究推測FASTKD4基因表達下調是通過PI3K-AKT信號通路抑制骨肉瘤細胞的增殖、轉移和誘導細胞凋亡,進而抑制FASTKD4表達,這可能成為改善骨肉瘤預后的一個可行方法。然而,FASTKD4在骨肉瘤進展中的潛在抑瘤機制涉及多個分子水平,需要進一步研究。下一步本課題組將進一步研究FASTKD4在骨肉瘤其他細胞中作用的分子機制,為臨床治療提供堅實的理論基礎。

