SPIB對食管癌增殖及上皮間質轉化的影響
方漢林,黃云龍,張仁泉
食管癌是全球最常見的惡性腫瘤之一。據報道[1],2020年全球食管癌新發病例數60.4萬,死亡數達到54.4萬。我國食管癌的發病率居第5位,病死率居第4位[2]。目前,手術治療聯合輔助放化療仍是食管癌的有效治療手段。但是,食管癌的5年存活率仍較低,約為30%~40%[3]。其中,約90%的食管癌為鱗狀細胞癌[3]。鱗狀細胞癌是一種高度轉移性生長和侵襲的上皮細胞惡性腫瘤。然而,關于食管癌的發生和轉移的分子學機制尚不清楚。SPIB是Ets家族轉錄因子的成員,位于19q染色體上,其在成熟B細胞向漿細胞分化和漿細胞樣樹突狀細胞分化中發揮重要作用[4-5]。研究表明,在肝細胞癌[6]、B細胞淋巴瘤[7]和非小細胞肺癌[8-10]中,SPIB是重要的預后因子,高表達SPIB患者的生存預后較差。SPIB通過調控SNAP47蛋白表達,進一步介導非小細胞肺癌的自噬過程[9]。Zhao et al[11]研究表明,與癌旁組織比較,食管癌中SPIB呈現高表達水平。然而,關于SPIB調控食管癌細胞增殖和轉移的作用機制尚未見報道。因此,該研究旨在通過體外實驗闡明SPIB對食管癌增殖及上皮間質轉化的作用機制。
1 材料與方法
1.1 主要試劑與儀器食管癌細胞(KYSE150、KYSE450、KYSE30)和食管正常上皮細胞(Het-1a)均購自中國科學院細胞庫;敲低組siSPIB-1/2 和對照組(siNC)購自上海生工生物有限公司;pCDH-SPIB及空載體購自北京擎科生物科技有限公司;RIPA裂解液、BCA蛋白檢測試劑盒、CCK-8試劑盒購自上海碧云天生物技術有限公司;GAPDH抗體、辣根過氧化物酶標記山羊抗鼠二抗購自北京中杉金橋公司;SPIB抗體購自武漢愛博泰克生物科技有限公司;CytoFLEX流式細胞儀購自美國貝克曼公司。
1.2 方法
1.2.1細胞培養 食管癌細胞(KYSE150、KYSE450、KYSE30)和食管正常上皮細胞(Het-1a)采用含10%胎牛血清的RPMI-1640培養基進行培養,培養條件為:37 ℃、5% CO2。
1.2.2siRNA和質粒轉染 在6孔板中接種KYSE150細胞,待細胞生長至約80%,進行siRNA(或質粒)轉染:將50 pmol siRNA(或2.5 μg質粒)和5 μl lipofectamine 2000 分別加入到2支含50 μl Opti-MEM 培養基的離心管中進行混勻,并將siRNA(或質粒)液體加入到轉染試劑中混勻。室溫放置5 min后,將上述混合液均勻加入到每個培養孔內。通過加入嘌呤霉素(2 μg/ml)篩選,構建穩定過表達SPIB的食管癌細胞系。siSPIB-1/2序列F:5′-GG ACCTATGGACCACTATACT-3′,R: 5′-CAAGGTTCCC TCTTGTCAGAT-3′。
1.2.3細胞增殖檢測 細胞密度按照3×103個/孔在96孔板上接種KYSE150細胞并培養過夜,轉染siSPIB-1/2和siNC,或接種Vector組和SPIB組KYSE30細胞。不同時間后,每孔加入10 μl CCK-8溶液,繼續培養孵育2 h。使用酶標儀(美國Bio-tek公司)測定吸光度值(450 nm)。以siNC組為參考,計算相對細胞增殖率。
1.2.4細胞劃痕實驗 當KYSE150細胞經過不同轉染處理后,按照5×105個/ml的密度接種于6孔板中,繼續培養。第2天,換成含0.5% 胎牛血清的培養基繼續培養12 h。再用黃色槍頭在孔板底部劃出平行的劃痕,并用PBS洗去漂浮細胞,繼續培養48 h。使用光學顯微鏡進行圖像采集。
1.2.5細胞侵襲實驗 細胞侵襲實驗采用美國Corning公司的Transwell系統,在小室底部預鋪基質膠(稀釋比例為 6 ∶1)。將經過不同轉染處理后的KYSE150細胞稀釋成細胞懸液(2×106個/ml),在6孔板內加入600 μl 含15%胎牛血清的培養基,在小室內加入100 μl 上述細胞懸液,繼續培養36 h。接下來,對小室的外面細胞進行染色:采用4%多聚甲醛溶液進行室溫固定,15 min后采用PBS洗滌,采用1%結晶紫染料進行染色,擦去小室的內面細胞。使用顯微鏡進行圖像采集。
1.2.6細胞周期檢測 將KYSE150細胞接種于6孔板中,培養過夜后,分別轉染siNC和siSPIB-1/2。48 h后,胰酶消化細胞并收集細胞進行細胞周期檢測:首先采用預冷的PBS溶液洗滌2次,然后用70%預冷乙醇固定,24 h后用預冷的PBS溶液洗滌2次,使用500 μl PI溶液進行染色,并避光孵育30 min(37 ℃)。用CytoFLEX流式細胞儀和CyExpert軟件分析染色細胞。采用Flow Jo軟件分析細胞周期G1/G0、S和G2/M期的細胞百分比。
1.2.7克隆形成實驗 將已構建好的穩定表達SPIB的KYSE30細胞系,細胞密度按照250個/孔接種于6孔板中。2周后,去除培養基,使用預冷PBS洗滌細胞2次,加入中性福爾馬林固定15 min,棄去固定液,加入結晶紫染色液染色15 min。使用PBS洗去多余的結晶紫染色液,并采用數碼相機進行拍照。
1.2.8Western blot實驗 采用預冷的RIPA裂解液(含1 mmol/L PMSF)裂解細胞10 min,以14 000 r/min離心5 min取上清液,即蛋白溶液。蛋白溶液通過BCA蛋白檢測試劑盒檢測蛋白樣品濃度。取35 μg蛋白加入到SDS-PAGE膠(10%)中進行分離并轉移到PVDF膜上。接下來,將PVDF膜置于5%脫脂奶進行封閉90 min后,棄去封閉液并與一抗孵育過夜(4 ℃)。使用TBS-T溶液洗滌3次,加入辣根過氧化物酶標記的山羊抗兔或鼠的二抗并孵育(室溫)。使用TBS-T溶液洗滌3次后,在目標條帶位置加超敏感化學發光顯色液,通過使用數字成像系統采集圖像。
1.2.9qRT-PCR實驗 細胞內總RNA使用細胞或組織RNA分離純化(FastPure Cell/Tissue Total RNA Isolation)試劑盒提取,并經HiScript II Q RT SuperMix試劑盒逆轉錄為cDNA,使用AceQ qPCR SYBR Green Master Mix試劑盒進行qRT-PCR實驗。SPIB引物F:5′-ACCATGCTCGCCCTGGA-3′,R:5′-GGCT AGCGAAGTTCTCC-3′;GAPDH引物F:5′-AGGTCG GTGTGAACGGATTTG-3′,R:5′-GGGGTCGTTGATG GCAACA-3′。
2 結果
2.1 SPIB在食管癌細胞系中的表達情況及其低表達對細胞增殖能力的影響與食管正常上皮細胞Het-1a比較,KYSE150等3株食管癌細胞系中SPIB mRNA和蛋白表達上升(P=0.000 1,F=126.90;圖1A、B)。進一步采用siRNA干擾技術分析,2條siRNA-SPIB均能有效地下調KYSE150細胞內SPIB蛋白表達(圖1C、D)。因此,通過CCK-8實驗顯示,下調SPIB表達可減弱KYSE150細胞的增殖能力,差異有統計學意義(48 h:P=0.009 0,F=29.76;72 h:P<0.000 1,F=89.51;圖1E)。
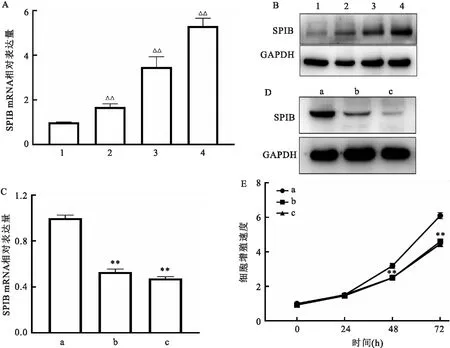
圖1 SPIB在食管癌細胞系中表達情況及其低表達對細胞增殖能力的影響
2.2 過表達SPIB對食管癌細胞增殖和克隆形成能力的影響通過構建過表達載體,成功在KYSE30細胞內穩定過表達SPIB蛋白(P<0.000 1,t=64.19;圖2A、B)。細胞增殖實驗表明,過表達SPIB促進KYSE30細胞增殖,差異有統計學意義(48 h:P= 0.000 1,t=14.06;72 h:P=0.000 7,t=9.363;圖2C)。SPIB亦增強KYSE30細胞的克隆形成能力,差異有統計學意義(P=0.002 0,t=7.15;圖2D、E)。
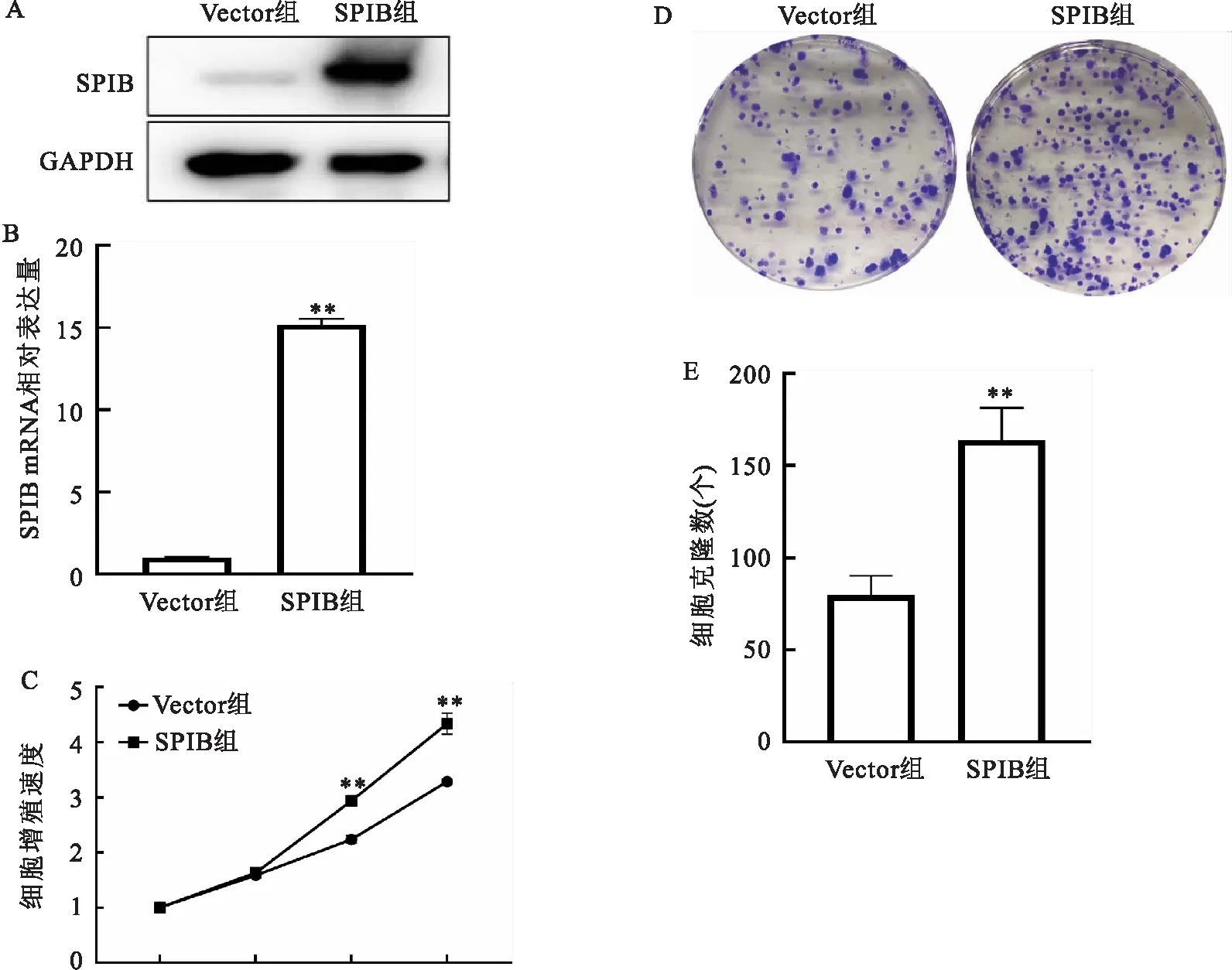
圖2 過表達SPIB對食管癌細胞增殖和克隆形成能力的影響
2.3 下調SPIB對食管癌細胞周期和Cyclin D1蛋白表達的影響為進一步了解SPIB對食管癌細胞周期的調控能力,采用流式細胞術檢測細胞周期,結果顯示:敲低食管癌細胞內SPIB表達,可以誘導細胞G1/G0期捕獲,降低S和G2/M期細胞比例,差異有統計學意義(圖3A、B,表1)。同時,下調表達SPIB進一步降低KYSE150細胞內Cyclin D1蛋白表達(圖3C)。
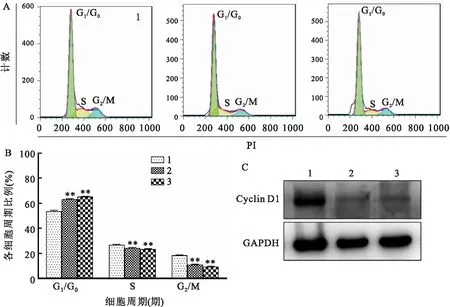
圖3 下調SPIB對食管癌細胞周期和Cyclin D1蛋白表達的影響
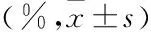
表1 下調SPIB對食管癌細胞周期的影響
2.4 下調SPIB蛋白表達對食管癌細胞上皮-間充質轉化能力的影響敲低KYSE150細胞內SPIB表達,可減弱細胞的遷移能力,差異有統計學意義(P<0.000 1,F= 305.00;圖4A、B)。Transwell實驗表明,siSPIB可抑制KYSE150細胞的侵襲能力,差異有統計學意義(P=0.004 7,F= 29.57;圖4C、D)。為進一步了解SPIB對食管癌細胞EMT相關蛋白表達的影響,通過Western blot檢測了細胞內N-cadherin和E-cadherin蛋白的表達水平,結果敲低SPIB表達,可以增加KYSE150細胞內E-cadherin蛋白表達,但減弱了N-cadherin蛋白的表達(圖4E)。

圖4 SPIB對食管癌細胞上皮-間質轉化能力及相關蛋白表達的影響
3 討論
食管癌是最常見的消化系統惡性腫瘤之一。雖然聯合手術與放化療能顯著提高患者的生存預后,但是5年總生存率仍然較低。因此,通過基礎實驗闡明食管癌發生發展的分子機制將有利于今后的抗食管癌治療。SPIB作為Ets家族轉錄因子的成員之一,在調控成熟B細胞的分化過程中發揮重要作用。Ho et al[6]研究表明結腸、肝臟和胃癌組織中SPIB蛋白表達水平顯著高于非腫瘤組織。研究[6, 8]表明,SPIB在肝癌和非小細胞肺癌等實體腫瘤中是重要的預后因子。
Zhao et al[11]通過對8例配對食管癌和癌旁正常組織進行GeneChip分析,發現了22個差異化表達轉錄因子,其中高表達的轉錄因子為:SPIB、BRCA1、MZF1、MAFG和NFE2L1,這提示SPIB可能作為一個促癌因子,調控食管癌增殖轉移。為驗證上述推測,本研究首先檢測了食管癌細胞系和正常食管上皮細胞中SPIB表達水平,結果顯示食管癌細胞中SPIB的mRNA和蛋白表達顯著高于食管上皮細胞。因此,推測SPIB可能是一個促癌因子,調控食管癌發展。由于在三株食管癌細胞系中,KYSE150細胞中SPIB表達最高,進行siRNA敲低實驗符合實驗設計,同時能更好反映SPIB對食管癌細胞生物學行為的影響;而KYSE30細胞中SPIB表達最低,siRNA干擾預實驗提示下調SPIB效果不明顯,無法進行后續實驗,故進行SPIB過表達實驗。此外,選擇不同細胞系進行正反方向驗證,可避免細胞系選擇單一而引起的結果偏差。分別通過siRNA和質粒轉染方式,下調和上調食管癌細胞中SPIB表達。細胞增殖實驗表明,過表達SPIB增強食管癌細胞增殖速度和克隆形成能力。敲低SPIB表達可顯著抑制Cyclin D1蛋白表達,誘導食管癌細胞停滯于G1期。遷移侵襲是食管癌的另一個惡性生物學行為。通過細胞劃痕實驗和Transwell系統檢測了SPIB低表達對食管癌上皮間質轉化行為的影響,結果顯示敲低SPIB表達可顯著抑制食管癌遷移侵襲。研究[8, 10]表明過表達SPIB可促進皮下移植瘤的肺部轉移,并顯著降低模型小鼠的總生存率[10]。研究[8]表明SPIB可通過靶向抑制緊密連接蛋白Claudin-2轉錄而抑制肺癌的早期轉移。本研究中,敲低SPIB表達可以增加食管癌細胞內E-cadherin蛋白表達,但抑制N-cadherin蛋白表達。因此,SPIB可通過調節E-cadherin和N-cadherin蛋白的表達,介導食管癌細胞的遷移侵襲能力。SPIB作為新發現的促癌轉錄因子,對眾多促癌因子起到正向調節作用。但在食管癌中,SPIB是否能通過轉錄調控方式調節促癌或抑癌因子表達,進一步影響食管癌的惡性行為需要進一步研究。
綜上所述,SPIB在食管癌細胞系中表達升高,可促進食管癌細胞增殖、遷移和侵襲,SPIB可能是今后食管癌診療的潛在靶點之一。

