circFAT1在非小細胞肺癌組織中表達及對細胞增殖和侵襲力的影響
徐至珺,王 炯,解明然,顏 宇,張 倩,周文勤
肺癌已成為我國發病率和死亡率位居首位的惡性腫瘤,其中,非小細胞肺癌(non-small cell lung cancer,NSCLC)是其主要病理學類型,約占80%以上[1],由于該腫瘤早期癥狀不典型,多數患者確診時已進展至中晚期,患者總體預后較差[2]。近年來,隨著靶向藥物治療技術的推廣應用,為攻克肺癌提供了新的契機[3]。因此,積極尋找NSCLC發生、進展中相關敏感基因,對NSCLC治療意義重大。環狀RNA(circular RNA,circRNA)作為廣泛存在于真核生物體內的一類帶有封閉共價環的非編碼RNA,可穩定的存在于生物體,不易被RNA酶降解,且具有組織表達相對特異的特點,在調控機體發育、代謝及多種疾病發生進展中發揮重要作用[4],近來發現,circRNA參與了惡性腫瘤侵襲轉移及多藥耐藥等過程[5]。circFAT1作為一種circRNA,已被發現在結直腸癌組織及細胞系中呈高表達[6],參與了骨肉瘤發生發展過程[7]。但其與NSCLC相關性鮮有報道。該研究分析NSCLC組織中circFAT1表達,并利用小分子干擾RNA(small interfering RNA,siRNA)技術沉默人NSCLC細胞系A549中circFAT1表達,評價其對細胞生物學功能的影響。
1 材料與方法
1.1 材料
1.1.1一般資料 選取2018年3月—2020年9月在安徽醫科大學第一附屬醫院行手術切除治療的NSCLC患者107例,其中,男65例,女42例,年齡35~74(55.85±11.37)歲;病理學類型:鱗狀細胞癌38例,腺癌69例;TNM分期:Ⅰ~Ⅱ期57例,Ⅲ~Ⅳ期50例;分化程度:低分化43例,中高分化64例;發生淋巴結轉移48例。術中留取NSCLC組織及距離腫瘤邊緣>5 cm的正常癌旁組織,迅速置于液氮中,-70 ℃保存。納入標準:① 術前未行任何治療;② 術后病理學檢查確診為NSCLC。排除標準:① 肺部嚴重感染者;② 繼發性肺癌及其他系統惡性腫瘤者;③ 心肝腎等重要臟器嚴重功能障礙者;④ 臨床資料不全者。本研究通過醫院倫理委員會批準,所有患者均行知情同意。
1.1.2主要試劑與設備 Trizol總RNA提取試劑和Lipofectamine 2000轉染試劑購自美國Invitrogen公司,逆轉錄和擴增試劑盒購自大連寶生物工程有限公司,circFAT1及內參引物序列由上海捷瑞生物工程有限公司設計合成,UV1800紫外分光光度計購自上海奧析科學儀器有限公司,人NSCLC細胞系A549購自南京科佰生物科技有限公司,DMEM培養液、胎牛血清、青-鏈霉素和胰蛋白酶購自美國Gibco公司,CCK-8試劑購自天津邁基生物科技有限公司,Transwell小室購自美國Coring公司,基質膠購自美國BD公司,Q5實時熒光定量PCR儀購自美國Bio-Rad公司。
1.2 方法
1.2.1RT-qPCR檢測NSCLC和癌旁組織中circFAT1表達 取NSCLC和癌旁組織,剪碎、超聲勻漿,用Trizol總RNA提取試劑提取總RNA,使用紫外分光光度計檢測其純度及濃度。按逆轉錄試劑盒說明進行逆轉錄獲得cDNA,使用Q5實時熒光定量PCR儀按擴增試劑盒說明對引物擴增,序列:circFAT1:上游5′-AACAGAAGAGAACTGGGGCG-3′,下游5′-GATCAGGGTGCCAATGGTGA-3′;GAPDH:上游5′-GATCAGGGTGCCAATGGTGA-3′,下游5′-TTTCTAGACGGCAGGTCAGG-3′。反應條件:94 ℃ 2 min,94 ℃ 30 s,56 ℃ 30 s,72 ℃ 30 s,連續38個循環,使用2-ΔΔCt法獲得circFAT1相對表達量。
1.2.2細胞培養與轉染 用含10%胎牛血清的DMEM培養液(含1%青-鏈霉素)對A549細胞培養,條件:5% CO2、37 ℃。待細胞密度在70%以上時,胰酶消化,接種于6孔板,每孔2.5×106個細胞,細胞融合度在80%以上時,使用Lipofectamine 2000轉染試劑分別對細胞轉染siRNA-circFAT1(si-circFAT1組)、無關序列(si-control組),另外設未轉染細胞作為空白組(blank組)。各組處理后繼續培養48 h。
1.2.3RT-qPCR術檢測細胞中circFAT1表達量 取各組轉染后培養48 h細胞,滴加細胞裂解液,其余步驟同“1.2.1”項下方法。
1.2.4CCK-8檢測細胞增殖情況 各組在轉染24 h后,胰酶消化,收集細胞,接種在96孔板,每孔2×103個細胞,在培養箱中分別于培養0、24、48、72和96 h時,向各孔加入CCK-8試劑10 μl,恒溫培養4 h,用酶標儀取450 nm波長處測定各孔光密度(optical density,OD)值。
1.2.5Transwell小室檢測細胞遷移和侵襲情況 取各組轉染后培養48 h細胞,胰酶消化,用無血清培養液對細胞重懸,密度調整為2.5×105個/ml,取細胞懸液200 μl加到Transwell小室上室,下室則加入正常培養液600 μl,用培養箱培養24 h,棄上室培養液,PBS沖洗,4%多聚甲醛固定,PBS再次沖洗,0.5%結晶紫染色15 min,顯微鏡下隨機取5個視野計數染色細胞數,取均數作為遷移細胞數。在檢測細胞侵襲情況時,將基質膠用培養液稀釋后對Transwell小室進行包被,過夜風干,其余步驟同檢測細胞遷移。
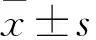
2 結果
2.1 NSCLC和癌旁組織中circFAT1表達量NSCLC組織中circFAT1相對表達量為(2.47±0.27),高于癌旁組織(1.02±0.15),差異有統計學意義(t=48.959,P<0.001)。
2.2 circFAT1在不同病理指標NSCLC組織中表達比較circFAT1在不同性別、年齡、病理學類型和腫瘤直徑的NSCLC組織中相對表達量差異無統計學意義(P>0.05),與TNM分期Ⅰ~Ⅱ期、中高分化、未發生淋巴結轉移比較,TNM分期Ⅲ~Ⅳ期、低分化和發生淋巴結轉移的NSCLC組織中circFAT1相對表達量升高,差異有統計學意義(P<0.05),見表1。
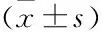
表1 circFAT1在不同病理指標NSCLC組織中表達比較
2.3 細胞中circFAT1表達量與si-control組和blank組比較,si-circFAT1組細胞中circFAT1相對表達量明顯降低,差異有統計學意義(F=138.245,P<0.001),見圖1。
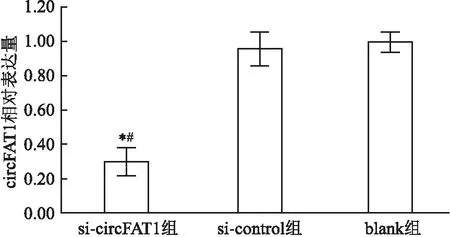
圖1 三組細胞中circFAT1的相對表達量
2.4 沉默A549細胞中circFAT1表達對增殖活性的影響與si-control組和blank組比較,si-circFAT1組細胞24、48、72和96 h時OD值均降低,差異有統計學意義(P<0.05),提示沉默circFAT1表達抑制A549細胞增殖活性。見圖2。
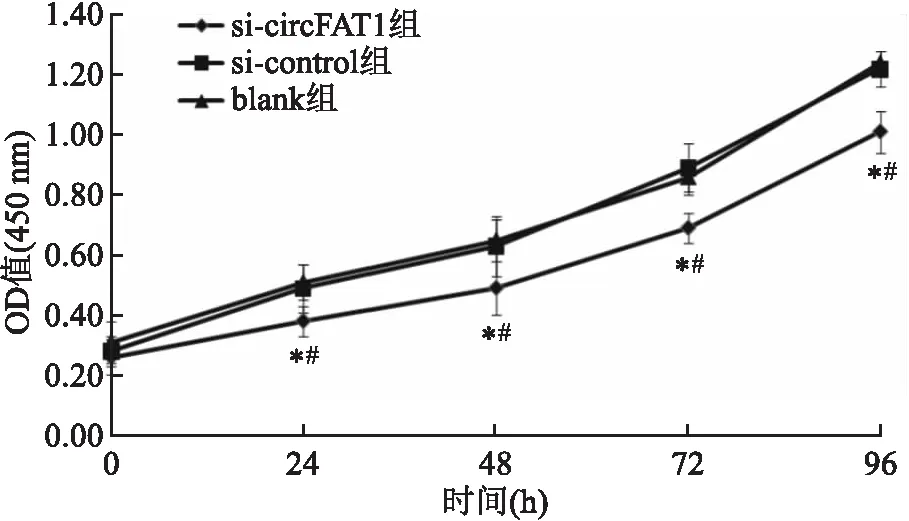
圖2 沉默A549細胞中circFAT1表達對增殖活性的影響
2.5 沉默A549細胞中circFAT1表達對遷移和侵襲能力的影響與si-control組和blank組比較,si-circFAT1組遷移細胞數和侵襲細胞數減少,差異有統計學意義(P<0.05),提示沉默circFAT1表達可抑制A549細胞遷移和侵襲能力。見表2,圖3、4。
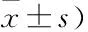
表2 三組細胞遷移和侵襲細胞數比較(個,
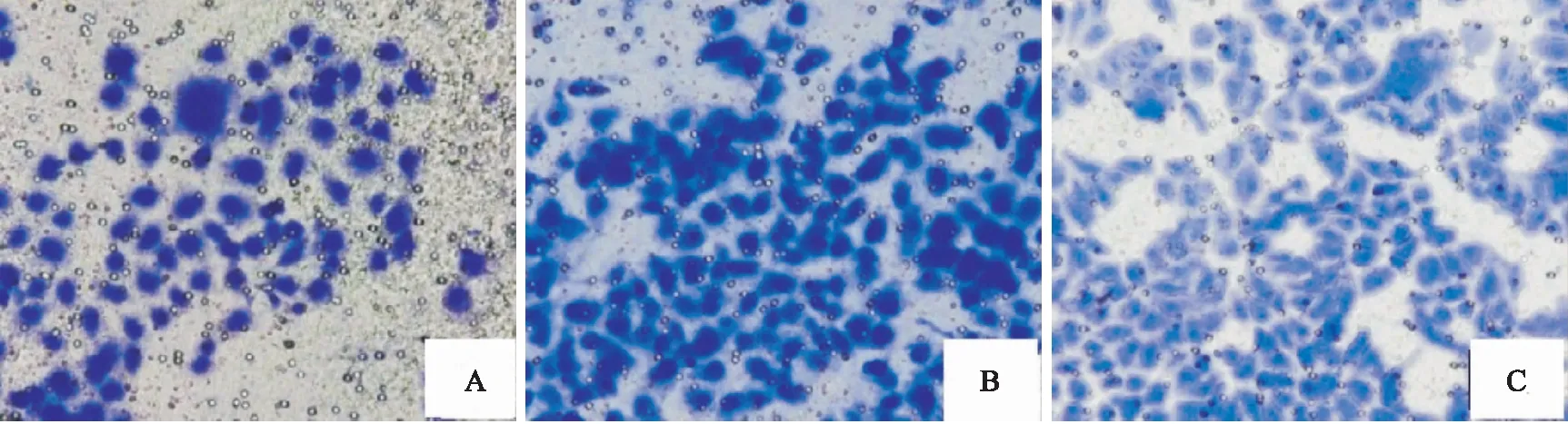
圖3 Transwell法檢測沉默A549細胞中circFAT1表達對遷移能力的影響 結晶紫染色×100
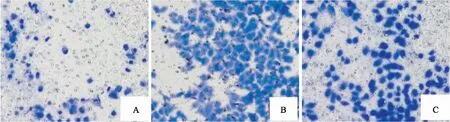
圖4 Transwell法檢測沉默A549細胞中circFAT1表達對侵襲能力的影響 結晶紫染色×100
3 討論
研究[8]發現,高侵襲性和易轉移是NSCLC細胞的主要特征,且是導致患者死亡的重要因素。因此,有必要針對NSCLC侵襲和轉移的相關機制開展研究,以指導臨床診療。circRNA是一類具有圓形結構且可穩定存在于細胞內的非編碼RNA,參與調控了小RNA的吸附、轉錄和剪切,同時在核糖體RNA處理及蛋白質與蛋白質間相互作用中發揮重要作用[9]。目前,其在惡性腫瘤中的作用開始受到重視。circFAT1作為一種circRNA,研究[10]發現,其可作為結直腸癌肝轉移的潛在預測指標。陳靖 等[11]報道,結直腸癌組織中circFAT1高表達且參與了癌細胞遷移和侵襲。亦有研究[12]發現,circFAT1促進了原發性肝癌進展。本研究顯示,NSCLC組織中circFAT1相對表達量高于癌旁組織,提示circFAT1可能參與了腫瘤發生。本研究結果顯示,TNM分期Ⅲ~Ⅳ期、低分化和發生淋巴結轉移的NSCLC組織中circFAT1相對表達量較TNM分期Ⅰ~Ⅱ期、中高分化、未發生淋巴結轉移明顯升高,進一步說明隨著NSCLC進展,circFAT1表達水平升高,提示circFAT1可能發揮癌基因功能參與了該腫瘤進展。
為進一步觀察circFAT1在NSCLC發生、進展中的作用,本研究采用siRNA技術沉默A549細胞中circFAT1基因表達,結果顯示,與si-control組和blank組比較,si-circFAT1組細胞中circFAT1相對表達量明顯降低,表明成功構建circFAT1低表達的細胞。有研究[6]報道,circFAT1可影響結直腸癌細胞增殖、凋亡和糖酵解。Liu et al[13]報道,circFAT1參與了骨肉瘤細胞增殖、遷移和侵襲。亦有研究[14]指出,circFAT1可通過miR-873/ZEB1軸促進甲狀腺癌增殖、遷移和侵襲。本研究結果顯示,與si-control組和blank組比較,si-circFAT1組細胞24、48、72和96 h時OD值均降低,遷移細胞數和侵襲細胞數減少,表明沉默circFAT1可抑制A549細胞增殖、遷移和侵襲能力,提示circFAT1可能參與了A549細胞增殖、遷移和侵襲過程,

