氧化數與靜電感應在有機化學教學中的應用
陶弘清


摘要:高中有機化學的課本呈現和一般教學過程大多注重有機物轉化的框架體系,以講述有機轉化事實為重點。這種模式下學生要對有機過程的本質進行探究存在很多困難。尤其是需要利用電子效應才能進行分析的有機反應,學生既不具有相關的知識基礎,也不具備相應的分析能力。面對這種現狀本文嘗試利用高中化學氧化數概念以及高中物理靜電感應的相關知識建立分析模型,利用高中學生現有知識從不同角度來理解電子效應和有機反應本質,實現學生化學學科核心素養尤其是證據推理與模型認知素養的培養。
關鍵詞:氧化數;靜電感應;電子效應;模型認知
文章編號:1008-0546(2022)04-0028-04
中圖分類號:G632.41
文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2022.04.006
在高中有機化學的教學過程中往往以各類有機物之間的相互轉為為框架,利用相關方程式為載體,突出了各類有機物官能團的轉化和相應的性質。這種教學模式對于初步建立學生的有機化學知識體系框架非常有利。但是其重事實輕理論分析的特點,往往使得學生在有機化學學習深入的過程中遇到理論分析或推測探究性問題時,完全找不到合理的理論切入點,基本不能形成有效的分析思路。導致學生對課內知識得心應手,卻對有一定信息背景的拓展型問題束手無策。面對這種教學現狀,一線教學過程中希望在原有框架上添加深入微觀結構層面的有機物結構性和原理性知識的呼聲越來越高。但是大量有機物結構性和原理性的理論知識往往艱深難懂,在一線教師講授以及學生理解的過程中都存在很多困難。所以如何用高中語言講好這些理論知識,實現講解過程中的知識降維處理,是當下有機教學中的一個重要課題。本文嘗試跨學科結合高中化學的氧化數概念以及高中物理中的靜電感應模型,來解決有機化學中電子效應部分知識的理解和應用,強化學生對有機化學反應本質的認識,在有機化學領域建立起證據推理與模型認知的化學學科核心素養。
一、氧化數視角下的電子效應
1.電子效應的基本內容和教學中存在的問題
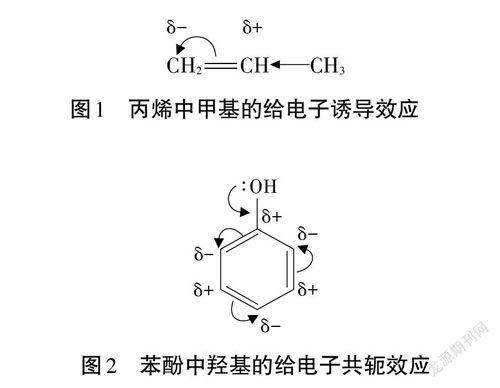
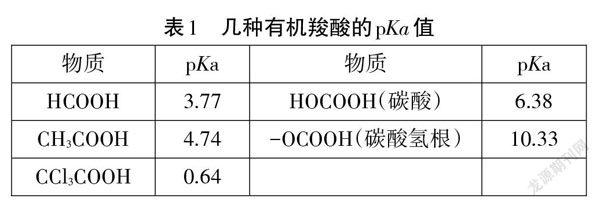
電子效應是解釋有機物性質,闡述有機反應歷程的重要工具。它是指在大多數有機反應中,由于分子中取代基的極化作用,使分子某些部分的電子密度下降或上升,從而帶部分正電荷或部分負電荷,稱為電子效應[1]。電子效應具體還可以根據極化作用方式細分為誘導效應、共軛效應、超共軛效應、場效應等或根據極化作用結果分為給電子效應或吸電子效應。利用電子效應可以很好地解釋有機化學反應中的選擇性問題,如利用甲基的給電子誘導效應(圖1)解釋丙烯不對稱加成中的馬氏規則;利用羥基的給電子共軛效應(圖2)解釋苯酚與濃溴水發生取代時苯環上的鄰對位定位效應。
電子效應雖然有強大的理論闡釋能力,但是核心的結構知識卻不在學生的知識框架中,所使用的分析描述方法如電子流向箭頭以及電性表示符號δ+、δ-對學生來說也十分陌生,很難迅速理解其背后的含義和使用方法。所以在學生理解原理和學會應用的過程中還需要適當的支架來連接電子效應和學生舊有的知識,搭建好知識跨越的臺階。
2.利用氧化數解決部分電子效應問題
電子效應中誘導效應是指由于共價鍵兩側的原子或基團吸引電子(電負性)能力不同導致成鍵電子云沿著原子鏈向某一側偏移的效應。這種電子云的偏移就導致某些原子或基團帶有部分的負電荷(用δ-表示)、某些原子或基團帶有部分的正電荷(用δ+表示)。通過電子云的偏移和電性的關系,不難發現高中知識中用于表征形式電荷的氧化數概念可以與誘導效應發生一定的遷移關系。
氧化數的正負正是由于電子分配的不均衡而形成,所以它可以用來表征元素在化合物中的形式電荷。其中氧化數為正值的原子就是正電荷的中心、氧化數為負值的原子就是負電荷的中心。通過氧化數就可間接完成誘導效應的分析,然后指導對有機反應的分析。例如下面以丙酮與氫氰酸加成為例進行分析:
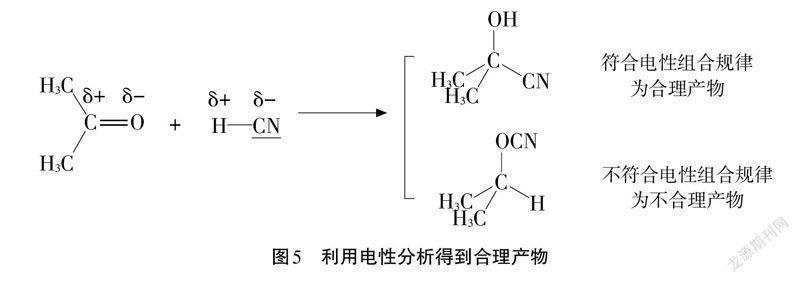
(1)先判斷丙酮中官能團羰基和氫氰酸中原子的氧化數,其中-CN作為整體進行氧化數分析,所得的結果如圖3。
(2)根據氧化數的判斷轉化為電性,正電荷中心用δ+表示,負電荷中心用δ-表示,所得結果如圖4。
(3)根據電性對正負電荷中心進行重新組合作用,同性電荷中心相互組合由于互斥導致產物不穩定,異性電荷中心相互吸引得到穩定的產物。這類分析方法還可以把有機反應與學生熟知的無機復分解反應過程進行練習,進一步降低了知識理解的難度和知識體系的關聯性。具體分析如圖5。
以上分析過程雖有一定程度的簡化,但是利用了學生已有的氧化數模型,合理降低了誘導效應的知識維度。符合化學學科證據推理與模型認知的核心素養要求,也為大學有機化學中親電、親核概念打下一定基礎,增強了不同層級知識間的關聯性和連貫性。
二、靜電感應的應用與電子效應
利用氧化數模型可以較好地解釋化學鍵的電子云偏移和反應中的電性組合問題,但是對于一些位置選擇類型的問題,氧化數模型卻不能給出很好的解釋。例如在苯酚當中,酚羥基鄰對位的C原子和間位的C原子氧化數均為-1,為何溴化過程中硝基選擇了鄰對位反應而不在間位反應。顯然氧化數模型已經不能單獨解決這類問題,還需要另外的模型加以補充,這里就可以用到物理中的靜電感應模型來解釋一系列由電子效應引發的有機反應選擇性的問題。
1.靜電感應模型概述
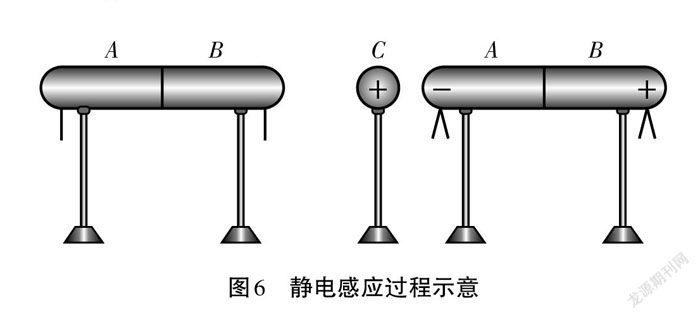
靜電感應是指在外部電場,如某些帶電體的作用下導體中電荷在導體中重新分布的現象[2]。例如圖6中A和B是連接的金屬導體,其上各自貼有金屬箔。把一個帶正電的金屬球C移近導體A,此時導體A因靜電感應帶上了相應負電,遠離C的導體B則帶上了與A等量的正電,貼在導體上的金屬箔也因為導體帶電而張開。
靜電感應產生的主要原因是在外加電場的作用下,導體中的電子定向移動,由于電荷同性相斥,異性相吸,正負電荷就會出現轉移。而在有機物中也存在類似的電荷轉移過程,例如苯酚中羥基的給電子共軛效應,使得苯環上出現了正負電荷相間隔的情況(見圖2)。但是給電子共軛效應的結構要求比較高,高中學生往往不具備分析復雜共軛體系的知識能力。是否可以利用靜電感應來分析有機物中電性的分布,本文將從三類情況出發分析建立模型。
2.靜電感應與苯環取代基定位效應
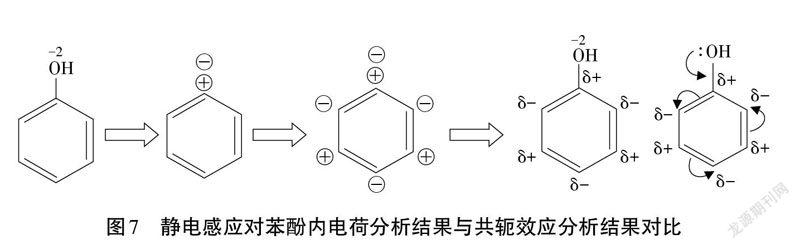
苯是典型的非極性分子,這表明雖然在苯分子中存在大π鍵,但是電荷分布是均勻的,并沒有出現負電荷集中或正電荷集中的碳原子,所以苯環中的六個碳原子是等價的。而苯酚分子則可以拆分為羥基和苯環兩個部分,由于羥基的存在改變了苯環上的電荷分布。由于直接和苯環相連的羥基氧是負電荷中心可被視為外加的負電荷,那么苯環大π鍵的離域電子將受到羥基氧的靜電感應,在與羥基相連的碳上將會感應出正電荷,而這個碳原子將繼續感應苯環上的其它碳原子,使得苯環上交替出現正負電荷中心。該分析過程與電子效應分析結果一致,實際是對電子效應本質的闡釋,電子效應中電子誘導或共軛的根本作用力來源正是靜電作用。其具體過程可以用圖7示意。
濃溴水中的溴單質如果與苯酚作用,該過程溴原子將得到電子被還原,所以缺乏電子的溴顯然會作用在負電荷比較集中的酚羥基鄰對位碳上。通過以上氧化數和靜電感應分析,可以幫助高中生在現有知識框架下確定苯酚與濃溴水反應的定位結果,也可以為后續電子效應的學習打下分析其本質的基礎。
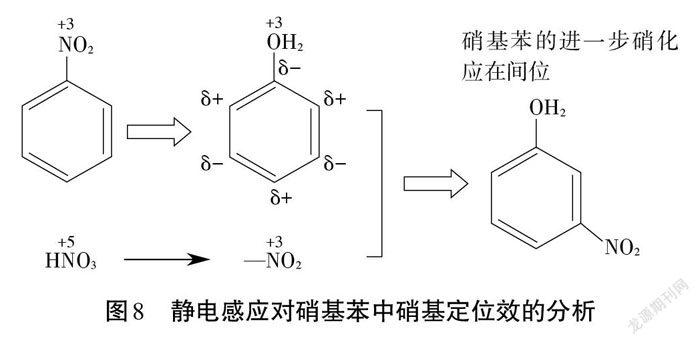
類似的分析流程也可以得到硝基苯繼續硝化過程中,苯環上硝基的間位定位效應(圖8)。
從結果來看,利用氧化數與靜電感應結合的分析結論與共軛效應分析結論基本一致。
3.靜電感應與馬氏規則
在高中有機化學中除了苯環上取代基具有定位的選擇性,烯烴的不對稱加成過程中也同樣存在選擇性問題。在高中課本中會提到馬爾科夫尼科夫規則即馬氏規則,但是該規則的描述過于經驗化,教學中則演化為“氫上加氫”口訣的記憶。學生完全抓不到規則背后的內涵,形成了對有機知識探究的障礙。出現這一問題的根本在于解釋馬氏規則的過程中除了涉及到誘導效應還會用到碳正離子的穩定性和超共軛電子效應,相較于誘導效應和共軛效應都更大地超越了學生現有的知識,教師很難進行深入細致的講解。但是拋開碳正離子的穩定性和超共軛電子效應其復雜的理論描述,追究以上理論的根本還是有機物中電性分布。所以該類問題依然可以使用氧化數與靜電感應結合的方法進行分析和處理。
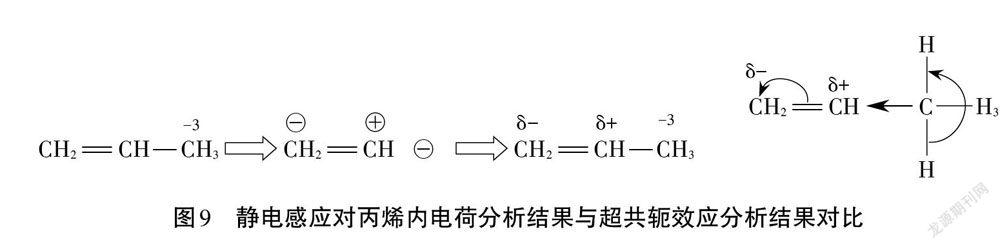
以丙烯與氯化氫加成的反應為例,可以將丙烯劃分為碳碳雙鍵和甲基兩個部分,其中甲基上的碳原子氧化數為-3,可以視為負電荷中心,將對碳碳雙鍵上的電子產生靜電感應,使得靠近甲基的雙鍵碳原子感應出正電荷,遠離甲基的雙鍵碳原子感應出負電荷。這樣的電性分布結果就使得氯化氫中正電荷中心的氫原子將作用到遠離甲基的雙鍵碳原子上,而該碳原子恰好是氫數較多的碳,體現出了“氫上加氫”的規則(圖9)。
靜電感應模型分析可以讓馬氏規則的使用不再經驗化,并且還可以解釋處理部分反馬氏規則的情況。例如3,3,3-三氟丙烯與鹵化氫的加成,因為三氟甲基上的碳不同于甲基上的碳,其所顯的是正價,是正電荷中心,靜電感應情況正好與甲基相反,所以該反應的結果是反馬氏規則的(圖10)。
4.靜電感應與有機物酸性
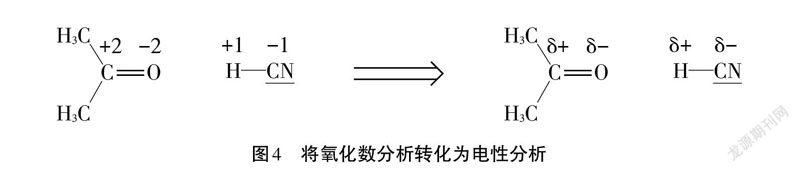
靜電感應模型除可以分析反應選擇性之外還可以對有機物本身的一些性質進行說明分析,如有機酸的酸性問題。表1列舉了幾種羧酸的pKa值[3]。
大部分有機物的酸性可以理解為羥基中氧氫鍵的共用電子對在一定作用下偏向氧原子造成共價鍵的異裂,氫以氫離子的形式電離。從造成有機物酸性的原理上來看,改變氧氫鍵中電子對偏離情況就可以改變有機物酸性的強弱。結合表1可以明顯發現與羧基直接相連原子可以通過不同的靜電感應影響酸性。其中乙酸、碳酸和碳酸氫根中與羧基相連的是氧化數為負的C、O原子,靜電感應的結果是羧基的負電荷相對會向羥基中氫一側移動,增加了電離的難度,其酸性相對較弱。而在甲酸和三氯乙酸中與羧基相連的是氧化數為正的C、H原子,靜電感應的結果是羧基的負電荷相對會向羥基中氧一側移動,價低了電離的難度,使得物質的酸性相對較強。
三、總結與反思
在有機化學的學習過程中,除了搭建有機物類型框架之外,滲透有機反應的原理,培養對有機反應進行分析的意識都是構建化學核心素養的必要基礎。從氧化數和靜電感應這類簡單模型切入,正是想利用不同的角度來說明電子效應、有機反應選擇性等原理問題,意在深化學生對有機化學本質的理解,使學生把握有機化學的內在邏輯,強化高中知識對復雜問題分析的有效性和遷移能力,突破一線教師在有機教學中所遇到的一些難點,改變有機教學中許多問題止于表象的現狀,最終實現化學核心素養的養成。但是本文以上的嘗試還停留在基礎階段,還需要在一線教學的不斷地實踐應用中完善,希望接下來能夠更好地服務于學生的發展。
參考文獻
[1]陳益,孫夕禮.從電子效應談把握《有機化學基礎》的學科內涵[J].化學教學,2016(5):3-7.
[2]趙金鳳.靜電感應中對稱性與疊加原理的應用[J].時代教育,2016(18):182.
[3]丁萍,繆建.淺談電子效應在有機化學中的應用[J].化學教學,2011(5):52-55.

