TCH新輔助化療對HER2陽性早期乳腺癌患者的療效及血清LCN-2水平表達的影響
毛琳
【摘要】 目的:研究TCH新輔助化療對人表皮生長因子受體2(HER2)陽性早期乳腺癌患者的療效及血清脂質運載蛋白-2(LCN-2)水平表達的影響。方法:將2017年5月-2020年3月鐵嶺市中心醫院收治的93例HER2陽性早期乳腺癌患者納入研究。采用電腦隨機數字表法將其分為研究組46例和常規組47例。常規組開展TAC新輔助化療,研究組則開展TCH新輔助化療。分析兩組療效、不良反應發生情況,比較兩組化療前后血清LCN-2、轉化生長因子-β1(TGF-β1)、血管內皮生長因子(VEGF)水平變化情況。結果:研究組總有效率高于常規組(P<0.05)。研究組化療1、3、6個療程后的血清LCN-2水平均低于常規組(P<0.05)。化療6個療程后,研究組血清TGF-β1、VEGF水平均低于常規組(P<0.05)。研究組不良反應發生率低于常規組(P<0.05)。結論:TCH新輔助化療應用于HER2陽性早期乳腺癌患者的治療中可獲得較為理想的效果,同時可降低血清LCN-2、TGF-β1、VEGF水平,減少不良反應的發生,具有較好的安全性。
【關鍵詞】 乳腺癌 人表皮生長因子受體2 TCH新輔助化療 脂質運載蛋白-2
Efficacy of TCH Neoadjuvant Chemotherapy on Early Breast Cancer Patients with Positive HER2 and Its Effect on Serum LCN-2 Level Expression/MAO Lin. //Medical Innovation of China, 2022, 19(06): 0-018
[Abstract] Objective: To study the efficacy of TCH neoadjuvant chemotherapy on human epidermal growth factor receptor 2 (HER2) positive early breast cancer patients and its effect on serum lipid carrier protein -2 (LCN-2) level expression. Method: A total of 93 patients with early breast cancer with positive HER2 who were admitted to Tieling Central Hospital from May 2017 to March 2020 were included in this study. They were divided into study group (n=46) and conventional group (n=47) by computer random number table method. TAC neoadjuvant chemotherapy was performed in the conventional group, and TCH neoadjuvant chemotherapy was performed in the study group. The efficacy and incidence of adverse reactions in the two groups were analyzed, and the levels of serum LCN-2, transforming growth factor-β1 (TGF-β1) and vascular endothelial growth factor (VEGF) were compared between the two groups before and after chemotherapy. Result: The total effective rate of study group was higher than that of conventional group (P<0.05). The serum LCN-2 levels in the study group were lower than those in the conventional group after 1, 3 and 6 courses of chemotherapy (P<0.05). After 6 courses of chemotherapy, the levels of serum TGF-β1 and VEGF in the study group were lower than those in the conventional group (P<0.05). The incidence of adverse reactions in the study group was lower than that in the conventional group (P<0.05). Conclusion: TCH neoadjuvant chemotherapy can achieve ideal effects in the treatment of early breast cancer patients with positive HER2, and can reduce serum LCN-2, TGF-β1 and VEGF levels, thus reducing the occurrence of adverse reactions and showing good safety.
[Key words] Breast cancer Human epidermal growth factor receptor 2 TCH neoadjuvant chemotherapy
Lipid carrier protein-2
First-author’s address: Tieling Central Hospital, Liaoning Province, Tieling 112000, China
doi:10.3969/j.issn.1674-4985.2022.06.004
乳腺癌屬于臨床上較為常見的女性生殖系統惡性腫瘤之一,當前乳腺癌的發病率正呈逐年攀升趨勢,且國內的發病率高出發達國家2%左右,是全球范圍內乳腺癌發病率增長率最快的國家之一,嚴重威脅女性生命健康安全[1-2]。相關研究數據顯示,臨床上約有30%的乳腺癌患者人表皮生長因子受體2(HER2)陽性,該類患者惡性程度較高,侵襲性較強,臨床治療難度較大,預后普遍不良[3]。化療是目前臨床上公認的治療HER2陽性乳腺癌有效方案,其中TCH新輔助化療在該病中的治療效果逐漸得到醫務人員的認可[4]。此外,脂質運載蛋白-2(LCN-2)是一種腫瘤標志物,于多種腫瘤中均存在異常高表達,且參與了和HER2陽性乳腺癌的發生、發展過程[5]。鑒于此,本文通過研究TCH新輔助化療對HER2陽性早期乳腺癌患者的療效及血清LCN-2水平表達的影響,旨在為該化療方案應用于HER2陽性早期乳腺癌患者的治療提供理論依據,現報道如下。
1 資料與方法
1.1 一般資料 將2017年5月-2020年3月鐵嶺市中心醫院收治的93例HER2陽性早期乳腺癌患者納入研究。采用電腦隨機數字表法將其分為研究組46例和常規組47例。納入標準:(1)所有受試者均與《外科學(第8版)》中所制訂的HER2陽性早期乳腺癌診斷標準相符[6];(2)均經病理檢查確診;(3)既往未接受過新輔助化療;(4)TNM分期為Ⅰ、Ⅱ期。排除標準:(1)心、肝、腎等臟器發生嚴重病變者;(2)合并其他惡性腫瘤者;(3)意識障礙或合并精神疾病者;(4)因故無法完成相關治療或失訪者。入組人員均于同意書上具名,醫院倫理委員會獲悉并核準本研究。
1.2 方法
1.2.1 治療方法 常規組開展TAC新輔助化療,即多西他賽注射液(生產廠家:正大天晴藥業集團股份有限公司,批準文號:國藥準字H20183209,規格:1 mL︰20 mg)75 mg/m2,第1天靜脈滴注;鹽酸表柔比星(生產廠家:浙江海正藥業股份有限公司,批準文號:國藥準字H20041211,規格:5 mL︰10 mg)80 mg/m2,第1天靜脈滴注;環磷酰胺(生產廠家:山西普德藥業有限公司,批準文號:國藥準字H14023686,規格:0.2 g)500 mg/m2,第1天靜脈滴注。以21 d為1個療程,連續治療6個療程。研究組則開展TCH新輔助化療,即多西他賽注射液75 mg/m2,第1天靜脈滴注;卡鉑注射液(生產廠家:齊魯制藥有限公司,批準文號:國藥準字H20020180,規格:10 mL︰100 mg)第1天靜脈滴注;曲妥珠單抗[生產廠家:Genentech Inc,批準文號:注冊證號S20060026,規格:440 mg(20 mL)/瓶],初始劑量為8 mg/kg,之后改為6 mg/kg,第1天靜脈滴注。以21 d為1個療程,連續治療6個療程。
1.2.2 標本采集 分別于治療前1 d以及治療1、3、6個療程后采集所有人員的晨起靜脈血4 mL。以8 cm作為離心半徑,3 500 r/min離心10 min,獲取血清保存于-80 ℃冰箱中備用待測。
1.3 觀察指標及判定標準 分析兩組療效,化療前后血清LCN-2、TGF-β1、VEGF水平變化情況,不良反應發生情況等方面的差異。(1)療效判定標準主要參照世界衛生組織(WHO)制訂的統一標準進行,①完全緩解(CR):腫瘤病灶全部消失;②部分緩解(PR):腫瘤病灶體積縮小50%及以上;③穩定(SD):腫瘤病灶體積縮小不足50%或增加不足25%;④惡化(PD):腫瘤病灶體積增加≥25%,或有新病灶出現[7]。總有效率=(CR例數+PR例數)/總例數×100%。(2)血清LCN-2、TGF-β1、VEGF水平的檢測主要是通過酶聯免疫吸附法完成,一應操作遵循試劑盒說明書完成。相關試劑盒均購自上海億豐生物有限公司。(3)不良反應以胃腸道反應、食欲降低以及血小板減少為主。
1.4 統計學處理 采用SPSS 22.0軟件對所得數據進行統計分析,計量資料用(x±s)表示,比較采用t檢驗;計數資料以率(%)表示,比較采用字2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組一般資料比較 研究組年齡31~60歲,平均(45.29±6.23)歲;腫瘤類型:小葉癌22例,浸潤性導管癌24例;TNM分期:Ⅰ期20例,Ⅱ期26例。常規組年齡31~60歲,平均(45.41±6.26)歲;腫瘤類型:小葉癌23例,浸潤性導管癌24例;TNM分期:Ⅰ期20例,Ⅱ期27例。兩組上述資料比較,差異均無統計學意義(P>0.05),具有可比性。
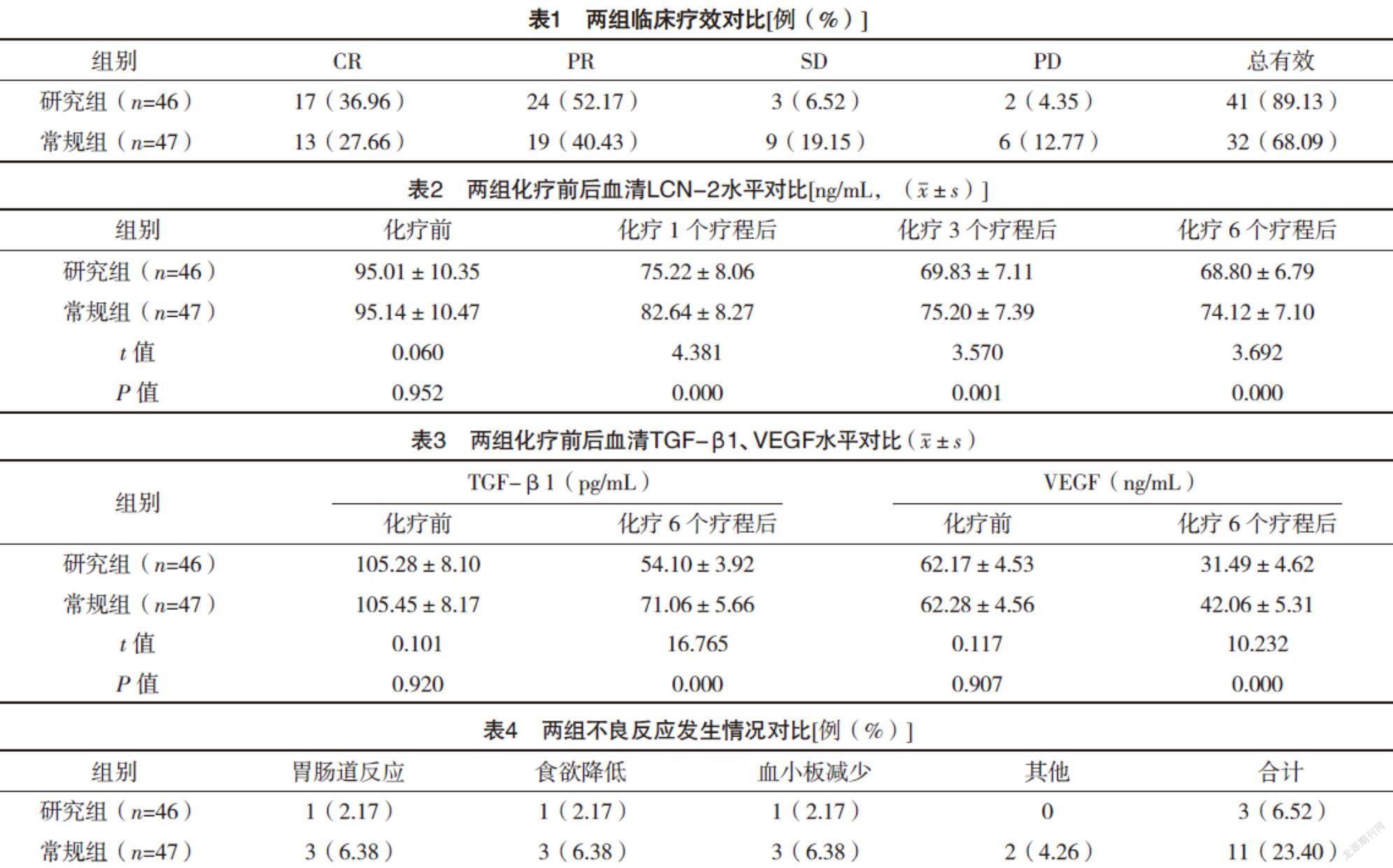
2.2 兩組臨床療效對比 研究組總有效率高于常規組,差異有統計學意義(字2=6.100,P=0.014),見表1。
2.3 兩組化療前后血清LCN-2水平對比 化療前,兩組LCN-2水平對比,差異無統計學意義(P>0.05);研究組化療1、3、6個療程后的血清LCN-2水平均低于常規組(P<0.05)。見表2。
2.4 兩組化療前后血清TGF-β1、VEGF水平對比 化療前,兩組血清TGF-β1、VEGF水平對比,差異均無統計學意義(P>0.05);化療6個療程后,研究組血清TGF-β1、VEGF水平均低于常規組(P<0.05)。見表3。
2.5 兩組不良反應發生情況對比 研究組不良反應發生率低于常規組(字2=5.182,P=0.023),見表4。
3 討論
乳腺癌作為一種全身性惡性腫瘤疾病,患者早期癥狀表現包括乳房腫塊、乳頭溢液以及腋窩淋巴結腫大等,且隨著病情的惡化,可能誘發器官病變,繼而對患者的生命安全造成極大威脅[8-11]。手術切除是臨床上治療乳腺癌的有效方式之一,尤其是早期乳腺癌患者接受手術切除后獲益匪淺。隨著近年來乳腺癌早期篩查、診斷技術的飛速發展,越來越多的早期乳腺癌患者被臨床檢出,從而使得有機會接受手術切除治療的病例與日俱增。然而,隨著人們生活水平的逐漸升高以及健康需求的日益提升,單純的手術切除治療已無法滿足患者需求。因此,針對乳腺癌的治療開始從單純手術治療逐步發展至以手術治療為主,化療為輔的綜合治療[12]。其中HER2陽性乳腺癌具有細胞毒性藥物的高耐藥性、惡性程度高以及病情進展迅速等特點[13],患者預后普遍較差,尋求一種積極有效的治療方案是廣大醫務工作者亟待解決的重要問題。
本文結果發現,研究組總有效率高于常規組。這提示了研究組治療方案可顯著提高HER2陽性早期乳腺癌患者臨床療效。究其原因,該化療方案中的曲妥珠單抗屬于人源化HER2單克隆抗體,可通過和HER2胞外結構域Ⅳ相結合,繼而對HER2的異常表達起到抑制作用,同時發揮拮抗HER2家族刺激腫瘤細胞增長的作用。而多西他賽屬于紫杉類抗腫瘤藥物之一,可通過刺激小管聚合成穩定的微管,繼而對腫瘤細胞分裂起到一定的抑制作用[14]。此外,LCN-2可通過調控E-鈣黏蛋白以及纖維連接蛋白表達,繼而促進上皮細胞的間質轉型,發揮調節細胞增殖、分化以及凋亡的作用。其在乳腺癌組織中的過表達增加了腫瘤浸潤、轉移的風險,且和患者預后不良明顯相關。而本研究結果顯示,研究組化療后1、3、6個療程的血清LCN-2水平均低于常規組。究其原因,研究組化療方案可通過對DNA合成進行抑制,繼而抑制腫瘤細胞增殖分裂,且研究組方案治療過程中患者發生耐藥的概率更低,從而可更好地抑制患者病情進展[15-17]。另外,研究組化療后血清TGF-β1以及VEGF水平均低于常規組。其中TGF-β1可發揮抑制組織上皮源性細胞的作用,其水平的升高往往反映了惡性腫瘤轉移風險增高,而VEGF是血管再生因子,在促進腫瘤增殖、生長方面起著積極促進作用。研究組化療方案中的曲妥珠單抗以及多西他賽聯合應用時具有一定的協同作用,因此可控制乳腺癌病情進展,提高治療效果。本文結果還顯示了研究組不良反應發生率低于常規組。這說明了研究組治療方案具有更好的安全性,其主要原因可能在于:該治療方案屬于全身性化療,其中多西他賽以及曲妥珠單抗具有協同作用,可明顯減少不良反應的發生[18-20]。
綜上所述,TCH新輔助化療治療HER2陽性早期乳腺癌患者的臨床效果較佳,可明顯降低血清LCN-2、TGF-β1、VEGF水平,有利于減少不良反應,安全性較佳。
參考文獻
[1]陳偉財,何勁松,吳恢升,等.TCH與TAC新輔助化療在HER-2過表達乳腺癌中的療效觀察[J].中國腫瘤臨床,2014,41(6):373-376.
[2]宋國紅,李惠平,邸立軍,等.真實世界吡咯替尼治療HER2陽性轉移性乳腺癌的療效及安全性[J].北京大學學報(醫學版),2020,52(2):254-260.
[3]辛靈,張虹,張爽,等.多西他賽+卡鉑聯合曲妥珠單抗方案對早期人表皮生長因子受體2陽性乳腺癌的新輔助治療效果[J].中華外科雜志,2021,59(3):222-227.
[4]徐巧萍,朱潔瑾,劉堅,等.HER-2陽性乳腺癌患者2種新輔助化療方案的藥物經濟學評價[J].中國現代應用藥學,2019,36(8):985-992.
[5]劉永霞,劉飛,高莉莉,等.血清sE-cadherin、LCN-2、MMP-9聯合檢測在乳腺癌早期診斷中的應用[J].現代腫瘤醫學,2021,29(11):1894-1898.
[6]周金妹,胡曉,張會強,等.曲妥珠單抗聯合蒽環類藥物對HER2陽性乳腺癌患者心臟功能影響臨床觀察[J].中華腫瘤防治雜志,2019,26(10):707-712.
[7]蘇猛,張星.循環腫瘤細胞評估行新輔助化療轉移性乳腺癌患者人類表皮生長因子受體2表達水平與療效及預后關系研究[J].臨床軍醫雜志,2021,49(4):427-428.
[8]周勇,李靖,彭世軍,等.HER-2過表達乳腺癌患者接受TCH與TAC新輔助化療后腫瘤惡性程度的評估[J].海南醫學院學報,2016,22(20):2471-2474.
[9]楊文強,劉敏,唐鐵雷,等.TCH新輔助化療方案治療HER-2陽性乳腺癌的療效及對患者ER、PR、HER-2及Ki67表達的影響[J].海南醫學,2020,31(20):2598-2601.
[10]徐玲,葉京明,朱賽楠,等.HER-2陽性早期乳腺癌TCH方案新輔助治療療效分析[J].中華醫學雜志,2018,98(12):907-911.
[11]張進儒,祁濤,劉海明,等.曲妥珠單抗治療失敗的HER-2陽性乳腺癌患者不同后續治療方案的療效及影響因素分析[J].現代腫瘤醫學,2021,29(1):61-65.
[12]崔志超,周立芝,馬杰,等.乳腺癌患者新輔助化療后ER、PR、HER2、Ki67表達變化及臨床意義[J].現代生物醫學進展,2020,20(10):1997-2000.
[13]朱曉敏,王浩楠,郭春龍,等.新輔助化療對乳腺癌患者激素受體、人表皮生長因子受體-2及炎性指標影響研究[J].臨床軍醫雜志,2019,47(2):196-198.
[14]王希佳,王剛.UGT2B7-161基因多態性預測接受EC-TH方案輔助化療HER-2陽性乳腺癌患者心臟毒性風險的價值[J].臨床腫瘤學雜志,2020,25(1):20-25.
[15]趙子偉,姚永強.吡咯替尼聯合槐耳顆粒治療人表皮生長因子受體2陽性晚期乳腺癌患者化療耐藥效果觀察[J].臨床軍醫雜志,2020,48(3):284-286.
[16]李思銳,楊芳,張德慧,等.曲妥珠單抗聯合紫杉醇新輔助化療人表皮生長因子受體2陽性乳腺癌的臨床效果觀察[J].中國醫學創新,2020,17(3):5-8.
[17] HUNTER F W,BARKER H R,LIPERT B,et al.Mechanisms of resistance to trastuzumab emtansine (T-DM1) in HER2-positivebreast,cancer[J].Br J Cancer,2020,122(5):603-612.
[18] ARAB A,YAZDIAN-ROBATI R,BEHRAVAN J.HER2-Positive,Breast,Cancer,Immunotherapy: A Focus on Vaccine Development[J].Arch Immunol Ther Exp (Warsz),2020,68(1):2-4.
[19]張凱,陳然,羅智輝,等.乳腺癌患者新輔助化療前后Ki-67、Tau表達水平與化療效果的關系分析[J].中國醫學創新,2019,16(22):63-66.
[20] EMENS L A,ESTEVA F J,BERESFORD M,et al.Trastuzumab emtansine plus atezolizumab versus trastuzumab emtansine plus placebo in previously treated, HER2-positive advanced breast cancer (KATE2): a phase 2, multicentre, randomised, double-blind trial[J].Lancet Oncol,2020,21(10):1283-1295.
(收稿日期:2021-07-29) (本文編輯:姬思雨)

