重慶地區辣椒疫霉交配型分布及對烯酰嗎啉的敏感性現狀
張世才 李怡斐 王春萍 楊小苗 段敏杰 黃任中 黃啟中

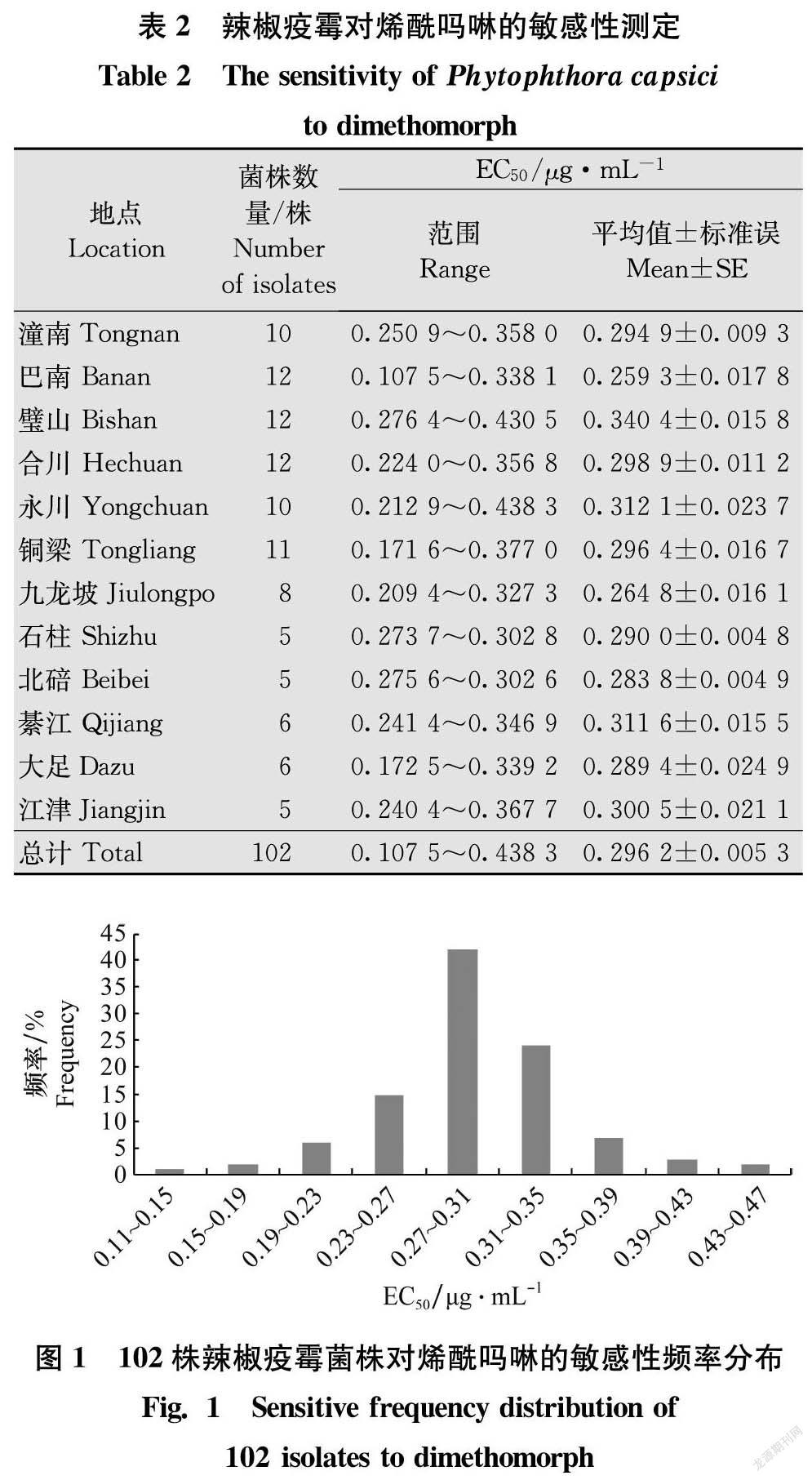
摘要 為明確重慶地區辣椒疫霉Phytophthora capsici交配型分布及對烯酰嗎啉的敏感性情況,對2019年-2020年分離的辣椒疫霉進行交配型和敏感性測定。研究發現重慶地區存在A1和A2兩種交配型,且兩者在大部分地區同時存在,測定的102株菌株中,24株菌株為A1交配型,78株為A2交配型,2種交配型的發生頻率分別為23.53%和76.47%。采自重慶潼南、巴南、石柱等地的102株辣椒疫霉菌株對烯酰嗎啉的敏感性測定結果顯示,其EC50分布在0.107 5~0.438 3 μg/mL之間,最不敏感菌株是最敏感菌株的4.1倍,平均EC50為(0.296 2±0.005 3)μg/mL。102株菌株對烯酰嗎啉的敏感性分布呈單峰曲線,未出現抗藥性病原菌亞群體。
關鍵詞 辣椒疫霉; 交配型; 烯酰嗎啉; 敏感性
中圖分類號: S436.418.1
文獻標識碼: A
DOI: 10.16688/j.zwbh.2021295
Abstract In order to clarify the mating type distribution of Phytophthora capsici and its sensitivity to dimethomorph in Chongqing, the mating types and sensitivity of P.capsici isolated in 2019-2020 were determined. The results showed that there were two mating types (A1 and A2) in Chongqing, and they existed in most areas at the same time. Among 102 isolates, 24 were A1 mating type and 78 were A2 mating type. The frequencies of two mating types were 23.53% and 76.47%, respectively. Their sensitivity to dimethomorph was tested, and the results showed that their EC50 values ranged from 0.107 5 to 0.438 3 μg/mL, with an overall mean of (0.296 2±0.005 3) μg/mL. The EC50 value of the most insensitive strain was 4.1 times of that the most sensitive strain.The distribution curve of sensitivity frequencies of P.capsici to dimethomorph was unimodal, and there was no resistant subpopulation among these isolates.
Key words Phytophthora capsici; mating type; dimethomorph; sensitivity
由辣椒疫霉Phytophthora capsici侵染引起的疫病是辣椒生產上的一種毀滅性土傳病害,在世界各地辣椒種植區均有發生[1]。P.capsici屬于異宗配合的卵菌,兩種不同的交配型菌株相互誘導才能發生有性生殖,產生的卵孢子具有更強的致病性、抗逆能力以及更廣泛的寄主植物[2]。有性生殖也是疫霉等植物病原菌遺傳變異的重要來源,因此,研究辣椒疫霉的交配型及分布,對辣椒疫霉的起源與演化、疫病發生規律及抗性育種材料的篩選等有重要意義。
在生產上,辣椒疫病的防治主要以培育抗病品種和化學藥劑為主[3]。烯酰嗎啉(dimethomorph)是一種羧酸酰胺類的內吸性殺菌劑,對霜霉屬Peronospora和疫霉屬Phytophthora卵菌病害具保護和治療作用,與苯基酰胺類殺菌劑無交互抗性[45]。……

