帕博麗珠單抗對PD-L1高表達的晚期肺腺癌患者的影響
李奕璇 趙敏 陳娜 馬靜
河南大學淮河醫院呼吸內科,開封 475000
肺腺癌是肺癌中的一種,屬于非小細胞癌,在女性肺癌患者中多見,多起源于支氣管黏膜上皮[1]。同其他類型的肺癌一樣,在腫瘤切除完全的情況下可增加生存率,但仍有近30%左右的患者術后會有復發的現象,對患者的身心均造成了不小的傷害[2]。而晚期肺腺癌患者因機體功能低下,且癌細胞的廣泛擴散,不能支持手術。腫瘤的發生與發展與機體的免疫機制有著密切聯系,免疫治療在癌癥系統性治療中占據了重要位置[3]。程序性細胞死亡受體-1(PD-L1)是一種重要的免疫抑制分子,具有下調免疫系統感應的作用,可使腫瘤細胞獲得免疫逃逸,促進腫瘤的惡性發展[4]。PD-L1 抑制劑可通過抑制 PD-1/PD-L1 信號通路,阻斷兩者結合,激活T 細胞的免疫反應,對腫瘤細胞進行識別、殺傷和清除,是目前臨床認為最為有效的治療方法[5]。帕博麗珠單抗作為PD-L1 抑制劑在肺癌患者中的應用得到臨床的廣泛關注,稱為肺癌的治療新星,基于此,本研究對河南大學淮河醫院采用帕博麗珠單抗治療的晚期肺腺癌患者進行療效觀察,探討其對細胞角化素蛋白片段 19(Cyfra21-1)、人半乳糖凝集素-3(Galectin-3)水平及PD-L1陽性表達率的影響。
資料與方法
1、一般資料
經河南大學淮河醫院倫理委員會審核通過,選取2019年5月至2021年5月在河南大學淮河醫院治療的70例晚期肺腺癌且PD-L1呈高陽性表達患者,男21例,女49例,年齡45~74(59.45±6.68)歲。(1)納入標準:①經病理學及影像學確診為晚期肺腺癌患者;②PD-L1 蛋白陽性表達率≥50%;③患者及家屬對本研究目的了解并同意入組。(2)排除標準:①合并其他惡性腫瘤者;②預計生存期不足6 個月者;③配合度較差者;④對本研究藥物及方法有禁忌者。
2、治療方法
患者在化療期間均給予營養支持及抗感染等基礎治療。藥品:帕博麗珠單抗注射液[注冊證號S20180019,愛爾蘭MSD Ireland(Carlow),100 mg/4 ml];用法:靜脈注射;用量:200 mg;時間:每3周1次。共持續使用12周,4個周期。
3、觀察指標
3.1、近期療效評估 參照《實體瘤治療療效評價標準》[6]對此次治療效果進行評估,分為完全緩解(CR)、部分緩解(PR)、疾病穩定(SD)、疾病進展(PD)4 級。以影像學表現為標準,當治療后病灶完全消失為CR;病灶范圍縮小30%及以上為PR;病灶范圍縮小不到30%或增大未超過20%為SD;病灶范圍增大20%及以上或有新病灶出現為PD。
3.2、血清學指標 于治療前及治療2、4周期后,抽取所有入組患者的空腹靜脈外周血,檢測Cyfra21-1、Galectin-3水平及PD-L1陽性表達率。檢測方法:采用酶聯免疫吸附試驗(ELISA)(試劑盒:上海酶聯生物科技有限公司)檢測患者Cyfra21-1、Galectin-3 水平;采用Western blot法檢測PD-L1 陽性表達率[一抗:PD-L1 多克隆抗體試劑采自武漢益普生物科技有限公司;二抗:羊抗小鼠免疫球蛋白G(IgG)單克隆抗體試劑盒采自北京百奧萊博科技有限公司]。
3.3、不良反應 記錄入組患者在治療期間出現淋巴細胞計數減少、血紅蛋白減少、肝功能異常等不良反應發生情況。
4、統計學處理
對本研究所得相關數據采用SPSS 21.0 統計學軟件進行分析,計數資料用例(%)表示,將滿足正態分布且方差齊的計量資料用()表示,組間差異采用兩樣本獨立t檢驗比較,組內多個時間點比較采用重復測量資料的方差分析,當P<0.05提示差異有統計學意義。
結 果
1、70例肺腺癌患者近期臨床療效情況
在治療 4 周期結束后,PR 26 例(37.14%),SD 34 例(48.57%),PD 10例(14.29%),總疾病控制率為85.71%。
2、70例肺腺癌患者治療前后血清學指標變化情況
由表 1 可知,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率在治療后有顯著下降趨勢,且隨著治療周期的推移,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率下降明顯(均P<0.05)。
表1 70例PD-L1高表達的晚期肺腺癌患者治療前后血清學指標變化情況()
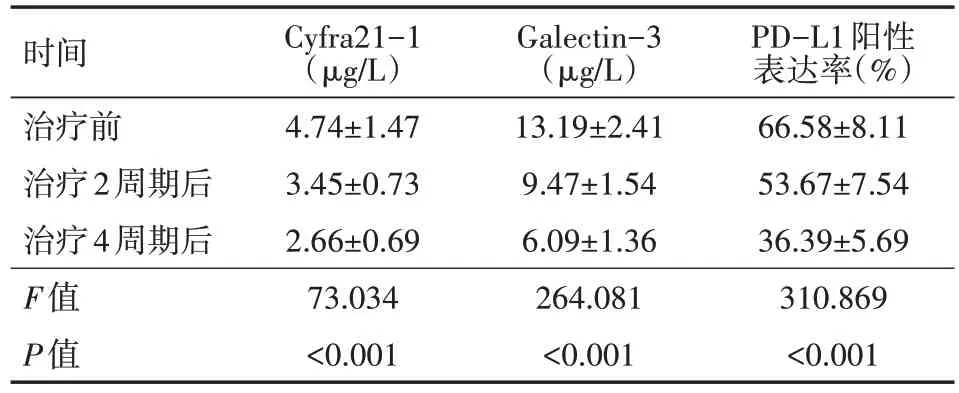
表1 70例PD-L1高表達的晚期肺腺癌患者治療前后血清學指標變化情況()
注:PD-L1為程序性細胞死亡受體-1,Cyfra21-1為細胞角化素蛋白片段19,Galectin-3為人半乳糖凝集素-3
PD-L1陽性表達率(%)66.58±8.11 53.67±7.54 36.39±5.69 310.869<0.001時間治療前治療2周期后治療4周期后F值P值Cyfra21-1(μg/L)4.74±1.47 3.45±0.73 2.66±0.69 73.034<0.001 Galectin-3(μg/L)13.19±2.41 9.47±1.54 6.09±1.36 264.081<0.001
3、不同療效肺腺癌患者治療前后血清學指標變化比較
由表 2 可知,在治療 4 周期后,療效為 PR 和 SD 的患者,較治療前比較,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率均有下降(均P<0.05);療效為PD 的患者,Cyfra21-1、Galectin-3 水平及PD-L1 陽性表達率與治療前比較差異均無統計學意義(均P>0.05)。治療4 周期后PR+SD 患者的Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率明顯低于PD患者(均P<0.05)。
表2 不同療效PD-L1高表達的晚期肺腺癌患者治療前后血清學指標變化比較()
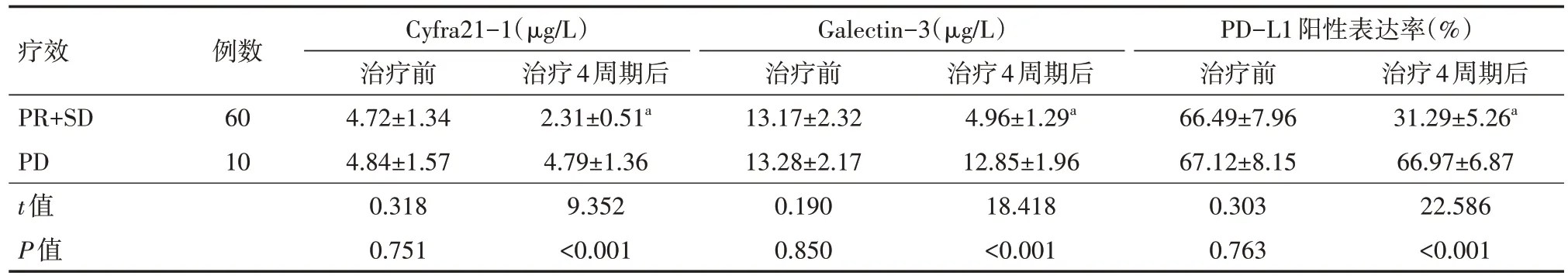
表2 不同療效PD-L1高表達的晚期肺腺癌患者治療前后血清學指標變化比較()
注:PD-L1為程序性細胞死亡受體-1,Cyfra21-1為細胞角化素蛋白片段19,Galectin-3為人半乳糖凝集素-3;PR為部分緩解,SD為疾病穩定,PD為疾病進展;與同組治療前比較aP<0.05
治療4周期后31.29±5.26a 66.97±6.87 22.586<0.001療效PR+SD PD t值P值例數60 10 Cyfra21-1(μg/L)治療前4.72±1.34 4.84±1.57 0.318 0.751治療4周期后2.31±0.51a 4.79±1.36 9.352<0.001 Galectin-3(μg/L)治療前13.17±2.32 13.28±2.17 0.190 0.850治療4周期后4.96±1.29a 12.85±1.96 18.418<0.001 PD-L1陽性表達率(%)治療前66.49±7.96 67.12±8.15 0.303 0.763
4、70例晚期肺腺癌患者治療過程中不良反應發生情況
在治療過程中,70 例晚期肺腺癌患者中有5 例出現淋巴細胞計數減少,3 例出現血紅蛋白減少,有2 例出現肝功能異常,總不良反應發生率為14.29%。不良反應均為Ⅰ~Ⅲ級,未出現Ⅳ級不良反應。
討 論
肺癌在我國惡性腫瘤中的發病率居于首位,嚴重威脅著我國人民的健康,肺腺癌是其中一種,起源于支氣管黏膜上皮,屬于腺上皮惡性腫瘤。腫瘤的預防和治療一直是醫學研究的熱點,近年來,隨著對腫瘤生理過程的深入研究,在機體免疫治療方向取得了很大的突破。PD-L1在諸多腫瘤細胞組織中呈高表達狀態,其通過與腫瘤細胞中的PD-1 結合,使腫瘤細胞逃離免疫系統的識別,從而促進腫瘤細胞的惡性發展[7]。帕博麗珠單抗作為PD-L1 免疫抑制劑的一種,具有肺癌治療新星之稱,對于中晚期肺腺癌患者、不適于手術治療者,免疫治療無疑是最佳選擇。本研究顯示,在治療4 周期結束后,總疾病控制率高達85.71%,說明帕博麗珠單抗治療PD-L1高表達的晚期肺腺癌患者有著較好的療效。
本研究顯示,70 例晚期肺腺癌患者經治療后,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率在治療后有顯著下降趨勢,且隨著治療周期的推移,Cyfra21-1、Galectin-3 水平及PD-L1 陽性表達率下降明顯。Cyfra21-1 是上皮源性的腫瘤標志物,廣泛分布于正常組織的上皮組織中,正常情況下在機體外周血以及淋巴結腫處于低水平狀態,當上皮組織癌變出現后,使Cyfra21-1 大量釋放,溶于組織液、體液及血液中,呈高表達狀態[8]。楊穎等[9]研究提到,Cyfra21-1 是非小細胞肺癌最有價值的血清腫瘤標志物。Galectin-3屬于半乳糖凝集素家族,存在于細胞核與細胞質間,有著調節細胞生長、分化和凋亡的作用,在腫瘤細胞中多有高陽性表達狀態[10],在齊德林等[11]的研究中顯示,Galectin-3水平的表達與肺癌腫瘤細胞淋巴結轉移有關。PD-L1/PD-1 信號通路是腫瘤免疫機制重要的途徑之一,抑制PD-L1 是免疫治療最主要的機制。這說明,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率可能可以作為療效評估的指標。本研究發現,在治療4 周期后,療效為PR 和SD 的患者,較治療前比較,Cyfra21-1、Galectin-3水平及PD-L1 陽性表達率均有下降;療效為PD 的患者,Cyfra21-1、Galectin-3 水平及 PD-L1 陽性表達率與治療前比較均無明顯差異。這提示,在治療過程中監測Cyfra21-1、Galectin-3 及 PD-L1 陽性表達率變化,對療效評估具有一定的價值。本研究發現,70 例晚期肺腺癌患者的總不良反應發生率僅為14.29%,且均未發生Ⅳ級不良反應。王蕓等[12]的研究中提出,帕博麗珠單抗治療晚期非小細胞癌患者未見明顯不良反應,本研究與其部分相似,說明帕博麗珠單抗的不良反應較小。
綜上所述,帕博麗珠單抗對PD-L1 高表達的晚期肺腺癌患者的疾病控制效果較好,可明顯降低Cyfra21-1、Galectin-3 及PD-L1 的陽性表達率,且不良反應較小。Cyfra21-1、Galectin-3 及 PD-L1 可作為治療效 果 的 觀察指標。
利益沖突所有作者均聲明不存在利益沖突

