口服藥物碳酸鑭輔助血液透析聯合血液灌流治療尿毒癥患者皮膚瘙癢的效果觀察
李寧寧
尿毒癥為各類腎臟疾病發展到終末期的典型臨床表現,在這一階段,患者由于腎功能衰竭,Ca2+、P3+、維生素D(Vit D)代謝障礙,生存受到威脅,必須通過血液透析凈化血液方可維持性命[1]。不過,在長期治療過程中,并發癥發生率高,其中,高磷血癥在我國尿毒癥血液透析患者中的發生率高達57.42%,這一并發癥會導致鈣磷代謝異常,引發繼發性甲狀旁腺功能亢進(SHPT),增加血管鈣化及皮膚瘙癢等并發癥的發生風險[2]。治療尿毒癥并發皮膚瘙癢的患者,需在血液透析的基礎上,采取局部止癢措施,但實踐證明效果不明顯,因為血液透析無法有效去除血漿中的毒素,需聯合血液灌流。因此,此次試驗將本院在2018年1 月~2019年6 月收治的60例尿毒癥皮膚瘙癢患者作為研究對象,旨在探究口服藥物碳酸鑭輔助血液透析聯合血液灌流在其中的臨床療效,報告如下。
1 資料與方法
1.1 一般資料 選取2018年1 月~2019年6 月本院收治的60例尿毒癥皮膚瘙癢患者,按照隨機抽樣法分成對照組和觀察組,每組30例。對照組男19例,女11例;年齡38~71 歲,平均年齡(53.10±5.97)歲;血液透析時間5~35個月,平均血液透析時間(22.57±5.86)個月;尿毒癥病程6個月~4年,平均尿毒癥病程(2.1±0.7)年。觀察組男18例,女12例;年齡39~72 歲,平均年齡(53.64±6.13)歲;血液透析時間5~35個月,平均血液透析時間(22.37±5.80)個月;尿毒癥病程6個月~4年,平均尿毒癥病程(2.2±0.7)年。兩組一般資料比較,差異均無統計學意義(P>0.05),具有可比性。
1.2 納入及排除標準 納入標準:①在血液透析前,有慢性腎損害史,血肌酐(Scr)>8 mg/dl,血尿氮素(BUN)>80 mg/dl,符合尿毒癥相關診斷標準,且存在皮膚瘙癢癥狀;②均知情簽署相關醫護同意書[3]。排除標準:①甲狀腺功能亢進及肝腎功能不全者;②高鈣血癥或低鈣血癥使用鈣劑治療者;③存在碳酸鑭禁忌證者。
1.3 方法
1.3.1 對照組 采取規律性血液透析治療,即采取費森尤斯4008B 型血液透析機以及空心纖維聚砜膜F6 透析器,選用碳酸氫鈉透析液,透析液流量調節為500 ml/min,血流量調節為200~300 ml/min,連續治療4 周,3~4 次/周,4.0~4.5 h/次,期間輔以皮膚局部止癢治療。連續進行1個月治療。
1.3.2 觀察組 患者給予口服藥物碳酸鑭輔助血液透析聯合血液灌流治療,將健帆生物科技集團股份有限公司生產的HA130 一次性血液灌流器串聯在血液透析器之前,同時,口服碳酸鑭咀嚼片(英國Hamol Limited,國藥準字HJ20171351),初始劑量為0.75 g/d,隨后增加至1.5~2.0 g/d,以獲得滿意療效。連續進行1個月治療。
1.4 觀察指標及判定標準 比較兩組患者治療前后的生化指標(Ca2+、P3+、PTH)以及臨床療效。治療前后,采用邁瑞BS-420 全自動生化分析儀,測定兩組Ca2+、P3+水平,采用美國雅培I-2000SR 全自動免疫化學發光分析儀,測定兩組血PTH 水平,計算平均值[4]。根據上述生化指標變化,綜合皮膚瘙癢癥狀緩解情況,將臨床療效分為:①顯效:經積極治療后,患者的皮膚瘙癢癥狀消除,體征恢復正常水平;②有效:經積極治療后,患者的皮膚瘙癢癥狀好轉,體征有所恢復;③無效:均達不到上述標準[5]。總有效率=(顯效+有效)/總例數×100%。
1.5 統計學方法 采用SPSS22.0 統計學軟件處理數據。計量資料以均數±標準差()表示,采用t檢驗;計數資料以率(%)表示,采用χ2檢驗。P<0.05 表示差異有統計學意義。
2 結果
2.1 兩組患者治療前后生化指標比較 治療前,兩組Ca2+、P3+、血PTH 比較,差異均無統計學意義(P>0.05)。治療后,觀察組Ca2+、P3+、血PTH 均優于對照組,差異均具有統計學意義(P<0.05)。見表1。
表1 兩組患者治療前后生化指標比較()
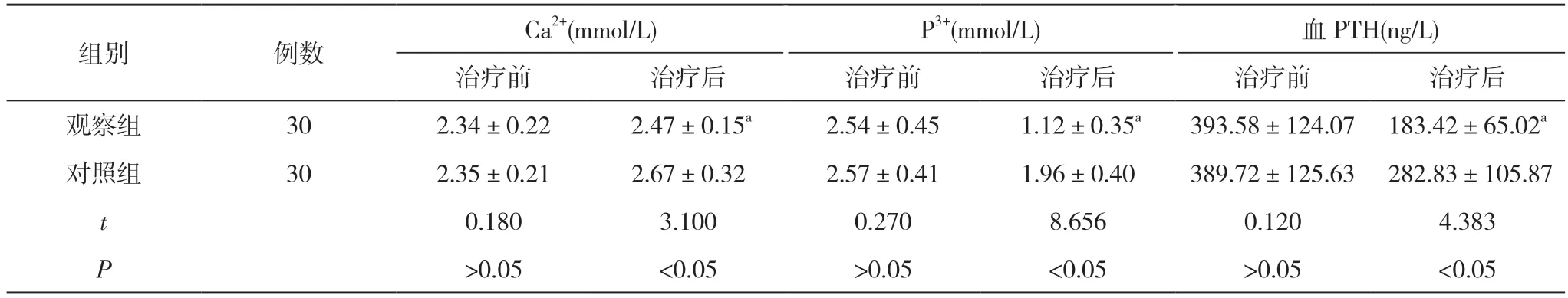
表1 兩組患者治療前后生化指標比較()
注:與對照組比較,aP<0.05
2.2 兩組臨床療效比較 觀察組治療總有效率96.67%高于對照組的66.67%,差異具有統計學意義(P<0.05)。見表2。
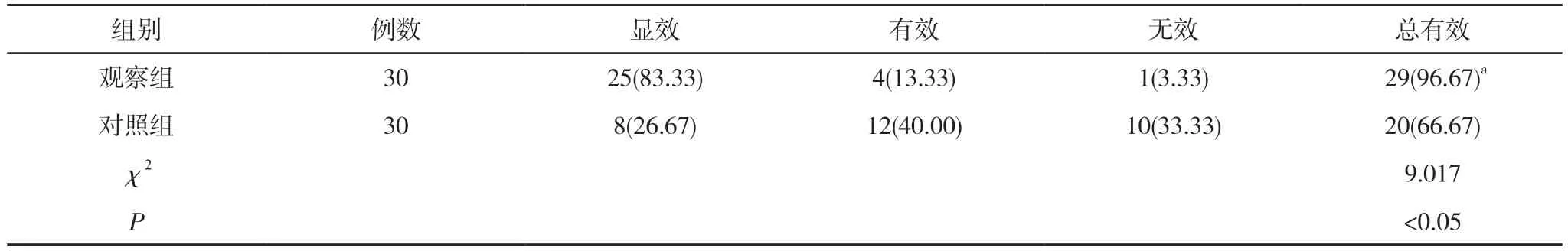
表2 兩組臨床療效比較[n(%)]
3 討論
終末期腎病(End stage renal disease,ESRD)患者發生尿毒癥瘙癢及慢性腎病相關性瘙癢的幾率>50%,這一癥狀會給患者帶來極大的困擾,嚴重影響其生活質量,必須及時治療。據研究,皮膚瘙癢的發生,與甲狀腺旁激素組織胺、鈣鹽、磷鹽等物質相關,而高磷血癥,則是繼發性甲狀旁腺功能亢進的始動因素,是誘發皮膚瘙癢的主要原因,因此,控制血磷水平,是控制皮膚瘙癢癥狀的關鍵性策略。
高磷血癥是尿毒癥血液透析期間發生率極高的并發癥,在嚴格飲食控制的情況下,患者磷元素攝入量高達1000 mg/d,借助透析可濾除800~900 mg,每周會積累1000 mg 的磷元素,遠遠超過治療指南中的血磷水平控制標準[6]。血液透析是一種能夠有效清除人體血液中滯留的小分子物質的手段,可清除尿毒癥患者體內的代謝廢物,維持水電解質平衡及酸堿平衡,但對于其中的中、大分子毒素則難以有效清除,而對于血液灌流方式來說利用對流、彌散相結合的方法,能夠使PTH 大分子物質及脂溶性毒素得到有效清除[7,8]。在此基礎上,本次重點提到口服碳酸鑭治療方法,其中碳酸鑭是一種非含鈣磷去除劑,藥物中的陽性三價鑭離子對于陰性磷酸根離子具有極強的吸附能力,二者可結合形成不溶于水、分子質量較大的復合物,這種物質無法通過血管基底膜進入血液,可有效降低血磷水平。相較于高磷血癥治療的傳統藥物,比如說鋁制劑、鈣制劑,碳酸鑭不會引起鋁中毒或者是高鈣血癥,安全性更高,值得借鑒及應用[9-12]。
在本次研究過程中,納入研究的對照組患者采取規律性血液透析方法醫治,觀察組患者則采取口服藥物碳酸鑭輔助血液透析聯合血液灌流方法醫治,研究結果表明:治療前,觀察組患者Ca2+、P3+、血PTH 與對照組比較,差異均無統計學意義(P>0.05)。治療后,觀察組Ca2+、P3+、血PTH 均優于對照組,差異均具有統計學意義(P<0.05)。觀察組治療總有效率96.67%高于對照組的66.67%,差異具有統計學意義(P<0.05)。研究結果數據表明,口服藥物碳酸鑭輔助血液透析聯合血液灌流治療方案具備實施的科學性及有效性;這與相關學者的研究成果較為相似。有學者表示,針對尿毒癥皮膚瘙癢患者,采取口服藥物碳酸鑭輔助血液透析聯合血液灌流治療的療效顯著,治療總有效率高達90.00%以上,與本研究結果相符,由此可見口服藥物碳酸鑭輔助血液透析聯合血液灌流治療的效果頗高。
綜上所述,口服藥物碳酸鑭輔助血液透析聯合血液灌流治療尿毒癥患者皮膚瘙癢的療效明顯,能夠使患者的皮膚瘙癢癥狀得到有效消除,進一步使患者的生存質量得到有效改善,所以,具備推廣及使用的價值。

