雙相障礙患者炎癥因子和膠質細胞源性神經營養因子與認知功能的關系
鐘育年, 趙義林, 肖文煥, 楊 翔, 徐 瑩
(江蘇省揚州市精神衛生防治中心/江蘇省揚州五臺山醫院 精神科, 江蘇 揚州, 225003)
雙相障礙是一種以躁狂和抑郁發作為特征的情緒障礙,這是一種中樞神經系統彌漫性生化改變的全身性疾病。患者因認知障礙導致的社會職業功能喪失和人際關系缺陷,是其核心特征之一。但目前這一現象的神經生物學基礎尚不清楚。研究[1-2]表明,炎癥和神經營養缺陷是雙相障礙病理生理學的重要因素,可能參與雙相障礙認知缺陷的內在機制。臨床研究報告雙相障礙躁狂期和抑郁期的免疫和炎癥水平發生變化,如急性期反應物、異常炎癥細胞因子水平和活化淋巴細胞亞群增加[3]。免疫功能障礙在認知障礙的發展中起著關鍵作用,但是炎癥對雙相障礙認知影響的研究數量有限。CHEN M H等[4]強調炎癥和氧化應激在雙相障礙中的作用,但有關炎癥機制如何影響這些患者認知障礙的數據不充分。中性粒細胞-淋巴細胞比(NLR)和血小板-淋巴細胞比(PLR)是外周炎癥標志物之一,很容易從血液循環獲取,但是其與精神疾病關系的研究文獻較少。
膠質細胞源性神經營養因子(GDNF)是轉化生長因子β家族中的一員,在海馬細胞的發育和功能中發揮作用,而內在海馬活動是精神疾病認知和癥狀的生物標志物[5]。GDNF不僅涉及許多生理過程,保護中樞神經系統和周圍神經系統免受變性,同樣涉及多種神經和精神疾病的發病機理,例如雙相障礙和精神分裂癥[2, 6]。因此GDNF是一種具有多種生物學功能的神經營養因子,其可能是炎癥與神經可塑性之間的橋梁。本研究比較雙相障礙患者和健康對照者NLR、PLR和GDNF, 并探討GDNF和炎癥的交互作用對認知功能的影響,現報告如下。
1 資料與方法
1.1 一般資料
雙相障礙患者均來自江蘇省揚州五臺山醫院住院部或門診部,隨機選擇患者55例納入本研究觀察組。納入標準: 患者年齡18~60歲,漢族; 符合雙相障礙DSM-Ⅳ診斷者; 患者病情處于穩定期,漢密爾頓抑郁量表評分<8分, Young氏躁狂量表評分<6分; 病程至少5年者; 進入研究前已接受口服心境穩定劑或抗精神病藥物劑量穩定至少12個月者; 提交書面知情同意書者。排除標準: 精神分裂癥或其他精神病的診斷史者; 精神發育遲滯或廣泛性發育障礙診斷者; 臨床顯著神經系統疾病或頭部損傷伴意識喪失者; 目前正在服用認知增強藥物,治療疼痛藥物或其他可能影響認知能力藥物者; 酗酒或吸毒依賴史者; 無法充分理解普通話或測試說明者。
對照組由當地健康志愿者54例組成,志愿者或其一級親屬無DSM-Ⅳ五軸診斷軸Ⅰ診斷的精神疾病,其余排除標準和雙相障礙患者一樣。2組在性別、年齡、受教育年限上差異均無統計學意義(P>0.05)。所有參與者均獲得書面知情同意,并經醫院倫理委員會批準。
1.2 方法
1.2.1 量表評定: 采用MCCB中文版認知測試中的3個量表進行患者和正常健康組認知領域的評估: 連線測試(TMT)、言語流暢性測驗(VFT)和Stroop測驗(斯楚普測驗),這些量表被翻譯成中文,心理測量特性良好(Cohen′s d 0.02~0.49)。重測信度,效度良好(組間相關系數0.73~0.94)[7]。
1.2.2 血液標本檢測: 從受試者身上采集空腹靜脈血樣,在他們進行神經心理測試的當天測量中性粒細胞、淋巴細胞和血小板計數,計算NLR和PLR。而GDNF的檢測需要先分離血清保存到-70 ℃冰箱待進一步分析。根據制造商的說明(Promega, Madison, WI, USA), 采用酶聯免疫吸附試驗進行GDNF血清濃度檢測。所有的樣品和標準品重復測量2次。由1名經驗豐富的實驗員一次性對同一批試劑盒上的所有平板進行檢測。標準曲線范圍為15.6~1 000.0 pg/mL。批內和批間變異系數分別為<5%和<10%。
1.3 統計學方法
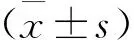
2 結 果
2.1 一般資料的比較
觀察組與對照組在年齡、性別、教育年限、吸煙狀態和體質量指數方面的差異均無統計學意義(P>0.05)。與對照組比較,觀察組NLR和PLR升高,而GDNF濃度降低; 在神經認知測試方面除Stroop-單詞和顏色外,觀察組認知表現均差于對照組,差異具有統計學意義(P<0.05), 見表1。

表1 2組一般資料比較
2.2 認知功能相關性分析
在雙相障礙患者中,受教育程度與VFT-動作(r=-0.429,P=0.001)和TMT-B(r=0.344,P=0.010)均存在相關性。NLR和GDNF(r=-0.415,P=0.002)、VFT-動作(r=-0.379,P=0.004)及TMT-B(r=0.597,P<0.001)均存在相關性。GDNF亦與VFT-動作(r=0.269,P=0.047)及TMT-B(r=-0.407,P=0.002)呈顯著相關。但是, PLR與神經認知測試之間未發現顯著相關性(P>0.05)。此外對照組NLR、PLR、GDNF和神經認知測試之間無顯著相關性(P>0.05)。
2.3 認知功能回歸分析
因為NLR和GDNF均與VFT-動作和TMT-B相關,此外NLR和GDNF亦相關,因此需要進一步采用分層回歸分析控制混雜因素,探討NLR和GDNF交互作用對認知功能的影響。首先以TMT-B為因變量,第1層模型中,將P<0.05的人口學變量及文獻報道有影響的臨床變量(年齡、受教育程度、病程)同時納入分析; 在第1層基礎上將炎癥指標NLR和GDNF作為第2層模型; 第3層在第1、2層基礎上納入交互變量NLR和GDNF交互作用進行分析。
研究發現第1層中R2=0.129, 說明單一的人口學和部分臨床數據不能預測認知功能。第2層中,R2=0.609, 增加了0.479, 說明炎癥因子(β=15.475,P<0.001)、GDNF(β=-0.016,P=0.046)可以預測TMT-B。第3層中,交互項(β=0.166,P<0.001)可以正向預測TMT-B, 其R2=0.914, 增加了0.305, 表明兩者交互作用可以解釋認知功能TMT-B總變異的30.5%, 見表2。當再次以VFT-動作為因變量時,未發現炎癥因子和GDNF存在交互作用影響認知表現(P>0.05)。

表2 雙相障礙患者TMT-B影響因素回歸分析
3 討 論
雙相障礙是一種復雜的精神疾病,其特征在于認知方面不同程度的損害,包括言語功能,處理速度和注意及記憶力。目前研究[8]顯示,即使和健康人有相同的智力和受教育水平,雙相障礙患者在臨床癥狀穩定后仍存在認知損害,范圍可能從接近正常到全部損害。MISKOWIAK K W等[9]發現雙相障礙患者除了語言學習任務以外的所有神經認知功能測驗都和正常人相似。SONKURT H O等[10]研究也表明雙相障礙存在相當大的認知異質性。本研究發現雙相障礙患者即使在穩定期,認知功能仍部分受損,尤其是執行功能。臨床研究中還發現雙相障礙患者的NLR和PLR比對照組升高, GDNF血清濃度降低,表明患者存在炎癥反應增加和神經營養缺陷,這和國內外的研究[11]結果相一致。此外NLR作為內皮功能障礙和炎癥的標志物具有預后和預測價值。KALELIOGLU T等[12]提出NLR和PLR在雙相障礙躁狂期甚至正常狀態中的病理生理學中都起作用。SAGLAM AYKUT D等[13]揭示NLR與雙相障礙躁狂發作住院患者的Stroop干擾評分呈負相關。GDNF對大腦的黑紋狀體和中腦邊緣單胺能系統具有保護效果,被認為是多巴胺能和5-羥色胺能,而這兩種遞質與雙相障礙的發病機制密切相關[14]。這些結果進一步支持炎癥和神經營養因子在雙相情感障礙病理生理學中的作用。但是觀察到的GDNF減少和炎癥因子含量增加是否由于病理或適應性反應仍有待確定。
認知缺陷是雙相障礙患者的核心癥狀,而認知與工作、人際關系、日常生活密切相關,因此探索認知缺陷的病理機制至關重要。在本研究中,神經心理學測試與NLR、PLR和GDNF之間的相關性分析顯示, NLR和GDNF分別與VFT-動作及TMT-B評分之間存在顯著的相關,這和國內外的研究結果一致[15-16]。TSENG H H等[17]發現炎癥狀態升高和神經營養因子降低均會對額顳葉認知能力,如記憶、注意力和執行功能,產生負面效果。這些證據支持雙相障礙患者升高的炎癥標志物水平和降低的GDNF濃度均與認知功能較差相關。
最新數據證實不同類型的免疫細胞和上皮細胞具有釋放GDNF家族配體并表達其受體的能力,從而參與修復炎癥后上皮屏障損傷[18]。GDNF是炎癥過程中的關鍵參與者,是連接神經元和上皮細胞之間的通訊員,參與造血細胞分化的調節以及在感染期間激活免疫系統反應[19]。此外,有證據表明GDNF部分由免疫細胞表達并調節促炎細胞因子的分泌,可用于治療炎癥性疾病[20], 而炎癥因子也影響GDNF的表達和調節,因此兩者之間相互影響相互依存。本研究結果GDNF和NLR相關符合這一觀點,同時還發現炎癥和神經營養因子存在交互作用對認知功能產生影響,這是研究創新點。尸檢研究[21]顯示,雙相障礙患者前額葉和前扣帶回皮質特定層的星形膠質細胞和小膠質細胞數量或密度降低。而星形膠質細胞主要分泌GDNF, 小膠質細胞負責清除中樞神經系統中損壞的神經,斑塊及感染性物質。此外,在腦免疫細胞的背景下, GDNF及其受體在炎癥條件下的小膠質細胞和相關巨噬細胞中表達,減少炎性細胞因子的分泌[22-23]。GDNF亦通過激活小膠質細胞功能幫助免疫系統從受感染的神經元中清除病毒。因此推測GDNF和炎癥因子NLR相互作用影響雙相障礙認知損害的病理機制。
本研究由于樣本量相對較少而存在一些局限性:首先,這項工作表明GDNF與執行功能(TMT反映執行功能)變化之間存在相關性,但無法解釋可能的因果關系,本研究無法區分GDNF水平的變化是否來自接觸抗精神病藥治療或雙相障礙自然精神病理學的結果;其次,神經心理測試時由于雙相障礙患者仍服用藥物,這可能會影響認知和促炎功能;最后,雖然2組患者的文化水平、吸煙狀況和體質量指數相匹配,但有一些不可控制的因素,如遺傳特征、生活方式、飲食運動和營養模式,對結果可能產生一定的混雜效應。因此本研究揭示了NLR和GDNF與TMT-B分數之間存在相關,還發現了兩者交互影響認知表現,這表明了認知功能復雜的病理生理機制。未來可采用前瞻性研究控制相關的混雜因素來確認炎癥和GDNF對雙相障礙患者認知功能的影響。

