基于國產后裝治療機及其后裝放療計劃系統的質控方法研究
劉子成,費振樂,劉苓苓,王真真,邵婧媛,崔相利
1. 中國科學院合肥腫瘤醫院 放療中心,安徽 合肥 230031;2. 安徽醫科大學 生物醫學工程學院,安徽 合肥 230032;3. 中國科學技術大學 研究生院科學島分院,安徽 合肥 230026
引言
宮頸癌是常見的婦科惡性腫瘤,發病率和死亡率在全球女性癌癥中占據第四位[1]。近距離放療是利用人體的自然腔道將放射源直接放置于治療部位或附近進行照射的一種模式,具有腫瘤組織受照劑量較高、周圍組織受照劑量較低、劑量跌落快等優點,廣泛應用于宮頸癌的治療中[2-3]。目前,后裝治療的質量保證標準不同,源活度計算和源到位精度等測量方法不統一,很多醫院單位在日常檢測中方法煩瑣且人為誤差較大[4-8]。為保證近距離治療的精準性和安全性,需要對后裝治療機及其計劃系統的質量控制提出嚴格要求。本研究主要探討和建立準確檢測后裝治療計劃系統和后裝治療機的質控方法。
1 材料與方法
1.1 設備和材料
192Ir高劑量率放射源(HDR-192):物理尺寸1.1 mm×6.5 mm、活性區尺寸0.7 mm×3.5 mm。檢測時放射源活度為140.6 GBq(3.8 Ci),科霖眾KL-HDR-C后裝治療機及后裝治療計劃系統(北京科霖眾醫學技術研究所,中國),大孔徑CT模擬定位機(飛利浦公司,美國),GAFCHROMIC?EBT3免洗膠片(ASHLAND,美國),EPSON Perfection V850Pro高端影像掃描儀(精工愛普生公司,日本),RIT 113膠片分析軟件。
1.2 測試內容與方法
1.2.1 圖像重建
選三個直徑分別為5、4.5和4 cm的標準模體,使用游標卡尺測量模體直徑,重復5次。再使用大孔徑CT模擬定位機掃描模體。掃描參數:電壓120 kV,曝光325 mAs,層厚3 mm。發送CT圖像到后裝計劃系統,利用系統自帶的測量工具測量模體直徑,重復5次后取平均值與實際測量值進行比較。
1.2.2 施源器自動重建
選取在中科院合肥腫瘤醫院進行三維腔內后裝治療的20例宮頸癌患者,年齡34~83歲,中位年齡為66.5歲。根據國際婦產科聯合會(International Federation of Gynecology and Obstetrics,FIGO)制定的標準[5],20例患者臨床分期為宮頸癌Ⅰ期1例、宮頸癌Ⅱ期10例、宮頸癌Ⅲ期7例、宮頸癌Ⅳ期2例。20例患者均為三通道施源器治療。在治療計劃系統(Treatment Planning System,TPS)中新建計劃plan 2,自動重建施源器通道,施源器駐留長度和駐留時間均與臨床計劃plan 1一致。臨床計劃plan 1均由物理師手動重建施源器通道。根據Report 89號報告[6]評估比較不同計劃中90%以上體積的臨床靶區(Clinical Target Volume,CTV)達到的處方劑量(D90);膀胱、直腸和乙狀結腸可以接受的最大劑量下0.1 cm3和2 cm3體積所接受的最小劑量(D0.1cc、D2cc)。數據分析采用SPSS 25.0軟件對所得結果進行配對t檢驗。P<0.05為差異具有統計學意義。
1.2.3 放射源最大輸出距離點的到位精度
輸源軟管一端與后裝機分度盤上任意出源通道連接,另一端緊貼膠片上,固定。在膠片上對施源導管最遠端進行標記。在操作間制定一個單通道最遠端駐留點的治療計劃,駐留時間為5 s,測量時源強為3.8 Ci。相同條件下重復測量5次。膠片曝光24 h后,使用掃描儀掃描膠片,掃描時分辨率設置為75 dpi。掃描后使用膠片分析軟件分析得出放射源活性中心與標記點之間的距離。如果到位精度無偏差,放射源活性中心與標記點之間的距離應為4.25 mm(放射源物理尺寸的1/2加1 mm施源軟管的壁厚)。根據測量值與理論值的偏差判斷放射源最大輸出距離點的到位精度。
1.2.4 放射源5 mm步退距離精度
輸源軟管一端與后裝機分度盤上任意出源通道連接,另一端緊貼膠片上,固定。在操作間制定一個單通道8個駐留點的治療計劃,步退距離為5 mm,每個點駐留時間為10 s。相同條件下重復測量5次。膠片曝光24 h后,使用掃描儀掃描膠片,掃描時分辨率設置為75 dpi。掃描后使用軟件分析圖像,得出相鄰駐留點之間形成的劑量峰。測量相鄰劑量峰之間的距離,判斷步退距離是否為5 mm。
1.2.5 放射源活度檢測
在自由空氣中,將輸源軟管一端與后裝機分度盤上第一出源通道連接,另一端插入井型電離室直至底部。將井型電離室與劑量計連接,在PTW Unidos E的參數調整界面上選擇 Electronic模式,量程改到最大的high檔,提前預熱5 min并歸零校準。井型電離室需要提前放置在治療機房30 min,使其與測量環境的溫度、氣壓一致。后裝治療機房中的氣壓和溫度等基礎數據均由空盒氣壓表進行采集。在操作間制定一個有15個駐留點、步退為5 mm、各點駐留時間為10 s的測試計劃。出源后記錄劑量計顯示的最大靈敏位置讀數,利用公式(1)計算源活度(Aapp)[7],相同條件下重復測量5次。

其中,Mu為源在井型電離室最大靈敏度位置的電流讀數(nA)或 60 s積分電荷(nC/60 s),CT·P為溫度氣壓修正因子;E為井型電離室及劑量計刻度系數,E=9.211×105Gy·m2·h-1·A-1;F 為192Ir源空氣比動勢能強度與源活度轉換系數,F=4.034×10-3Gy.m2.h-1.A-1.Ci-1。
環境溫度、氣壓校正因子計算方法如公式(2)所示。
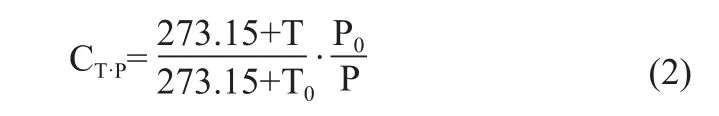
式中,T為環境溫度讀數,單位為℃;T0為標準條件溫度(22℃);P0為標準條件氣壓(101.3 kPa);P表示環境氣壓讀數,單位為kPa。
2 結果
2.1 圖像重建
標準模體實測平均值分別為4.98、4.49和3.98 cm,重建后系統工具測量的直徑平均值為5.06、4.46和4 cm(表1)。重建測量值與實際測量值之間相對誤差均小于1 mm。根據NCC/T-RT 002-2019后裝治療機的質量控制和質量保證[8]判斷,符合其中圖像重建直徑的相對誤差應<±1 mm的要求。
表1 圖像重建結果統計(cm,±s)
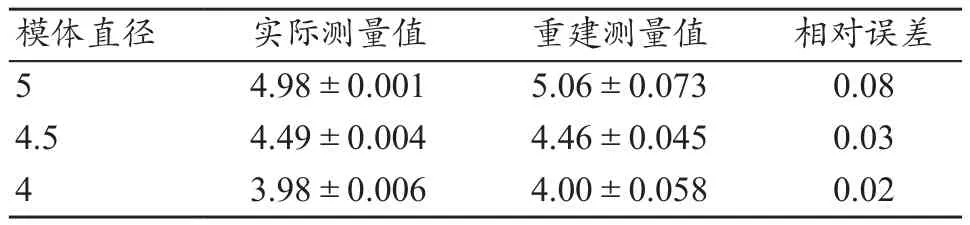
表1 圖像重建結果統計(cm,±s)
模體直徑 實際測量值 重建測量值 相對誤差5 4.98±0.001 5.06±0.073 0.08 4.5 4.49±0.004 4.46±0.045 0.03 4 3.98±0.006 4.00±0.058 0.02
2.2 施源器通道自動重建
使用TPS中自動重建施源器通道功能,施源器駐留長度和駐留時間均與臨床計劃一致,臨床計劃中施源通道均為物理師手動逐點重建。統計自動重建計劃和臨床計劃的腫瘤靶區和危及器官受量并進行比較(表2)。分析結果表明:腫瘤靶區D90、膀胱D2cc和D0.1cc、直腸D2cc、乙狀結腸D2cc和D0.1cc劑量參數差異均無統計學意義(P>0.05);直腸D0.1cc劑量參數有統計學意義(P=0.03)。此外自動重建計劃的膀胱D2cc和D0.1cc的平均值均大于手動重建的膀胱受照劑量;直腸D2cc和D0.1cc的平均值均小于手動重建的直腸受照劑量。
表2 20例患者后裝計劃中施源器通道重建結果統計(cGy,±s)
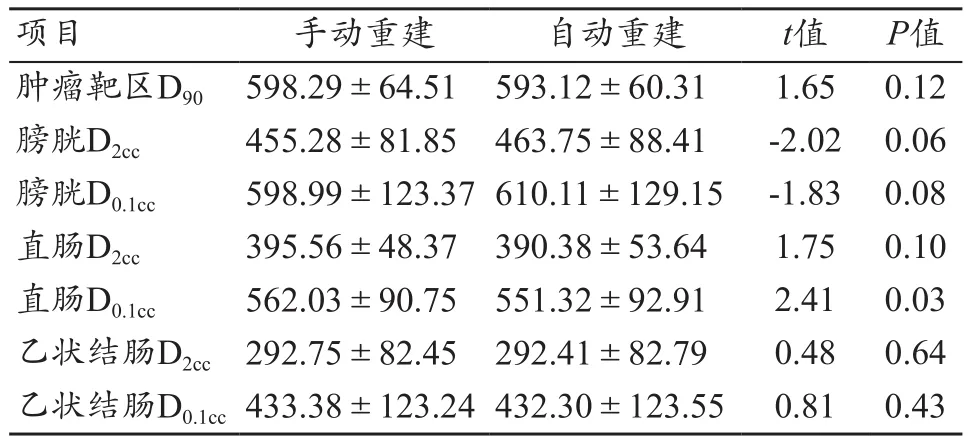
表2 20例患者后裝計劃中施源器通道重建結果統計(cGy,±s)
項目 手動重建 自動重建 t值 P值腫瘤靶區D90 598.29±64.51 593.12±60.31 1.65 0.12膀胱D2cc 455.28±81.85 463.75±88.41 -2.02 0.06膀胱D0.1cc 598.99±123.37 610.11±129.15 -1.83 0.08直腸D2cc 395.56±48.37 390.38±53.64 1.75 0.10直腸D0.1cc 562.03±90.75 551.32±92.91 2.41 0.03乙狀結腸D2cc292.75±82.45 292.41±82.79 0.48 0.64乙狀結腸D0.1cc433.38±123.24 432.30±123.55 0.81 0.43
2.3 最大輸出距離點到位精度分析
根據膠片分析的Profile圖可得源活性中心產生了明顯的劑量峰(圖1a)。劑量曲線上可看出最遠距離標記點對劑量曲線的波動,記錄最大波動點與活性中心點之間距離(圖1b)。5次測量結果平均值為(4±0.05)mm,與理論值4.25 mm平均偏差為0.25 mm(表3)。根據NCC/T-RT 002-2019后裝治療機的質量控制和質量保證[8]中,放射源最大輸出到位精度應<±1 mm,符合要求。

圖1 最大輸出距離點到位精度膠片和軟件分析結果圖

表3 源到位精度驗證結果(mm)
2.4 放射源5 mm步退距離精度分析
根據膠片分析的Profile圖得出8個駐留點產生了8個劑量峰值,通過測量相鄰峰值之間的距離判斷5 mm步退距離是否存在偏差(圖2)。8個駐留點形成的7個步退距離平均值為(5.04±0.05)mm,與理論值5.00 mm偏差為0.04 mm(表4),符合WS 262-2017后裝γ源近距離治療質量控制檢測規范[7]要求,放射源退位精度<±1 mm,符合國家衛生職業要求。
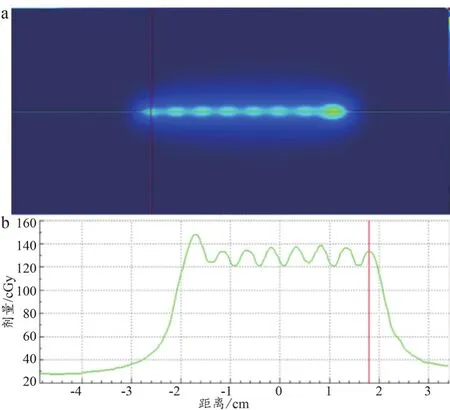
圖2 5 mm步退距離精度軟件分析結果圖

表4 源步距精度驗證結果(mm)
2.5 放射源活度檢測
測量時機房溫度為29℃,環境氣壓為100.6 kPa,根據公式(2)計算得出溫度氣壓修正因子(CT·P)為1.017。劑量儀顯示的最大靈敏位置讀數(Mu)為35.67 nA。根據公式(1)計算得出源活度為8.404 Ci,標稱源活度為8.44 Ci,相對誤差為0.43%。符合WS 262-2017后裝γ源近距離治療質量控制檢測規范[7]要求,放射源活度誤差范圍為±5%。
3 討論
后裝放療的劑量線分布梯度大且多為單次大劑量照射,治療過程中的誤差都可能導致患者受照劑量與計劃劑量不一致,由劑量偏差導致的后果難以評估和彌補[9-10]。劑量的準確性會直接增加腫瘤原發病灶劑量缺失和周圍正常組織毒副反應加重的可能性[11-12]。因此后裝治療機和后裝治療計劃系統的質量控制和質量保證至關重要。
后裝機中的192Ir放射源半衰期短(74.2 d),一年中需要更換多次。后裝機在使用過程中,送絲輪的漲緊力、步進電機的精度等都會發生改變,導致機器到位精度和步退精度變差。這樣容易影響源在治療時不能到達指定位置,從而使患者受照劑量產生偏差,影響療效。后裝機廠家一般配有出源長度標尺以進行源到位精度的測量。目測法[13-14]步驟煩瑣且由操作和主觀因素引起的誤差較大。本研究使用免沖洗膠片測量源到位精度和步退精度,通過測量源活性中心實際到達的位置,檢測結果較目測法更精準。趙紅福等[15]發現采用輻射顯色膠片確定環形施源器駐留位置偏移量是一種簡便且精確的測量方法。于浪等[16]建立了通過視頻圖像和膠片分析確定后裝放射源的駐留位置的檢測手段也發現膠片測量法較可靠。膠片測量法所產生的誤差是客觀存在的。測量結果中會出現不同的不確定度來源:① 在相同條件下測量所得結果有所不同,例如多次測量到位和退位精度時,膠片劑量峰與標記點之間距離有所不同,引入A類不確定度;② 膠片的種類較多,分辨率和靈敏度也有所區分,以及掃描儀設備本身誤差都將引入B類不確定度;③ 不同實驗人員對施源器到位的最大距離標記點存在不同判斷,將引入A類不確定度[17-18]。
在后裝放療計劃系統中制定治療計劃,192Ir源外觀活度決定了患者的治療時間,從而影響治療總劑量。源的外觀活度發生較大偏差,會直接導致患者所受劑量產生誤差(超劑量或欠劑量)。本研究參照WS262-2017利用井型電離室測量源外觀活度,檢測結果較穩定。目前,后裝放射源校準的方式有井型電離室、指型電離室和在模體中測量[19-20]。Bondel等[21]研究3種不同的源校準方法,測量結果之間的最大偏差為1%,但井型電離室具有長期穩定性好、操作簡便等優點,推薦使用井型電離室進行源外觀活度測量。
施源器重建精度會影響放射源駐留位置,進而影響劑量分布。本研究采用劑量體積直方圖參數評估傳統手動逐點重建法和施源庫自動重建法對宮頸癌患者受照劑量的影響。由結果可知,自動重建法腫瘤靶區D90和直腸D2cc平均劑量均比手動重建法的結果小5 Gy;膀胱D2cc平均劑量比手動重建法的結果大8 Gy;兩種方法所得乙狀結腸D2cc平均劑量幾乎無差別。兩種方法所得腫瘤靶區D90、膀胱D2cc、直腸D2cc和乙狀結腸D2cc均無統計學差異(P>0.05)。手動逐點重建法和施源庫自動重建法之間無統計學差異,但自動重建法容易受到施源器金屬偽影和CT固有的容積效應影響,導致出現重建的施源器通道無法應用于臨床的情況。自動重建法的膀胱和直腸平均劑量與手動逐點重建之間的差異超過5 Gy,可能存在重建偏差。Schindel等[22]發現T&O施源器重建偏差存在于腹背方向,所以施源器重建偏差對直腸的劑量影響較明顯。
4 結論
本研究所使用的國產后裝治療機及其后裝放療計劃系統可以很好地應用于臨床治療。采用井型電離室可準確測量源活度;膠片測量法測量放射源到位和退位精度結果較可靠;TPS中施源器自動重建法雖存在一定偏差但可應用于臨床。本文介紹的驗證方法簡單準確,對后裝機及其計劃系統的驗收和常規質控具有一定參考意義。

