紅細胞在網狀微血管結構內的運動仿真研究
王振華,朱燕文,張權,邸文奇,尚禹
中北大學 信息與通信工程學院,山西 太原 030051
引言
微循環是指微動脈與微靜脈之間微血管網絡中的血液循環,其基本功能是利用紅細胞的運動實現血液與組織細胞的物質交換[1-2]。微循環是生命的基本特征之一,是人體各個系統組織和器官的組成部分,是最小功能單位的“支架”。微血管的構型反映了組織和器官的特點,并與組織和器官的功能相適應。因此,微循環中的血流量的高低直接影響身體的各臟器[3-4]。局部腦灌注量的不足造成的缺血性腦卒中、組織血流異常增高、組織血氧水平偏低以及氧代謝增高等都是腫瘤血流動力學的臨床表現[5];此外微循環血流測量還有助于幫助醫師及時調整和優化手術方案。因此精準地計算微血管血流值對于生命科學前沿基礎研究以及臨床診斷治療都具有重要意義。
近紅外漫射光相關譜(Diffuse Correlation Spectroscopy,DCS)技術是目前常用于微血管血流監測的技術手段[6-10]。DCS通過光場時間自相關函數來評估紅細胞運動的快慢來反映微血管系統的血流,其計算依靠紅細胞的運動狀態,由于目前還沒有對微血管中紅細胞運動狀態的詳細研究,這阻礙了微血管血流的準確測量以及對實驗數據的正確解釋。得到一個精確的血流值無論對于疾病診斷還是治療效果評估,都非常重要。由于微循環過于微小,無法直接肉眼觀察出其中紅細胞的變化,需要借助高分辨率顯微鏡(例如實時成像倒置顯微鏡)才能觀察和記錄其中的變化,這給微血管紅細胞的動力學研究[11-18]造成了非常大的困難。部分研究從微觀角度利用晶格Boltzmann方法建立了三維紅細胞顆粒的運動模型,分析了三維紅細胞在流體中受力計算不精確和旋轉的問題[19-20];部分研究使用蒙特卡羅(Monte Carlo)仿真對血管網狀結構和層流剖面進行模擬,并基于漫射光譜理論推導了考慮擴散和平流散射體的運動[21-22];Causin等[23]提出了一個數學計算模型來研究柔性微血管網絡中紅細胞的運動。Gould等[24]提出一種將先進的顯微鏡數據與大規模血流動力學模擬相結合的新方法去量化血管構筑對大腦微循環的影響。但是由于微血管內結構復雜,目前并沒有從宏觀的角度對紅細胞在微血管網狀結構內的運動軌跡進行詳細的描述[25-26]。
本文首次運用流體力學軟件COMSOL Multiphysics建立了微血管模型仿真,模擬了微血管中紅細胞的運動軌跡,計算得出紅細胞的速度和位移與時間之間的關系,并進行多種流速的模型計算,得到流速與紅細胞運動的關系。微血管模型仿真技術的開展為深入了解組織微循環的機制和精確的血流測量提供了有價值的信息。
1 方法
1.1 微血管仿真模型的搭建
根據微血管系統的網狀結構,利用流體力學計算軟件COMSOL Multiphysics建立有限元模型,具體方法如下。首先,建立仿真幾何模型:利用COMSOL Multiphysics軟件內嵌的建模工具實現幾何建模,中間扁平立方體(長3 cm,寬1 cm,高0.5 cm)部分是微血管部分,并且設置了1 mm的厚度,兩端的圓柱體(長0.1 cm,圓直徑0.5 cm)作為微血管網絡兩端的動脈和靜脈血管。一端作為入口,一端作為出口(圖1)。此外,在血管模型內部添加小球來模擬微血管錯綜復雜的分布情況(血液里除了紅細胞的靜態物質,如上皮細胞等)。添加多物理場:本文使用到的是層流模塊和粒子追蹤模塊,在入口處設置了固定的流速作為入口處粒子(紅細胞)的初始速度。此外,在血管內部按照對數正態分布函數來隨機釋放粒子,該類粒子代表的是隨機產生或者從外部滲透進入血管內部的紅細胞。添加層流模塊中的重力、布朗運動力、邊界應力等用來模擬人體微血管紅細胞的真實受力情況,最后利用物理場控制網絡中的極細化進行網格劃分,完成模型搭建。在仿真中,設置t=0時刻在入口處釋放1000個粒子,之后隨機釋放的粒子是按照對數正態分數函數來隨機釋放的,共釋放40次,每次釋放的粒子數為100個,這些粒子釋放的初始位置是隨機的,共隨機釋放4000個粒子,模型總計釋放5000個粒子。設置時間為1 s,隨后整個模型系統運行計算5 s,得到所有粒子的不同時刻的坐標數據。
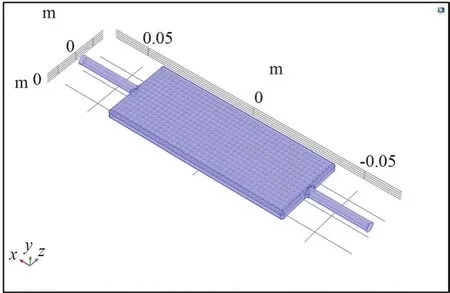
圖1 微血管仿真模型
1.2 數據處理
通過COMSOL Multiphysics模型計算后導出每秒的粒子坐標軌跡文件,應用MATLAB中編寫的程序對粒子軌跡進行處理,為了得到穩定的數據分析結果,選取紅細胞活動最穩定時間段(即第5 s)中單位時間的粒子位移數據進行分析。將模型中第4 s與第5 s這兩個時間點的粒子坐標數據利用位移計算公式(1)得到每個粒子在這一秒的位移值,隨后取這些粒子位移的平均值。為了驗證流速與紅細胞運動之間的關系,本文進行了5種不同流速的微血管模型仿真(即流速分別為100、150、200、300、400 mL/h),并且將各流速模型中第5 s大量粒子(5000個)的位移進行了統計,得到平均結果。除此之外,將每個流速下的粒子仿真過程重復進行3次,得到位移方差小于1%以確認結果的穩定性。
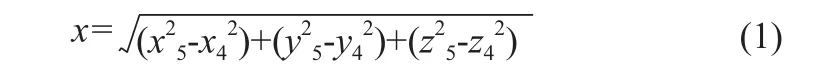
2 結果
圖2顯示了紅細胞粒子的瞬態速度場,以此建立粒子運動。由于在微血管模型的入口處添加了粒子的初始速度,所以紅細胞是不均勻速度分布的。相比而言,微血管模型內部的粒子適合均勻的速度,因此紅細胞的運動速度表現得更加均勻。由于受到外部速度因素以及內部的布朗運動因素的影響,紅細胞運動是有向模型和無向模型的混合運動。

圖2 微血管模型速度場
圖3~4顯示了在兩個代表性時間(即1 s和5 s)模型中紅細胞粒子的位移分布。從局部放大的圖中可以清楚地看到,當時間從1 s變到5 s時,血管模型內的紅細胞粒子的軌跡有明顯的位移變化,這種位移分布是由粒子速度和其所在的復雜的微血管系統決定的,宏觀的紅細胞粒子軌跡分布模式反映了實際的微脈管系統中紅細胞的運動軌跡。相比從微觀角度模擬單個紅細胞的運動狀態,以及在機體外利用顯微鏡觀察紅細胞的運動形態的方法,本文的仿真結果從宏觀角度首次將紅細胞在機體內的微循環運動軌跡進行了詳細的描述,為了解組織微循環的機制提供了有價值的信息。
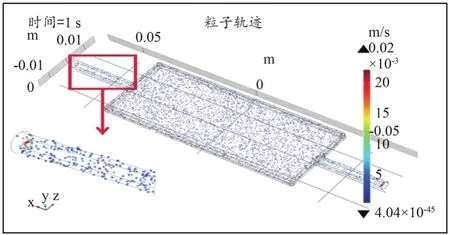
圖3 1 s時粒子軌跡
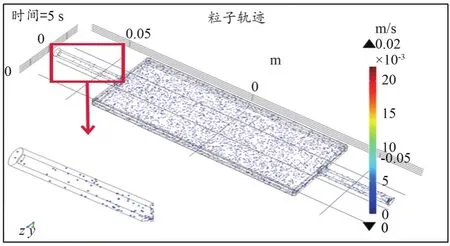
圖4 5 s時粒子軌跡
圖5顯示了不同流速下粒子在1 s內的平均位移。可見,隨著流速的增大,粒子的平均位移也隨之增大。隨著流速從100 mL/h增大到400 mL/h,粒子的平均位移從0.22 cm增大到0.84 cm,顯示了流速與紅細胞運動的關系:流速越大,紅細胞粒子運動越快。
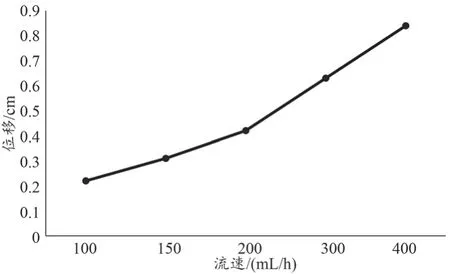
圖5 不同流速下粒子1 s內的平均位移
3 討論
本文根據流體力學原理以及粒子追蹤技術,首次利用COMSOL Multiphysics多物理場仿真軟件建立了微血管的仿真模型,并進行血流動力學的分析,描述了紅細胞在微血管中的運動狀態。根據微血管仿真模型的分析結果得到了紅細胞粒子運動軌跡,每個紅細胞粒子在不同時刻的位置、速度以及與時間的關系等。將粒子運動位移坐標數據進行處理得到了宏觀流速與紅細胞運動的關系,即流速越大,紅細胞運動越劇烈,速度越快。當流速從100 mL/h逐漸增加至400 mL/h時,粒子在1 s內的平均位移從0. 22 cm增大到0. 84 cm,并且二者的關系不完全是線性的。本文的結果先進性主要有以下兩點:① 首次基于流體力學以及粒子追蹤技術,利用COMSOL Multiphysics多物理場仿真軟件建立了微血管網絡仿真模型,從宏觀的角度分析了紅細胞的運動軌跡;② 通過多個流速模型仿真,對紅細胞位移數據進行計算,得到了宏觀流速與紅細胞運動的關系。相比于從微觀角度模擬單個紅細胞的運動狀態,以及在機體外利用顯微鏡觀察紅細胞運動形態的方法,本文的仿真結果從宏觀角度詳細地描述了機體內微血管網絡的紅細胞的運動軌跡,有利于探索紅細胞的運動規律,為闡明微循環作用機制提供理論基礎。本文初步嘗試了微血管紅細胞的動力學仿真,并且微血管模型仿真中對混合物類型進行了相對比較簡單的分類,并未考慮所有因素,接下來會對混合物的類型進行調整優化,建立一個更加精確的微血管仿真模型,并且與顯微鏡觀察下的紅細胞運動軌跡相對比,進行更全面的研究。全面反映物理和生物學機制的微血管模型將是未來主要的研究方向。本文建立了微血管的仿真模型,描述了紅細胞的運動軌跡,闡明了宏觀流速與微觀紅細胞運動的規律,這為深入了解組織微循環的機制和精確地血流測量提供了有價值的信息,因此在未來的生理和臨床研究中具有巨大的潛力。
4 結論
人體組織的微血管血流對于很多疾病檢測以及臨床診斷有重要意義,由于組織微循環過于微小,目前尚缺乏對微血管中紅細胞運動狀態的詳細研究。針對此問題,本文利用COMSOL Multiphysics多物理場仿真軟件中的層流模塊和粒子追蹤模塊建立了微血管的仿真模型并進行血流動力學的分析,獲得了紅細胞在微血管中的運動狀態。根據血流動力學的分析結果,在后處理中導出紅細胞位移的坐標數據,通過仿真多個流速模型且將紅細胞的運動位移數據進行計算,得到了宏觀流速與紅細胞運動的關系,即流速越大,紅細胞運動越劇烈,速度越快。作為一項先導研究,本文建立了反映物理和生物學機制的紅細胞運動軌跡的微血管仿真模型,這有助于微血管血流值的精確測量以及計算,對于生命科學前沿基礎研究以及臨床診斷治療都具有重要意義。

